Применение Реамберина в интенсивной терапии перитонита, осложненного полиорганной недостаточностью
Статьи
А. Ю. Яковлев, Г. А. Бояринов, Р. М. Зайцев, Н. В. Емельянов, В. Б. Семенов, Е. В. Дудина
Методическое пособие подготовлено сотрудниками Военно-медицинского института ФСБ России и Нижегородской областной клинической больницы им. Н. А. Семашко. Авторы:
Яковлев Алексей Юрьевич — доктор медицинских наук, доцент кафедры анестезиологии, реаниматологии и трансфузиологии Военно-медицинского института ФСБ России;
Бояринов Геннадий Андреевич — заслуженный врач РФ, доктор медицинских наук, профессор, академик АМТН РФ, начальник кафедры анестезиологии, реаниматологии и трансфузиологии Военно-медицинского института ФСБ России;
Зайцев Роман Михайлович — заслуженный врач РФ, кандидат медицинских наук, врач-хирург, главный врач ГУЗ «Нижегородская областная больница им. Н. А. Семашко»;
Емельянов Николай Васильевич — кандидат медицинских наук, врач-хирург, заместитель главного врача ГУЗ «Нижегородская областная больница им. Н. А. Семашко» по хирургии;
Семенов Владимир Борисович — врач-анестезиолог-реаниматолог, заведующий отделением реанимации и интенсивной терапии ГУЗ «Нижегородская областная больница им. Н. А. Семашко»;
Дудина Екатерина Владимировна — кандидат биологических наук, старший научный сотрудник научно-иследовательского отдела Военно-медицинского института ФСБ России.
Методическое пособие посвящено применению реамберина при полиорганной недостаточности у больных перитонитом. Показана необходимость включения реамберина в комплексную послеоперационную интенсивную терапию и дозозависимую коррекцию метаболических расстройств, эндотоксикоза и органных дисфункций.
Методическое пособие ориентировано на врачей анестезиологов-реаниматологов, хирургов, трансфузиологов.
Рецензия
на методическое пособие А.Ю. Яковлева, Г.А.Бояринова, Р.М. Зайцева, Н.В. Емельянова, В.Б. Семенова, Е.В. Дудиной Применение «Реамберина» в интенсивной терапии перитонита, осложненного полиорганной недостаточностью».
Методическое пособие А.Ю. Яковлева, Г.А. Бояринова, Р.М. Зайцева. Н.В. Емельянова, В.Б. Семенова. Е.В. Дудиной «Применение «Реамберина» в интенсивной терапии перитонита, осложненного полиорганной недостаточностью» (Нижний Новгород, 2007). подготовленное сотрудниками Военно-медицинского института ФСБ России и Нижегородской областной клинической больницы им. Н.А. Семашко, посвящено применению реамберина при полиорганной недостаточности у больных перитонитом.
Основным направлением снижения летальности при перитоните, осложненном мультиорганной дисфункцией, в настоящее время служит разработки и применение патофизиологически обоснованных методов коррекции гомеостаза. Независимо от вида гипоксии, сопровождающей МОД, в основе всех характерных для нее нарушений лежит недостаточность главной клеточной энергообразующей системы митохондриального окислительного фосфорилирования. В связи с этим разработка методов фармакологической коррекции внутриклеточного метаболизма при критических состояниях любого генеза приобретает особую значимость. Одним из перспективных направлений интракорпоральной детоксикации является использование инфузионных антигипоксантов, в частности, реамберина.
Авторы подробно описывают патофизиологические особенности действия реамберина у больных перитонитом и приводят подробную характеристику указанного препарата.
Используя современные методы исследования (шкалы SOFA и APACHE II, биохимические данные), авторы оценили течение послеоперационного перитонита, осложненного МОД у 108 пациентов, которым наряду с внутриаортальной комплексной терапией, включающей антибактериальную, инфузионную терапию, коррекцию нарушений ВЭБ, парентеральное питание, назначали различные дозы реамберина.
Выявлено, что применение реамберина в дозе 800 мл/сутки сопровождается тенденцией к восстановлению нарушений метаболизма, но после окончания инфузии изменение метаболизма и системы ПОЛ/АОС указывают на недостаточность коррекции проявлений гипоксии и необходимость повторного применения реамберина.
Увеличение объема вводимого препарата до 1600 мл/сутки в первые 48 часов после прекращения введения препарата, с другой – сокращением сроков гиперпируватемии (купирование синдрома гиперкатаболизма-гиперметаболизма). Реамберин можно рассматривать как эффективное патогенетическое средство коррекции гипергликемических осложнении у больных в критических состояниях.
Показаниями к использованию реамберина в дозе 1600 мл/сутки являются гиперлактатемия выше 4 мкмоль/л, гиперпируватемия выше 200 мкмоль/л, отношение лактат/пируват более 20 у.е., гипергликемия более 10 ммоль/л.
Торможение процессов перекисного окисления липидов и стабилизация антиоксидантной защиты на фоне традиционной (800 мл) и форсированной (1600 мл) терапии реамберином способствует поддержанию равновесия этой наиболее уязвимой при критических состояниях системы.
Применение реамберина, не влияя на динамику эндотоксикоза в первые сутки, начиная со вторых оказывает дозозависимую коррекцию эндотоксикоза, что обеспечивает уменьшение степени тяжести состояния пациентов и выраженности органных дисфункций, определяемых с помощью шкал APACHE II и SOFA.
Таким образом, авторами пособия убедительно показана эффективность инфузионного антигипоксанта реамберина у больных перитонитом, осложненным мультиорганной дисфункцией.
Все выше изложенное позволяет рекомендовать пособие А.Ю. Яковлева, Г.А. Бояринова, Р.М. Зайцева, Н.В. Емельянова, В.Б. Семенова, Е.В. Дудиной «Применение «Реамберина» в интенсивной терапии перитонита, осложненною полиорганной недостаточностью» к печати как весьма актуальное и нужное.
Заведующий кафедрой анестезиологии, реаниматологии и интенсивной терапии ГОУ ВПО «СПбГМУ им. акад. И.П.Павлова» Федерального агентства по здравоохранению и социальному развитию д.м.н., проф. В.А. Корячкин
Рецензия
на методическое пособие «Применение «реамберина» в интенсивной терапии перитонита, осложненного полиорганной недостаточностью»
Авторами обобщен собственный клинический опыт интенсивной терапии перитонита, осложненного полиорганной недостаточностью, полученный на клинических базах кафедры анестезиологии, реаниматологии и трансфузиологии Военно-медицинского института ФСБ России.
Методическое пособие содержит необходимые сведения для обоснованности выводов, сделанных авторами. Достаточный клинический материал, широкий спектр изучаемых показателей, охватывающий оценку степени повреждения метаболических процессов, реакции свободнорадикального окисления липидов и противодействующем им антиоксидантной системы организма, позволяют считать патофизиологически целесообразным применение реамберина в раннем послеоперационном периоде у больных перитонитом. Особую оценку необходимо дать применяемому мониторингу метаболических показателей. Во время введения изучаемого препарата авторами впервые показана зависимость течения метаболических процессов от экзогенного поступления субстратного антигипоксанта. На основании отмеченного восстановления анаэробной направленности после окончания введения традиционно используемой дозы реамберина доказана необходимость увеличения до 1600 мл суточной дозы реамберина в первые двое суток послеоперационной терапии. Основным лабораторным критерием назначения увеличенных объемов реамберина служит уровень лактатемии выше 4 ммоль/л.
Авторами показано, что положительное действие реамберина первично по отношению к коррекции расстройств метаболизма, за счет которых происходит и компенсация синдрома зндотоксикоза и синдрома полиорганной недостаточности. Сдерживающее воздействие метаболической терапии реамберином на течение катаболических процессов при перитоните и купирование синдрома гиперкатаболизма является универсальным, повышает эффективность таких лечебных мероприятии как детоксикация и нутритивная поддержка, что может быть использовано врачами, занимающимися этими направлениями интенсивной терапии больных в критических состояниях любой этнологии.
Методическое пособие предназначено для врачей анестезиологов-реаниматологов, хирургов и трансфузиологов.
Заключение: Рекомендовать методическое пособие «Применение «Реамберина» в интенсивной терапии перитонита, осложненного полиорганной недостаточностью» к печати.
Заведующий кафедрой анестезиологии-реаниматологии и неотложной педиатрии ФПК и ПП ГОУ ВПО «Санкт-Петербургская государственная педиатрическая медицинская академия» Федерального агентства по здравоохранению и социальному развитию, академии, д.м.н., профессор Ю.С. Александрович
Введение
Лечение больных с тяжелыми гнойно-септическими осложнениями заболеваний органов брюшной полости представляет одну из актуальных задач медицины критических состояний. Применительно к тяжелым формам перитонита в последние десятилетия прочно утвердилась концепция септического шока и синдрома полиорганной недостаточности (СПОН).
В последние годы накапливается все больше сведений, что эндотоксикоз и развивающиеся грубые нарушения метаболизма являются главным патогенетическим звеном тяжелых форм перитонита и СПОН.
Это служит обоснованием разработки и применения патофизиологически обоснованных методов коррекции гомеостаза и считается в настоящее время основным направлением снижения общей летальности при перитоните.
Одно из основных мест в формировании эндотоксикоза и СПОН отводится нарушениям метаболизма клетки [1–3, 5, 10, 13, 15]. Формирование гипоксических повреждений при перитонеальном эндотоксикозе зависит от многих факторов: нарушения легочной оксигенации, контрактильности миокарда, периферической микроциркуляции, синдрома гиперкатаболизма-гиперметаболизма и развития патологии тканевого метаболизма [4, 11, 14]. Однако независимо от вида гипоксии в основе всех характерных для нее нарушений лежит недостаточность главной клеточной энергообразующей системы митохондриального окислительного фосфорилирования [1, 12]. В связи с этим разработка методов фармакологической коррекции внутриклеточного метаболизма при критических состояниях любого генеза приобретает особую значимость.
Одним из перспективных направлений интракорпоральной детоксикации является использование инфузионных антигипоксантов, несомненная эффективность которых при критических состояниях доказана многими исследователями. В России в настоящее время зарегистрировано три инфузионных препарата, содержащих субстратные антигипоксанты — мафусол (15 г фумарата/л раствора), реамберин (15 г сукцината/л раствора) и стерофундин (1,5 г малата/л раствора).
Среди этих препаратов особое место занимает реамберин — первый препарат, содержащий стабильную растворимую форму сукцината — аниона янтарной кислоты. Превращение янтарной кислоты в организме связано с продукцией энергии, необходимой для обеспечения жизнедеятельности. Она является продуктом пятой и субстратом шестой реакции в цикле Кребса. Янтарная кислота является стимулятором синтеза восстановительных эквивалентов в клетке, обеспечивая поддержание метаболизма всех органических кислот цикла Кребса. Эндогенное и экзогенное пополнение клеточного пула сукцината способствует снижению уровня содержания органических кислот в крови с восстановлением их клеточной утилизации, экскреции кислых продуктов обмена из организма, что указывает на стимулирование аэробной фазы тканевого дыхания. Биологическое значение данного явления заключается в быстром ресинтезе АТФ клетками и в повышении их антиоксидантной резистентности.
Но главные преимущества сукцината перед другими метаболическими субстратами наиболее ярко проявляются в условиях гипоксии, на начальных этапах которой продукция эндогенного сукцината и скорость его окисления возрастает. При декомпенсации эндогенной продукции янтарной кислоты наступает торможение цикла трикарбоновых кислот (ЦТК), активация анаэробного гликолиза. В этот момент и до развития необратимых биохимических повреждений возникает зависимость восстановления энергообмена от сукцината, в том числе и от экзогенного его поступления. В этих условиях при нарастании физиологического содержания янтарной кислоты отмечается ускорение реакций цикла трикарбоновых кислот (фумаровой, яблочной и др.), снижение концентрации лактата и цитрата, накапливающихся в клетках при гипоксии, восстанавливается уровень эндогенного НАД, от содержания которого зависят скорости протекания начальных реакций ЦТК. Результатом этих процессов является восстановление потребления кислорода тканями за счет усиления транспорта электронов в дыхательной цепи митохондрий.
В экспериментах in vivo было показано, что применение сукцината приводило к прироступотребления кислорода тканями и увеличению продукции углекислоты, воды и тепла. С противогипоксическим действием сукцината тесно связано и его предупреждающее и корригирующее действие на процессы свободнорадикального окисления. Стабилизации системы ПОЛ/АОС способствует и стимулирующее действие сукцината на синтез церулоплазмина — белка, составляющего лабильную антиоксидантную систему организма.
К дополнительным, но не менее важным эффектам экзогенного сукцината относят стимуляцию сукцинатоксидазного окисления янтарной кислоты с восстановлением ее потребления в дыхательной цепи митохондрий и возрастанием активности антиоксидантной функции глутатиона, а также стимуляцией белкового метаболизма.
Ключевая роль сукцината среди всех субстратов цикла Кребса определяет и его значительный вклад в предупреждение реперфузионных повреждений в условиях нарушенного кислородного баланса.
Второй патофизиологической основой возникновения критических состояний является эндотоксикоз, обусловленный наличием в организме в необычных количествах токсических веществ или ядов. Развивающаяся гипоксия является причиной избыточного накопления промежуточных продуктов обмена, приводя к прогрессированию эндотоксикоза. Кроме того, поступающие извне ксенобиотики, в том числе и микробного происхождения, определяют самостоятельно развивающиеся нарушения всех звеньев системы транспорта кислорода и метаболизма, что делает изучение и последующее клиническое применение антигипоксантов у больных перитонитом патогенетически обоснованным и перспективным.
Скорость окисления субстратов цикла Кребса возрастает при эндогенных интоксикациях. В условиях эндотоксикоза пополнение пула интермедиатов цикла Кребса, в том числе и экзогенное, является необходимым для восстановления и последующего поддержания темпов энергообразования, соответствующих потребностям организма, органов, тканей и клеток.
Как известно, печень и эндотелий являются основными местами метаболизма ксенобиотиков. Именно эти органы и становятся мишенью эндотоксикоза с последующим развитием СПОН. Известная высокая скорость протекания метаболических процессов в печени (в покое — 30% энергопроизводства в органе весом не более 1,5% массы тела) подразумевает и их уязвимость при развитии гипоксии. Выявленная в первую очередь гепатотропность препаратов, содержащих янтарную кислоту, по-видимому, и является одной из причин коррекции эндотоксикоза при их включении в комплекс интенсивной терапии критических состояний.
Таким образом, в основе универсального лечебно-профилактического действия янтарной кислоты и ее соединений лежит модифицирующее влияние на процессы тканевого метаболизма — клеточное дыхание, систему ПОЛ/АОС, синтез белков. При этом эффекты экзогенного введения янтарной кислоты зависят от дозы антигипоксанта, режима его введения и исходного функционального состояния тканей, а конечный результат выражается в оптимизации параметров их функционирования. Такие свойства сукцината являются основой патофизиологического обоснования назначения реамберина больным перитонитом и дифференцированного подхода к его дозировке.
Характеристика препарата
Реамберин представляет собой сбалансированный полиионный раствор, содержащий: натрия хлорида — 6,0 г;
калия хлорида — 0,3 г;
магния хлорида — 0,12 г;
N-(1-дезокси-d-глюцитол-1 ил)
N-метиламмония натрия сукцината — 15,0 г;
воду для инъекций — до 1 л.
Ионный состав раствора: натрия — 142,4 ммоль;
калия — 4,0 ммоль;
магния — 1,2 ммоль;
хлорида — 109,0 ммоль;
сукцината — 44,7 ммоль;
N-метилглюкаммония — 44,7 ммоль.
Осмолярность — 320 мосм/л.
Материалы и методы исследования
Обследовано 108 больных (средний возраст 54,3 года) послеоперационным перитонитом, осложненным полиорганной недостаточностью (оценка по шкале SOFA более 10 баллов). Всем больным проводилась внутриаортальная комплексная терапия, включающая в себя антибактериальную, инфузионную терапию, коррекцию нарушений ВЭБ, парентеральное питание (до 3000 ккал/сутки). Препараты крови и жировые эмульсии вводились внутривенно. В исследование вошли пациенты с послеоперационным перитонитом, с исходным Мангеймерским индексом тяжести перитонита, превышающим 30 баллов и свидетельствующим о высокой вероятности летального исхода заболевания.
В зависимости от применения реамберина больные были разделены на 3 группы, сравниваемые по тяжести исходного состояния, сопутствующей патологии и сложности оперативного вмешательства:
- в 1-й группе (53 пациента) проводилась внутриаортальная интенсивная терапия;
- во 2-й группе (36 больных) дополнительно с момента начала внутриаортальной инфузии вводился реамберин в количестве 800 мл/сутки. Продолжительность терапии реамберином составляла 10 суток;
- в 3-й группе (19 пациентов) в первые двое суток после операции доза реамберина увеличивалась до 1600 мл/сутки, в последующем составляла 800 мл/сутки. Общая продолжительность терапии реамберином составляла 10 суток. Увеличение дозы реамберина у пациентов этой группы обусловлено поиском путей преодоления относительной резистентности метаболических нарушений к традиционной интенсивной послеоперационной терапии.
Объем суточной инфузионной терапии у всех больных не имел отличий и составлял в среднем 50–60 мл/кг/сутки.
Критериями исключения из исследования явились:
- летальный исход вследствие прогрессирования СПОН в первые 24 часа после операции;
- невозможность адекватной хирургической санации;
- применение методов эктракорпоральной детоксикации в комплексе послеоперационной интенсивной терапии.
Динамическая оценка тяжести состояния и органных дисфункций проводилась с помощью шкал APACHE II и SOFA.
Комплексное исследование клинико-лабораторных показателей выполнялось при поступлении больного в отделение реанимации и в течение первых 8 суток после операции. Артериальная и венозная кровь на биохимические анализы забиралась в утренние часы.
Клинико-биохимические показатели крови (гемоглобин, гематокрит, количество эритроцитов, лейкоцитов и тромбоцитов, лейкоформула, ЛИИ, глюкоза, концентрация билирубина, мочевины, креатинина, молочной, пировиноградной кислот и электролитов в плазме, содержание общего белка) исследовались при помощи унифицированных методик [7].
Уровень веществ низкой и средней молекулярной массы (ВНиСММ) в плазме, моче и на эритроцитах определяли по методике С.В. Оболенского и соавт. [8]. Принцип метода основан на определении спектра поглощения безбелкового супернатата плазмы в ультрафиолетовой области (238–302 нм). В норме содержание ВНиСММ в плазме — 6,82–10,4 у. е., в моче и на эритроцитах — 30 у. е.
Расчет индекса синдрома эндогенной интоксикации (ИСЭИ), равный отношению произведения плазменной и эритроцитарной ВНиСММ к ВНиСММ мочи, проводился по формуле [9]: ИСЭИ = ВНиСММ пл. Ч ВНиСММ эр./ВНиСММ мочи
(норма — 5,32±0,48)
Катаболический пул ВНСММ плазмы и мочи рассчитывался по формуле [6]: (Е238 + Е242 +… + Е258) Ч 4,
в норме не более 4–5 у. е. (10–15% от ВНиСММ пл.)
Исследование газов и КЩС артериальной и венозной крови проводилось с помощью аппаратов «Ciba-Corning M 288» и «Ciba-Corning M 348».
Эффективность применения реамберина у больных перитонитом
У больных перитонитом, осложненным полиорганной недостаточностью, гипоксия и связанные с ней нарушения метаболизма являются одним из важнейших факторов пато- и танатогенеза.
Реамберин применяется в лечении больных перитонитом, осложненного СПОН, для коррекции выраженных нарушений метаболизма и эндотоксикоза.
Выявлена многонаправленность терапевтического воздействия инфузий реамберина на механизмы формирования и поддерживания патологического процесса при перитоните.
Исследования метаболизма определили исходно выраженный дисбаланс энергообразования в сторону анаэробных процессов, резистентный не только к традиционной инфузионной терапии, но и сохраняющий свою актуальность при использовании обычных объемов реамберина (800 мл/сутки) (табл. 1). Тенденция к восстановлению нарушений метаболизма и системы ПОЛ/АОС после окончания инфузии 800 мл реамберина (2-я группа больных) одновременно свидетельствует о необходимости применения реамберина и недостаточности коррекции проявлений гипоксии традиционно применяемыми дозами препарата. Известно, что именно длительность гипоксии, наряду с ее выраженностью, определяет прогрессирование эндотоксикоза и полиорганной дисфункции, что служит основанием для увеличения объемов вводимого сукцинатсодержащего препарата до 1600 мл/сутки в первые 48 часов после операции (3-я группа). Достаточность увеличенной до 1600 мл реамберина антигипоксической терапии определяется отсутствием достоверного «синдрома рикошета» после прекращения введения препарата (рис. 1).
Другим достоверным аргументом эффективности аэробного переориентирования метаболизма с помощью реамберина является дозозависимое увеличение пируватемии во время инфузии изучаемого препарата (рис. 2). Сокращение же сроков гиперпируватемии наряду с положительным азотистым балансом показывает купирование синдрома гиперкатаболизма-гиперметаболизма на восьмые сутки после операции, что значительно повышает эффективность такого метода интенсивной терапии, как нутритивная поддержка.
Таблица 1
Динамика метаболических показателей у больных 1-й, 2-й и 3-й групп (М±m)
| Группа больных | Этапы исследования |
|---|
| Исходно | В конце инфузии реамберина | Через 2 часа после инфузии реамберина | 1-е сутки (до введения реамберина) | 1-е сутки (в конце введения реамберина) | 1-е сутки (через 2 часа после введения реамберина) | 2-е сутки | 5-е сутки | 8-е сутки |
|---|
| Лактат, мкмоль/л |
| 1-я | 5,99±0,29 | — | — | 4,65±0,220 | — | — | 3,93±0,220 | 2,91±0,200 | 2,09±0,110 |
| 2-я | 6,10±0,41 | 4,59±0,330 | 5,46±0,25 | 4,27±0,270 | 3,40±0,200 | 3,75±0,220 | 3,34±0,200,1 | 2,06±0,150,1 | 1,45±0,130,1 |
| 3-я | 5.83±0,32 | 4,07±0,370 | 4,10±0,310,2 | 3,61±0,280,1 | 3,01±0,250 | 3,12±0,200,2 | 2,73±0,270,1 | 1,68±0,140,1,2 | 1,43±0,170,1 |
| Пируват, мкмоль/л |
| 1-я | 0,216±0.007 | — | — | 0,204±0,007 | — | — | 0,198±0,006 | 0,170±0,0090 | 0,152±0,0070 |
| 2-я | 0,212±0,009 | 0,224±0,011 | 0,216±0,013 | 0,230±0,012 | 0,247±0,0080 | 0,224±0,010 | 0,210±0,015 | 0,148±0,0090 | 0,136±0,0080,1 |
| 3-я | 0,209±0,011 | 0,252±0,0090,2 | 0,223±0,015 | 0,228±0,013 | 0,255±0,0100 | 0,236±0,012 | 0,206±0,011 | 0,152±0,0070 | 0,129±0,06060,1 |
| Глюкоза, ммоль/л |
| 1-я | 10,06±0,33 | — | — | 8,90±0,200 | — | — | 7,98±0,210 | 6,81±0,170 | 4,85±0,150 |
| 2-я | 10,19±0,31 | 9,47±0,26 | 9,69±0,23 | 8,16±0,280 | 7,52±0,270 | 7,55±0,210 | 7,22±0,250,1 | 6,25±0,190,1 | 4,67±0,130 |
| 3-я | 10,36±0,26 | 9,05±0,190 | 8,91±0,210,2 | 7,97±0,250,1 | 7,02±0,180 | 7,11±0,150 | 7,01±0,220,1 | 5,96±0,120,1 | 5,03±0,160 |
| Глюкоза/лактат, ед. |
| 1-я | 1,67±0,14 | — | — | 2,00±0,18 | — | — | 2,29±0,130 | 2,34±0,120 | 2,39±0,140 |
| 2-я | 1,65±0,18 | 2,06±0,14 | 1,77±0,19 | 2,16±0,130 | 2,25±0,100 | 2,11±0,09 | 2,44±0,120 | 3,03±0,190,1 | 3,20±0,170,1 |
| 3-я | 1,74±0,19 | 2,25±0,150 | 2,23±0,170,2 | 2,25±0,200 | 2,37±0,160 | 2,30±0,140 | 2,59±0,100,1 | 3,54±0,170,1 | 3,48±0,110,1 |
| Лактат/пируват, ед. |
| 1-я | 28,32±0,88 | — | — | 23,28±1,280 | — | — | 20,72±0,680 | 17,2±1,010 | 13,89±0,890 |
| 2-я | 28,67±1,98 | 20,49±1,620 | 25,27±1,73 | 19,97±1,970 | 13,82±1,760 | 16,74±1,380 | 16,10±1,660 | 13,53±1,400,1 | 10,61±1,040,1 |
| 3-я | 27,97±1,42 | 16,08±1,360,2 | 18,42±1,500,2 | 15,94±1,670,1 | 11,96±1,420 | 13,16±1,120,2 | 13,11±1,260,1 | 10,52±1,060,1,2 | 10,65±1,170,1 |
| Азотистый баланс, г азота/сутки |
| 1-я | — | — | — | –16,99±0,83 | — | — | –12,27±0,510 | –3,51±0,240 | –0,48±0,110 |
| 2-я | — | — | — | –17,74±0,42 | — | — | –9,93±0,580,1 | –2,19±0,360,1 | 2,07±0,210,1 |
| 3-я | — | — | — | –18,94±0,651 | — | — | –9,04±0,700,1 | –1,94±0,340,1 | 3,85±0,270,1,2 |
0 — достоверность относительно исходного уровня (p<0,05); 1, 2 — достоверность относительно значений 1-й группы на одинаковых этапах исследования (p<0,05).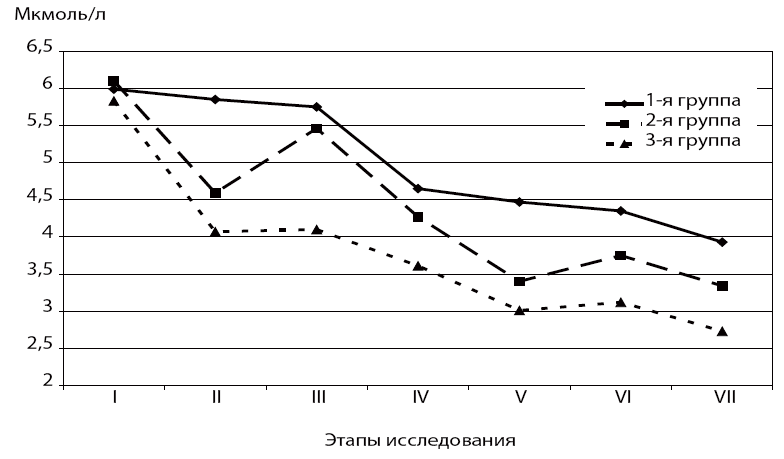
Рис. 1. Динамика лактата в раннем послеоперационном периоде
Этапы исследования: I — исходно; II — в конце инфузии реамберина; III — через 2 часа после инфузии реамберина; IV — 1-е сутки после операции (до введения реамберина); V — 1-е сутки после операции (в конце введения реамберина); VI — 1-е сутки после операции (через 2 часа после введения реамберина); VII — 2-е сутки после операции.
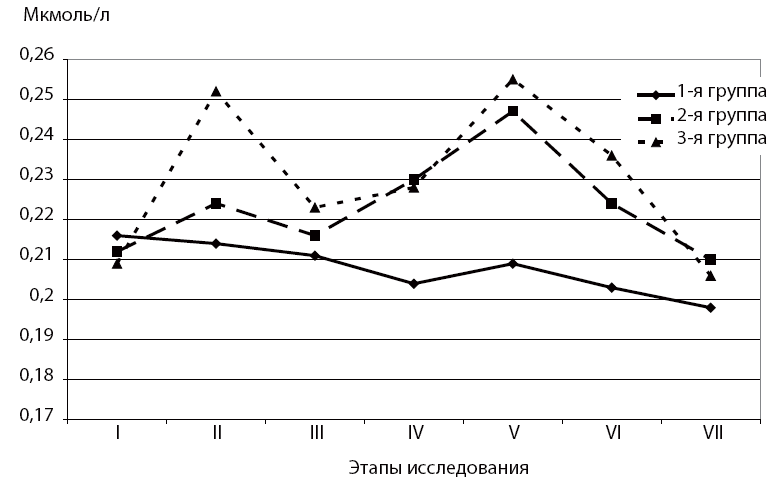
Рис. 2. Динамика пирувата в раннем вослеоперационном периоде
Этапы исследования: I — исходно; II — в конце инфузии реамберина; III — через 2 часа после инфузии реамберина; IV — 1-е сутки после операции (до введения реамберина); V — 1-е сутки после операции (в конце введения реамберина); VI — 1-е сутки после операции (через 2 часа после введения реамберина); VII — 2-е сутки после операции.
Введение реамберина в дозе 800 и 1600 мл позволяет снизить уровень гипергликемии, а также ее продолжительность без увеличения объемов инсулинотерапии и взаимосвязанного риска гипогликемических осложнений.
В первые сутки интенсивной терапии при введении 1600 мл реамберина отмечается снижение в среднем более чем на 2 ммоль/л гипергликемии, что позволяет рассматривать предлагаемый метод лечения в качестве эффективного патогенетического средства коррекции гипергликемических осложнений у больных в критических состояниях.
Значения индексов лактат/пируват и глюкоза/лактат, являющихся маркерами направленности метаболических процессов, подтверждают необходимость интенсификации антигипоксической направленности интенсивной терапии больных перитонитом в первые 48 часов после операции. Выявленные положительные корригирующие эффекты экзогенного введения сукцината позволяют рекомендовать включение реамберина в комплекс ранней послеоперационной терапии в дозе 800 мл/сутки. В случае гиперлактатемии выше 4 мкмоль/л, гиперпируватемии выше 200 мкмоль/л, отношения лактат/пируват более 20 у. е., гипергликемии более 10 ммоль/л требуется увеличение суточной дозы вводимого препарата до 1600 мл/сутки в первые 48 часов после операции. Критерием эффективности проводимой терапии является купирование лабораторных маркеров нарушений метаболизма.
Использование реамберина позволяет сократить проявления гипоксии до уровня, повышающего эффективность других методов лечения, так как гиперлактатемия выше 4 ммоль/л является относительным противопоказанием для начала проведения нутритивной поддержки. Купирование гиперлактатемии и тесно взаимосвязанного с ней метаболического ацидоза косвенно способствует повышению чувствительности клеток и рецепторов к проводимой этиотропной и патогенетической терапии перитонита и абдоминального сепсиса.
Известно, что в условиях гипоксии нарушается баланс свободнорадикального окисления и антирадикальной защиты. Снижение проявлений тканевой гипоксии и напряженности ее лабораторных проявлений, на наш взгляд, определяет и антиоксидантные свойства реамберина, предупреждающего разбалансировку системы ПОЛ/АОС и поддерживающего функционирование ее наиболее лабильной церулоплазминовой составляющей (табл. 2).
Таблица 2
Динамика показателей системы ПОЛ/АОС у больных 1-й, 2-й и 3-й групп (М±m)
| Группа больных | Этапы исследования |
|---|
| При поступлении | Через 6 часов | 1-е сутки | 2-е сутки | 5-е сутки | 8-е сутки |
|---|
| ДК, ед. оп. пл/ол |
| 1-я | 0,454±0,016 | 0,473±0,020 | 0,484±0,12 | 0,517±0,0140 | 0,526±0,0100 | 0,515±0,0090 |
| 2-я | 0,445±0,021 | 0,478±0,018 | 0,480±0,014 | 0,499±0,0150 | 0,491±0,0151 | 0,462±0,0131 |
| 3-я | 0,460±0,017 | 0,469±0,021 | 0,473±0,017 | 0,479±0,0121 | 0,462±0,0141 | 0,457±0,0101 |
| МДА, мкмоль/л |
| 1-я | 6,49±0,19 | 7,33±0,320 | 7,82±0,260 | 7,68±0,410 | 7,31±0,290 | 7,18±0,250 |
| 2-я | 6,58±0,24 | 7,24±0,230 | 7,60±0,320 | 7,04±0,48 | 6,42±0,321 | 6,40±0,29 |
| 3-я | 6,62±0,27 | 7,30±0,19 | 7,41±0,23 | 6,71±0,32 | 6,12±0,351 | 6,03±0,181 |
| Общая АОА, у. е. |
| 1-я | 0,090±0,003 | 0,091±0,002 | 0,092±0,001 | 0,087±0,002 | 0,086±0,002 | 0,085±0,002 |
| 2-я | 0,091±0,003 | 0,092±0,002 | 0,091±0,002 | 0,090±0,001 | 0,091±0,0011 | 0,092±0,0021 |
| 3-я | 0,089±0,002 | 0,089±0,003 | 0,090±0,003 | 0,092±0,002 | 0,093±0,0021 | 0,093±0,0011 |
| Церулоплазмин, мг/л |
| 1-я | 240,3±13,1 | 231,9±15,9 | 219,4±13,1 | 208,0±10,50 | 198,9±8,40 | 205,6±10,20 |
| 2-я | 245,8±14,5 | 230,6±9,1 | 217,3±13,4 | 221,5±8,6 | 227,1±9,11 | 251,4±8,71 |
| 3-я | 239,7±12,2 | 230,1±16,4 | 225,7±11,9 | 230,2±7,5 | 232,0±10,31 | 247,4±12,51 |
0 — достоверность относительно исходного уровня (p<0,05); 1, 2 — достоверность относительно значений 1-й группы на одинаковых этапах исследования (p<0,05).Экзогенно вводимый сукцинат позволяет дозозависимо блокировать переход первичных продуктов липопероксидации во вторичные (МДА). Энергостабилизирующее действие реамберина способствует сокращению сроков купирования «оксидантного стресса». Торможение процессов перекисного окисления липидов (ПОЛ) и стабилизация антиоксидантной защиты (АОЗ) на фоне традиционной (800 мл) и форсированной (1600 мл) терапии реамберином способствует поддержанию равновесия этой наиболее уязвимой при критических состояниях системы.
Следующим этапом исследования была оценка влияния реамберина на течение эндогенной интоксикации у больных перитонитом, осложненного СПОН. Установлено, что ведущим механизмом формирования и декомпенсации эндотоксикоза является накопление ВНиСММ плазмы и эритроцитов, особенно их крупномолекулярной, катаболической фракции, с нарушением почечной экскреции эндотоксинов (табл. 3). Применение реамберина не влияет на динамику параметров, характеризующих эндотоксикоз в первые 24 часа после начала интенсивной терапии. Однако, начиная со вторых суток применения обычных (800 мл/сутки) и повышенных (до 1600 мл/сутки) объемов инфузии реамберина, регистрируется дозозависимая коррекция эндо токсикоза. Следовательно, детоксицирующее действие реамберина во многом вторично и следует за коррекцией метаболических нарушений. Использование сукцинатсодержащего инфузионного препарата в повышенной суточной дозировке в первые 48 часов позволяет предупредить гиперкатаболические процессы, характеризующиеся накоплением ВНиСММ в спектре длин волн 238–258 нм. Применение реамберина, особенно в увеличенной до 1600 мл/сутки дозировке в первые 48 часов после операции, способствует сокращению сроков декомпенсации эндотоксикоза и его последующему ускоренному купированию.
Таким образом, коррекция эндотоксикоза экзогенно вводимым сукцинатом значительно расширяет арсенал патогенетически обоснованных методов посиндромной интенсивной терапии больных перитонитом, осложненного СПОН.
Таблица 3
Динамика показателей эндотоксикоза у больных 1-й, 2-й и 3-й групп (М±m)
| Группа больных | Этапы исследования |
|---|
| При поступлении | Через 6 часов | 1-е сутки | 2-е сутки | 5-е сутки | 8-е сутки |
|---|
| ВНиСММ венозной плазмы, у. е. |
| 1-я | 34,38±0,30 | 33,97±0,34 | 33,63±0,25 | 33,48±0,210 | 31,03±0,240 | 28,02±0,150 |
| 2-я | 34,49±0,25 | 33,99±0,22 | 33,44±0,210 | 32,84±0,240 | 30,07±0,180,1 | 26,48±0,190,1 |
| 3-я | 34,72±0,31 | 34,03±0,26 | 33,27±0,300 | 32,50±0,220,1 | 29,67±0,250,1 | 26.55±0,210,1 |
| ВНиСММ 238–258 нм венозной плазмы, у. е. |
| 1-я | 17,95±0,55 | 17,88±0,42 | 18,16±0,50 | 20,19±0,360 | 19,47±0,400 | 19,02±0,35 |
| 2-я | 17,86±0,42 | 17,96±0,35 | 17,99±0,42 | 19,46±0,460 | 18,69±0,36 | 18,37±0,41 |
| 3-я | 18,15±0,37 | 18,10±0,46 | 18,11±0,39 | 19,03±0,32 | 18,02±0,351 | 17,49±0,451 |
| ВНиСММ венозных эритроцитов, у. е. |
| 1-я | 34,57±0,25 | 34,49±0,27 | 34,36±0,29 | 34,25±0,26 | 33,48±0,210 | 32,29±0,180 |
| 2-я | 34,46±0,17 | 34,51±0,24 | 34,17±0,21 | 33,87±0,30 | 32,64±0,160,1 | 31,47±0,210,1 |
| 3-я | 34,43±0,30 | 34,40±0,22 | 33,85±0,25 | 33,41±0,210 | 32,18±0,260,1 | 31,24±0,250,1 |
| ВНиСММ мочи, у. е. |
| 1-я | 36,84±1,46 | 38,41±1,53 | 42,26±1,260 | 48,98±1,350 | 79,26±1,190 | 81,19±1,350 |
| 2-я | 37,73±1,51 | 38,94±1,64 | 42,84±1,380 | 58,71±1,270,1 | 86,39±1,740,1 | 83,57±1,490 |
| 3-я | 37,90±1,13 | 37,95±1,35 | 43,85±2,010 | 63,37±1,590,1 | 85,93±1,520,1 | 80,17±1,190,1 |
| ИСЭИ, у. е. |
| 1-я | 32,09±0,79 | 30,45±1,11 | 27,38±1,300 | 23,48±0,910 | 13,08±0,600 | 11,25±0,500 |
| 2-я | 31,58±1,11 | 30,08±0,98 | 26,08±1,030 | 20,95±0,890 | 11,32±0,510,1 | 9,84±0,340,1 |
| 3-я | 31,48±0,89 | 30,72±0,75 | 25,60±1,410 | 17,05±1,160,1,2 | 11,08±0,420,1 | 9,93±0,390,1 |
0 — достоверность относительно исходного уровня (p<0,05); 1, 2 — достоверность относительно значений 1-й группы на одинаковых этапах исследования (p<0,05).Купирование реамберином метаболических нарушений и эндотоксикоза обеспечивает уменьшение степени тяжести состояния пациентов и выраженности органных дисфункций, определяемых с помощью общепринятых шкал APACHE II и SOFA (табл. 4). Увеличение дозы вводимого реамберина до 1600 мл/сутки достоверно влияет на сроки купирования полиорганной недостаточности. Полученный положительный результат применения антигипоксанта достигается на фоне комплексной этиопатогенетической терапии.
Таблица 4
Динамика тяжести состояния больных 1-й, 2-й и 3-й групп, баллы (М±m)
| Группа больных | Этапы исследования |
|---|
| При поступлении | Через 6 часов | 1-е сутки | 2-е сутки | 5-е сутки | 8-е сутки |
|---|
| APACHE II, баллы |
| 1-я | 28,56±0,69 | 28,78±0,91 | 28,31±0,77 | 25,93±0,530 | 22,28±0,640 | 18,89±0,480 |
| 2-я | 28,99±0,81 | 28,53±0,99 | 27,65±0,49 | 23,88±0,770,1 | 20,09±0,440,1 | 15,93±0,550,1 |
| 3-я | 28,40±0,95 | 28,16±0,57 | 26,39±0,73 | 21,76±0,500,1,2 | 18,92±0,490,1 | 14,87±0,610,1 |
| SOFA, баллы |
| 1-я | 10,70±0,37 | 10,06±0,27 | 9,72±0,300 | 8,89±0,250 | 6,61±0,220 | 4,19±0,180 |
| 2-я | 10,60±0,39 | 10,01±0,36 | 9,41±0,280 | 8,27±0,320 | 5,72±0,200,1 | 2,78±0.210,1 |
| 3-я | 10,47±0,44 | 9,63±0,370 | 8,97±0,240 | 8,06±0,390 | 5,44±0,310,1 | 2,68±0,260,1 |
0 — достоверность относительно исходного уровня (p<0,05); 1, 2 — достоверность относительно значений 1-й группы на одинаковых этапах исследования (p<0,05).В ходе исследования эффективности реамберина у больных перитонитом, осложненного полиорганной недостаточностью, токсического действия препарата на систему кровообращения, дыхания, почечную и печеночную функцию не было. Аллергические реакции, связанные с инфузией препарата, не наблюдались.
Проведенный сравнительный анализ выявил эффективность инфузионного антигипоксанта реамберин у больных перитонитом, а также дозозависимость получаемых антигипоксических, детоксицирующих и корригирующих СПОН эффектов экзогенно вводимого сукцината. Учитывая, что конечная результативность интенсивной терапии во многом зависит от продолжительности полиорганной дисфункции, применение инфузионных антигипоксантов в патофизиологически обоснованных увеличенных дозировках целесообразно не только у больных абдоминальным сепсисом, но и в медицине критических состояний вообще.
Список литературы
- Алиев С. А., 1. Султанов Г. А., Эфендиев М. А. Некоторые аспекты патогенеза гипоксии и нефармакологические методы ее коррекции при гнойном перитоните // Вестник интенсивной терапии. 2003. № 2. С. 20–27.
- Альес В. Ф., Степанова Н. А., Гольдина О. А., Горбачевский Ю. В. Патофизиологические механизмы нарушений доставки, потребления и экстракции кислорода при критических состояниях. Методы их интенсивной терапии // Вестник интенсивной терапии. 1998. № 2. С. 8–12.
- Гельфанд Е. Б., Гологорский В. А., Гельфанд Б. Р. Клиническая характеристика абдоминального сепсиса у хирургических больных // Consilium medicum. Инфекция и антимикробная терапия. 2000. № 2 (4). С. 9–15.
- Гельфанд Б. Р., Сергеева Н. А., Макарова Л. Д., Чеснокова Т. Т., Багдатьев В. Е. Метаболические нарушения при инфекционнотоксическом шоке у больных перитонитом // Хирургия. 1988. № 2. С. 84–88.
- Гирш А. О., Долгих В. Т., Мороз В. В. и др. Комбинированная детоксикация у больных разлитым гнойным перитонитом, протекающим на фоне сахарного диабета // Эфферентная терапия. 2004. Т. 10, № 1. С. 13–16.
- Медицинские лабораторные технологии. Справочник / Под ред. проф. А. И. Карпищенко. Санкт-Петербург: Интермедика, 2002. 600 с.
- Меньшиков В. В. Лабораторные методы исследования в клинике. М.: Медицина, 1987. 365 с.
- Оболенский С. В., Малахова М. Я., Ершов А. Л. Диагностика стадий эндогенной интоксикации и дифференцированное применение методов эфферентной терапии // Вестн. хир. 1991. № 3. С. 95–100.
- Шукевич Л. Е., Шукевич Д. Л., Григорьев Е. В. Новый подход к диагностике синдрома эндогенной интоксикации при абдоминальном сепсисе // Материалы 4-й международной конференции «Актуальные аспекты экстракорпорального очищения крови в интенсивной терапии» Москва. 2004. С. 94–95.
- Alberti K. G. M. M. Biochemical consequenses of hipoxia // J. Clin. Path. 1977. Vol. 3. Suppl. 11. P. 14.
- Bone R. Reevaluation of the role of cellular hypoxia and bioenergetic failure in sepsis // JAMA-1992. Vol. 18. P. 1503–1510.
- Dong Y. L., Sheng C. Y. Metabolic abnormalities of mitochondrial redox potential in postburn multiple system organ failure // Burns. 1992. Vol. 18, № 4. P. 283–286.
- Kinney J. M. Metabolic response of the critically ill patient // Crit. Care Clinics. 1995. Vol. 11, № 3. P. 569–585.
- Prondzinsky R., Witthaut R., Stache N. et al. The heart in infection and MODS (multiple organ dysfunction syndrome) // Wien. Klin. Wschr. (Suppl.). 1997. № 1. P. 3–24.
- Small N., Messiah A., Edouards A. Role of systemic inflammatory responsesyndrome and infection in the occurrence of early multiple organ dysfunction syndrome following severe trauma // Intens. Care Med. 1995. Vol. 21, № 10. P. 813–817.
Список сокращений
| АОА | — | антиоксидантная активность |
| АОС | — | антиоксидантная система |
| АТФ | — | аденозинтрифосфат |
| ВНиСММ | — | вещества низкой и средней молекулярной массы |
| ВЭБ | — | водно-электролитный баланс |
| ДК | — | диеновые конъюгаты |
| ИСЭИ | — | индекс синдрома эндогенной интоксикации |
| МДА | — | малоновый диальдегид |
| ПОЛ | — | перекисное окисление липидов |
| СПОН | — | синдром полиорганной недостаточности |
| ЦТК | — | цикл трикарбоновых кислот |
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)