Особенности предоперационной подготовки пациентов с ожогами и хроническими язвами различной этиологии к аутодермопластике
Статьи
*М. В. Варганов, А. А. Микличев, К. Д. Богданов
ФГБОУ ВО «Ижевская государственная медицинская академия Минздрава России», Ижевск
Features of Preoperative Preparation of Patients with Burns and Chronic Ulcers of Various Etiology for Autodermoplasty
*M. V. Varganov, A. A. Miklichev, K. D. Bogdanov
Izhevsk State Medical Academy of the Ministry of Health of the Russian Federation, Izhevsk
Проанализировно влияние различных схем предоперационной подготовки к аутодермопластике на показатели приживаемости кожного лоскута и длительность госпитализации у пациентов с ожогами и ранами различной этиологии. В зависимости от схемы подготовки пациенты были разделены на группы и подгруппы: I группа (22 пациента) получала в предоперационном периоде NPWT-терапию в течение 5 дней в комплексном лечении с препаратом Реамберин — внутривенно капельно со скоростью 40—60 кап./мин, 500 мл, 1 раз в день в течении 5 суток. В свою очередь пациенты были разделены на подгруппы: 1А подгруппа (17 человек) получала комплексное лечение без антибиотикотерапии, 1В подгруппа (5 человек) получали антибиотикотерапию. Во II группу вошли 30 пациентов, получающих в подготовительный период вакуум-терапию. Пациенты также были разделены по подгруппам: 2А (16 человека) получали NPWT-терапию без антибиотиков, 2В (14 человек) — вакуум-терапию совместно с антибиотикотерапией. В III группу (сравнения, n=52) были включены пациенты, которым подготовку проводили традиционными способами с применением антибактериальной терапии и местного использования различных вариантов повязок и мазей. В динамике проведено морфогистологическое исследование биоптатов ран с определением площади фибробластов, площади ядра фибробластов и количества сосудов. После проведения аутодермопластики определялась приживаемость кожного лоскута с учётом сроков госпитализации. При сравнении схем предоперационной подготовки пациентов с ожогами и хроническими язвами различной этиологии площадью 1—5% к аутодермопластике наиболее эффективной показала себя схема, включающая NPWT-терапию и Реамберин курсом 5 дней: на её фоне отмечено улучшения фибробластогенеза и кровоснабжения раны что сопровождалось улучшением приживаемости кожного лоскута до 90,0±9,9%, что сократило сроки госпитализации пациентов — средняя продолжительность предоперационного периода оказалась меньше в 2,5 раза, постоперационного — в 1,9 раза, чем у пациентов группы сравнения (р<0,05). Полученные результаты позволяют рекомендовать применение данной схемы в предоперационной подготовке к аутодермопластике пациентов с ожогами и хроническими язвами различной этиологии площадью 1—5%.
Ключевые слова: предоперационная подготовка, NPWT-mepanuu, фибробластогенез, койко/дни, Реамберин.
The influence of various schemes of preoperative preparation for autodermoplasty on the rates of skin graft survival and the duration of hospitalization in patients with burns and wounds of various etiologies was analyzed. Patients were divided into groups and subgroups depending on the preparation scheme. Group I (22 patients) received negative pressure wound therapy (NPWT) during the preoperative period for 5 days in combination with reamberin — intravenous drip at a rate of 40-60 drops/min, 500 ml, once a day for 5 days. Those patients were divided into subgroups: subgroup 1A (17 people) received complex treatment without antibiotic therapy, subgroup 1B (5 people) received antibiotic therapy. Group II consisted of 30 patients, who received vacuum therapy during the preparatory period. Group II patients were also divided into subgroups: 2A (16 people) received NPWT without antibiotics, 2B (14 people) — vacuum therapy together with antibiotic therapy. Group III (comparison, n=52) included patients who were treated using traditional methods, including antibiotic therapy and topical use of various dressings and ointments. Follow-up morphohistological study of wound biopsies was carried out in order to determine the area of fibroblasts, the area of fibroblast nucleus, and the number of vessels. After skin autografting, skin flap survival rate was determined, taking the time of hospitalization into account. Upon comparison of preoperative preparation schemes used for patients with burns and chronic ulcers of various etiologies with a surface area of 1—5% appropriate for skin autografting, the scheme that included NPWT and reamberin for 5 days proved to be the most effective: an improvement in fibroblastogenesis and blood flow to the wound was noted in this group of patients, which was accompanied by an improvement in the skin flap survival rate up to 90.0±9.9%, which, in turn, reduced the duration of patient’s hospital stay — the average duration of the preoperative period was 2.5 times shorter, postoperative — 1.9 times shorter than in the comparison group (p<0.05). The results obtained make it possible to recommend the use of this scheme in the preoperative preparation for skin autografting for patients with burns and chronic ulcers of various etiologies with the surface area of 1—5%.
Keywords: preoperative preparation, NPWT, fibroblastogenesis, bed-days, reamberin.
Введение
В настоящее время одной из главных задач как в хирургии, так и в комбустиологии является подготовка раны к аутодермопластике. Использование стандартных методов подготовки с применением различных вариантов повязок и мазей в комбинации с антибактериальной терапией приносит недостаточную эффективность.
С одной стороны, длительное применение антибиотиков может привести к нарушению перфузионных свойств ткани, что в свою очередь влечёт за собой лизис и отторжение кожного лоскута. Так же применение антибиотикотерапии способствует появлению антибиотикорезистентных штаммов и, как следствие, снижение иммунитета. С другой стороны, традиционные методы лечения помимо практической неэффективности влекут за собой и экономическую как для всего здравоохранения, так и для отдельной больницы [1]. Длительная подготовка раны к аутодермопластике, продолжительный послеоперационный период и неудачные пересадки кожного лоскута вследствие неэффективной подготовки раны — экономические недостатки метода, которые увеличивают сроки госпитализации и, как следствие, расходы бюджета стационара, в связи с чем актуальным является поиск более эффективных схем лечения.
Одним из них является метод лечения ран отрицательным давлением (Negative Pressure Wound Тrеаtmеnt — NPWT). Его принцип действия основывается на поддержании контролируемого отрицательного давления в области раны, что способствует созданию условий для очищения раневого ложа и созревания грануляционной ткани. Показано, что влияние вакуума снижает парциальное давление в раневой поверхности и стимулирует образование новых сосудов, что проявляется увеличением объёма грануляционной ткани [2]. Включение в схемы предоперационной подготовки раны к аутодермопластике NPWT способствует подготовке раневого ложа, что проявляется «сочными» грануляциями, снижением объёмов отделяемого и уменьшением перифокального воспаления и отёка, при этом возможно ухудшение кровотока в тканях с и так обеднённым кровоснабжением, которое может приводить к развитию ишемии [3—6]. Решить проблему может включение в лечение Реамберина (ООО «НТФФ «ПОЛИСАН», г. Санкт-Петербург) — препарата с антигипоксическим и антиоксидантным действием, оказывающего положительный эффект на аэробные процессы в клетке, уменьшающего продукцию свободных радикалов и способствующего восстановлению энергетического потенциала клеток. Реамберин способствует активизации ферментативных процессов цикла Кребса и утилизации жирных кислот и глюкозы клетками, тем самым нормализует кислотно-щелочной баланс и газовый состав крови [7].
Цель работы — анализ влияния различных схем предоперационной терапии на показатели приживаемости кожного лоскута и длительность госпитализации.
Материал и методы
Проведён анализ 104 историй болезни пациентов (50 мужчин и 54 женщины) с ожогами и хроническими язвами различной этиологии площадью 1—5%, находившихся на стационарном лечении в комбустиологическом отделении БУЗ УР «1 РКБ МЗ УР» в период с 2014 по 2019 гг.
У большинства 70 (67,4%) пациентов были гранулированные раны, у 25 (24%) — трофические язвы и у 9 (8,6%) пациентов — гнойно-некротические раны. Всем больным после предоперационной подготовки было проведено оперативное лечение ран.
В зависимости от схемы терапии сопровождения в предоперационный период пациенты были поделены на 3 группы. Первая группа (22 пациента), получала в предоперационном периоде NPWT-терапию в течение 5 дней в комплексном лечении с препаратом Реамберин (ООО «НТФФ «ПОЛИСАН», г. Санкт-Петербург). Препарат вводился внутривенно капельно со скоростью 40-60 кап./мин, 500 мл, 1 раз в день в течение 5 суток. В свою очередь пациенты были разделены на подгруппы: 1А подгруппа (17 человек) получала комплексное лечение без антибиотикотерапии, 1В подгруппа (5 человек) получали антибиотикотерапию (табл. 1).
Таблица 1.
Спектр антибиотиков, использованных в терапии пациентов в предоперационный период (абс, %)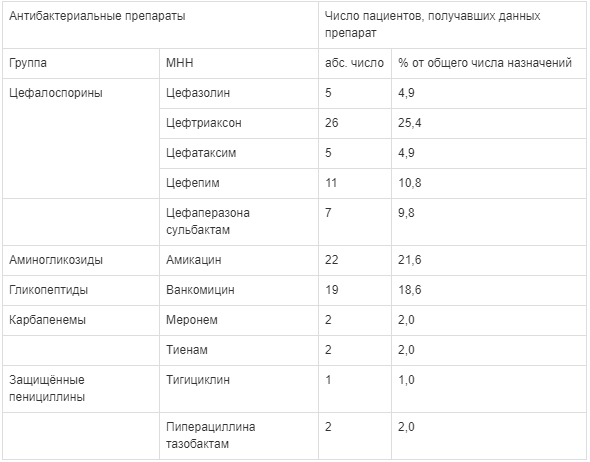 Во вторую группу вошли 30 пациентов, получающих в подготовительный период NPWT-терапию. Пациенты так же были разделены по подгруппам: 2А (16 человека) получали вакуум-терапию без антибиотикотерапии, 2В (14 человек) — вакуум-терапию совместно с антибиотикотерапией. В группу сравнения вошли 52 пациента, которым подготовку проводили традиционными способами с применением антибактериальной терапии и местного использования различных вариантов повязок и мазей.
Во вторую группу вошли 30 пациентов, получающих в подготовительный период NPWT-терапию. Пациенты так же были разделены по подгруппам: 2А (16 человека) получали вакуум-терапию без антибиотикотерапии, 2В (14 человек) — вакуум-терапию совместно с антибиотикотерапией. В группу сравнения вошли 52 пациента, которым подготовку проводили традиционными способами с применением антибактериальной терапии и местного использования различных вариантов повязок и мазей.
Группы были однородными по полу и возрасту (табл. 2).
Таблица 2.
Поло-возрастное распределение пациентов в зависимости от схем терапии (абс., %)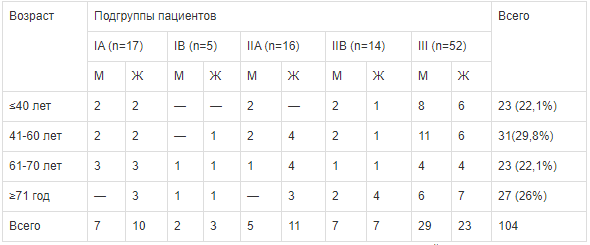 Дизайн исследования был согласован на совещании Кафедры факультетской хирургии ФГБОУ ВО «ИГМА» М3 РФ (Протокол № 7 от 25 декабря 2017 г.). От всех пациентов, включённых в исследование, было получено информированное согласие.
Дизайн исследования был согласован на совещании Кафедры факультетской хирургии ФГБОУ ВО «ИГМА» М3 РФ (Протокол № 7 от 25 декабря 2017 г.). От всех пациентов, включённых в исследование, было получено информированное согласие.
У пациентов групп I и II до наложения аппарата NPWT-терапии и после его снятия перед операцией в операционной в процессе некроэктомий раневой поверхности были взяты биоптаты: по два образца размером 1x1 мм с края раны с захватом краевого эпидермиса и из центра раны.
Полученный материал был отправлен в БУ3 УР Республиканское патологоанатомическое бюро М3 УР (426039 г. Ижевск, Воткинское шоссе, 85), где проведена его обработка и подготовка к исследованию: фиксация в 10% растворе формалина с последующей проводкой через спирты восходящей концентрации (30—96%) и заливкой в парафин. Гистологические срезы окрашивали гематоксилином и эозином, исследовали методами световой микроскопии (на микроскопе Биолам Р11 (Россия)) при увеличении Х400 в десяти полях зрения для каждого препарата. Снимки были получены с помощью цифровой камеры микроскопа РСЕ-МЕ 100 Micro-ocular на увеличении 50 мкм в формате *.jpg.
Морфометрию проводили с помощью программы ImageJ, основанной на Java. Проводился подсчёт: площади фибробластов, площади ядра фибробластов, количества сосудов, диаметра сосудов.
После аутодермопластики проводилась оценка приживаемости кожного лоскута. Оценку эффективности лечения выполняли ежедневно. Определяли площадь раны и вычисляли индекс заживления по следующей формуле: где: S — площадь ожога при предыдущем измерении, мм2; Sn — площадь ожога при данном измерении, мм2; Т — интервал между измерениями, сут, выражался в % [8].
где: S — площадь ожога при предыдущем измерении, мм2; Sn — площадь ожога при данном измерении, мм2; Т — интервал между измерениями, сут, выражался в % [8].
Статистическую обработку данных проводили с помощью программы SPSS 23.0. Для оценки нормальности распределения использовали критерий Колмогорова—Смирнова. В случае, если распределение признака не отличалось от нормального, для описания использовали среднее и стандартную ошибку средней (M±m), сравнение проводили с помощью параметрических методов статистики. В случае отличия распределения от нормального использовали непараметрические критерий Н Круаскала Уолеса для независимых выборок и Уилкоксона для зависимых выборок. Равенство дисперсий оценивалось по критерию Ливиня. Для выявления статистически значимых различий между группами использовали однофакторный, многофакторный и многомерный дисперсионный анализы с апостериорной оценкой значимых различий между группами попарно с использованием критерия Шеффе и Бонферони при равенстве дисперсий и Геймс-Хоуэлл и Тамхейна Т2 при предположении о неравенстве дисперсий, также использовался критерий Стьюдента (t). Корреляционные связи между показателями выявляли с использованием критерия Пирсона. Различия считали статистически значимыми при P<0,05.
Результаты и обсуждение
Анализ результатов приживаемости кожного лоскута у пациентов после аутодермопластики выявил различия в зависимости от схемы предоперационной подготовки (табл. 3).
Таблица 3.
Показатели приживаемости кожного лоскута у пациентов в зависимости от схемы предоперационной подготовки (M±m)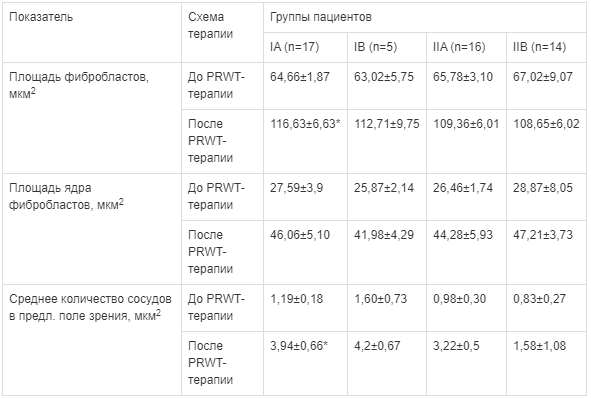 Примечание. * - сравнение показателя в динамике, достоверность р≤0,05.
Примечание. * - сравнение показателя в динамике, достоверность р≤0,05.
Выявлено, что включение в схемы предоперационной подготовки пациентов сочетания NPWT-терапии и Реамберина оказывает положительное влияние на фибробластогенез, что выражается в увеличение площади фибробластов в 1,8 раза (с 64,66±1,87 до 116,63±6,63 мкм2).
При этом среднее количество сосудов увеличилось в 3,3 раза: с 1,19±0,18 до 3,94±0,66 мкм2 против 0,98±0,30 и 3,22±0,5 мкм2 — в группе сравнения, p≤0,05. Наряду с этим отмечено, что при включении в схему предоперационной подготовки антибиотиков (группы IB и IIB) кровоснабжение раневой поверхности восстанавливалось медленнее: с 1,60±0,73 до 4,2±0,67 мкм2 и с 0,83±0,27 до 1,58±1,08 мкм2, соответственно (p>0,05).
Кроме того, выявлено более выраженное положительное влияние схем предоперационной терапии без включения антибиотиков на динамику увеличения среднего количества сосудов: у пациентов из IA и IIA групп в 3,3 раза (с 1,19±0,18 до 3,94±0,66 мкм2 и с 0,98±0,30 до 3,22±0,5 мкм2, соответственно), в то время как у пациентов, получивших в схеме антибиотики на фоне NPWT-терапии и Реамберина — в 2,6 раза (с 1,60±0,73 до 4,2±0,67 мкм2), антибиотики и NPWT-терапию — в 1,9 раза (с 0,83±0,27 до 1,58±1,08 мкм2). Выявленные особенности зависимости ангиогенеза от включения в терапию антибиотиков требуют дальнейшего изучения.
Улучшение фибробластогенеза и кровоснабжения раны на фоне NPWT-терапии и Реамберина, способствует повышению приживаемости кожного лоскута — 90,0±9,9% и более эффективно, чем при присоединении антибактериальной терапии — 78,75±4,38% и при моно NPWT-терапии — 88,82±10,7%, соответственно, p>0,05 (табл. 4).
Таблица 4.
Приживаемость кожного лоскута у пациентов в зависимости от схемы предоперационной подготовки (M±m, %)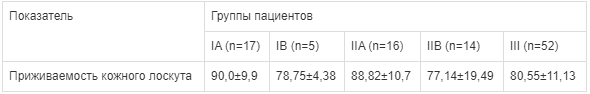 Анализ эффективности предоперационной подготовки с точки зрения сроков госпитализации показал, что наиболее эффективной (и короткой по срокам) была схема, включающая NPWT-терапию и Реамберин (группа IA), составившая в среднем 7,94±3,33 койко/дней, что было в 2,5 раза быстрее, чем у пациентов, получивших традиционную подготовку к операции — 19,81±9,44 койко/дней, соответственно, p<0,05 (табл. 5).
Анализ эффективности предоперационной подготовки с точки зрения сроков госпитализации показал, что наиболее эффективной (и короткой по срокам) была схема, включающая NPWT-терапию и Реамберин (группа IA), составившая в среднем 7,94±3,33 койко/дней, что было в 2,5 раза быстрее, чем у пациентов, получивших традиционную подготовку к операции — 19,81±9,44 койко/дней, соответственно, p<0,05 (табл. 5).
Таблица 5.
Длительность госпитализации в зависимости от схемы предоперационной терапии (M±m, койко/дни)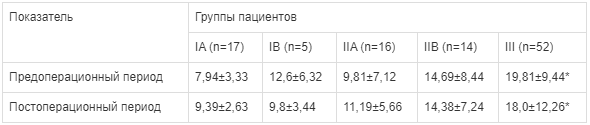 Примечание. * - р<0,05, при сравнении между IA III.
Примечание. * - р<0,05, при сравнении между IA III.
Таким образом, при сравнении нескольких схем предоперационной подготовки пациентов к аутодермопластике наиболее эффективной показала себя схема, включающая NPWT-терапию и Реамберин курсом 5 дней: на фоне улучшения фибробластогенеза и кровоснабжения раны приживаемость кожного лоскута составила 90,0±9,9% и как следствие, средняя продолжительность предоперационного периода оказалась меньше в 2,5 раза, постоперационного — в 1,9 раза, чем у пациентов группы сравнения (р<0,05).
Процесс заживления ран включает в себя непрерывные межклеточные и клеточно-матрикс-ные взаимодействия и состоит из взаимно перекрывающихся фаз: воспаление, сокращение раны, реэпителизация и ремоделирование. При нарушениях последовательности механизмов возможна хронизация процесса и формирование язв и рубцов.
За счёт повышения клеточной пролиферации, усиления синтеза коллагена и протеинов, активации местного кровотока и снижения выраженности раневой экссудации NPWT-терапия оказывает положительное влияние на все стадии процесса [2]. Основные клетки дермы фибробласты определяют морфофункциональное состояние кожи при восстановительных процессах в зоне раневого дефекта. Они участвуют в реорганизации и уплотнении межклеточного матрикса, продуцируют белки внеклеточного матрикса (коллагены I — V типов, проэластин, фибронектин и др.), различные факторы роста (фактор роста фибробластов (FGF), эпидермальный фактор роста (EGF), фактор роста кератиноцитов (KGF), факторы роста эндотелия сосудов (VEGF-A, B, C, D) и др.), ферменты (матриксные металлопротеиназы (ММП-1, 2, 3, 9) и др.), а также ряд цитокинов [3]. Полученные в исследовании данные о достоверном увеличении площади фибробластов коррелируют с приживаемостью кожного лоскута.
Общеизвестно, что янтарная кислота оказывает опосредованное положительное влияние на уровень микрокровотока, что связано со снижением выраженности внутриклеточного ацидоза за счёт ускорения оборота дикарбоновой части цикла Кребса в эндотелиоцитах и снижения уровня пирувата и лактата [9, 10]. Увеличение количества АТФ и активация окислительного фосфорилирования приводит к нормализации функционального состояния эндотелиального русла (купированию внутриклеточной гипоксии). Установлено, что под действием Реамберина, в состав которого входит янтарная кислота, снижается интенсивность процессов перекисного окисления липидов, повышаются антиоксидантные и антигипоксантные возможности организма, в том числе за счёт индукции HIF-1a (гипоксией индуцированного фактора 1а), который в свою очередь ответственен за формирование основы долговременной адаптации тканей к гипоксии [11, 12]. Эти данные косвенно подтверждены результатами настоящего исследования — у пациентов, получивших Реамберин, отмечено выраженное увеличение количества сосудов, что также положительно повлияло на приживаемость кожного лоскута.
Таким образом, схема, включающая NPWT-терапию и Реамберин курсом 5 дней, обусловила улучшение фибробластогенеза и кровоснабжения раны и, следовательно, ускорение приживаемости кожного лоскута до 90,0±9,9%. Как следствие, средняя продолжительность предоперационного периода у пациентов этой группы оказалась меньше в 2,5 раза, постоперационного — в 1,9 раза, чем у больных группы сравнения (р<0,05).
Выводы
При сравнении схем предоперационной подготовки пациентов с ожогами и хроническими язвами различной этиологии площадью 1—5% к аутодермопластике наиболее эффективной показала себя схема, включающая NPWT-терапию и Реамберин курсом 5 дней: на её фоне отмечено улучшения фибробластогенеза и кровоснабжения раны что сопровождалось улучшением приживаемости кожного лоскута до 90,0±9,9%
Применение схемы, включающей NPWT-терапию и Реамберин курсом 5 дней, сократило сроки госпитализации пациентов: средняя продолжительность предоперационного периода оказалась меньше в 2,5 раза, постоперационного — в 1,9 раза, чем у пациентов группы сравнения (р<0,05).
Полученные результаты позволяют рекомендовать применение данной схемы в предоперационной подготовке к аутодермопластике пациентов с ожогами и хроническими язвами различной этиологии площадью 1—5%.
Сведения об авторах:
Варганов Михаил Владимирович — д. м. н., профессор кафедры факультетской хирургии ФГБОУ ВО «ИГМА» М3 РФ.
Микличев Алексей Александрович — ФГБОУ ВО «ИГМА» М3 РФ, Санкт-Петербург.
Богданов Кирилл Дмитриевич — ФГБОУ ВО «ИГМА» М3 РФ, Санкт-Петербург.
ЛИТЕРАТУРА
1. Бесчастнов В.В., Павленко И.В., Багрянцев М.В., Кичин В.В., Перетягин П.В, Орищенко А.В., Рябков М.Г. Современные подходы к техническим аспектам свободной аутодермопластики. Вестник экспериментальной и клинической хирургии. — 2018. — Т. XI. — № 1. — С. 59—69. / Beschastnov V.V., Pavlenko I.V., Bagryancev M.V., Kichin V.V., Peretyagin P.V., Orishhenko A.V., Ryabkov M.G. Modern approaches to the technical aspects of free autodermoplasty. Vestnik Ehksperimental'noj i Klinicheskoj Khirurgii 2018; XI (1): 59—69. [in Russian]
2. Бесчастнов В.В., Измайлов С.Г., Багрянцев М.В., Орлинская Н.Ю., Лукоянычев Е.Е., Миронов А.А. Активность процессов репаративной регенерации в условиях локальной циркуляторной гипоксии околораневой области. Новости хирургии. — 2015. — Т. 23. — № 6. — С. 612—618. / Beschastnov V.V., Izmajlov S.G., Bagryantsev M.V., Orlinskaya N.YU., Lukoyanychev E.E., Mironov A.A. The activity of the processes of reparative regeneration in the conditions of local circulatory hypoxia of the near-cranial region. Novosti Khirurgii 2015; 23 (6): 612—618.
3. Оболенский В. H., Ермолов А.А., Аронов Л.С., Родоман Г.В., Серов Р.А. Применение метода локального отрицательного давления в комплексном лечении острых гнойно-воспалительных заболеваний мягких тканей. Хирургия. Журнал им. Н. И. Пирогова. — 2012. — № 1. — С. 50—55. / Obolenskij V. N., Ermolov A.A., Aronov L.S., Rodoman G.V., Serov R.A. Application of the method of local negative pressure in the complex treatment of acute purulent-inflammatory diseases of soft tissues. Hirurgija. Zhurnal im. N.I. Pirogova 2012; 1: 50—55. [in Russian]
4. Morykwas M.J., Argenta L.C., Shelton-Brown E.I., VcGuirt W. Vaccuum-assisted cljsure: a new method for wound control end treatment animal studies an basic foundation. Ann Plast Surg 1997; 38 (6): 553—562.
5. Часнойть А.Ч., Жилинский Е.В., Серебряков А.Е., Лещенко В.Т. Механизмы действия вакуумной терапии ран. Международные обзоры: клиническая практика и здоровье. — 2015. — № 4. — С. 25—35. / Chasnojt' A.Ch., Zhilinskij E.V., Serebrjakov A.E., Leshhenko V.T. Mechanisms of action of vacuum therapy of wounds. Mezhdunarodnye Obzory: Klinicheskaja Praktika i Zdorov'e 2015; 4: 25—35. [in Russian]
6. Часнойть А.Ч., Подгайский В.Н., Кошельков Я.Я. Мазолевский Д.М., Жилинский Е.В. Вакуумная терапия ран с использованием генератора «WaterLily»: учеб.-метод.пособие. Минск: БелМАПО, 2014. — 59 с. / Chasnojt' A. Ch., Podgajskij V.N., Koshelkov Ja.Ja. Mazolevskij D.M., Zhilinskij E.V. Vacuum therapy of wounds using the generator «WaterLily»: studies.-method. allowance Minsk: BelMAPO, 2014; 59. [in Russian]
7. Sano H., Ichioka S., Sekiya N. Influence of oxygen on wound healing dynamics: assessment in a novel wound mouse model under a variable oxygen environment PloS One 2012; 7 (11): 502—512.
8. Реамберин: клинические и экспериментальные исследования. Реферативный сборник научных работ, процитированных в PubMed. Под.ред. Белова В.Г., СПб.: 2013. — 288 с. / Reamberin: clinical and experimental studies. Abstract collection of scientific papers cited in PubMed. Pod. red. Belova V.G., SPb.: 2013; 288. [in Russian]
9. Песчанский В.С., Шнейдер А.Б., Бондаренко В.Д. Математическое моделирование скорости заживления кожных ран в эксперименте. Механические повреждения мягких тканей. Под ред. С.Д. Попова. Вып. 76. Горький: 1976. — С.100—103. / Peschanskij V.S., SHnejder А.В., Bondarenko V.D. Mathematical modeling of the healing speed of skin wounds in the experiment. Mechanical damage to soft tissues. Pod red. S.D. Popova. Vyp. 76. Gor'kij: 1976; 100—103. [in Russian]
10. Mills E., O'Neill LA. Succinate: a metabolic signal in inflammation Trends Cell Biol. 2014 May; 24 (5): 313-320.
11. Левченкова О.С., Новиков В.Е. Индукторы регуляторного фактора адаптации к гипоксии. Российский медико-биологический вестник имени академика И.П. Павлова. — 2014. — № 2. — С. 135-145. / Levchenkova O.S., Novikov V.E. Inductors of the regulatory factor for adaptation to hypoxia. Rossijskij Mediko-Biologicheskij Vestnik Imeni Akademika I.P. Pavlova 2014; 2: 135-145. [in Russian]
12. Новиков В. Е., Левченкова О. С. Гипоксией индуцированный фактор (HIF-1a) как мишень фармакологического воздействия. Обзоры по клинической фармакологии и лекарственной терапии. — 2013. — Т. 11 (2). — С. 8-16. / Novikov V. E., Levchenkova O. S. Hypoxia induced factor (HIF -1a) as a target of pharmacological effects. Obzory po Klinicheskoj Farmakologii i Lekarstvennoj Terapii 2013; 11 (2): 8-16. [in Russian].
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)