Возможности коррекции метаболических нарушений с использованием реамберина в остром периоде травмы
Статьи
Герасимов Л.В.1, Марченков Ю.В.2, Волков Д.П.1, Родионов Е.П.1, Измайлов В.В.2
1ГКБ им. С.П. Боткина, 2Москва ФГБУ «НИИ общей реаниматологии им. В.А. Неговского», Москва
Обследовано 56 больных в возрасте 18-60 лет, поступивших в реанимационное отделение № 18 ГКБ им. С.П. Боткина с диагнозом «тяжелая сочетанная травма». Проведена сравнительная оценка влияния полиэлектролитного раствора «Реамберин» на кислотно-основное состояние, осмоляльность и электролитный состав плазмы у больных в остром посттравматическом периоде. Установлено, что на фоне традиционной инфузионной терапии у больных отмечались метаболический ацидоз и гиперхлоремия. В группе, получавшей реамберин, уже на 2-е сутки происходила нормализация кислотно-основного состояния у 82% больных, а также отмечались более низкие показатели концентрации хлоридов. Применение реамберина существенно не влияло на осмоляльность плазмы и частоту развития алкалоза в остром периоде травмы.
Ключевые слова: тяжелая сочетанная травма; метаболический ацидоз; инфузионная терапия; реамберин.
Possibility of correction of metabolic disorders with reamberin in acute period of traumatic injury
Gerasimov LV1 Marchenkov YuV2 Volkov DP.1 Rodionov EP1 Izmailov VV2
1City clinical hospital named after S.P. Botkin, Moscow, Russia;
2V.A.Negovsky Scientific Research Institute of General Reanimatology, Moscow, Russia
56 patients at the age of 18-60 years with severe trauma were examined. Influence of the polyelectrolytic «Reamberin» solution on an acid-base state, osmolarity and electrolytic composition of plasma in the acute posttraumatic period was evaluated. It was found that patients, who was treated by isotonic sodium chloride solution and Ringer’s solution, had metabolic acidosis and hyperchloremia. In contrast, in the reamberin group 82% of patients had lower concentrations of chloride and had nothing acid-base disturbances on the second day after trauma. Reamberin didn't influence on plasma osmolarity and the rate of metabolic alkalosis during the acute period of a trauma.
Key words: severe trauma; metabolic acidosis; fluid therapy; reamberin.
Восстановление и поддержание баланса жидкости и электролитов, нормальной осмолярности плазмы и кислотно-основного равновесия являются одной из главных задач инфузионной терапии в остром периоде травмы наряду с восстановлением внутрисосудистого объема.
При этом в первые сутки после травмы мы, как правило, сталкиваемся с лактат-ацидозом, который усугубляется ятрогенными метаболическими нарушениями, связанными с проведением агрессивной инфузионной терапии, - дилюционным и гиперхлоремическим ацидозом (ГХМА).
Хотя есть множество исследований, в которых продемонстрирована прямая связь между степенью ацидоза и летальностью у больных в критическом состоянии [1-4], очевидно, что причиной неблагоприятного исхода является не столько сам ацидоз, сколько лежащая в его основе проблема.
Однако бесспорным фактом является и то, что метаболический ацидоз независимо от происхождения вызывает целый ряд серьезных негативных последствий, таких как угнетение сократимости миокарда, снижение сердечного выброса, ограничение перфузии тканей, макро- и микрореологические расстройства. [5, 6]. Доказано, что ацидоз способствует усилению воспалительного ответа [7] и повышает риск развития осложнений, например острого повреждения легких [8]. Установлено, что гиперхлоремия, лежащая в основе ГХМА, снижает почечный и висцеральный кровоток [9, 10] и приводит к развитию почечной недостаточности у части больных [11].
Это убеждает нас в необходимости определения качественного состава инфузионных сред, применяемых в остром периоде тяжелой травмы, в том числе исходя из данных об их влиянии на метаболический профиль больного.
В экспериментах in vitra и in vivo показано, что кристаллоидный раствор, оптимальный с точки зрения влияния на кислотно-основное состояние (КОС), должен иметь разницу сильных ионов (strong ions difference) не менее 24 мэкв/л [12, 13]. Только в этом случае можно избежать развития дилюционного и гиперхлоремического ацидоза. Если мы имеем дело с уже развившимся ацидозом, то для его коррекции требуется раствор с разницей сильных ионов (РСИ) более 24 мэкв/л [14, 15].
К сожалению, наиболее широко используемые в клинической практике кристаллоидные растворы - изотонический раствор хлорида натрия и раствор Рингера - не отвечают этим требованиям (табл. 1).
Таблица 1
Характеристики кристаллоидных растворов
|
Показатель, мэкв/л
|
NaCl 0,9%
|
Раствор Рингера
|
Реамберин
|
|
Na+
|
154
|
147
|
147
|
|
K+
|
-
|
4
|
4
|
|
Ca2+
|
-
|
2,25
|
-
|
|
Mg2+
|
-
|
1
|
1,25
|
|
Cl-
|
154
|
156
|
109
|
|
HCO3-
|
-
|
-
|
-
|
|
Лактат
|
-
|
-
|
-
|
|
Сукцинат
|
-
|
-
|
44,7
|
|
РСИ (SID)
|
0
|
0
|
43
|
|
Осмоляльность, ммоль/л
|
308
|
309
|
310
|
Одним из немногих препаратов, доступных в нашей стране и соответствующих описанным характеристикам, является препарат «Реамберин», относящийся к группе инфузионных антигипоксантов. Реамберин, являясь изотоничным и изотоничным полиэлектролитным раствором, имеет РСИ 43 мэкв/л, что позволяет рассматривать его в качестве перспективного корригирующего раствора в ситуации тяжелой сочетанной травмы, сопровождающейся шоком и гипоперфузией.
В то же время в доступной литературе отсутствуют исследования о возможности коррекции метаболического ацидоза у больных с травмой и кровопотерей с использованием реамберина, а также данные о его влиянии на электролитный состав и осмолярность плазмы крови.
Таким образом, целью нашего исследования была оценка влияния реамберина на КОС, осмолярность и электролитный состав плазмы у больных в остром посттравматическом периоде.
Одновременно исследовали изменения пластических свойств эритроцитов, являющиеся чувствительным маркером сдвигов в ионном балансе и кислотно-щелочном равновесии.
Материал и методы. Обследовано 56 мужчин и женщин в возрасте 18-60 лет, поступивших на стационарное лечение в АРЦ № 18 ГКБ им. С.П. Боткина.
Критерии включения:
- диагноз «тяжелая сочетанная травма»;
- наличие гипотензии на догоспитальном или раннем госпитальном этапе;
- тяжесть по APACHE II при поступлении от 20 до 28 баллов;
- объем кровопотери 20-40 мл/кг.
Критерии исключения из исследования:
- тяжелая черепно-мозговая травма;
- острая почечная недостаточность;
- сахарный диабет;
- терминальное состояние;
- повторное кровотечение;
- смерть, наступившая в первые 3 сут после поступления.
Методом конвертов больные были рандомизированы на 2 группы: 1-я группа (n=28): традиционная инфузионная терапия, 2-я группа (n=28): традиционная инфузионная терапия с добавлением реамберина.
Под традиционной инфузионной терапией подразумевалась терапия, тактика и стратегия которой определялись: 1) волемическим статусом; 2) видом дисгидрии. В первые сутки инфузионную терапию проводили до достижения целевых значений АДср > 60 мм рт. ст., ЦВД 50-100 мм вод. ст. и скорости диуреза более 20 мл/ч.
Среди кристаллоидных растворов на догоспитальном и раннем госпитальном этапах использовали раствор Рингера, изотонический раствор хлорида натрия, а также по показаниям - растворы глюкозы, из коллоидных растворов - препараты модифицированного желатина.
Начиная с первых суток инфузионную терапию проводили дифференцированно после проведения процедуры рандомизации.
Во 2-й группе в составе инфузионной терапии использовали реамберин в дозе 1000 мл в 1-е сутки, 500 мл на 2-е и 3-и сутки.
Всем больным, находящимся на ИВЛ в режиме IPPV, проводили нормовентиляцию.
Лабораторное обследование включало: общий клинический анализ крови с помощью аппарата ADVIA 60 hematology system, динамический мониторинг КОС, а также электролитного и газового состава крови с помощью газового анализатора ABL 800 FLEX (Radiometer, Копенгаген).
При этом оценивали следующие показатели: осмоляльность, концентрация основных ионов (Na+,K+,Cl-); pH; ВЕ - избыток/ дефицит оснований; SB - стандартный бикарбонат; AG - анионная разница плазмы (Anion Gap); AG corr. - анионная разница, скорректированная по альбумину и рассчитанная по формуле AG corr. = AG calc. + 2,5 (4,4 - A); Gap-gap (ΔAG/ΔНСО3) - «разница разниц» - различие между повышением анионной разницы и снижением концентрации бикарбоната, рассчитанное по формуле (AGизм.-12)/(24-SВизм.) [16].
Для грубой оценки сдвигов КОС использовали следующие критерии: для ацидоза - НСО3 < 20 ммоль/л, BE<-3 ммоль/л; для алкалоза - НСО3 > 27 ммоль/л, BE > 3 ммоль/л. Декомпенсированный ацидоз (ацидемия) регистрировали при pH < 7,2.
Измерения показателей КОС и электролитного состава проводили в 4 этапа:
I - в 1-е сутки от момента получения травмы (перед инфузией реамберина);
II - на 2-е сутки через 2 ч после инфузии;
III - на 3-и сутки через 2 ч после инфузии;
IV - на 4-е сутки.
Больным в 1-й группе измерения проводили в аналогичные временны е промежутки после инфузии раствора Рингера.
Пластические свойства эритроцитов оценивали по показателю деформируемости с помощью автоматического лазерного агрегометра деформометра LADE («РеоМедЛаб», Россия) путем оценки деформации эритроцитов в сдвиговом потоке методом лазерной дифрактометрии. При этом при воздействии максимальной скорости сдвига 4500 с-1 регистрировали интегральный показатель, характеризующий способность клетки к деформации - индекс предельной деформируемости эритроцита (IDmax) [17].
Для определения границ нормальных значений показателя IDmax проведены микрореологические исследования крови 20 здоровых доноров (12 мужчин, 8 женщин, средний возраст 29 ± 3,1 года).
Исследование деформируемости в обеих группах проводили 1 раз в сутки на протяжении 4 дней в одно и то же время.
Статистический анализ результатов исследования выполнен с использованием программы Statistica. Стандартная обработка данных включала вычисление средних величин (М) и стандартных отклонений (а). Сравнение вариационных рядов осуществляли с помощью парного t-теста Стьюдента, а также непараметрическими критериями (Уилкоксона, Манна-Уитни, Z-критерий), различия считали достоверными при p < 0,05. Для оценки корреляционной связи использовали коэффициент корреляции Пирсона (г).
Результаты исследования и их обсуждение. Демографические показатели в группах не различались (табл. 2). Также не различались объем и характер инфузионно-трансфузионной терапии, проводившейся в первые сутки после травмы (табл. 3). Ни один больной, включенный в исследование, не получал в составе инфузионной терапии гидрокарбонат натрия.
Таблица 2
Сравнительная характеристика больных в группах (M ± σ)
|
Показатель
|
1-я группа
|
2-я группа
|
|
Число больных
|
28
|
28
|
|
Пол (м/ж)
|
20/8
|
19/9
|
|
Средний возраст, годы
|
37,4 ± 3,7
|
32,5 ± 3,9
|
|
Объем кровопотери, мл
|
1631± 359
|
1564±410
|
|
Тяжесть по APACHE II при поступлении, баллы
|
24,8 ± 2,34
|
25,1 ± 2,15
|
Таблица 3
Объем (в мл) инфузионно-трансфузионной терапии в первые сутки на одного больного (M ± σ)
|
Растворы
|
1-я группа (n = 28)
|
2-я группа (n = 28)
|
|
Кристаллоиды
|
4627 ± 1411,8
|
4515 ± 1342,1
|
|
Коллоиды
|
562 ± 259,5
|
580 ± 2511,1
|
|
СЗП
|
461 ± 271,2
|
398 ± 243,5
|
|
Эритроцитарная масса
|
276 ± 314,5
|
225 ± 302,9
|
Примечание. СЗП - свежезамороженная плазма.
Осмолярность и показатели электролитов при поступлении находились в пределах нормальных значений, за исключением хлора, количество которого было повышено в обеих группах (табл. 4).
Таблица 4
Динамика лабораторных показателей в группах на этапах исследования (M ± σ)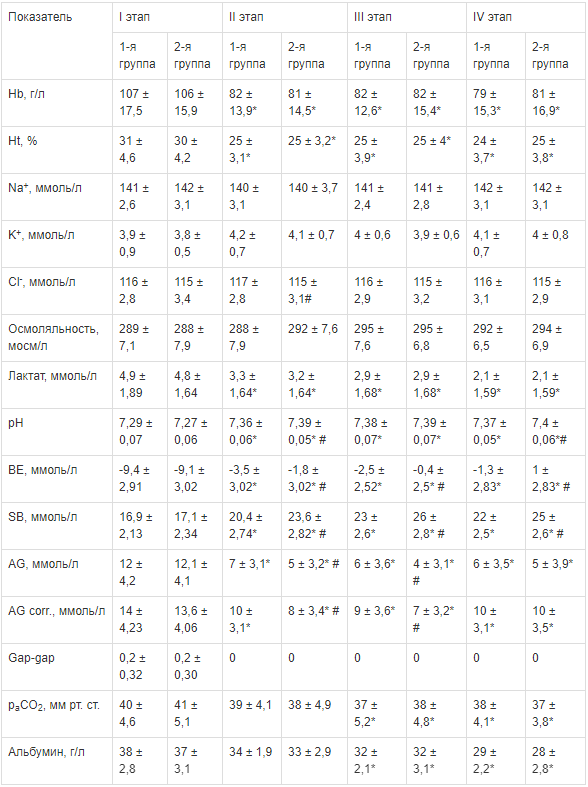 Примечание. * -р < 0,05 по сравнению с I этапом; #-р < 0,05 по сравнению с 1-й группой.
Примечание. * -р < 0,05 по сравнению с I этапом; #-р < 0,05 по сравнению с 1-й группой.
По данным КОС метаболический ацидоз в первые сутки отмечался у 52 (92%) из 56 больных. В 36% случаев это был компенсированный ацидоз, в 54% - субкомпенсированный и в 5% - декомпенсированный ацидоз. При этом анионная разница была нормальной, что характерно для лактат-ацидоза, а «разница разниц» (Gap-gap) - значительно меньше единицы, что говорило о наличии ГХМА и его вкладе в общие нарушения. Иными словами, несмотря на снижение количества бикарбоната, анионная разница находилась в пределах нормы за счет компенсаторной гиперхлоремии. Респираторный компонент ацидоза отмечался у 4 (7%) человек, у большинства больных показатели paCO2 находились в пределах нормальных значений.
Для изучения связи различных факторов, характеризующих тяжесть состояния при поступлении, с лабораторными данными проведен корреляционный анализ таких факторов, как уровень гемоглобина, тяжесть по APACHE II, объем кровопотери, длительность гипотензии, индекс Альговера, АДср на догоспитальном этапе, АДср при поступлении, средний объем инфузионной терапии в первые сутки. При этом максимальный статистически значимый уровень корреляции получен между длительностью гипотензии и уровнем лактата (r = 0,43; р < 0,05), между объемом инфузионной терапии в первые сутки и уровнем хлоридов (r = 0,65; р < 0,01), а также объемом инфузионной терапии в первые сутки и дефицитом оснований (r = 0,32; р < 0,05).
В дальнейшем на протяжении исследования показатели электролитов и осмолярности плазмы в 1-й группе достоверно не менялись и находились в пределах нормальных значений, за исключением хлорида, уровень которого повышен на всех этапах с максимумом на 2-е сутки (см. табл. 3).
В отношении показателей КОС отмечалась следующая динамика. Уже на 2-е сутки показатели рН, SB и BE достоверно увеличивались. Тем не менее по данным рН метаболический ацидоз сохранялся на 2-е сутки у 55% больных. В то же время на основании показателей дефицита оснований и стандартного бикарбоната метаболический ацидоз диагностирован у 63% обследованных, что говорит о наличии респираторной компенсации у части больных (рис. 1). Сочетание высоких показателей хлора и стремящаяся к нулю «разница разниц» (ΔAG/ΔHCO3) на фоне значимого снижения лактатемии (р < 0,05) говорит о растущем вкладе в метаболические нарушения ГХМА. Подтверждением этого является также показатель скорректированной анионной разницы (AG corr.), который находился в пределах нормальных значений на протяжении всего исследования. Метаболический ацидоз в данной ситуации обусловлен увеличением почечной экскреции бикарбоната и уменьшением его реабсорбции для компенсации увеличенного количества анионов (хлоридов). Уровень бикарбоната при этом снижается значительно больше, чем увеличивается анионная разница, поэтому отношение ΔAG/ΔHCO3 («разница-разниц») меньше единицы.
Рис. 1. Распределение больных в 1-й группе по преобладающим сдвигам КОС.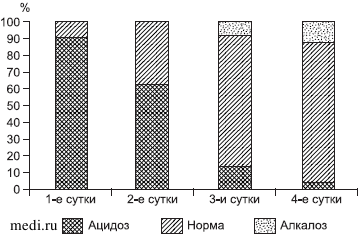
На 3-и и 4-е сутки основные показатели, характеризующие КОС, возвращались в границы нормальных значений, значительно снижался уровень лактата (р < 0,001). Увеличивалась разница AG и AG corr., связанная с прогрессирующей гипо-альбуминемией, обусловленной в том числе значительной дилюцией (снижение Ht с 31 до 25%). В то же время у 4 (14%) больных на 3-и сутки еще отмечался метаболический ацидоз (см. рис. 1).
На 4-е сутки большинство больных имели нормальные показатели КОС, лишь у одного сохранялся метаболический ацидоз, а у 3 больных отмечался сдвиг в сторону метаболического алкалоза (рис. 2).
Рис. 2. Распределение больных во 2-й группе по преобладающим сдвигам КОС.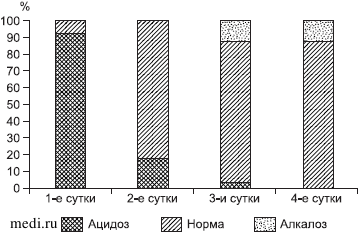
Динамика лабораторных показателей во 2-й группе также представлена в табл. 4.
Как видно из этой таблицы, на протяжении всего исследования показатели осмолярности и уровня большинства электролитов достоверно не отличались от 1-й группы, за исключением концентрации хлора, которая во 2-й группе была достоверно ниже, чем в 1-й группе (р < 0,05), на 2-е сутки.
Наиболее значимые отличия наблюдались в отношении показателей КОС. Так, во 2-й группе уже на 2-е сутки показатели SB были достоверно выше, чем в 1-й группе традиционной инфузионной терапии. Также отличались значения pH и ВЕ. В целом на 2-е сутки по данным BE метаболический ацидоз сохранялся лишь у 5 (18%; р = 0,002) больных по сравнению с 1-й группой, на 3-и сутки - у одного больного. Тогда же (на 3-и сутки) у трех больных после инфузии реамберина зарегистрирован метаболический алкалоз. У двух из них алкалоз разрешился через 6 ч, у третьего сохранялся вплоть до 4-х суток. В целом распределение больных в зависимости от сдвигов КОС на 4-е сутки в группах практически не различалось. Значения анионной разницы во 2-й группе были несколько ниже, чем в 1-й группе, за счет того, что рост уровня бикарбоната не сопровождался одновременным увеличением концентрации хлора. Показатель Gap-gap в эти сроки в обеих группах стремился к нулю в связи с нормализацией уровня бикарбоната.
У всех больных в обеих группах показатели напряжения углекислоты в артериальной крови находились в пределах нормальных значений, хотя примерно у 40% больных отмечалась умеренная гипервентиляция.
Индекс деформируемости эритроцитов (IDmax) исходно был значительно снижен в обеих группах по сравнению с нормальными значениями (0,39-0,42) (рис. 3). В 1-й группе он также оставался сниженным и на 2-е сутки (0,37 ± 0,022 усл. ед.) и только на III и IV этапах увеличивался, приближаясь к нижней границе нормальных значений. Во 2-й группе индекс деформируемости увеличивался уже на 2-е сутки, составляя 0,385 ± 0,031 усл.ед., что выше аналогичного показателя в 1-й группе (р < 0,05). В дальнейшем показатели между группами не различались.
Рис. 3. Динамика индекса деформируемости эритроцитов (IDmax) в группах. 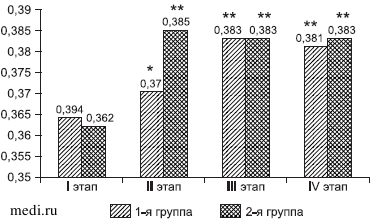
* - р < 0,05 по сравнению со 2-й группой; ** - р < 0,05 по сравнению с I этапом.
При оценке связи между индексом деформируемости эритроцитов и лабораторными показателями статистически достоверную связь получили со значениями лактата (р = 0,32; р < 0,05) концентрацией глюкозы (р = 0,21; р < 0,05), осмолярностью (р = - 0,32; р < 0,05), уровнем альбумина (р = 0,23; р < 0,05) и pH (р = 0,23; р < 0,05). В то же время достоверной связи с показателями BE и SB выявлено не было.
Результаты в отношении динамики нарушений КОС в раннем посттравматическом периоде в значительной мере совпадают с данными аналогичных исследований по популяции реанимационных больных в целом, когда метаболический ацидоз, имеющийся при поступлении, на протяжении нескольких суток сменяется алкалозом [18]. Отличия состоят в большей выраженности и устойчивости сдвигов КОС в кислую сторону у больных с травмой. Следует также отметить существенный вклад гиперхлоремии и ГХМА в общую картину нарушений КОС, особенно на 2-е сутки после травмы. Очевидно, что гиперхлоремия обусловлена активным использованием несбалансированных электролитных растворов, что подтверждается также высокой корреляцией между концентрацией хлора и объемом инфузионной терапии. Связь между объемом инфузионной терапии и значениями BE может также косвенно свидетельствовать о наличии дилюционного ацидоза.
Наиболее вероятной причиной развившегося у нескольких больных к 3-м суткам алкалоза является разрешившийся лактат-ацидоз и начавшийся активный метаболизм лактата до бикарбоната на фоне его уже восстановившихся запасов. Возможно также и влияние других факторов, таких как потери электролитов из желудочно-кишечного тракта и гипокалиемия.
Эффективность использования реамберина для коррекции имевшегося метаболического ацидоза подтверждается практически полным восстановлением показателей КОС до нормальных значений уже на 2-е сутки после травмы. Можно предположить, что такой результат достигнут в том числе благодаря меньшей перегрузке хлором в группе, где использовался реамберин. В то же время хотя разница в содержании хлора в реамберине и растворе Рингера достаточно значительна и составляет 47 ммоль/л, отчасти неожиданным результатом стали различия в концентрации хлора между группами на 2-е сутки, особенно учитывая сравнительно небольшой объем переливаемого реамберина относительно общего объема внесосудистого пространства, где происходит его распределение.
При этом реамберин не влиял на концентрацию в плазме других электролитов и ее осмоляльность.
Важным результатом представляется также отсутствие статистически значимых различий в количестве случаев развития метаболического алкалоза на фоне применения реамберина и без него, что говорит в пользу безопасности использования растворов с высокой РСИ в остром периоде травмы.
В то же время возможность более длительного применения реамберина у этих больных на фоне нормальных показателей КОС требует дополнительного обсуждения и изучения. На данном этапе очевидной является необходимость контроля показателей КОС при применении реамберина (особенно многократном) на фоне эупротонемии.
Исходно низкие показатели деформируемости эритроцитов в обеих группах с наибольшей вероятностью обусловлены не в последнюю очередь метаболическими сдвигами в плазме крови, что подтверждается также совпадением динамики восстановления показателей КОС и морфологии эритроцитов, а также литературными данными о связи между ацидозом, вызывающим отек эритроцитов, уровнем лактата и вязкостью крови [19].
При этом стабилизация показателей КОС во 2-й группе приводила одновременно к восстановлению пластических свойств эритроцитов, хотя данное заключение не исключает возможности непосредственного влияния реамберина на мембрану эритроцита, что требует дополнительных исследований.
Использование в составе инфузионной терапии сбалансированных полиэлектролитных растворов с увеличенной разницей сильных ионов позволяет быстро купировать нарушения кислотно-основного состояния у больных в остром периоде травмы.
Выводы
1. На фоне применения традиционных кристаллоидных растворов нарушения кислотно-основного состояния в остром периоде травмы представлены лактат-ацидозом, гиперхлоремическим и дилюционным ацидозом.
2. В группе, где использовался реамберин, уже на 2-е сутки происходила нормализация показателей кислотно-основного состояния у 82% больных, а также отмечались более низкие показатели концентрации хлоридов.
3. Включение в состав инфузионной терапии реамберина не влияло на осмоляльность плазмы и частоту развития алкалоза в остром периоде травмы.
4. В группе, где использовался реамберин, отмечали более высокие показатели деформируемости эритроцитов.
ЛИТЕРАТУРА/ REFERENCES
1. Gauthier P.M.1., Szerlip H.M. Metabolic acidosis in the intensive care unit. Crit. Care Clin. 2002; 18(2): 289-308.
2. Hatherill M., Waggie Z., Purves L., Reynolds L., Argent A. Mortality and the nature of metabolic acidosis in children with shock. Intensive Care Med. 2003; 29: 286-91.
3. Maciel A.T., Park M. Differences in acid-base behavior between intensive care unit survivors and nonsurvivors using both a physicochemical and a standard base excess approach: a prospective, observational study. J. Crit. Care. 2009; 24(4): 477-83.
4. Martin M.1., Murray J., Berne T., Demetriades D., Belzberg H. Diagnosis of acid-base derangements and mortality prediction in the trauma intensive care unit: the physiochemical approach. J. Trauma. 2005; 58(2): 238-43.
5. Kaplan L.J., Spiros Frangos. Clinical review: Acid-base abnormalities in the intensive care unit - part II. Crit. Care. 2005; 9(2): 198-203.
6. Stengl ... et al. Effects of clinically relevant acute hypercapnic and metabolic acidosis on the cardiovascular system: an experimental porcine study. Crit. Care. 2013; 17: R303.
7. Rhee P., Wang D., Ruff P., Austin B., DeBraux S., Wolcott K. et al. Human neutrophil activation and increased adhesion by various resuscitation fluids. Crit. Care Med. 2000; 28: 74 8.
8. Pedoto A., Caruso J.E., Nandi J., Oler A., Hoffmann S.P., Tassiopoulos A.K. et al. Acidosis stimulates nitric oxide production and lung damage in rats. Am. J. Respir. Crit. Care Med. 1999; 159: 397-402.
9. Wilcox C.S: Regulation of renal blood flow by plasma chloride. J. Clin. Invest. 1983; 71: 726-35.
10. Wilkes N.J., Woolf R., Mutch M., Mallett S.V., Peachey T., Stephens R., Mythen M.G: The effects of balanced versus saline-based hetastarch and crystalloid solutions on acid-base and electrolyte status and gastric mucosal perfusion in elderly surgical patients. Anesth. Analg. 2001; 93: 811-6.
11. Yunos N.M., Bellomo R., Glassford N., Sutcliffe H., Lam Q., Bailey M. Chloride-liberal vs. chloride-restrictive intravenous fluid administration and acute kidney injury: an extended analysis. Intensive Care Med. 2015; 41(2): 257-64.
12. Langer T., Carlesso E., Protti A., Monti M., Comini B., Zani L. et al. In vivo conditioning of acid-base equilibrium by crystalloid solutions: an experimental study on pigs. Intensive Care Med. 2012; 38: 686-93.
13. Morgan T.J., Venkatesh B., Hall J. Crystalloid strong ion difference determines metabolic acid-base change during in vitro haemodilution. Crit. Care Med. 2002; 30: 157-60.
14. Carlesso E., Maiocchi G., Tallarini F., Polli F., Valenza F., Cadringher P., Gattinoni L. The rule regulating pH changes during crystalloid infusion. Intensive Care Med. 2011; 37: 461-8.
15. Morgan T.J. Clinical review: the meaning of acid-base abnormalities in the intensive care unit—effects of fluid administration. Crit. Care. 2005; 9: 204-11.
16. Rastegar А. Use of the ΔAG/ΔHCO3 ratio in the diagnosis of mixed acid-base disorders. J. Am. Soc. Nephrol. 2007; 18: 2429-31.
17. Фирсов Н.Н., Джанашия П.Х. Введение в экспериментальную и клиническую гемореологию. М.; 2008.
18. Mæhle1 K., Haug B., Flaatten H., Nielsen E.W. Metabolic alkalosis is the most common acid-base disorder in ICU patients. Crit. Care. 2014; 18: 420.
19. Reinhart W.H., Gaudenz R., Walter R. Acidosis induced by lactate, pyruvate, or HCl increases blood viscosity. J. Crit. Care. 2002; 17(1): 68-73.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)