Оптимизация послеоперационной медикаментозной терапии инфекционного эндокардита у пациентов с врожденными клапанными пороками сердца
Статьи
Опубликовано в журнале:
Хирургия 3, 2016
doi: 10.17116/hirurgia2016351-55
К.м.н. И.С. Чистяков1, д.м.н., проф. А.П. Медведев2, д.м.н., проф. В.В. Пичугин2
1ГБУЗ НО «Специализированная кардиохирургическая клиническая больница», Нижний Новгород; 2ГБОУ ВПО «Нижегородская государственная медицинская академия» Минздрава России, Нижний Новгород
Optimization of postoperative medical therapy of infective endocarditis in patients with congenital valvular heart disease
I.S. Chistyakov1, A.P. Medvedev2, V.V. Pichugin2
1Specialized Hospital for Cardiac Surgery, Nizhny Novgorod; 2Nizhny Novgorod State Medical Academy, Russian Ministry of Health, Nizhny Novgorod
Цель исследования — оценка эффективности препарата реамберин в послеоперационной терапии больных с врожденными пороками клапанов сердца. Проведен анализ эффективности комбинированной схемы терапии 74 пациентов с клапанными врожденными пороками сердца, осложненными инфекционным эндокардитом. Приведены показания к хирургическому лечению, особенности оперативной техники и возникающие технические сложности при выполнении подобных операций, обусловленные воспалительными изменениями и деструкцией тканей, а также пути их преодоления. Для коррекции метаболических расстройств в послеоперационный период 47 пациентам (основная группа) был назначен реамберин: 400 мл/сут однократно внутривенно капельно в течение первых 5 дней после операции. 27 пациентам (контрольная группа) проведена инфузионная терапия по классической схеме в зависимости от тяжести состояния. Помимо стандартного клинико-лабораторного обследования, для оценки эффективности применения реамберина исследовалась активность каталазы, креатинфосфокиназы в сыворотке крови в динамике (1, 3 и 5-е сутки после операции). Хирургическая тактика в комплексном лечении больных с клапанными врожденными пороками сердца, включающая санацию полостей сердца, увеличение частоты швов и применение укрепляющих прокладок из синтетического материала, предотвращающего травмирование швами воспаленных тканей, позволяет достигнуть хороших ближайших и отдаленных результатов. Используя каркасные полоски из политетрафторэтилена, удается восстановить целостность деструктированного клапанного фиброзного кольца и имплантировать механический протез. Включение препарата реамберин в схему терапии инфекционного эндокардита в раннем послеоперационном периоде ускоряет восстановление нормального метаболизма кардиомиоцитов, что ведет к более раннему купированию признаков сердечной недостаточности и повышает общую эффективность лечения.
Ключевые слова: инфекционный эндокардит, врожденные пороки сердца, врожденные клапанные пороки, операция, хирургическая коррекция, реамберин, метаболические нарушения, сердечная недостаточность.
The purpose of this study was to evaluate the effectiveness of combined surgical and medical treatment of infective endocarditis in patients with congenital valvular heart disease when included in a regimen of the drug Reamberin. In this regard, the analysis of the effectiveness of a combination regimen of 74 patients with valvular congenital heart diseases complicated with infective endocarditis. Given the indications for surgical correction operative technique features and possible technical difficulties in carrying out such operations, due to the inflammatory changes and tissue destruction, and ways to overcome them. For the correction of metabolic disorders in the postoperative period, 47 patients (main group) was appointed Reamberin: once, intravenous drip 400 ml/day during the first 5 days after surgery. 27 patients (control group) was conducted infusion therapy depending on the severity of the condition according to the classical scheme. In addition to standard clinical and laboratory examination, to assess the effectiveness of Reamberin was investigated catalase activity of CPK in blood serum in the dynamics of observation (1, 3 and 5 days after surgery). It is revealed that surgical approach, used in complex treatment of patients with valvular congenital heart diseases, including reorganization of the cavities of the heart, increasing the frequency of joints and the use of reinforcing strips of synthetic material that prevents the cutting of sutures through the inflamed tissue has achieved good short-and long-term results. Infective endocarditis and destruction of the valvular annulus fibrosus the use of a frame of strips of polytetrafluoroethylene allows you to restore its integrity and to implant a mechanical prosthesis. The inclusion in the regimen of patients with infective endocarditis complicated by cardiac insufficiency in the early postoperative period the drug Reamberin improves the efficiency of treatment by a more rapid restoration of the normal metabolism of cardiomyocytes and accelerates elimination of signs of heart failure.
Keywords: infective endocarditis, congenital heart disease, valvular disease, surgery, surgical correction, Reamberin, metabolic disorders, heart failure.
Введение
Несмотря на большое количество исследований и публикаций, проблему инфекционного эндокардита (ИЭ) в настоящее время нельзя считать решенной. Об этом свидетельствует сохраняющийся высокий уровень заболеваемости и летальности при данной патологии [3, 7]. Сложность своевременной диагностики ИЭ влечет высокую частоту осложнений и, зачастую, неудовлетворительные результаты лечения [2, 3].
Существенной проблемой, на которую обращено внимание многих исследователей, является невысокая эффективность этиотропной терапии инфекционного эндокардита, обусловленная образованием микробных вегетаций, не доступных для полноценной санации консервативными методами [1, 5]. Другой важной проблемой является сердечная и полиорганная недостаточность, часто осложняющая течение ИЭ [9]. Ее решение особенно актуально для пациентов, перенесших операцию с искусственным кровообращением на фоне инфекционного эндокардита, поскольку большая операционная травма является дополнительным триггером развития метаболических нарушений [4, 8].
Для решения этих проблем в нашей клинике применяется комплексный подход к лечению ИЭ, включающий хирургическую санацию камер сердца с коррекцией повреждения клапанов, периоперационную антибиотикотерапию и коррекцию метаболических нарушений с применением реамберина (ООО «НТФФ «ПОЛИСАН», Санкт-Петербург) — препарата, обладающего антигипоксическим и антиоксидантным действием, оказывающего положительный эффект на аэробные процессы в клетках, уменьшающего продукцию свободных радикалов и восстанавливающего энергетический потенциал клеток. Положительные эффекты реамберина из учены при ряде патологий, в том числе хирургического профиля [6, 10].
Цель исследования — оценить эффективность комбинированного хирургического и медикаментозного лечения инфекционного эндокардита у пациентов с врожденными пороками клапанов сердца при включении в схему терапии препарата реамберин.
Материал и методы
Проведен анализ эффективности комбинированной схемы терапии 74 пациентов в возрасте от 12 лет до 61 года с клапанными врожденными пороками сердца (ВПС), осложненными ИЭ, получивших лечение в Специализированной кардиохирургической клинической больнице Н. Новгорода в 2001—2014 гг. Нозологические формы врожденных пороков сердца были представлены двухстворчатым аортальным клапаном (АК) со стенозом — 58 (78,4%) пациентов; пролапсом митрального клапана (МК) с регургитацией — 5 (6,7%) пациентов; врожденной недостаточностью МК — 5 (6,7%) пациентов; врожденной недостаточностью АК (синдром Марфана) — 4 (5,4%) пациента; врожденным стенозом трехстворчатого АК — 1 (1,4%) пациент; аномалией Эбштейна (порок трехстворчатого клапана — ТК) — 1 (1,4%) пациент.
Показаниями к хирургическому лечению служили: прогрессирующая сердечная недостаточность (СН), обусловленная клапанной деструкцией; регургитация на клапанах сердца III—IV степени; инфекционный процесс, который не удавалось купировать медикаментозно; крупные подвижные вегетации и абсцессы сердца, выявленные по данным ЭхоКГ; наличие тромбоэмболических осложнений [4, 5, 9].
У всех пациентов оперативное вмешательство выполняли через срединную стернотомию, которая позволяет создать хорошую экспозицию и выполнить адекватную коррекцию внутрисердечной патологии. Подключение аппарата искусственного кровообращения проводили по стандартной методике с канюляцией восходящей аорты и полых вен через правое предсердие. Для декомпрессии левых отделов сердца и профилактики воздушной эмболии при восстановлении сердечной деятельности на конечном этапе операции дренировали левые камеры сердца через коллектор правых легочных вен.
Основополагающим принципом хирургической коррекции поражения клапанов у больных с ИЭ служили полноценное устранение гемодинамических нарушений, обусловленных клапанной деструкцией, механическая и химическая санация камер сердца [5, 9]. Характер поражения внутрисердечных структур отличался значительной вариабельностью.
Основной этап операции во всех случаях начинали с механической санации камер сердца. Она заключалась в иссечении пораженных инфекционным процессом клапанных структур, удалении вегетаций, инфицированных тромбов и кальциевых конгломератов с пристеночного эндокарда и клапанных структур, вскрытии и удалении экссудата из полости абсцессов сердца.
Вслед за механической санацией проводили химическую обработку инфицированных полостей сердца 0,05% раствором хлоргексидина биглюконата, который заливали в полости сердца и выдерживали экспозицию не менее 5 мин. Процедуру повторяли не менее 3 раз. Отдельные участки эндокарда после удаления вегетаций обрабатывали перманганатом калия или йодопироном. Необходимым условием эффективной хирургической санации было полное иссечение инфицированных и некротизированных структур, которые препятствовали выполнению реконструктивных вмешательств [8]. Поскольку большинство больных поступали в хирургический стационар в поздние сроки заболевания, с выраженной деструкцией клапанов сердца, в структуре хирургических вмешательств превалировало протезирование клапанов: протезирование АК — у 56 (75,6%) пациентов, сочетанное протезирование АК и МК — у 9 (12,1%) пациентов, протезирование МК — у 7 (9,5%) пациентов, открытая аортальная вальвулопластика — у 1 (1,4%) пациента и биопротезирование ТК — у 1 пациента.
Техника клапанного протезирования у пациентов с активным ИЭ имела ряд особенностей, обусловленных необходимостью фиксации протеза к воспаленным рыхлым тканям фиброзного кольца. Для профилактики прорезывания швов увеличивали их частоту и в ряде случаев применяли укрепляющие прокладки из политетрафторэтилена. Иногда при выполнении механической санации приходилось иссекать часть фиброзного кольца клапана, что требовало его последующей реконструкции. С этой целью при протезировании АК формировали опору для искусственного клапана путем пликации начального отдела аорты [5, 9]. В ряде случаев швы для фиксации протеза проводили через основание передней створки МК или стенку аорты с выколом наружу. В двух случаях при необходимости реконструкции фиброзного кольца МК применяли опорную полоску из политетрафторэтилена (рис. 3).
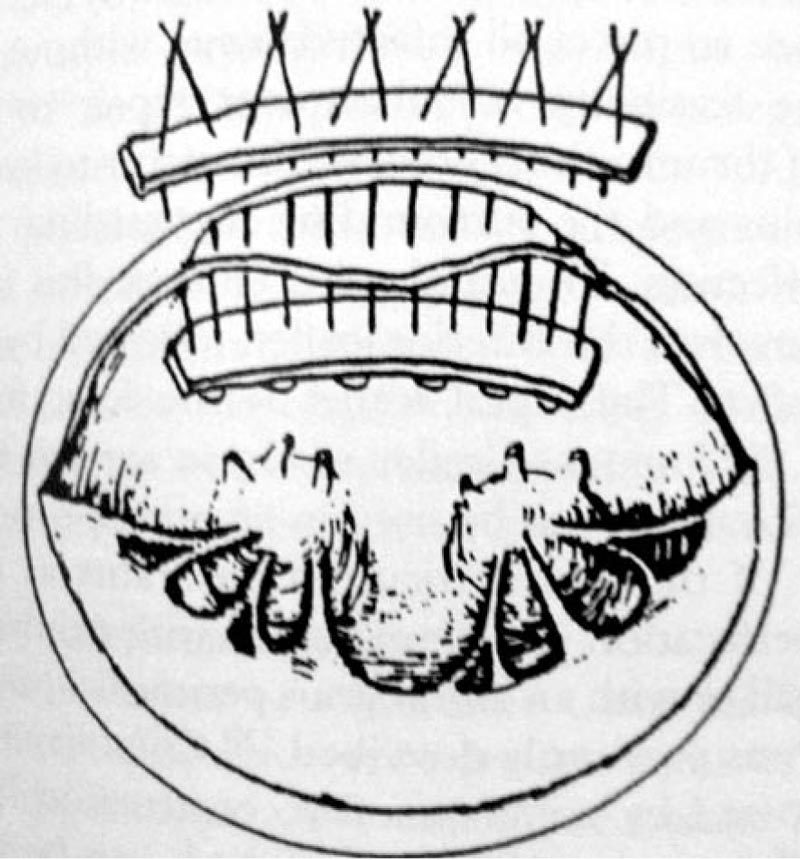
Рис. 3. Схема пластики фиброзного кольца с применением опорной полоски из политетрафторэтилена (цит. по: David D. Yuh, Luca A. Vricella, William A. Baumgartner. McGraw Hill Companies, 2007; 651).
Качественная хирургическая санация сердца создавала благоприятные предпосылки для последующей этиотропной терапии, направленной на подавление остаточных очагов инфекции. Антибактериальную терапию проводили по ступенчатой схеме, основанной на лабораторных данных об активности инфекционного процесса (уровень прокальцитонина в крови) и тяжести полиорганной недостаточности (оценка по шкале SOFA). Уровень прокальцитонина ≥2 нг/мл или сумму баллов по шкале SOFA≥8 считали показанием к деэскалационной терапии с применением карбопенемов в комбинации с ванкомицином/даптомицином. При уровне прокальцитонина <2 нг/мл и сумме баллов по шкале SOFA<8 назначали комбинацию антибактериального препарата широкого спектра действия с препаратом, обладающим высокой антистафилококковой активностью.
Поскольку большинство оперированных пациентов в раннем послеоперационном периоде страдали острой сердечной недостаточностью, важную роль в схеме послеоперационного лечения отводили коррекции метаболических нарушений, связанных с исходно тяжелым состоянием больных, большой операционной травмой и перенесенным искусственным кровообращением [1]. Для коррекции метаболических расстройств 47 пациентам (основная группа) был назначен реамберин: 400 мл/сут однократно внутривенно капельно в течение первых 5 дней после операции. 27 пациентам (контрольная группа) проведена инфузионная терапия по классической схеме в зависимости от тяжести состояния.
Помимо стандартного клинико-лабораторного обследования, для оценки эффективности применения реамберина исследовались активность каталазы в плазме крови по Королюку (1998) и креатинфосфокиназы (КФК) в сыворотке крови на биохимическом анализаторе Rochre Cobax Integra 400 plus (Швейцария) в динамике (1-е, 3-и, 5-е сутки после операции). Парциальное напряжение кислорода в артериальной крови (РаО2) определяли на газовых анализаторах Roche Cobax b121, Roche Cobax b221 сразу после перевода пациента из операционной, а затем каждые 12 ч в течение 2 сут.
Статистическую обработку полученных данных осуществляли с помощью пакета прикладных программ Microsoft Excel 2007, Statistica 6.0, с использованием параметрических (t-тест) и непараметрических (критерий Манна—Уитни) методов вариационной статистики.
Результаты и обсуждение
Анализ полученных клинико-лабораторных данных выявил, что включение реамберина в схему лечения пациентов с клапанными врожденными пороками сердца (ВПС), осложненными ИЭ, в раннем послеоперационном периоде сопровождалось положительной динамикой ферментативной активности: уровень активности каталазы (рис. 4) в основной группе к 5-м суткам по сравнению с 1-ми сутками увеличился на 54,2% (с 5,4 до 11,8 Ед/л), в то время как в контрольной группе — только на 35,8% (с 5,2 до 8,1 Ед/л) (р<0,05), что может быть объяснено положительным влиянием янтарной кислоты на антиоксидантную систему организма.
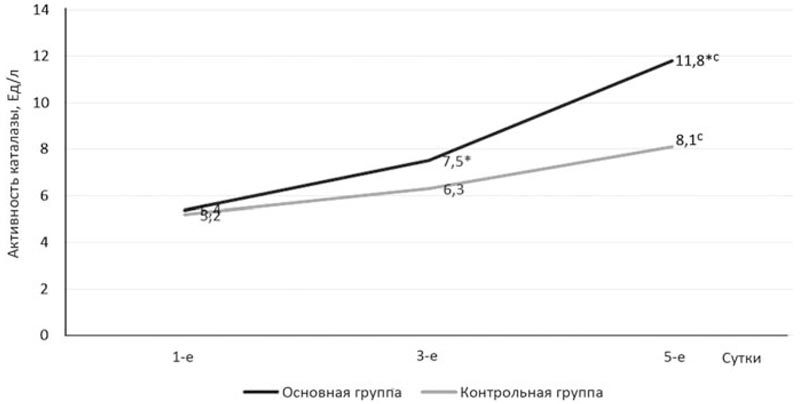
Рис. 4. Динамика активности каталазы в плазме крови.
* — достоверно относительно группы контроля (р≤0,05); *с — достоверно относительно значений 1-х суток в своей группе (р≤0,05).
В то же время активность КФК (рис. 5) к 5-м суткам наблюдения после хирургического вмешательства по сравнению с уровнем 1-х суток у пациентов, получавших реамберин, снизилась на 68,6% (с 618,4 до 194,6 Ед/л), в то время как в контрольной — на 50,1% (с 722,5 до 360,0 Ед/л) (р≤0,05), что можно расценить как показатель более быстрого функционального восстановления кардиомиоцитов на фоне интоксикации и хирургической травмы.
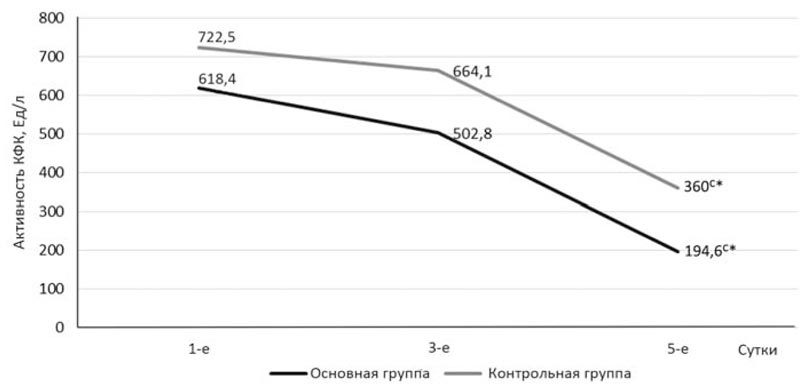
Рис. 5. Динамика активности креатинфосфокиназы в плазме крови.
* — достоверно относительно группы контроля (р≤0,05); с* — достоверно относительно значений 1-х суток в своей группе (р≤0,05).
Анализ исследования парциального давления кислородом артериальной крови (РаО2) (рис. 6) в течение первых 2 сут после операции выявил достоверно более высокий уровень кислорода в крови у пациентов основной группы по сравнению с контрольной, что говорит об отсутствии гипоксии у больного к моменту перевода на спонтанное дыхание и служит подтверждением антигипоксического эффекта реамберина. Так, через 14 ч после операции РаО2 в крови у пациентов основной группы составило 279 мм рт.ст., в то время как в контрольной — 218 мм рт.ст. (на 21,8% меньше), через 26 ч в основной группе — 246 мм рт.ст., в контрольной — 164 мм рт.ст. (на 33,3% меньше) (р<0,05).
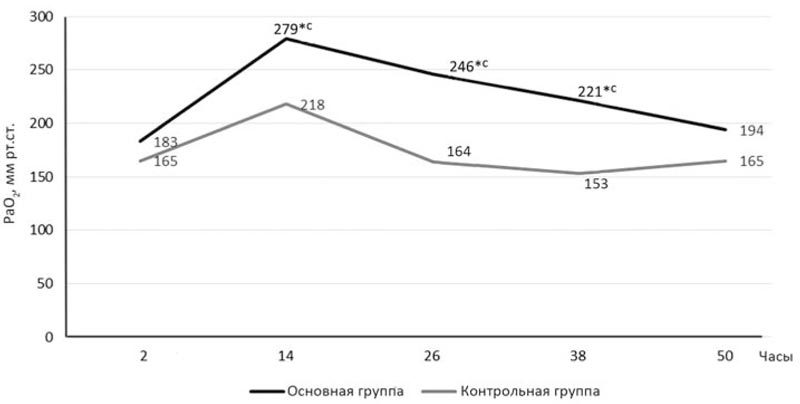
Рис. 6. Динамика парциального напряжения кислорода в артериальной крови.
* — достоверно относительно группы контроля (р≤0,05); *с — достоверно относительно значений 1-х суток в своей группе (р≤0,05).
Большинство — 68 (91,8%) — пациентов были выписаны из стационара с отсутствием клинических и лабораторных признаков воспалительного процесса. В динамике наблюдения (через 2,5 мес) был зарегистрирован 1 случай рецидива ИЭ у пациента, перенесшего протезирование АК и МК, в результате последующего репротезирования АК и МК и санации полостей сердца инфекционный процесс был купирован.
Анализ исходов лечения выявил, что госпитальная летальность среди всех обследованных пациентов составила 8,1% (6 пациентов), причинами служили: острая сердечная недостаточность (4 случая), полиорганная недостаточность (1 случай) и массивная тромбоэмболия легочной артерии из глубоких тибиальных вен (1 случай).
Выводы
Хирургическая тактика, использованная в комплексном лечении больных с клапанными врожденными пороками сердца, включающая санацию полостей сердца, увеличение частоты швов и применение укрепляющих прокладок из синтетического материала, предотвращающих прорезывание швов через воспаленные ткани, позволила достигнуть хороших ближайших и отдаленных результатов. При ИЭ и деструкции клапанного фиброзного кольца применение каркасных полосок из политетрафторэтилена позволяет восстановить целостность фиброзного кольца и имплантировать механический протез.
Включение в раннем послеоперационном периоде препарата реамберин в схему терапии ИЭ, осложненного сердечной недостаточностью, повышает эффективность лечения за счет ускоренного восстановления нормального метаболизма кардиомиоцитов и купирования признаков сердечной недостаточности.
Литература
- Бабаев М.А., Еременко А.А., Минболатова Н.М. и др. Синдром полиорганной недостаточности у больных после операции в условиях искусственного кровообращения. Хирургия. 2013;2:119-123.
- Гаджиев А.А., Рознерица Ю.В., Попов Д.А. и др. Инфекционный эндокардит у пациентов с врожденными пороками сердца: принципы лечения и профилактики. Детские болезни сердца и сосудов. 2007;1:3-13.
- Дюжиков А.А., Углов А.И., Старовойтенко Г.И. и др. Хирургическое лечение инфекционного эндокардита. Грудная и сердечнососудистая хирургия. 2001;6:28-31.
- Земскова Е.Н., Добротин С.С., Щербакова С.В. Эхокардиографические показания к оперативному лечению первичного острого инфекционного эндокардита. Материалы II Международного симпозиума «Клиническая эхокардиография». СПб. 1996;41-42.
- Идов Э.М., Резник И.И. Клапанный инфекционный эндокардит (эволюция, клиника, лечение). 2009.
- Ивницкий Ю.Ю., Головко А.И., Софронов Г.А. Янтарная кислота в системе средств метаболической коррекции функционального состояния резистентности организма. СПб.: Лань; 1998.
- Шевченко Ю.Л. и др. Инфекционный эндокардит как хирургическая проблема в России. Вестник хирургии. 2004;2:12-16.
- Крикунов А.А., Исаенко В.В., Бойко Н.Н. и др. Эффективность реконструктивных операций при инфекционном эндокардите левых отделов сердца. Бюллетень НЦССХ им. А.Н. Бакулева РАМН «Сердечно-сосудистые заболевания». Тезисы. М. 2006; 7:3:21.
- Поляков В.П., Николаевский Е.Н., Хубулава Г.Г. и др. Инфекционный эндокардит (современное состояние проблемы). Самара. 2007;340.
- Реамберин — инфузионный раствор для интенсивной терапии в педиатрической клинике. Под ред. Романцова М.Г. СПб.: Полисан; 2002.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)