Обоснование применения Реамберина в комплексном лечении больных с острой тонкокишечной непроходимостью
Статьи
Опубликовано в журнале:
«Вестник хирургии», 2017, Том 176 • № 1
В. Д. Скрипко1, А. Л. Коваленко2, В. А. Заплутанов3
1 Ивано-Франковский национальный медицинский университет (ректор — проф. Н. М. Рожко), Украина; 2 Институт токсикологии Федерального медико-биологического агентства (дир. — д-р мед. наук М. Б. Иванов), Санкт-Петербург; 3 Санкт-Петербургская государственная химико-фармацевтическая академия (ректор — проф. И. А. Наркевич)
Цель работы — оценить эффективность реамберина в комп лексном лечении пациентов с острой тонкокишечной непроходимостью. В основу исследования легли результаты комплексного обследования 202 больных с острой тонкокишечной непроходимостью (ОТКН), которые находились на стационарном лечении в хирургическом отделении Ивано-Франковской центральной городской клинической больницы в течение 2009–2015 гг. В зависимости от получаемого лечения все больные были разделены на 2 группы. 1-ю группу составили 100 больных с ОТКН, комплексное лечение которых проводилось по общепринятой схеме. 2-ю группу составили 102 больных с ОТКН, которым дополнительно к общепринятому лечению назначали препарат «Реамберин», который вводили внутривенно капельно по 800 мл/сут на протяжении 7 дней. Дополнительное применение препарата «Реамберин» в комплексном лечении больных с ОТКН способствовало более быстрому снижению таких показателей, как лейкоцитарный индекс интоксикации, индекс интоксикации, уровень молекул средней массы, снижало образование малонового диальдегида с одновременной стимуляцией антиоксидантной системы, способствовало нормализации активности органоспецифических ферментов печени. Использование реамберина при острой тонкокишечной непроходимости является патогенетически обоснованным.
Ключевые слова: острая тонкокишечная непроходимость, эндогенная интоксикация, реамберин
Substantiation of reamberin application in complex treatment of patients with acute small bowel obstruction
V. D. Skripko1, A. L. Kovalenko2, V. A. Zaplutanov3
1 Ivano-Frankovsk National Medical University, Ukraine; 2 Institute of Toxicology of Federal Biomedical Agency, St. Petersburg; 3 Saint-Petersburg State Chemical-Pharmaceutical Academy
The study evaluated the efficacy of reamberin in complex treatment of patients with acute small bowel obstruction. Methods. The research is based on the results of complex examination of 202 patients with acute small bowel obstruction (ASBO). The patients were hospitalized in Ivano-Frankovsk central municipal clinical hospital at the period from 2009 to 2015. The patients were divided into two groups according to the method of treatment. The complex treatment using common method was applied for the first group of 100 patients with ASBO. The complex treatment using common method and reamberin intravenously (800 ml/day) during 7 days was applied for the second group of 102 patients. Results. The application of reamberin reduced a lot of indices such as leukocytic intoxication, intoxication index, level of middle mass molecule, formation of malonic dialdehyde. The drug stimulated antioxidant system and normalized organ-specific liver enzymes. Conclusions. The application of reamberin is pathogenetically validated in cases of ASBO.
Key words: acute small bowel obstruction, endogenous intoxication, reamberin
Введение. Острая тонкокишечная непроходимость (ОТКН) и её осложнения остаются одной из наиболее сложных и актуальных проблем неотложной абдоминальной хирургии [2, 7]. ОТКН сопровождается значительным нарушением метаболического гомеостаза в организме, приводит к инвалидизации и высокой летальности — 20–65% [5, 9].
Эндогенная интоксикация (ЭИ), являясь сис темным процессом, включающим значительное разнообразие нарушений метаболического гомеостаза, является патогенетической основой осложнений и формирования полиорганной недостаточности при OТКН, которая, в свою очередь, приводит к угнетению механизмов ауторегуляции гомеостаза до уровня, несовместимого с жизнью. Поэтому понимание патогенеза в формировании эндотоксикоза дает возможность в выборе тактики лечения больных с ОТКН [3, 12, 14].
Важное значение в формировании эндотоксикоза играет энтеральная недостаточность, которая характеризуется нарушением механической, секреторной и всасывающей функции приводящего отдела тонкой кишки, вызывает задержку прохождения кишечного содержимого и нарастание количества и изменения активности бактериальной флоры, которая интенсивно размножается, вызывая усиление процессов брожения и гниения с избыточным образованием высокотоксичных метаболических компонентов, кишечных ядов, продуктов деструкции клеток слизистой оболочки кишки с последующим поступлением их в кровь, что является патогенетическим звеном начала развития дисфункции органов и формирования полиорганной недостаточности [4, 6, 10, 13].
Исходя из вышесказанного, при ОТКН одной из основных задач являются детоксикация организма и восстановление его энергообеспечения. Таким требованиям отвечает инфузионный сукцинатсодержащий раствор реамберин (ООО «НТФФ «ПОЛИСАН», Россия), обладающий антигипоксантным, антиоксидантным, дезинтоксикационым и гепатопротекторным свойством.
Материал и методы. В основу исследования положены результаты комплексного обследования 202 человек больных с ОТКН, которые находились на стационарном лечении в хирургическом отделении Ивано-Франковской центральной городской клинической больницы в течение 2009–2014 гг. Группой контроля были 30 практически здоровых лиц. Среди обследованных больных мужчин было 98 (48,5%), а женщин — 104 (51,5%). По возрастному цензу наибольшее количество пациентов составляли люди зрелого возраста (44–59 лет) (47,5%), что, безусловно, указывает на социально-экономическое значение данной проблемы. Наиболее частой причиной возникновения ОТКН было наличие спаечного процесса в брюшной полости (55,4%), как следствие ранее перенесенных оперативных вмешательств на органах брюшной полости. При поступлении в стационар всем пациентам проводили стандартные лабораторные и инструментальные обследования.
Оценку эндогенной интоксикации (ЭИ) проводили оп ределением показателей лейкоцитарного индекса интоксикации (ЛИИ) по Я. Я. Каль-Калифу, индекса интоксикации (ИИ) по методике М. Н. Тарелкиной, содержания молекул средней массы (МСМ) по методу И. А. Габриэлян, интенсивности образования малонового диальдегида (МДА) по методу Е. Н. Коро бейникова. Спектрофотометрическое определение диеновых конъюгат (ДК) выполняли методом В. Б. Гаврилова. Определение активности церулоплазмина (ЦП) и насыщенности железом трансферрина (НЖТ) проводили по методу Г. А. Бабенко. Активность каталазы (Кат.) крови определяли по А. Н. Баху. Всем больным проводили определение активности органоспецифических ферментов печени. Активность аргиназы (АРГ) измеряли по В. А. Храмову, активность орнитинкарбамоилтрансферазы (ОКТ) — по Рейхарду в модификации Мерете, активность щелочной фосфатазы (ЩФ), холинэстеразы (ХЭ), сорбитолдегидрогеназы (СоДГ), лактатдегидрогеназы (ЛДГ) определяли с использованием стандартных наборов для печеночных проб (наборы «Филисит-Диагностика»). Все анализы проведены на базе аккредированной биохимической лаборатории ГВУЗ «ИваноФранковский национальный медицинский університет».
В зависимости от получаемого лечения все больные были разделены на 2 группы. 1-ю группу составили 100 больных с ОТКН, комплексное лечение которых проводили по общепринятой схеме, согласно рекомендациям Минздрава Украины от 02.04.2010 г. № 297 (Стандарты оказания медицинской помощи больным с неотложными хирургическими заболеваниями органов брюшной полости). 2-ю группу составили 102 больных с ОТКН, которым дополнительно к общепринятому лечению назначали препарат янтарной кислоты — «Реамберин»: его вводили внутривенно капельно по 800 мл/сут со скоростью не более 90 кап/мин. Введение препарата начинали при комплексной предоперационной подготовке, а также сразу после завершения оперативного лечения в условиях реанимации. Курс лечения составлял 7 дней.
Статистическую обработку полученных результатов проводили с использованием стандартного пакета программ Statistica 10.0 for Windows. На основе полученных результатов была создана база данных, в которую вносили как параметрические, так и непараметрические критерии оценки состояния пациента. Для описания переменных с нормальным распределением использовали среднее арифметическое значение (М) и его статистическую погрешность (m). Описание переменных, распределение которых отличалось от нормального, осуществлено с помощью медианы (Ме), нижнего и верхнего квартилей. Оценка достоверности различий средних велечин для выборок с нормальным распределением проведена с использованием критерия Стьюдента. При сравнении показателей, распределение которых не соответствовало закону нормальности, в двух независимых группах использован критерий Манна—Уитни. Проводили парный факторный корреляционный анализ с расчетом коэффициента корреляции Пирсона — r, для параметрических данных и коэффициента ранговой корреляции Спирмена для непараметрических данных.
Результаты. Как видно из табл. 1, после восстановления проходимости тонкой кишки у больных 1-й группы с применением традиционного лечения наблюдалось постепенное снижение ЛИИ, ИИ и МСМ как на 5–7-е, так и на 12–14-е сутки послеоперационного периода по сравнению с показателями до лечения (р<0,05; р1<0,05), но нормализация данных показателей так и не наступала (р3<0,05). Во 2-й группе больных с дополнительным применением раствора реамберина показатели ЛИИ, ИИ и МСМ более интенсивно менялись в направлении нормализации как на 5–7-е сутки, так и на 12–14-е сутки послеоперационного периода (р<0,05; р1<0,05). После лечения показатели ЛИИ, ИИ и МСМ во 2-й группе были достоверно ниже по сравнению с 1-й группой (р2<0,05). После завершения лечения больных 2-й группы нормализация данных показателей наступала у большинства больных (р3<0,05).
Таблица 1
Динамика показателей эндогенной иноксикации в зависимости от получаемого лечения, Me (q1; q3)
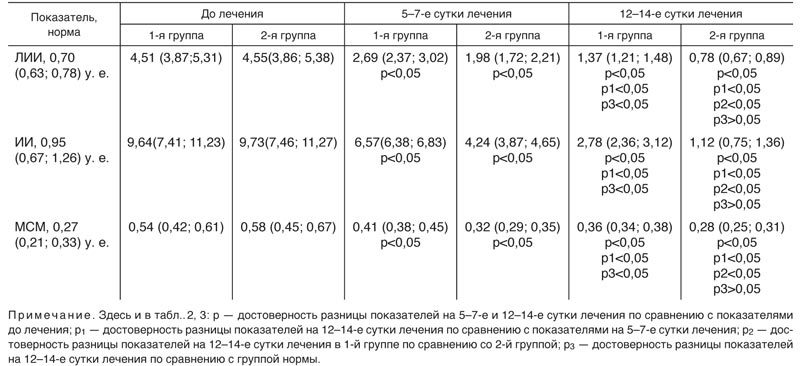
Отмечено, что при поступлении больных на стационарное лечение наблюдается интенсивное нарастание показателей перекисного окисления липидов (ПОЛ) — МДА и ДК в сыворотке крови на фоне снижения активности ферментов антиоксидантной системы (АОС). Как видно из табл. 2, в процессе лечения 1-й группы больных уровень МДА и ДК на 5–7-е сутки постепенно снижался (р<0,05). После завершения лечения больных 1-й группы содержание ДК и МДА не соответствовало физиологической норме (р3<0,05).
Таблица 2
Динамика состояния системы ПОЛ—АОЗ в зависимости от получаемого лечения, Me (q1; q3)
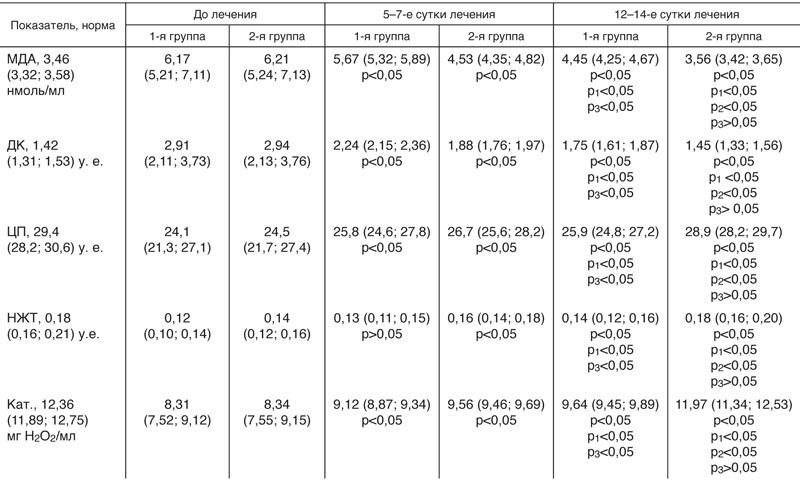
Во 2-й группе больных с ОТКН уровень этих показателей более активно снижался по сравнению с показателями до лечения (р<0,05; р1<0,05). После завершения лечения у больных 2-й группы с дополнительным применением реамберина в комплексном хирургическом лечении содержание продуктов, показатели ПОЛ—МДА и ДК — соответствовали физиологической норме (р3<0,05).
В процессе комплексного хирургического лечения у больных 1-й группы на 5–7-е сутки происходило постепенное увеличение в сыворотке крови активности ЦП, НЖТ и Кат. (р<0,05). После завершения лечения активность данных ферментов физиологической норме не соответствовала (р3<0,05). Дополнительное применение в комплексном хирургическом лечении у больных 2-й группы препарата «Реамберин» значительно интенсивнее меняло показатели активности ЦП, НЖТ и Кат. в направлении физиологической нормы (р<0,05; р1<0,05; р2<0,05). После завершения лечения у большинства больных 2-й группы наблюдалась нормализация показателей активности антиоксидантных ферментов в сыворотке крови (р3<0,05).
Анализ полученных результатов исследований показал, что ОТКН как в дооперационном, так и особенно в послеоперационном периоде сопровождается значительным нарушением функционального состояния гепатоцитов.
С нарастанием эндотоксикоза как в дооперационном, так и в послеоперационном периоде, в обеих группах исследуемых пациентов наблюдались изменения активности органоспецифических ферментов в сыворотке крови — маркеров функционального состояния печени, которые коррелировали со стадией кишечной непроходимости и ее продолжительностью.
Как видно из табл. 3, в процессе лечения больных 1-й группы активность АРГ постепенно снижалась, но на 5–7-е сутки лечения достоверно не отличалась от показателей до лечения (р>0,05). На 12–14-е сутки лечения активность АРГ достоверно снизилась (р<0,05; р1<0,05), однако не достигла нормальных значений (р3<0,05). У больных 2-й группы наблюдали более интенсивное снижение активности АРГ на 5–7-е сутки и после завершения лечения (р<0,05; р1<0,05). Активность АРГ отвечала нормальному уровню после завершения лечения (р3>0,05).
Таблица 3
Динамика активности органоспецифических ферментов печени у больных с ОТКН в зависимости от получаемого лечения, Me (q1; q3)
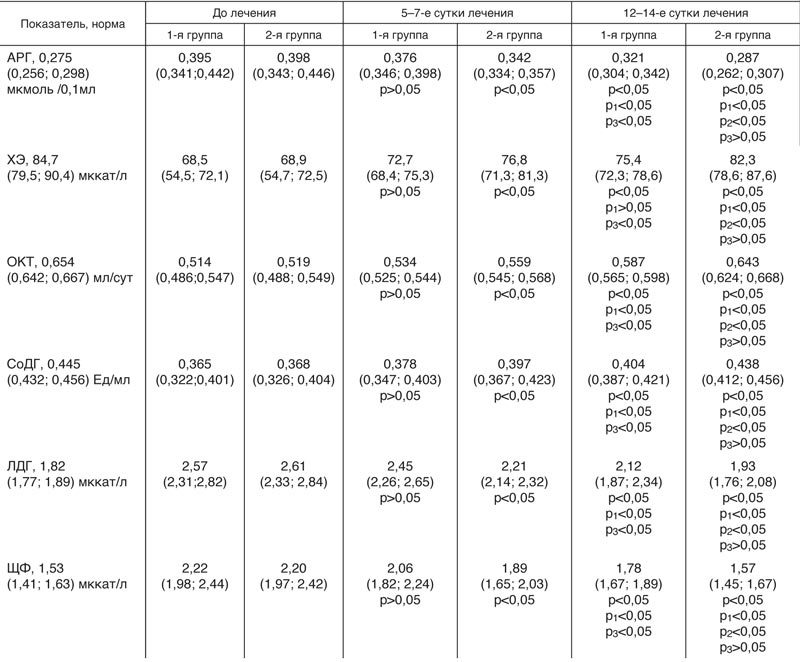
После проведенного лечения у больных 2-й группы активность ХЭ росла более интенсивно и уже на 5–7-е сутки составила 76,8 мккат/л (р<0,05). После завершения проведенного лечения активность данного фермента отвечала физиологической норме (р3>0,05).
В 1-й группе больных достоверное повышение активности ОКТ наблюдали только после завершенния лечения (р<0,05; р1<0,05), но нормализации показателя активности ОКТ не наступало (р3<0,05). Во 2-й группе больных активность фермента ОКТ изменялась в направлении нормализации более интенсивно и уже на 5–7-е сутки повышалась по сравнению с показателями до лечения (р<0,05). После завершения лечения активность данного фермента нормализовалась (р3>0,05). В процессе общепринятого лечения 1-й группы больных активность данного фермента менялась в направлении нормализации только на 12–14-е сутки лечения (р<0,05; р1<0,05), но к физиологической нормы не возвращалась (р3<0,05).
Лечение 2-й группы больных приводило к более выраженному снижению активности СоДГ как на 5–7-е, так и на 12–14-е сутки (р<0,05; р1<0,05), и после завершения проведенного курса лечения активность данного фермента в сыворотке крови соответствовала норме (р3>0,05). Под влиянием проведенного лечения больных 1-й группы активность данного фермента достовер но уменьшилась только после завершения лечения (р<0,05; р1<0,05), но нормальному уровню не соответствовала (р3<0,05).
Установлено достоверное повышение активности ЩФ у больных с ОТКН до лечения (р<0,05). Применение традиционного лечения больных 1-й группы не вызывало положительных сдвигов в изменении активности ЩФ, которая на 5–7-е сутки не отличалась от показателей до лечения (р>0,05). После завершения лечения активность ЩФ достоверно снижалась (р<0,05; р1<0,05), но значения группы нормы не достигала (р3<0,05). Лечение больных 2-й группы способствовало интенсивному снижению активности ЩФ уже на 5–7-й день лечения (р<0,05) с последующей нормализацией после завершения лечения (р3>0,05).
Обсуждение. При клиническом обследовании больных независимо от причин ОТКН ведущую роль в формировании критического состояния в организме больных играет нарастание ЭИ, интенсивность которой в значительной степени зависит от времени развития тонкокишечной непроходимости.
Дополнительное применение препарата «Реамберин» в комплексном лечении больных с ОТКН способствует достоверно более быстрому снижению показателей ЭИ (ЛИИ, ИИ и МСМ) по сравнению с общепринятой терапией.
Универсальным механизмом в интенсификации эндо токсикоза является развитие оксидативного стресса, который является инициатором активации свободнорадикальных процессов на основе стимуляции ПОЛ мембран клеток. Накопление промежуточных и конечных продуктов ПОЛ — МДА и ДК, которые вызывают разрушение микросомальных и митохондриальных структур, сопровождающееся усиленным распадом белков с высвобождением биологически активных аминов и МСМ, формирует общий статус эндотоксикоза [1, 8, 11]. Применение в комплексном лечении ОТКН препарата «Реамберин» обеспечило сокращение времени коррекции оксидативного стресса за счет предупреждения нарастания активности свободнорадикального окисления и образования продуктов ПОЛ с одновременной стимуляцией АОС.
Результаты исследований изменения активности органоспецифических ферментов в сыворотке крови, которые являются маркера ми функционального состояния гепатоцитов, четко указывают на достоверные ранние нарушения функции печени на фоне энтеральной недостаточности. Установлено, что у больных 1-й группы нормализация показателей активности исследуемых ферментов не наступала после оперативного восстановления проходимости тонкой кишки и зависела от тяжести нарушения функционального состояния печени, в результате чего эти показатели даже после завершения лечения не возвращались к физиологической норме, что указывало на необходимость дополнительного применения соответствующей интенсивной терапии. Добавление к общепринятому лечению раствора реамберина у пациентов 2-й группы способствовало нормализации активности органоспецифических ферментов печени.
Выводы. Препарат «Реамберин» в комплексном хирургическом лечении больных с ОТКН способствует уменьшению выраженности эндогенной интоксикации и индуцирует активность ферментного звена антиоксидантной защиты, блокирует образование свободных радикалов, а также нормализирует уровни органоспецифических ферментов печени, что патогенетически обосновывает его использование при острой тонкокишечной непроходимости.
Литература [Reference]
- Бабак О. Я. Влияние комбинации реамберина и циклоферона на показатели синдрома эндогенной «метаболической» интоксикации у больных на неалкогольный стеатогепатит // Украинск. морфол. альманах. 2011. № 2. С. 11–15 [Babak O. Ja. Vlijanie kombinacii reamberina i cikloferona na pokazateli sindroma jendogennoj «metabolicheskoj» intoksikacii u bol’nyh na nealkogol’nyj steatogepatit // Ukrainsk. morfol. al’manah. 2011. № 2. P. 11–15].
- Бенедикт В. В. О значении энергообеспечения тонкой кишки в патогенезе ее функциональной непроходимости при распространенном перитоните и кишечной непроходимости // Госпитальная хир. 2010. № 2. С. 59–62 [Benedikt V. V. O znachenii jenergoobespechenija tonkoj kishki v patogeneze ee funkcional’noj neprohodimosti pri rasprostranennom peritonite i kishechnoj neprohodimosti // Gospital’naja hir. 2010. № 2. P. 59–62].
- Бондарев В. И. Выбор хирургической тактики при остром разлитом перитоните // Хирургия Украины. 2005. № 13. С. 96–99 [Bondarev V. I. Vybor hirurgicheskoj taktiki pri ostrom razlitom peritonite // Hirurgija Ukrainy. 2005. № 13. P. 96–99].
- Вилкинсон Д. Принципы и методы диагностической энзимологии. М.: Медицина, 1981. 512 с. [Vilkinson D. Principy i metody diagnosticheskoj enzimologii. M.: Medicina, 1981. 512 p.].
- Гринёв М. В., Голубева А. В. Проблема полиорганной недостаточности // Вестн. хир. 2005. № 3. С. 110–114 [Grinjov M. V., Golubeva A. V. Problema poliorgannoj nedostatochnosti // Vestn. hir. 2005. № 3. P. 110–114].
- Гриценко С. Н., Корогод С. Н. Интенсивная терапия больных перитонитом с полиорганной дисфункцией // Госпитальная хир. 2013. № 3. С. 127–128 [Gricenko S. N., Korogod S. N. Intensivnaja terapija bol’nyh peritonitom s poliorgannoj disfunkciej // Gospital’naja hir. 2013. № 3. P. 127–128].
- Ерюхин И. А., Петров В. П., Ханевич М. Д. Кишечная непроходимость. СПб.: Питер, 1999. 448 с. [Erjuhin I. A., Petrov V. P., Hanevich M. D. Kishechnaja neprohodimost’. SPb.: Piter, 1999. 448 p.].
- Косинец В. А., Сачек М. Г., Кондратенко Г. Г. Применение препарата реамберин в комплексной терапии распространенного гнойного перитонита // Хирургия. 2010. № 1. С. 59–63 [Kosinec V. A., Sachek M. G., Kondratenko G. G. Primenenie preparata reamberin v kompleksnoj terapii rasprostranennogo gnojnogo peritonita // Hirurgija. 2010. № 1. P. 59–63].
- Косинец В. А., Смагина А. Н. Реамберин в комплексном лечении хирургических заболеваний // Хирургия. 2012. № 7. С. 93–96 [Kosinec V. A., Smagina A. N. Reamberin v kompleksnom lechenii hirurgicheskih zabolevanij // Hirurgija. 2012. № 7. P. 93–96].
- Милюков В. Е., Антипов Е. Ю., Сапин Н. Г. Патогенетическое обоснование лечебной тактики при острой тонкокишечной непроходимости // Вестн. хир. гастроэнтерол. 2008. № 1. С. 42–51 [Miljukov V. E., Antipov E. Ju., Sapin N. G. Patogeneticheskoe obosnovanie lechebnoj taktiki pri ostroj tonkokishechnoj neprohodimosti // Vestn. hir. gastrojenterol. 2008. № 1. P. 42–51].
- Моргунов С. С. Коррекция реамберином тканевой гипоксии и состояние проантиоксидантной системы у хирургических больных с гастродуоденальным кровотечением // Вестн. интенсивной тер. 2008. № 3. С. 58–62 [Morgunov S. S. Korrekcija reamberinom tkanevoj gipoksii i sostojanie proantioksidantnoj sis temy u hirurgicheskih bol’nyh s gastroduodenal’nym krovotecheniem // Vestn. intensivnoj ter. 2008. № 3. P. 58–62].
- Шевчук И. М., Клименко Ю. А. Ранние маркеры печеночной дисфункции и ее коррекция у больных острым распространенным перитонитом // Госпитальная хир. 2010. № 2. С. 20–24 [Shevchuk I. M., Klimenko Ju.A. Rannie markery pechenochnoj disfunkcii i ee korrekcija u bol’nyh ostrym rasprostranennym peritonitom // Gospital’naja hir. 2010. № 2. P. 20–24].
- Яковлев А. Ю. Коррекция метаболизма больных перитонитом — к вопросу о средствах и тактике применения антигипоксантов // Вестн. интенсивной тер. 2007. № 1. С. 91–94 [Jakovlev A. Ju. Korrekcija metabolizma bol’nyh peritonitom — k voprosu o sredstvah i taktike primenenija antigipoksantov // Vestn. intensivnoj ter. 2007. № 1. P. 91–94].
- Wiesner W., Mortele K. Small bowel ischemia caused by strangulation in complicated small bowel obstruction. CT findings in 20 cases with histopatological correlation // JBR BTR. 2011. № 94. Р. 309–314.
Сведения об авторах:
Скрипко Василий Дмитриевич, д-р мед. наук проф., кафедра хирургии ПО, Ивано-Франковский национальный медицинский университет, 76018, Украина, г. Ивано-Франковск, ул. Галицкая, 2;
Коваленко Алексей Леонидович, д-р биол. наук доц., вед. науч. сотр., Институт токсикологии Федерального медико-биологического агентства, 192019, Санкт-Петербург, ул. Бехтерева, 1;
Заплутанов Василий Андреевич, ассистент кафедры фармакологии и клинической фармакологии, Санкт-Петербургская государственная химико-фармацевтическая академия, 197022, Санкт-Петербург, ул. Проф. Попова, 14
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)