Влияние антигипоксантов на результаты лечения распространенного перитонита у детей
Статьи
Опубликовано в журнале:
Хирургия 12, 2016
doi: 10.17116/hirurgia20161288-92
К.м.н. В.А. Завьялкин1, д.м.н. М.А. Барская1, А.В. Варламов2, к.м.н. А.И. Кузьмин1, В.Г. Родионов2, В.В. Щуклова2, Е.В. Терехова2, С.В. Гамов2
1 ФГБОУ ВО «Самарский государственный медицинский университет Минздрава России»; 2 ГБУЗ «Самарская областная клиническая больница им. В.Д. Середавина», Самара, Россия
Цель – улучшение результатов лечения распространенного гнойного перитонита у детей с помощью оптимизации инфузионной терапии включающей в себя использование комбинированных препаратов – антигипоксанта Реамберина и гепатопротектора Ремаксола. Материал и методы. Исследованы 269 пациентов в возрасте от 1 года до 15 лет с распространенным гнойным перитонитом, находившихся на лечении в детских хирургических отделениях Самары с 2001 по 2015 г. В основную группу вошли 179 детей, у которых применяли оптимизированную инфузионную терапию. В основной группе было выделено две подгруппы: 69 детей, в инфузионной терапии которых использовали Реамберин, и 110 пациентов, в лечении которых применяли Реамберин и Ремаксол. В хирургическом лечении использовали лапароскопическую санацию брюшной полости. Комплексное обследование включало изучение динамики уровня лейкоцитов, лейкоцитарного индекса по Кальф-Калифу, СОЭ, температуры, общей концентрации альбумина, уровня трансаминаз. Исследован катамнез 48 пациентов с определением толщины комплекса интима-медиа в проекции базилярной, плечевой и бедренной артерий. Результаты. При исследовании сравниваемых показателей основной и контрольной групп обнаружено более быстрое снижение симптомов интоксикации (лейкоцитоз, ЛИИ, температура тела), исчезновение энтеральной недостаточности, восстановление белково-синтетической функции печени, уменьшение цитолитического и мезенхимально-воспалительного синдромов в основной группе, особенно в подгруппе с Ремаксолом. Вывод. Применение Реамберина и Ремаксола в инфузионной терапии позволило добиться улучшения результатов лечения распространенных гнойных перитонитов у детей. Изучение катамнеза с исследованием комплекса интима-медиа выявило, что у детей, перенесших распространенный гнойный перитонит, в дальнейшем развиваются признаки эндотелиальной дисфункции (ЭТДФ). Разработанные клинические рекомендации значительно уменьшают риск развития признаков ЭТДФ, тем самым снижая возможное появление патологии сосудов у пациентов, перенесших в детстве распространенный гнойный перитонит.
Ключевые слова: распространенный перитонит, гепатопротектор, Ремаксол, Реамберин, лапароскопическая санация брюшной полости.
Influence of the antihypoxantic therapy on children with generalized peritonitis
V.A. Zavyalkin1, M.A. Barskaya1, A.V. Varlamov2, A.I. Kuzmin1, V.G. Rodionov2, V.V. Schuklova2, E.V. Terekhova2, S.V. Gamov2
1 Samara State Medical University, Ministry of Health of Russia; 2 Samara Regional Clinical Hospital named after V.D. Seredavin
Aim. To improve the results of treatment of a widespread purulent peritonitis in children by optimizing fluid therapy includes the use of combined treatment: reamberin and remaxol. Matherial and methods. We studied 269 patients aged 1 to 15 years with a widespread purulent peritonitis treated at the children’s surgical departments in Samara from 2001 to 2015. The study group included 179 children who used the optimized infusion therapy. In the study group was allocated to 2 groups: 69 children in infusion therapy which used reamberin and 110 patients in which treatment was applied reamberin and remaxol. The surgical treatment used laparoscopic sanation of the abdomen. Comprehensive survey included a study of dynamics of the white blood cell count, leukocyte index Kalf-Caliph, erythrocyte sedimentation rate, temperature, total albumin concentration, transaminase levels. Catamnesis studied 48 patients with the definition of complex intima-media thickness in the projection of basilar, brachial and femoral arteries. Results. A study compared indicators of both groups, revealed a more rapid reduction of intoxication symptomps (leukocytosis, LII, body temperature), the disappearance of enteric disease, recovery of protein-synthetic function of the liver, decrease of cytolytic and mesenchymal-inflammatory syndromes in the main group, especially in the subgroup in which treatment was included remaxol. Conclusions. The use of reamberin and remaxol in infusion therapy led to improvement of the results of the treatment of common purulent peritonitis in children. Study catamnesis with the study of the intima-media revealed that children undergoing widespread purulent peritonitis further develop signs of endothelial dysfunction. The developed clinical recommendations to significantly reduce the risk of developing signs of endothelial dysfunction, thereby reducing the possible appearance of vascular pathology in patients who underwent childhood widespread purulent peritonitis.
Keywords: diffuse peritonitis, remaxol, reamberin, laparoscopy sanitation of abdomen.
Введение
Несмотря на усовершенствование методик хирургического лечения гнойно-воспалительных заболеваний, внедрение современных антибактериальных препаратов, лечение детей с тяжелыми гнойно-септическими осложнениями патологии органов брюшной полости (ОБП) является одной из актуальных проблем хирургии [1, 2, 6]. Сохраняющаяся летальность в некоторых клиниках, высокая частота осложнений и последующее значительное снижение качества жизни оставляют проблему лечения распространенного гнойного перитонита у детей открытой [3, 7].
Эндогенная интоксикация, возникающая при гнойно-воспалительных заболеваниях ОБП, осложняющая течение послеоперационного периода у 5-10% пациентов, является результатом кишечной недостаточности. Воспалительная реакция ОБП приводит к гиперактивации симпатического звена регуляции моторики кишечника и выбросу цитокинов (медиаторов воспаления), а также гормонов и метаболитов. Итогом является возникновение нарушения работы мигрирующего электрического комплекса кишки с развитием пареза кишечника, ишемии его стенки, нарушением резорбтивной и барьерной функций кишки. Следующая волна патологических механизмов с глубоким нарушением белкового метаболизма и водно-электролитного баланса, которая захватывает не только интерстициальный, но и клеточный сектор, приводит к транслокации эндотоксинов из просвета желудочно-кишечного тракта (ЖКТ) в брюшную полость, системный, а также портальный кровотоки. Соответственно ЖКТ становится источником мощной эндогенной интоксикации бактериальной и дисметаболической природы [2, 3].
Высокое значение при распространенном гнойном перитоните имеет процесс активации перекисного окисления липидов с повышением фосфолипазы А2 и последующим подавлением антиоксидантной защиты, приводящий к деструкции мембран клеток, нарушению гомеостаза и развитию метаболического дисбаланса в различных органах и тканях, особенно в печени и кишечнике [4, 5].
В формировании гипоксических повреждений при перитонеальном эндотоксикозе играют роль многие факторы: нарушения оксигенации миокарда и периферической микроциркуляции, развитие синдрома гиперкатаболизма-гиперметаболизма, развитие патологии тканевого метаболизма. Однако вне зависимости от вида гипоксии в основе всех характерных для нее нарушений лежит недостаточность клеточной энергообразующей системы митохондриального окислительного фосфорилирования.
В связи с этим оптимизация инфузионной терапии, способствующей фармакологической коррекции внутриклеточного метаболизма при гнойно-воспалительных заболеваниях брюшной полости, имеет большую значимость. Одним из современных методов интракорпоральной детоксикации является использование инфузионных препаратов-антигипоксантов, эффективность которых при критических состояниях доказана многими исследованиями [4, 5].
Среди современных препаратов особое место занимает инфузионный раствор Реамберин. Данный препарат содержит стабильную растворимую форму янтарной кислоты (сукцинат). Превращение янтарной кислоты в организме связано с продукцией энергии, необходимой для обеспечения его жизнедеятельности. Являясь продуктом, а также субстратом 6-й реакции в цикле Кребса, она служит стимулятором синтеза восстановительных эквивалентов в клетке, которые обеспечивают поддержание метаболизма всех органических кислот цикла Кребса. Экзогенное и эндогенное пополнение клеточного пула сукцината способствует значительному снижению уровня органических кислот крови с восстановлением их клеточной утилизации, экскреции кислых продуктов обмена из организма, что указывает на стимулирование аэробной фазы тканевого дыхания. Биологическое значение данного явления заключается в более быстром ресинтезе АТФ клетками и повышении их антиоксидантной резистентности.
Ключевой ролью сукцината среди всех субстратов цикла Кребса является его вклад в предупреждение реперфузионных повреждений, особенно в условиях значительных нарушений кислородного баланса. Развивающаяся гипоксия при эндотоксикозе является причиной значительного накопления промежуточных продуктов обмена, которые приводят к прогрессированию эндотоксикоза. Поступление извне ксенобиотиков, в том числе эндогенного происхождения, определяет самостоятельно развивающееся нарушение всех звеньев транспорта кислорода и метаболизма, что делает клиническое применение Реамберина обоснованным. Ретикулоэндотелиальная система печени и эндотелий сосудов являются основными местами метаболизма ксенобиотиков. Именно эти органы и становятся мишенью эндотоксинов и, соответственно, поражаются при развитии эндотоксикоза с последующим возникновением синдрома полиорганной недостаточности. Высокая скорость метаболических процессов в печени подразумевает их уязвимость в условиях развития гипоксии [4, 5]. Все вышесказанное служит обоснованием применения в инфузионной терапии при распространенном гнойном перитоните антигипоксанта Реамберина и гепатопротектора Ремаксола (ООО «НТФФ «ПОЛИСАН», Санкт-Петербург).
Кроме того, изучение дисметаболических последствий перитонита выявило, что при хирургическом абдоминальном сепсисе, сопровождающем практически все абдоминальные катастрофы, как и при атеросклерозе, инициирующая роль принадлежит одному и тому же фактору, а именно эндотоксину грамотрицательной микрофлоры, который реализует свой патологический потенциал в дисфункцию эндотелия. В работах В.С. Савельева (2009) [2, 3] эндотелиальная дисфунция является главной причиной сердечно-сосудистых заболеваний и смертности от сердечно-сосудистых осложнений у пациентов, перенесших перитонит.
В доступной литературе нет данных о состоянии эндотелия у детей, перенесших перитонит, и о влиянии эндотелиальной дисфункции на будущее качество жизни ребенка. В связи с этим определилась цель нашего исследования – оценка возможности улучшения результатов лечения распространенного гнойного перитонита у детей с помощью оптимизации инфузионной терапии, включающей в себя использование комбинированных препаратов Реамберин и Ремаксол.
Материал и методы
Материалом для настоящего исследования стал накопленный опыт лечения детей с распространенным гнойным перитонитом в детских хирургических отделениях СГКБ №1 им. Н.И. Пирогова и СОКБ им. В.Д. Середавина.
Изучены результаты лечения 269 детей с распространенным гнойным перитонитом различной этиологии, и находившихся на лечении в вышеназванных отделениях с 2001 по 2015 г. Возраст детей составил от 1 года до 15 лет.
В основную группу вошли 179 детей, у которых использовали оптимизированную патогенетическую терапию. Выделены 2 подгруппы: 1-я подгруппа – 69 пациентов (в патогенетической терапии использовали Реамберин в дозировке 10 мл/кг в сутки внутривенно капельно, суточная доза распределяли на 2 введения); 2-я подгруппа – 110 детей (в лечении применяли Реамберин и Ремаксол в суточных дозировках по 5 мл/кг, в одном введении использовали Реамберин, в другом, через 12 ч, – Ремаксол). Препараты назначали как в предоперационной подготовке, так и при послеоперационной терапии в последующие 4-5 дней (до стабилизации состояния ребенка). На применение гепатопротектора Ремаксол у детей получено разрешение биоэтического комитета (решение НОУ ВПО Самарского медицинского института «Реавиз» от 15.04.2011 г.).
Все дети основной группы получали нутритивную поддержку в режиме трофического питания специализированными препаратами.
В хирургическом лечении использовали в основном лапароскопическую санацию брюшной полости.
Комплексное обследование включало изучение динамики уровня лейкоцитов, лейкоцитарного индекса интоксикации (ЛИИ) по Кальф-Калифу, СОЭ, общей концентрации альбумина, уровня трансаминаз, С-реактивного белка, прокальцитонинового теста.
С целью изучения состояния эндотелия исследован катамнез 48 пациентов с определением толщины комплекса интима-медиа в проекции базилярной, плечевой и бедренной артерий.
У 95 пациентов с распространенным перитонитом выполняли среднесрединную лапаротомию, санацию и дренирование брюшной полости.
У 174 детей операция выполнена из лапароскопического доступа. После устранения причины распространенного гнойного перитонита проведена санация брюшной полости с последующим дренированием через надлобковый троакар. В 53 наблюдениях дренировали правый или левый боковые каналы через контрапертуру.
Причиной распространенного перитонита у 16 пациентов явились деструктивные изменения дивертикула Меккеля – выполнена видеоассистированная резекция тонкой кишки с наложением анастомоза конец в конец. У 8 детей причиной гнойного перитонита явилась перфорация тонкой кишки инородными телами (магниты); инородные тела удалены, перфорации ушиты.
Группу сравнения составили 84 ребенка с распространенным гнойным перитонитом. В этой группе использовали стандартную инфузионную терапию растворами кристаллоидов и коллоидов: глюкозы 5 и 10%, натрия хлорида 0,9%, альбумина 10%, волювена 6%.
Результаты
Оценивая уровень лейкоцитов у детей с распространенным гнойным перитонитом при поступлении в стационар, мы выявили его значимое увеличение во всех группах сравнения. Динамика уровня лейкоцитов обнаружила статистически достоверное снижение показателей на 3-и сутки у пациентов основной группы по сравнению с контрольной (p≤0,5). Изучение динамики уровня лейкоцитов показало статистически достоверное снижение этого показателя на 3-и сутки в основной группе пациентов (10,3 ・109±1,2) по сравнению с контрольной (16,4 ・109±1,5) при p=0,006 и на 5-е сутки в основной группе (до нормы: 6,3 ・109±0,6) по сравнению с контрольной (13,6 ・109±1,1) при p=0,001 (рис. 1).
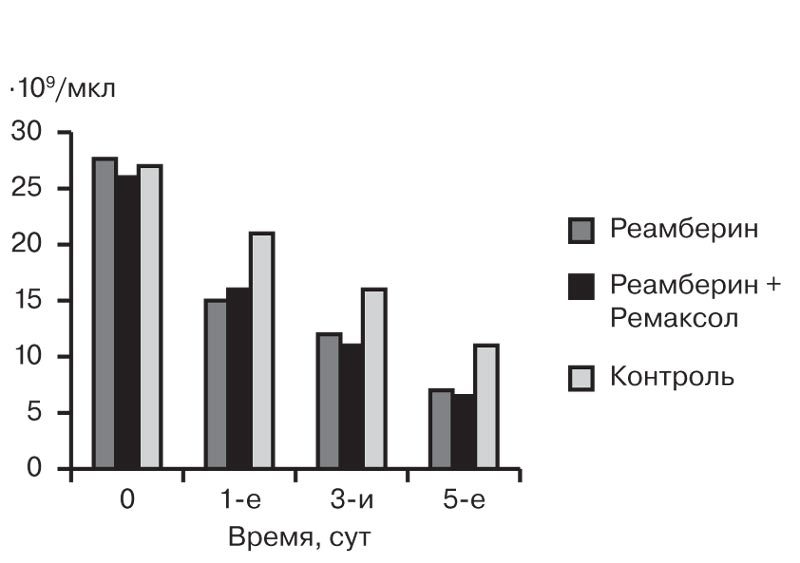
Рис. 1. Динамика лейкоцитоза у детей с распространенным гнойным перитонитом.
Результаты анализа динамики показателя ЛИИ по Кальф-Калифу у детей с распространенным гнойным перитонитом выявили статистически значимое увеличение как в основной (до 3,8±0,4), так и в контрольной (3,7±0,3) группах, p≤0,5. Через 1 и 3 дня обнаружено более значимое достоверное снижение ЛИИ у пациентов основной группы (до 2,1±0,2, p=0,01, и 1,52±0,3 соответственно) по сравнению с контрольной группой (до 2,2±0,3 и 3,23±0,2 соответственно). Через 5 дней результаты сравнения ЛИИ у больных основной группы достоверно подтвердили снижение данного показателя практически до нормы (1,13±0,2) в отличие от ЛИИ у детей контрольной группы (1,83±0,2) (p≤0,5) (рис. 2).
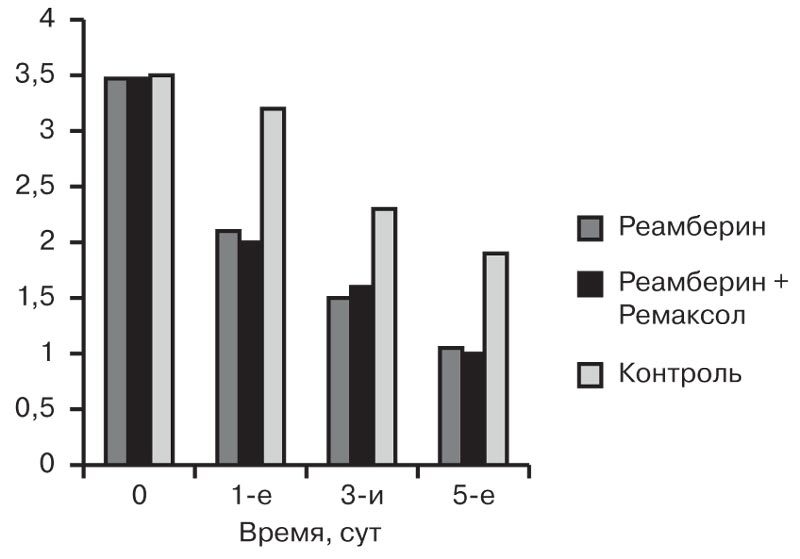
Рис. 2. Динамика ЛИИ с распространенным гнойным перитонитом.
Изучение изменений СОЭ выявило через 1 и 3 дня значимое снижение данного показателя у детей основной группы (до 15,3±1,2 и 12,7±0,9 мм/ч соответственно) по сравнению с детьми контрольной группы (до 21,7±0,9 и 16,4±1,1 мм/ч соответственно), p≤0,5. Через 5 сут результаты анализа СОЭ выявили достоверное уменьшение практически до нормы у детей основной (5,4±0,7 мм/ч) и контрольной (13,4±0,9 мм/ч) групп, p=0,01.
Исследование динамики регрессии кишечной недостаточности обнаружило достоверно значимое ее купирование у пациентов основной группы уже на 2-е сутки по сравнению с контрольной группой, в которой нормализация данного показателя происходила на 3-5-е сутки, в среднем на полтора дня позже p≤0,5.
Динамика показателя общей концентрации альбумина определила статистически достоверное восстановление данного показателя у детей, особенно во 2-й подгруппе, где применялся антигипоксант Реамберин в сочетании с гепатопротектором Ремаксолом (в основной группе через 1 и 3 дня – до 38,4±2,3 и 41,3±1,5 г/л соответственно и на 5-е сутки – до 44,3±1,9 г/л по сравнению с контрольной группой).
Изучение динамики снижения уровня трансаминаз (аспартат- и аланинаминотрансфераза – АсАТ и АлАТ) показали статистически достоверное (p≤0,5) снижение уровня АсАТ и АлАТ через 3 дня у пациентов 2-й подгруппы основной группы (терапия Реамберином+Ремаксолом) по сравнению с детьми контрольной группы.
Разработаны клинические рекомендации у детей, перенесших распространенный гнойный перитонит. Кроме стандартной диеты и противоспаечной терапии, с целью эндотелиопротекции мы рекомендуем применение желчегонных препаратов (хофитол в течение 14 дней), эубиотиков (хилак форте в течение 4 нед в возрастной дозировке), сорбентов (полисорб 2 нед в возрастной дозировке) и с целью эндотелиопротекции – цитофлавин (4 нед в возрастной дозировке).
Изучение состояния эндотелия у пациентов как в основной группе, так и в контрольной группе, выявило статистически значимое утолщение комплекса интима-медиа в полтора раза до 0,073-0,084 мкм по сравнению с возрастной нормой (рис. 3).
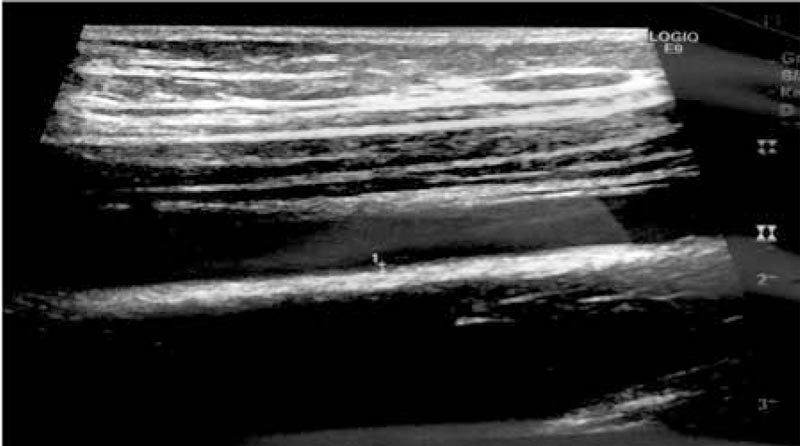
Рис. 3. Толщина комплекса интима-медиа у детей с распространенным гнойным перитонитом при выписке из стационара.
У 36 пациентов основной группы применяли оптимизированные клинические рекомендации, у 12 детей из контрольной группы их не применяли. Выявлено, что у пациентов основной группы через 3 года толщина комплекса интима-медиа пришла к возрастной норме (0,037-0,048 мкм) (рис. 4).
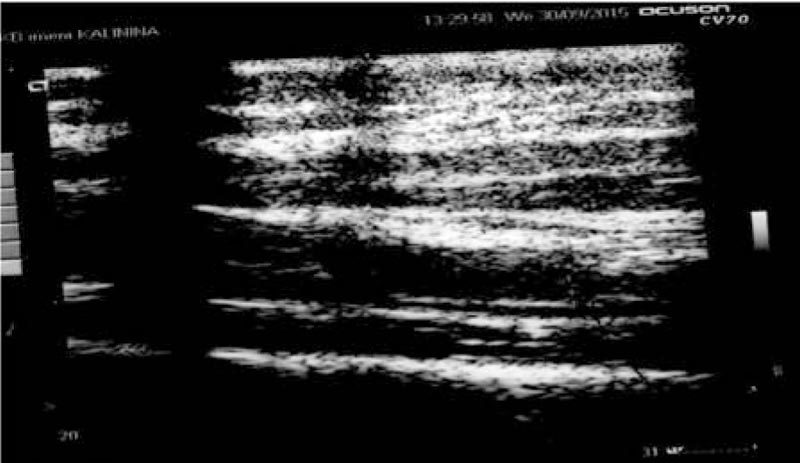
Рис. 4. Толщина комплекса интима-медиа у детей основной группы через 3 года после выписки из стационара.
А у детей контрольной группы обнаружено значимое утолщение комплекса через 3 года (в полтора раза по сравнению с возрастной нормой до 0,063-0,078 мкм (p≤0,5) (рис. 5).
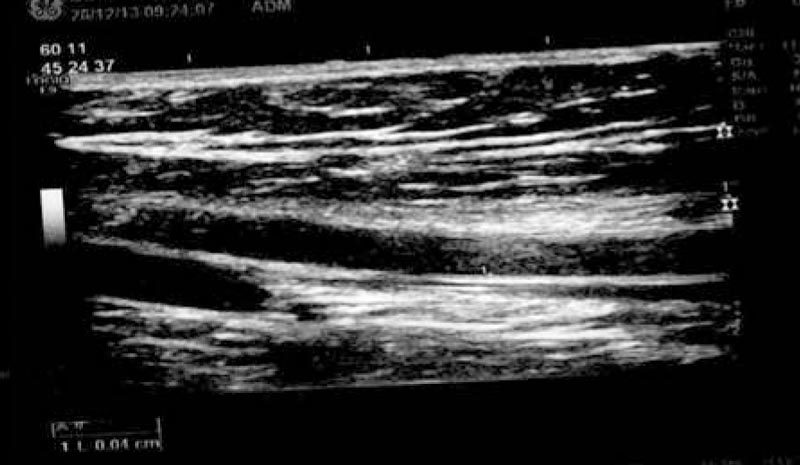
Рис. 5. Толщина комплекса интим-медиа у детей контрольной группы через 3 года после выписки из стационара.
Заключение
Исследование сравнимых показателей основной и контрольной групп обнаруживает более быстрое снижение симптомов интоксикации, таких как лейкоцитоз, лейкоцитарной индекс интоксикации; исчезновение энтеральной недостаточности, более быстрое восстановление белковой синтетической функции печени, уменьшение цитолитического и мезенхимально-воспалительного синдрома в основной группе, особенно в подгруппе с применением в инфузионной терапии Реамберина и Ремаксола.
Изучение катамнеза с исследованием комплекса интим-медиа вывило, что у пациентов, перенесших распространенный гнойный перитонит, в дальнейшем развиваются признаки ЭТД (значительное статистически достоверное утолщение комплекса интим-медиа по сравнению с возрастными нормами). В этой группе соответственно значительно выше риск развития в последующем сосудистой патологии.
Таким образом, разработанные клинические рекомендации значительно уменьшают риск развития признаков ЭТД, тем самым снижая возможное появление патологии сосудов у пациентов, перенесших в детстве распространенный гнойный перитонит.
Литература
- Завьялкин В.А., Барская М.А., Варламов А.В., Быков Д.В., Кузьмин А.И., Бородин Р.В., Родионов В.Г., Фролова Ю.В. Оптимизация лечения распространенного гнойного перитонита у детей. Хирургия. 2015;7:65-68.
- Перитонит. Практическое руководство. Под ред. Савельев В.С., Гельфанда Б.Р., Филимонова М.И. М.: Литтерра; 2006.
- Петухов В.А., Семенов Ж.С. Перитонит и эндотелиальная дисфункция: руководство для врачей. М.: Макс Пресс; 2011.
- Яковлев А.Ю. Реамберин в практике инфузионной терапии критических состояний. Практические рекомендации. СПб. 2007.
- Яковлев А.Ю., Бояринов Г.А., Зайцев Р.М., Емельянов Н.В., Семенов В.Б., Дудина Е.В. Применение Реамберина в интенсивной терапии перитонита, осложненного полиорганной недостаточностью. Методическое пособие. Нижний Новгород: Тактик-Студио; 2008.
- Hotchkiss RS, Karl IE. The pathophysiology and treatment of sepsis. N Engl J Med. 2003;348:138-150.
- Solomkin JS, Mazuski JE, Baron EJ, Sawyer RG, Nathens AB, DiPiro JT, Buchman T, Dellinger EP, Jernigan J, Gorbach S, Chow AW, Bartlett J. Infectious Diseases Society of America. Guidelines for the selection of anti-infective agents for complicated intra-abdominal infections. Clin Infect Dis. 2003;37(8):997-1005.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)