Ацетил-L-карнитин (карницетин) в лечении начальных стадий болезни Альцгеймера и сосудистой деменции
СтатьиОпубликовано в журнале:
Журнал неврологии и психиатрии, 9, 2011
Д.м.н., проф., рук. отдела С.И. Гаврилова*, д.м.н., в.н.с. Я.Б. Калын, к.м.н., в.н.с. И.В. Колыхалов, к.псих.н., ст.н.с. И.Ф. Рощина, д.м.н., в.н.с. Н.Д. Селезнева
Acetyl-L-carnitine (carnicetine) in the treatment of early stages of Alzheimer’s disease and vascular dementia
S.I. Gavrilova, Ya.B. Kalyn, I.V. Kolykhalov, I.F. Roshchina, N.D. Selezneva
Отдел по изучению болезни Альцгеймера и ассоциированных с ней расстройств Научного центра психического здоровья РАМН, Москва
Терапевтическую эффективность, безопасность и переносимость ацетил-L-карнитина (АЛК) изучали в процессе проведения двойного слепого плацебо-контролируемого 12-недельного исследования в группах больных с мягкой (начальной) деменцией, обусловленной болезнью Альцгеймера (БА) и сосудистой деменцией (СД). АЛК применялся в дозах от 2250 до 3000 мг в сутки. Оценка состояния больных проводилась по ряду шкал (MMSE, CGI и др.), а также с использованием нескольких психологических тестов, направленных на определение когнитивных функций. Терапевтический эффект АЛК в 2,8 раза превышал таковой при использовании плацебо. По показателям общего клинического улучшения (шкала CGI) он был достоверно более высоким у пациентов с БА по сравнению с СД, при этом он не зависел от тяжести исходного когнитивного дефицита. Установлена хорошая переносимость препарата. Карницетин в указанных дозах рекомендован для применения у больных с БА и СД на начальной стадии заболевания.
Ключевые слова: болезнь Альцгеймера, сосудистая деменция, начальная стадия болезни, мягкое когнитивное снижение, ацетил-L-карнитин (карницетин).
Efficacy, safety and tolerability of acetyl-L-carnitine (ALC) were studied during the double-blind placebo-controlled 12-week trial in patients with mild (initial) dementia caused by the Alzheimer’s disease (AD) and vascular dementia (VD). ALC was administered in doses from 2250 to 3000 mg per day. Patient’s state was assessed with some scales (MMSE, CGI etc) and a battery of neuropsychological tests. The treatment effect of ALC was 2,8 times higher than in placebo-treated patients. The clinical improvement by CGI scores was significantly better in AD patients compared to VD and did not depend on the severity of baseline cognitive deficit. The drug was well-tolerated. Carnicetine can be recommended in the abovementioned doses for treatment of early stages of AD and VD.
Key words: Alzheimer’s disease, vascular dementia, initial stage of disease, mild cognitive impairment, acetyl-L-carnitine (carnicetine).
Ацетил-L-карнитин (АЛК) — мозгоспецифичное производное L-карнитина (ЛК) — природного низкомолекулярного соединения, которое содержится в организме человека и животных. АЛК синтезируется из ЛК в мозговой ткани, печени и почках при участии фермента карнитинацетилтрансферазы и ацетил-КоА (ацетил-кофермента А).
Одна из важных функций ЛК — перенос жирных кислот из цитоплазмы в матрикс митохондрий для образования в процессе бета-окисления энергии, которая необходима для функционирования всех клеток, организма [6]. В свою очередь синтезированный АЛК представляет собой легкодоступный субстрат для запуска энергозависимых обменных процессов в митохондриях, поставляя ацетильную группу непосредственно в матрикс митохондрии для образования ацетил-КоА без расходования АТФ и кислорода. Метаболическое равновесие между АЛК и ЛК является основой ацетильной буферной системы организма. Образование АЛК препятствует истощению внутриклеточной концентрации КоА-SH (КоА, находящегося в свободном состоянии), что особенно важно для сохранения нормального функционирования клетки.
Препараты на основе АЛК и ЛК относятся к так называемым энерготропным препаратам, способным восстанавливать нарушенный клеточный энергетический метаболизм. В недавно проведенных исследованиях было установлено, что нарушение функций митохондрий играет роль триггерного механизма, запускающего апоптоз — программируемую клеточную гибель. Поскольку апоптоз играет важную роль в развитии нейродегенеративных процессов, возможность подавить или уменьшить разрушение митохондрий представляется актуальной задачей в разработке методов лечения и превентивной терапии болезни Альцгеймера (БА) и других деменций позднего возраста. За рубежом препараты АЛК в последние годы находят все более широкое применение в клинической практике [14]. К настоящему времени вышло большое число публикаций, посвященных экспериментальному и клиническому изучению АЛК.
При пероральном введении отечественного препарата на основе АЛК — карницетина экспериментальным животным (на модели БА), была обнаружена его антиамнестическая активность и способность улучшать процесс обучения, не вызывая побочных эффектов седативного и миорелаксирующего характера. Результаты исследования Т.А. Ворониной и Р.У. Островской [1] свидетельствуют о том, что по эффективности отечественный препарат АЛК сопоставим с зарубежными.
В экспериментальных и клинических исследованиях было установлено, что фармакологическое и терапевтическое действие АЛК отличается от действия карнитина. АЛК воздействует как нейропротекторный фактор по отношению к клетке и ее органеллам, в особенности митохондриям; он проявляет себя также как трофический фактор, способствующий восстановлению клеточной структуры. Нейротрофическая и нейропротективная эффективность АЛК была доказана с помощью широкого спектра методов на различных моделях, в частности, показано его модулирующее действие на активность фактора роста нейронов (ФРН) [3, 19, 21]. Было также установлено, что он влияет на работу мозга, улучшая память, настроение и познавательные функции, поддерживает нормальное функционирование иммунной системы [18], снижает образование липофусцина [2] и проявляет антиоксидантные свойства. Благодаря своему структурному сходству с ацетилхолином, АЛК оказывает холиномиметическое действие. АЛК стимулирует синтез ацетилхолина из холина в мозге млекопитающих, действуя как донор активированных ацетильных групп [25]. Он способен модулировать функцию не только холинергической, но и дофаминергической систем [12, 13]. АЛК усиливает действие серотонина, а также защищает клетки мозга от нейротоксического эффекта глутамата [22]. Имеются данные о способности АЛК повышать клеточную концентрацию аспартата, глутамата и таурина [24]. При длительном применении АЛК увеличивает плотность NMDA-рецепторов в гиппокампе, коре и стриатуме и препятствует уменьшению их плотности в условиях старения [9].
Широкий спектр нейрохимических свойств АЛК проявляется в его действии на когнитивную сферу. Он, в частности, улучшает нарушенные скополамином процессы памяти в тесте водного лабиринта Морриса [16]. Результаты экспериментальных исследований показали, что АЛК обладает антиамнестической активностью, способностью улучшать процессы обучения, показатели неассоциативной памяти, оказывать позитивный эффект на мнестические функции. В большой серии экспериментов было показано [11], что введение АЛК может замедлить патологические процессы у старых крыс (у которых обычно снижен уровень карнитина), вызванные окислительной деструкцией митохондрий. В условиях ишемии с последующей реперфузией АЛК предохраняет от свободнорадикального окисления белка в лобной коре и может уменьшить уровень мозгового повреждения [4, 8].
Большой интерес представляют данные R. Epis и соавт. [10], касающиеся влияния АЛК на метаболизм бетаамилоидного пептида (БАП) на моделях клеточной линии нейробластомы и в первичных гиппокампальных культурах. Результаты этого исследования подтверждают, что положительные эффекты AЛК, которые отмечены в большом числе клинических исследований, в значительной степени обусловлены специфическим биологическим механизмом действия этого соединения на метаболизм БАП. Фактически АЛК оказывает непосредственное влияние на первичную причину патогенеза БА, то есть на бетаамилоидный каскад, способствуя усилению альфасекретазной активности и непосредственно действуя на освобождение неамилоидогенного метаболита, что может привести к снижению уровня БАП.
За последнее десятилетие был проведен целый ряд исследований с использованием АЛК в лечении деменций, включая БА, а также при старческой депрессии и возрастных нарушениях памяти.
Проведенные контролируемые клинические испытания [7, 15, 17, 20, 23] препарата на основе АЛК в ряде европейских стран, а также в Японии и США у пациентов с БА и деменцией различного генеза показали, что он улучшает когнитивные функции у психически здоровых пожилых людей и при деменциях различного генеза, как первично-дегенеративного (БА), так и сосудистого. Хотя результаты использования АЛК для лечения БА в целом противоречивы, большинство исследователей отмечают положительный эффект в отношении когнитивных функций, не уступающий эффекту ацетилхолинергических препаратов [23]. В целом можно отметить, что применение АЛК замедляет степень прогрессирования заболевания, улучшает память, некоторые параметры деятельности мыслительных функций и поведения у больных БА и другими деменциями. В большей степени это относится к пациентам с ранним началом болезни (до 65 лет) и быстрым прогрессированием деменции. Представляет интерес сообщение [5] о терапевтической эффективности комбинации антихолинэстеразных препаратов (в частности, донепезила и ривастигмина) с АЛК при лечении БА.
Учитывая энерготропные, нейропротективные свойства и возможное антиамилоидное действие АЛК, а также его хорошую переносимость в пожилом возрасте, использование этого препарата при лечении деменций позднего возраста представлялось весьма перспективным.
Цель настоящего исследования состояла в оценке безопасности и переносимости приема АЛК (карницетина) в дозе 2250—3000 мг в сутки внутрь (в 2 приема) у пожилых пациентов с начальными проявлениями БА и сосудистой деменции (СД), эффективности исследуемого препарата в отношении нарушений когнитивных функций и повседневной активности у пожилых пациентов с начальными проявлениями БА и СД при указанном выше режиме дозирования.
Материал и методы
Клиническое испытание эффективности и безопасности применения АЛК проводилось в Отделе по изучению болезни Альцгеймера и ассоциированных с ней расстройств Научного центра психического здоровья РАМН с соблюдением протокола, правил GCP и действующих нормативных требований. Исследование выполнялось как двойное слепое плацебо-контролируемое.
В исследование были включены 60 больных, составивших 2 группы по 30 человек в каждой. Больные получали закодированные препараты, один из которых соответствовал карницетину в дозе от 2250 до 3000 мг, другой — плацебо. Общая продолжительность терапии составила 12 нед.
Критерии включения пациентов в исследование были следующие: диагноз БА или СД, установленный в соответствии с критериями МКБ-10; возраст больных от 45 до 95 лет включительно; для женщин — состояние постменопаузы или отсутствие способности к зачатию по другим причинам (гистерэкстомия, стерилизация и др.); наличие мягкой деменции по критериям Clinical Dementia Rating (CDR-1) на момент скринингового визита; оценка в баллах не менее 18 и не более 26 по шкале Mini-Mental State Examination (MMSE) на момент скринингового визита; наличие нейровизуализационных признаков БА (атрофия гиппокампа, прогрессирующая церебральная атрофия) или цереброваскулярного заболевания (пост-ишемические кистозные изменения, выраженный лейкоареозис, церебральная атрофия) по данным КТ или МРТ, сделанных в течение 2 лет до скринингового визита; наличие постоянно проживающего совместно с пациентом ближайшего родственника или другого попечителя, который осуществляет наблюдение и уход за больным; отсутствие противопоказаний к приему препарата внутрь в течение предусмотренного времени; отсутствие в анамнезе инсульта не менее чем в течение 2 лет до включения в исследование; отсутствие показаний к одновременному проведению терапии препаратами, способными исказить результаты исследования; отсутствие грубого двигательного или сенсорного дефекта или иных нарушений, которые могут затруднить оценку первичных или вторичных переменных; отсутствие тяжелых или нестабильных соматических заболеваний; отсутствие других клинически значимых неврологических или психических заболеваний.
Клиническое исследование выполнялось по специально разработанному протоколу с использованием унифицированных индивидуальных карт больных. Оно во всех случаях начиналось с периода скрининга продолжительностью 4 нед. Оценка эффектов препарата производилась по клиническим и психометрическим шкалам с применением стандартных тестов на память, внимание, беглость речи, интеллект и психомоторные функции (MMSE, CGI, модифицированные субтесты «инициация», «концептуализация» и «память» шкалы Маттиса (MDRS); тест рисования часов), и оценки активности в повседневной жизни по шкале IADL (Individual Activity of Daily Living).
Указанные выше 2 группы пациентов были равны по численности и близки по возрасту и диагностическому распределению (табл. 1). Пациенты 1-й группы получали препарат карницетин; пациенты 2-й группы — плацебо. Состояние пациентов в процессе исследования оценивалось дважды: непосредственно перед началом лечения (0 день) и через 12 нед терапии.
| Показатель | 1-я группа (n=30) | 2-я группа (n=30) |
| Средний возраст, годы | 70,9±7,0 | 70,9+7,5 |
| Мужчины | 14 | 7 |
| Женщины | 16 | 23 |
| Клинический диагноз | ||
| БА | 16 | 15 |
| СД | 14 | 15 |
| Средняя оценка по шкале MMSE, баллы | 20,6±2,6 | 21,2±2,4 |
Результаты
В 1-й группе больных полностью курс лечения прошли 29 пациентов: 1 больной выбыл в связи с отказом от дальнейшего участия в исследовании на 8-й нед терапии. Во 2-й группе завершили исследование 27 больных: 1 пациент выбыл в связи с нежелательными явлениями и отказом от лечения после 2 нед терапии, 2 больных отказались от дальнейшего лечения в связи с отсутствием терапевтического эффекта.
Динамика состояния когнитивных функций по шкале ММSЕ
Статистически достоверное улучшение состояния когнитивных функций по сравнению с исходным уровнем отмечалось только у больных 1-й группы (рис. 1). Кроме того, в этой группе наблюдалось достоверное улучшение по сравнению с исходным уровнем оценок по отдельным пунктам шкалы MMSE: воспроизведение после интерференции 3 ранее запомненных слов, повторение набора слов «никаких, если, и, или, но», а также перерисовывание пересекающихся пятиугольников (табл. 2). У больных 2-й группы достоверных изменений ни суммарной оценки, ни оценок по отдельным пунктам шкалы ММSЕ не наблюдалось.
| Пункт шкалы MMSE | 1-я группа | 2-я группа | ||
| 0 день | через 12 нед | 0 день | через 12 нед | |
| Ориентировка во времени | 3,0±1,2 | 3,1±1,6 | 3,2±1,1 | 3,0±1,5 |
| Ориентировка в месте | 4,3±0,7 | 4,3±0,8 | 4,3±0,7 | 4,3±0,9 |
| Повторение 3 слов | 3,0±0,2 | 3,0±0,2 | 3,0±0 | 3,0±0 |
| Серийный счет | 2,1±1,6 | 2,2±1,9 | 2,1±1,3 | 2,2±1,6 |
| Воспроизведение 3 слов после интерференции | 0,6±0,9 | 1,2±1,3* | 1,0±1,0 | 1,2±1,2 |
| Называние предметов | 2,0±0 | 2,0±0 | 2,0±0 | 2,0±0 |
| Повторение фразы | 0,3±0,5 | 0,5±0,5 | 0,2±0 | 0,3±0,5 |
| Выполнение команды | 2,7±0,4 | 2,8±0,5 | 2,9±0,4 | 2,8±0,5 |
| Чтение | 1,0±0,2 | 1,0±0,2 | 0,9±0,3 | 0,9±0,3 |
| Письмо | 1,0±0 | 1,0±0,2 | 1,0±0,2 | 1,0±0,5 |
| Рисунок | 0,6±0,5 | 0,7±0,5* | 0,7±0,5 | 0,7±0,5 |
| Суммарная оценка | 20,6±2,6 | 21,7±4,5* | 21,2±2,4 | 21,1±3,8 |
| Примечание. * — p | ||||
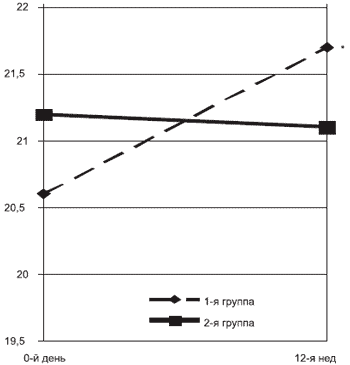 |
| Рис. 1. Терапевтическая динамика средних суммарных показателей по шкале MMSE в 1-й и 2-й группах больных. По оси ординат — баллы. Здесь и на рис. 2—4, 6, 9 звездочкой отмечены достоверные различия между группами на 12-й нед на уровне p |
 |
| Рис. 2. Терапевтический эффект по показателю состояния когнитивных функций по разным тестам шкалы MMSE в 1-й и 2-й группах больных. |
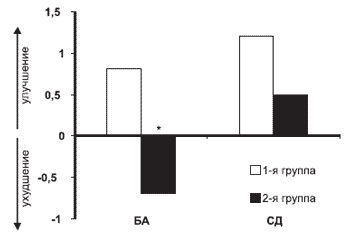 |
| Рис. 3. Терапевтический эффект в отношении показателей когнитивного функционирования по шкале MMSE у больных БА и СД в 1-й и 2-й группах больных. |
У больных СД не выявлено достоверных различий в эффекте терапии по динамике суммарных оценок шкалы MMSE к моменту окончания терапии ни в 1-й, ни во 2-й группе по сравнению с исходным уровнем. В обеих группах у больных СД наблюдалась положительная динамика суммарных среднегрупповых показателей, однако различия между группами не были достоверными (см. рис. 3). У больных СД, леченных карницетином (1-я группа), достоверно улучшилось воспроизведение 3 ранее запомненных слов после интерференции. Во 2-й группе достоверной положительной динамики не наблюдалось ни по одному из пунктов шкалы MMSE.
Динамика выполнения больными теста рисования часов
Достоверная положительная динамика средних суммарных оценок по тесту рисования часов отмечена только в 1-й группе к окончанию периода терапии (табл. 3).
| Шкала | 1-я группа | 2-я группа | ||
| 0 день | через 12 нед | 0 день | через 12 нед | |
| Тест рисования часов | 2,5±0,9 | 2,6±1,0* | 2,5±0,8 | 2,6±0,9 |
| IADL | 16,3±4,2 | 15,7±4,7 | 13,8±3,8 | 14,0±4,7 |
| Модифицированные субтесты шкалы Маттиса | ||||
| инициация | 28,0±4,3 | 28,8±5,1* | 28,8±3,8 | 28,7±4,7 |
| концептуализация | 18,2±2,9 | 18,5±3,2 | 18,9±2,6 | 18,8±2,9 |
| память | 7,3±3,4 | 7,6±3,9 | 8,0±3,4 | 8,2±3,7 |
| Примечание. * — p | ||||
Динамика когнитивных функций по субтестам шкалы Маттиса
Оценка когнитивных функций производилась по следующим субтестам шкалы MDRS: «инициация», «концептуализация» и «память».
Только у больных, леченных карницетином (1-я группа) была установлена статистически достоверная положительная динамика средних оценок по субтесту «инициация», который включает исследование вербальных ассоциаций, динамического праксиса, реципрокной координации и графомоторной пробы (см. табл. 3, рис. 4).
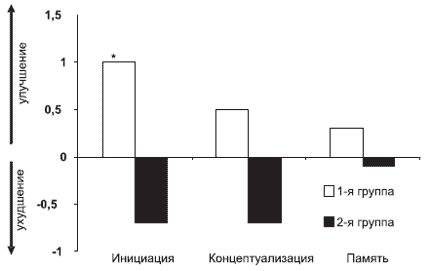 |
| Рис. 4. Динамика показателей когнитивного функционирования по сравнению с исходным уровнем по шкале Маттиса у больныхБА в 1-й и 2-й группах больных. |
Анализ динамики когнитивного функционирования больных БА по шкале Маттиса показал определенные различия между терапевтическими группами. У больных 1-й группы наблюдалось улучшение состояния когнитивных функций по всем субтестам шкалы, тогда как во 2-й группе эти показатели ухудшились (cм. рис. 4). Что касается динамики показателей по шкале Маттиса у больных СД, то в этом случае существенных различий между терапевтическими группами отмечено не было (рис. 5).
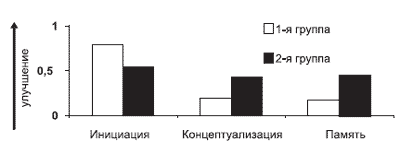 |
| Рис. 5. Динамика показателей когнитивного функционирования по сравнению с исходным уровнем по шкале Маттиса у больных СД в 1-й и 2-й терапевтических группах. |
Динамика функциональных нарушений по шкале IADL Улучшение по шкале IADL (изменение среднегрупповой оценки к периоду окончания терапии) у больных 1-й группы было достоверным по сравнению с больными 2-й группы, т.е. нарушения повседневной активности у больных 1-й группы достоверно уменьшились по сравнению с пациентами 2-й (рис. 6). Тенденция была отмечена у больных БА: в 1-й группе к моменту окончания терапии наблюдалось улучшение (недостоверное) этого показателя (–0,6 балла), а во 2-й группе — недостоверное ухудшение (+0,8 балла) (рис. 7).
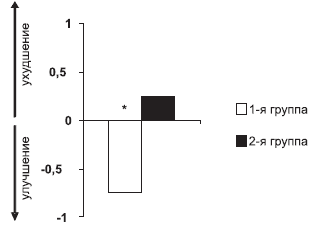 |
| Рис. 6. Динамика показателей нарушений повседневной активности по шкале IADL по сравнению с исходным уровнем в 1-й и 2-й группах больных. |
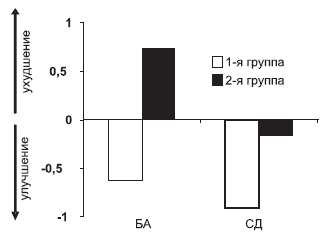 |
| Рис. 7. Динамика показателей нарушений повседневной активности по шкале IADL по сравнению с исходным уровнем у больных БА и СД в 1-й и 2-й группах больных. |
У больных СД в обеих терапевтических группах установлено улучшение (недостоверное) среднегрупповой оценки по шкале IADL по сравнению с началом терапии, соответственно в 1-й группе на –0,8 балла, во 2-й — на –0,2 балла (см. рис. 7).
Эффективность терапии по шкале CGI
Анализ эффективности терапии по шкале CGI показал, что доля больных, состояние которых улучшилось в процессе лечения, была в 1,5 раза больше в 1-й группе по сравнению со 2-й (соответственно 56,7 и 20,0%), при этом доля больных с незначительным ухудшением состояния на момент окончания терапии в 1-й группе составила 13,3%, а во 2-й — 33,3% (рис. 8).
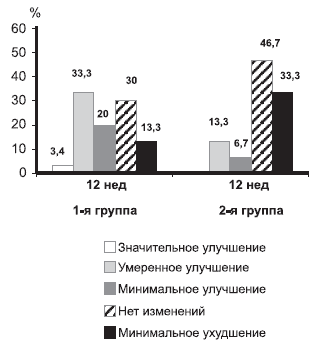 |
| Рис. 8. Разделение больных (в %) по эффективности терапии через 12 нед по показателям шкалы CGI в 1-й и 2-й группах больных. |
Среди больных БА из 1-й группы доля пациентов, имевших ту или иную степень улучшения по шкале CGI на момент окончания терапии, оказалась достоверно большей по сравнению со 2-й группой (соответственно 56,3 и 6,7%) и, наоборот, во 2-й группе оказалось достоверно больше больных БА с ухудшением состояния по сравнению с 1-й группой (соответственно 46,7 и 6,3%) (рис. 9).
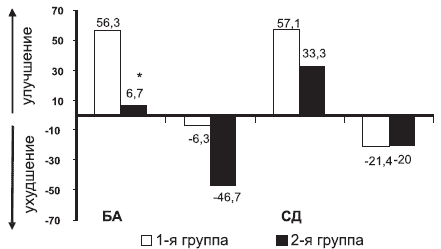 |
| Рис. 9. Распределение больных БА и СД (%) по эффективности терапии по показателям шкалы CGI в 1-й и 2-й группах больных. |
У больных СД различия по шкале CGI между группами были статистически недостоверными, хотя в 1-й группе оказалось почти в 1,7 раза больше пациентов с улучшением состояния по сравнению со 2-й группой (см. рис. 9).
Осложнения и нежелательные эффекты терапии
Серьезных нежелательных явлений не было установлено ни в одной из групп больных.
Нежелательные эффекты терапии наблюдались у 4 (13,3%) больных 1-й группы и у 1 (3,3%) больного 2-й группы. Преждевременно прервана терапия из-за нежелательных эффектов (тошнота, рвота, развившиеся на 2-й нед терапии) только у 1 больного из 2-й группы. У 2 пациентов 1-й группы через 4 нед после начала терапии появились симптомы речедвигательной гиперактивности. У одного из них одновременно усилились имевшиеся ранее конфабуляторные расстройства и бредовые идеи ущерба. После назначения нейролептической терапии (сонапакс, пропазин) выраженность этих явлений значительно уменьшилась. У 2 больных 1-й группы на 4-й нед терапии (доза 3000 мг в сутки) появились тошнота, вялость, но после снижения дозы до 2250 мг в сутки эти явления прошли и больные успешно завершили курс терапии.
Лабораторные анализы и ЭКГ
У 16 больных (по 8 в 1-й и во 2-й группах) к моменту окончания терапии было установлено клинически незначимое повышение АСТ и АЛТ. У 4 пациентов 1-й группы, напротив, к моменту окончания лечения изначально повышенные уровни АСТ и АЛТ нормализовались.
У 5 больных 2-й группы незначительно повысился уровень глюкозы в крови, 3 из них страдали сахарным диабетом до начала исследования.
У 3 больных из 1-й и 1 больного из 2-й группы клинически незначимо повысились уровни холестерина и креатинина. Незначительное повышение уровня мочевины было обнаружено у 2 больных (по 1 больному в каждой группе).
На ЭКГ клинически незначимая отрицательная динамика отмечалась у 4 больных 1-й группы и 2 больных 2-й группы: усиление брадикардии — по 1 больному в каждой группе; замедление внутрижелудочковой проводимости — у 1 больного из 2-й группы; синусовая аритмия — у 2 больных 1-й группы; усиление синусовой тахикардии — у 1 больного из 1-й группы.
У 5 больных 1-й группы и 1 больного из 2-й группы после окончания курса терапии, напротив, отмечалась положительная динамика ЭКГ-показателей.
Обсуждение
Двойное слепое плацебо-контролируемое исследование, проведенное в параллельных группах больных БА и СД с начальной (мягкой) деменцией, равных по численности (по 30 человек в каждой группе) и практически идентичных по диагностическому распределению, возрасту больных и тяжести когнитивного дефицита к началу исследования, позволило установить терапевтическую эффективность карницетина, применявшегося в дозах 2250—3000 мг в сутки, по сравнению с плацебо. Оценка эффективности терапии (по шкале CGI) показала достоверно большую частоту (в 2,8 раза) наступления позитивного эффекта у больных, получавших карницетин по сравнению с группой плацебо. Терапевтический эффект карницетина подтвержден достоверным улучшением когнитивных функций больных (при оценке по когнитивным шкалам: MMSE, тесту рисования часов и одному из субтестов («инициация») шкалы Маттиса по сравнению с эффектом терапии в группе плацебо. По ряду других когнитивных тестов (в частности, субтестам шкалы Маттиса «концептуализация» и «память») также установлены преимущества карницетина по сравнению с плацебо, которые, однако, не достигли уровня статистической достоверности. Эффективность карницетина подтверждается также достоверно большим (по сравнению с группой плацебо) терапевтическим эффектом в отношении нарушений повседневного функционирования (оценка по шкале IADL).
Терапевтический эффект в отношении общего клинического улучшения состояния больных (шкала CGI) был достоверно выше у больных БА по сравнению с больными СД. Различия в терапевтическом эффекте карницетина у больных БА и СД не зависели от исходной тяжести когнитивного дефицита.
Терапевтический эффект в отношении когнитивного функционирования оказался достоверно более значимым у больных БА (по шкале MMSE, субтесту «инициализация» шкалы Маттиса, оценивающим ассоциативную деятельность, динамический праксис, реципрокную координацию, а также письмо и рисунок). Больший терапевтический эффект по субтестам «память» и «концептуализация» также отмечался при БА по сравнению с СД, однако, различия по динамике этих показателей не достигали уровня статистической достоверности.
Терапевтический эффект карницетина в отношении расстройств повседневного функционирования также оказался более выраженным (однако, не на уровне статистической достоверности) у больных БА по сравнению с СД.
Была подтверждена безопасность препарата и его хорошая переносимость (серьезных нежелательных явлений не наблюдалось).
Таким образом, при двойном слепом плацебоконтролируемом исследовании, проведенном в параллельных группах больных с мягкой (начальной) деменцией, обусловленной БА и СД, была установлена терапевтическая эффективность карницетина по сравнению с плацебо и хорошая переносимость препарата.
Полученные результаты позволяют рекомендовать карницетин в дозах от 2250 до 3000 мг в сутки для применения у больных с БА и СД на начальной стадии заболевания.
Литература
1. Воронина Т.А., Островская Р.У. Отчет об экспериментальном изуче- нии нейропсихотропной активности ацетил-L-карнитина. НИИ фармакологии РАМН. М 2000.
2. Amenta F., Ferrante F., Lucreziotti R. et al. Reduced lipofuscin accumulation in senescent rat brain by long-term acetyl-L-carnitine treatment. Arch Gerontol Geriatr 1989; 9: 147—153.
3. Angelucci L., Ramacci M.T., Taglialatela G. et al. Nerve growth factor binding in aged rat central nervous system: effect of acetyl-L-carnitine. J Neurosci Res 1988; 20: 491—496.
4. Bagetta V., Barone I., Ghiglieri V. Acetyl-l-Carnitine selectively prevents post-ischemic LTP via a possible action on mitochondrial energy metabolism. Neuropharmacology 2008; 55: 2: 223—229.
5. Bianchetti A., Rozzini R., Trabucchi M. Effects of acetyl-L-carnitine in Alzheimer’s disease patients unresponsive to acetylcholinesterase inhibitors. Curr Med Res Opin 2003; 19: 4: 350—353.
6. Bremer J. Carnitine-metabolism and functions. Physiol Rev 1983; 63: 1420—1480.
7. Brooks J.O. 3rd, Yesavage J.A., Carta A., Bravi D. Acetyl-L-carnitine slows decline in younger patients with Alzheimer’s disease: a reanalysis of a double- blind, placebo-controlled study using the trilinear approach. Int Psychoger 1998; 10: 193—203.
8. Calvani M., Arrigoni-Martelli E. Attenuation by acetyl-L-carnitine of neurological damage and biochemical derangement following brain ischemia and reperfusion. Int J Tissue React 1999; 21: 1—6.
9. Castorina M., Ambrosini A.M., Pacific L. et al. Age-dependent loss of NMDA receptors in hippocampus, striatum, and frontal cortex of the rat: prevention by acetyl-L-carnitine. Neurochem Res 1994; 19: 795—798.
10. Epis R., Marcello E., Gardoni F. et al. Modulatory effect of acetyl-l-carnitine on amyloid precursor protein metabolism in hippocampal neurons. Eur J Pharmacol 2008; 597: Issues 1—3: 51—56.
11. Hagen T.M., Moreau R., Suh J.H., Visioli F. Mitochondrial decay in the aging rat heart. Ann NY Acad Sci 2002; 959: 491—507.
12. Harsing L.G.Jr., Sershen H., Toth E. et al. Acetyl-L-carnitine releases dopamine in rat corpus striatum: an in vivo microdialysis study. Eur J Pharmacol 1992; 218: 117—121.
13. Imperato A., Ramacci M.T., Angelucci L. Acetyl-Lcarnitine enhances acetylcholine release in the striatum and hippocampus of awake freely moving rats. Neurosci Lett 1989; 107: 251—255.
14. Soczynska J.K., Kennedy S.H., Chow C.S.M. Expert Opin Investig Drugs 2008; 17: 6: 827—843.
15. Montgomery S.A., Thal L.J., Amrein R. Meta-analysis of double blind randomized controlled clinical trials of acetyl-L-carnitine versus placebo in the treatment of mild cognitive impairment and mild Alzheimer’s disease. Int Clin Psychopharmacol 2003; 18: 61—71.
16. Pascale A., Milano S., Corsico N. et al. Protein kinase C activation and antiamnesic effect of acetyl-L-carnitine: in vitro and in vivo studies. Eur J Pharmacol 1994; 65: 1—7.
17. Pettegrew J.W., Klunk W.E., Panchalingam K. et al. Clinical and neurochemical effects of acetyl-L-carnitine in Alzheimer’s disease. Neurobiol Aging 1995; 16: 1—4.
18. Pettegrew J.W., Levine J., McClure R.J. Acetyl-L-carnitine physical-chemical, metabolic, and therapeutic properties: relevance for its mode of action in Alzheimer’s disease and geriatric depression. Molecular Psychiatry 2000; 5: 616—632.
19. Piovesan P., Pacifici L., Taglialatela G. et al. Acetyl-L-carnitine treatment increases choline acetyltransferase activity and NGF levels in the CNS of adult rats following total fimbria-fornix transection. Brain Res 1994; 633: 77—82.
20. Sano M., Bell K., Cote L. et al. Double-blind parallel design pilot study of acetyl levocarnitine in patients with Alzheimer’s Disease. Arch Neurol 1992; 49: 1137—1141.
21. Taglialatela G., Caprioli A., Giuliani A. et al. Spatial memory and NGF levels in aged rats: natural variability and effects of acetyl-L-carnitine treatment. Exp Gerontol 1996; 31: 577—587.
22. Tempesta E., Janiri L., Pirrongelli C. Stereospecific effects of acetylcarnitine on the spontaneous activity of brainstem neurones and their responses to acetylcholine and serotonin. Neuropharmacology 1985; 24: 43—50.
23. Thal L.J., Carta A., Clarke W.R. et al. A 1-year multicenter placebo-controlled study of acetyl-L-carnitine in patients with Alzheimer’s Disease. Neurology 1996; 47: 705—711.
24. Toth E., Harsing L.G., Sershen H. et al. Effect of acetyl-L-carnitine on extracellular amino acid levels in vivo in rat brain regions. Neurochem Res 1993; 18: 573—578.
25. White H.L., Scates P.W. Acetyl-L-carnitine as a precursor of acetylcholine. Neurochem Res 1990; 15: 597—601.



