Психовегетативные, астенические и когнитивные нарушения при дисплазии соединительной ткани: выбор оптимальной терапии
СтатьиОпубликовано в журнале:
Фарматека № 7 — 2012
С.Н. Дума, О.В. Лисиченко, Г.В. Лукьянова
НИИ терапии СО РАМН, Новосибирск Представлены результаты оценки эффективности и безопасности использования препарата ацетил-L-карнитин (Карницетин) при астенических, психовегетативных и когнитивных нарушениях для 60 пациентов с дисплазией соединительной ткани в сравнении с немедикаментозной и общеукрепляющей терапией. Установлено, что терапия Карницетином ослабляет проявления астении, уменьшает неврологическую и вегетативную симптоматику, способствует значимому улучшению по всем когнитивным шкалам.
Ключевые слова: дисплазия соединительной ткани, астенические нарушения, психовегетативные нарушения, когнитивные нарушения, ацетил-L-карнитин
The article presents the results of the evaluation of the efficacy and safety of use of acetyl-L-carnitine (Carnicetine) in asthenic, psycho-vegetative and cognitive impairment in 60 patients with connective tissue dysplasia in comparison with non-pharmacological and bracing therapy. It was found that the therapy with Carnicetine reduces the manifestations of asthenia, reduces neurological and vegetative symptoms with significant improvement in all cognitive scales.
Key words: connective tissue dysplasia, asthenic disorders, psychovegetative disorders, cognitive impairment, acetyl-L-carnitine
Одно из первых мест среди наследственных болезней занимают синдромы, связанные с нарушением биосинтеза или деградацией волокнистых структур соединительной ткани (СТ). Дисплазия СТ (ДСТ) – это нарушение развития СТ в эмбриональном и постнатальном периодах, которое происходит вследствие генетически измененного фибриллогенеза внеклеточного матрикса. ДСТ приводит к расстройству гомеостаза на тканевом, органном и организменном уровнях в виде различных морфофункциональных нарушений со стороны висцеральных и локомоторных органов с прогредиентным течением. При ДСТ наблюдаются весьма разнообразные клинические проявления, т. к. универсальных патологических повреждений СТ не существует [1].
Наиболее характерные клинические проявлениями ДСТ:
- скелетные изменения: астеническое телосложение, долихостеномелия (непропорционально длинные конечности), арахнодактилия (длинные тонкие пальцы), различные виды деформации грудной клетки (сколиозы, кифозы и лордозы позвоночника, синдром “прямой спины”), плоскостопие и др.; эти изменения связаны с нарушением строения хряща и задержкой созревания эпифизарной зоны роста, что проявляется удлинением трубчатых костей; в основе деформаций грудной клетки лежит неполноценность реберных хрящей;
- изменения со стороны кожи: гиперэластичность, истончение, склонность к травматизации и образованию шрамов в виде “папиросной бумаги” или келоидных рубцов;
- изменения со стороны мышечной системы: уменьшение мышечной массы, в т. ч. сердечной и глазодвигательной мускулатуры, что приводит к снижению сократительной способности миокарда и миопии;
- патология суставов: чрезмерная подвижность (гипермобильность), склонность к вывихам и подвывихам, обусловленная слабостью связочного аппарата;
- патология органов зрения: одно из самых частых проявлений ДСТ, представлено миопией различной степени, дислокацией хрусталика, увеличением длины глазного яблока, плоской роговицей, синдромом голубых склер;
- поражения сердечно-сосудистой системы, которые весьма разнообразны и нередко определяют прогноз; обычно диагностируются анатомические изменения клапанов сердца: дилатация фиброзных колец и пролапсы, аномальные хорды, расширение восходящего отдела аорты и легочной артерии с последующим формированием мешотчатой аневризмы; кроме того, деформации грудной клетки и позвоночника приводят к развитию различных типов торакодиафрагмального сердца;
- поражение сосудов проявляется аневризматическими расширениями артерий среднего и мелкого калибра и очень часто – варикозным расширением вен нижних конечностей;
- бронхолегочные поражения касаются как бронхиального дерева, так и альвеол; чаще всего диагностируют бронхоэктазы, простую и кистозную гипоплазию, буллезную эмфизему и спонтанный пневмоторакс;
- с патологией почек связывают нефроптоз и реноваскулярные изменения.
К неврологическим симптомам ДСТ относят разнообразные проявления вертеброгенного синдрома в виде ювенильного остеохондроза, межпозвонковых грыж, спондилолистеза, вертебробазилярной недостаточности. Однако в структуре клинической симптоматики пациентов с ДСТ наиболее часто лидируют психовегетативные нарушения, такие как вегетососудистая дистония, нейро-циркуляторная дистония, панические атаки. Они формируются одними из первых уже в раннем детстве и рассматриваются как обязательный компонент диспластического фенотипа. У пациентов с ДСТ часто обнаруживается также астенический синдром, который проявляется снижением работоспособности, ухудшением переносимости физических и психоэмоциональных нагрузок, повышенной утомляемостью, когнитивными нарушениями нейродинамического типа. Он выявляется в дошкольном и школьном, подростковом и молодом возрасте, сопровождая пациентов с ДСТ на протяжении всей жизни.
Наряду с присущими этим пациентам нарушениями в психической сфере в виде невротических расстройств, депрессии, ипохондрии, тревожнофобических расстройств, нервной анорек-сии возникают выраженные проблемы в сфере физической и социальной адаптации. В возрасте 14–15 лет проявления ДСТ усугубляются астеническими, вегетативными, тревожными и когнитивными симптомами. Известно, что пациенты с ДСТ формируют группу повышенного психологического риска с заниженной субъективной оценкой собственных возможностей, сниженными уровнями претензий, эмоциональной устойчивости и работоспособности, повышенными уровнями тревожности, ранимости, депрессивности. Закономерным следствием психологического дистресса становится ограничение социальной активности, ухудшение качества жизни и значительное снижение социальной адаптации, наиболее актуальные в подростковом возрасте.
Указанные синдромы тесно связаны с вопросами профессиональной подготовки, профессиональной пригодности и прогноза жизни подростков. Зачастую эта достаточно многочисленная группа пациентов остается без адекватной коррекции. Поэтому на сегодняшний день весьма актуальна проблема профилактики и лечения больных ДСТ с астеноневротическими, тревожновегетативными и когнитивными синдромами.
Традиционно при лечении ДСТ рекомендуют широко использовать такие методы, как психологическая поддержка, индивидуализация режима дня, лечебная физкультура, физиотерапия и массаж. Важна и диетотерапия с учетом повышенной потребности пациента в белках, незаменимых аминокислотах и микроэлементах. К медикаментозным методам следует отнести применение препаратов, позволяющих стимулировать коллагенообразование. Это прежде всего аскорбиновая кислота, препараты мукополисахарид-ной природы (хондроитинсульфат), витамины группы В (В1, В2, В3, В6) и микроэлементы (медь, цинк, магний). Рекомендовано включать в схемы лечения курсовую метаболическую терапию [5]. Специального обсуждения заслуживает терапия ацетил-L-карнитином (Карницетин; ООО “ПИК-ФАРМА”, Россия). L-карнитин (ЛК) и его производные, такие как ацетил-L-карнитин (АЛК), выполняют в организме человека важнейшую функцию. Они переносят остатки жирных кислот из цитоплазмы в матрикс митохондрий для образования энергии, необходимой для функционирования всех клеток, тканей и систем организма [2, 9]. В последние года АЛК начал широко использоваться в коррекции митохондриальных дисфункций различной этиологии наряду с ЛК и коэнзимом-Q [2, 3, 5]. Анализ многочисленных литературных источников позволяет сделать вывод, что АЛК имеет дополнительные, отличные от ЛК фармакологические свойства, которые позволяют использовать его в качестве лекарственного средства при астенических, психовегетативных и когнитивных нарушениях. Он свободно проходит через гематоэнцефаличе-ский барьер, легче усваивается клеточными структурами и быстрее включается в митохондрии, может функционировать как донор ацетильной группы для молекулы холина, образуяацетилхолин, и более эффективен, чем ЛК, в нейропротекции, улучшая когнитивные функции [3, 10]. Показано, что АЛК влияет на работу мозга за счет широкого спектра нейрохимических свойств: повышает клеточную концентрацию аспартата и таурина, при длительном введении увеличивает плотность NMDA-рецепторов. АЛК способен модулировать эффекты не только холинергической, но и дофа-минергической системы, усиливает действие серотонина, защищает клетки мозга от избытка глутамата и аммиака, чем можно объяснить его выраженное нейропротекторное действие [11–13, 15, 16].
Целью настоящего исследования явилась оценка клинической эффективности и переносимости АЛК (Карницетина) при лечении пациентов с ДСТ с выраженными астеноневро-тическими, тревожновегетативными и когнитивными синдромами.
Материал и методы
Объектом открытого сравнительного клинического исследования стали 60 пациентов с подтвержденным диагнозом ДСТ, находящихся на диспансерном учете у генетика в поликлинике НИИ терапии СО РАМН. Средний возраст больных составил 21,5 года.
Критерии исключения из исследования:
- лечение препаратами, влияющими на функции центральной нервной системы в течение 4 недель, предшествующих началу исследования;
- нестабильные сопутствующие заболевания, требующие лечения изменяющимися дозировками лекарств;
- депрессии в анамнезе или при оценке по шкале Гамильтона (> 10 баллов);
- наличие признаков хронического алкоголизма, лекарственной и наркотической зависимости;
- беременность.
Пациенты были распределены в две группы: основную (1-я группа) и контрольную (2-я группа). Пациенты 1-й группы получали монотерапию АЛК в суточной дозе 0,5 г (2 капсулы Карницетина по 295 мг). Пациентам контрольной группы проводили стандартную терапию ДСТ (немедикаментозная терапия: адекватный режим, лечебная физкультура, диетотерапия – использование продуктов, обогащенных белком, витаминами и микроэлементами, препараты магния) в течение 8 недель.
В программу обследования входили оценка соматического статуса (артериальное давление, частота сердечных сокращений, антропометрические данные, анализы мочи и крови, электрокардиография, ультразвуковое исследование сердца и почек); изучение когнитивных функций с использованием таблиц Шульте (исследование скорости обработки информации, концентрации внимания; норма – 40–50 секунд), теста Векслера (исследование скорости обработки информации, зрительно-моторной координации и избирательного внимания; норма – 40 секунд и более), теста 12 слов Гробера–Бушке (сумма непосредственного и отсроченного воспроизведения), Монреальской шкалы когнитивных нарушений (норма – сумма баллов не менее 26).
Применены следующие методы оценки вегетативных нарушений.
Опросник для выявления признаков вегетативных нарушений (заполняется пациентом); норма – до 15 баллов, сумма более 15 баллов говорит о высокой вероятности наличия синдрома вегетативной дисфункции (Вейн А.М., 1998).
Схема исследования для выявления признаков вегетативных нарушений (заполняется врачом); норма – до 25 баллов, сумма более 25 баллов говорит о высокой вероятности наличия синдрома вегетативной дисфункции (Вейн А.М.,1998).
Психовегетативные и астенические расстройства исследовались с помощью следующих шкал:
- Шкала Гамильтона для оценки тревоги (HARS); критерии оценки: 6 баллов и меньше – норма, 7–13 баллов – могут быть тревожные расстройства, 14–20 баллов – тревога, 21–28 баллов – симптоматическая тревога, более 29 баллов – выраженная тревога.
- Шкала субъективной оценки астении (MFI-20); показатели астении оценивались по 5 субшкалам: общая астения (норма до 12), физическая астения (норма до 12),снижение активности (норма до 12), снижение мотивации (норма до 12), психическая астения (норма до 12).
- Шкала глобального клинического воздействия для оценки улучшения (CGI-I); сравнительная оценка 1-й и 2-й групп.
- Шкала общего впечатления пациента; сравнительная оценка 1-й и 2-й групп.
Статистическая обработка данных используемых тестов и шкал проводилась при помощи компьютерной программы SPSS, версия 11.5. Для обработки данных использовались непараметрические критерии Уилкоксона– Манна–Уитни. При сравнении вариационных рядов учитывались достоверные различия.
Результаты исследования
У пациентов двух исследуемых групп выявлены: астенический синдром – 98 %; тревога – 95%; вегетативные симптомы – 82%; когнитивные нарушения – 47 %. Оценка астенических расстройств в основной группе к 60-му дню терапии показала, что у пациентов, получавших АЛК, достоверно уменьшились проявления общей астении (p Было выявлено статистически значимое улучшение по нейродинамическим когнитивным шкалам: Гробера–Бушке и Шульте (p Установлен благоприятный профиль безопасности АЛК в суточной дозе 0,5 г/сут. Побочные эффекты в 1-й группе наблюдались у 3 пациентов, во 2-й группе – у 1; из исследования никто не выбыл. Основными жалобами, предъ-являемыми пациентами в начале тера-пии, были дискомфорт в желудке и тошнота – 4 человека.
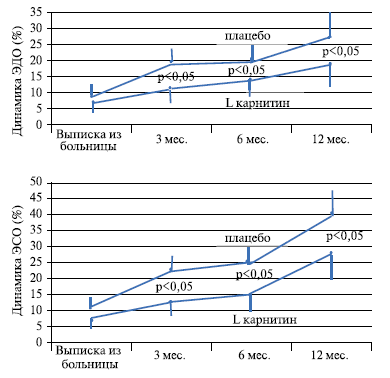
Рис. 1. Оценка динамики астенических нарушений (MFI-20) в основной группе до и после лечения Карницетином
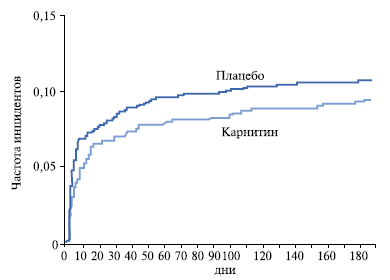
Рис. 2. Оценка динамики тревожно-вегетативных и когнитивных нарушений в основной группе до и после лечения Карницетином
Сравнение результатов лечения в группах показало, что по шкале общего впечатления самого пациента к 30-му дню лечения существенных различий между основной и контрольной группами не наблюдалось, однако к концу исследования количество позитивных ответов в 1-й группе было существенно большим, чем во 2-й: значительно преобладало мнение об улучшении и сильном улучшении, тогда как в группе сравнения у половины пациентов улучшение было незначительным или отсутствовало (в основной группе – у 6,6 %; рис. 3).
Оценка динамики состояния пациентов по шкале клинического воздействия–улучшения СGI-I в группах показала, что к 30-му дню лечения Карницетином частота улучшения и сильного улучшения составила в 1-й группе 90 % (оценка базировалась не только на субъективном мнении пациента, но и на динамике исследуемых шкал), тогда как во 2-й группе подобная оценка имела место только среди 46,6 % пациентов (почти в 2 раза реже). Более выраженная положительная динамика (76,7 % больных с выраженным улучшением против 50,1 %) сохранялась в основной группе и на момент завершения лечения (рис. 4).
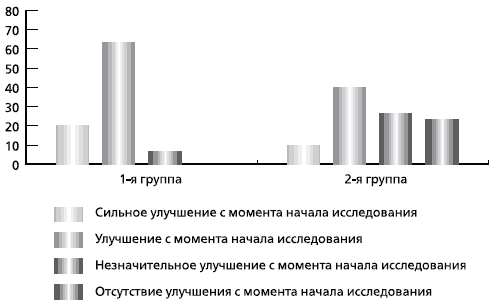
Рис 3. Распределение доли пациентов по шкале общего впечатления на 60-й день лечения в основной (1-й) группе и контрольной (2-й) группе
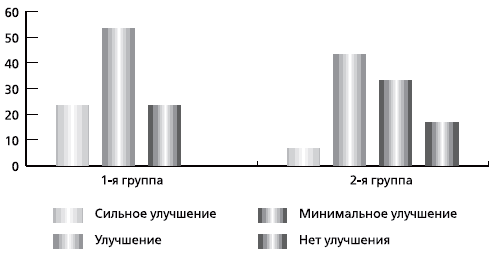
Рис 4. Сравнительная динамика по шкале клинического воздействия-улучшения CGI-I в двух исследуемых группах на 60-й день терапии г/сут. Побочные эффекты в 1-й группе наблюдались у 3 пациентов, во 2-й группе – у 1; из исследования никто не выбыл. Основными жалобами, предъявляемыми пациентами в начале терапии, были дискомфорт в желудке и тошнота – 4 человека.
Выводы
- У пациентов с ДСТ выявлена следующая неврологическая симптоматика: астенический синдром – 98 %; тревога – 95 %; симптомы вегетативной дисфункции – 82 %; когнитивные нарушения – 47 %.
- Карницетин в суточной дозе 0,5 г/сут статистически достоверно снизил проявления общей астении, психической астении (p Включение Карницетина (0,5 г/сут) в терапию пациентов с ДСТ достоверно уменьшает неврологическую симптоматику.
- Выявлено статистически значимое улучшение по всем исследуемым когнитивным шкалам у получавших Карницетин пациентов. Клинически значимое улучшение ряда когнитивных функций нейродинамического типа (концентрация внимания, скорость выполнения заданий, память) и общего самочувствия пациентов отмечено к 30-му дня терапии.
- На 60-й день исследования при лечении Карницетином статистически достоверно снизились тревожность. Установлен благоприятный профиль безопасности Карницетина в дозе 0,5 г/сут.
Литература
- Кадурина Т.И., Горбунова В.Н. Дисплазия соединительной ткани. Руководство для врачей. СПб., 2009. 714 с.
- Копелевич В.М. Применение ацетил L-карнитина (карницетин) в клинической практике. Методическое пособие. М., 2010, 28 с.
- Копелевич В.М. Витаминоподобные соединения L-карнитина и ацетил-Lкарнитина:от биохимических исследований к медицинскому применению // Укр. биохим. журн. 2005. № 77. С. 24-45.
- Нечаева Г.И., Викторова И.А. Дисплазии соединительной ткани: терминология, диагностика, тактика ведения пациентов. Омск, 2007. 188 с.
- Сухоруков В.С. К разработке рациональных основ энерготропной терапии // Рациональная фармакотерапия 2007. № 2. С. 40-47.
- Торшин И.Ю., Громова О.А. Дисплазии соединительной ткани, магний и нуклеотидные полиморфизмы // Кардиология 2008. № 10. С. 57-64.
- Шабалов Н.П., Арсентьев В.Г. Педиатрия: национальное руководство. М., 2009. № 1. С. 298-320.
- Aliev G, Liu J, ShenkJC, et al. Neuronal mitochondrial energy metabolism. Neuropharmacol 2008;55(2):223-29.
- Angelucci L, Ramacci MT, Taglialatela G, et al. Nerve growth factor binding in agedrat central-nervous system:effect of acetyl-L-carnitine. J Neurosci Res 1988;20:491-96.
- Bremer J. Carnitine-metabolism and functions. Physiol Rev 1983;63:1420-80.
- Castorina M, Ambrosini AM, Pacific L, et al. Agt-dependent loss of NMDA receptors in hippocampus, stpiatum andfrontal cortex of the rat: prevention by acetyl-Lcarnitine. Neurochem Res 1994;19:795-98.
- Harsing LG Jr, Sershen H, Toth E, et al. Acetyl-Lcarnitine releases dopamine in ratcorpus striatum: an in vivo microdialysis study. Eur J pharmacol 1992;218:117-21.
- ImperatoA, Rammacci MT, Angelucci L. Acetyl-Lcarnitine enhances acetylcholine release in the striatum and hippocampus of awakefreely moving rats. Neurosci Lett 1989;107:251-55.
- Liu J, Head E, Kuratsune H, et al. Comparison of the effekts of L-carnitine Ann NY Acad Sci 2004;1033:117-31.
- Pettegrew JW, Levine J, McClure RJ, Acetyl-Lcarnitine physical-chemical, metabolic, andtherapeutic properties: relevance for its mode of action in Alzheimers disease and geriatric depression. Molecul Psychiat 2000; 5:616-32.
- Tempesta E, Janiri L, Pirrongelli C. Stereospecific effects of acetylcarnitineon the spontaneous activity of brainstem neurones and their responses to acetyicholine and serotonin. Neuropharmacology 1985;24: 43-50.
- Tsuji A. Functional relevance of carnitine transporter OCTN2 tobrain distribution of L-carnitine and acetyl-Lcarnitine across the blood-brainbarrier. J Neirochem 2001 ;79: 959-69.
Информация об авторах:
Дума Светлана Николаевна – кандидат медицинских наук, старший научный сотрудник, заведующая консультативно-диагностическим отделением клиники, врач-невролог ФГБУ НИИ терапии СО РАМН.
Лисиченко Ольга Вадимовна – кандидат медицинских наук, доцент, врач-генетик консультативно-диагностического отделения клиники ФГБУ НИИ терапии СО РАМН.
Лукьянова Галина Витальевна – клинический ординатор-терапевт ФГБУ НИИ терапии СО РАМН.



