Метаанализ применения ацетил-L-карнитина при диабетическом периферическом нейропатии
СтатьиОпубликовано в журнале:
« РМЖ » №4, 2017
Резюме
Роль дефицита ацетил-L-карнитина (АЛК) и L-карнитина (ЛК) в развитии периферической диабетической нейропатии обсуждается в литературе, но клинических подтверждений этому имеется мало.
В проведенный метаанализ включено 6 статей, в которых суммарное число больных диабетом составило 711. Данные 3-х РКИ,в которых 340 больных лечились АЛК и сравнивались с 203, получавшими плацебо, и со 115 пациентами, получавшими метилкобаламин, показали, что АЛК уменьшает болевые ощущения (СPС= -0,45; 95% ДИ: от -0,86 до -0,04; P=0,03; I2=85%). По сравнению с контролем добавление АЛК увеличивало как скорость прохождения импульса, так и амплитуду реакции, что было показано на примере сенсорной и моторной составляющих локтевого нерва. По сравнению с исходными показателями добавление АЛК/ЛК увеличивало скорость проведения нервных импульсов по всем исследованным чувствительным и моторным волокнам (за исключением локтевого и малоберцового нервов), а также амплитуду реакции для каждого из нервов.
Неблагоприятные явления обычно ограничивались минимальными побочными эффектами.
Было доказано, что АЛК уменьшает боли, обусловленные диабетической полинейропатией, по сравнению с активным и плацебо-контролем, кроме того, при той же патологии АЛК улучшал электромиографические показатели.
Ключевые слова: ацетил-L-карнитин, нейропатия, диабет, метаанализ.
Для цитирования: Метаанализ применения ацетил-L-карнитина при диабетической периферической нейропатии //РМЖ. 2017. № 4. С. 1-1.
Abstract
Meta-analysis of the use of acetyl-L-carnitine with diabetic peripheral neuropathy
The role of deficiency of acetyl-L-carnitine (ALC) and L-carnitine (LC) in the development of peripheral diabetic neuropathy is discussed in the literature, but there is little clinical evidence for this.
The meta-analysis includes six articles, with the total number of 711 diabetic patients. Three RCTs (340 patients were treated with ALC vs. 203 placebo and 115 patients received methylcobalamine) showed that ALC reduces pain perception (SMD = 0.45; 95% CI: 0.86 to 0.04; P = 0.03; 12 = 85%). Compared to control, the addition of ALC increased both nerve conduction velocity and amplitude response for ulnar nerve (both sensory and motor component). Compared to baseline values, the addition of ALC/LC improved the nerve conduction velocity for all the sensory and motor nerves (except ulnar and peroneal) and the response amplitude for each of the nerves. Adverse events were usually limited to minimal side effects.
It has been proved that ALC reduces the pain caused by diabetic polyneuropathy, compared with active and placebo-controls, and improves electromyographic parameters in these patients.
Key words: Acetyl-L-carnitine, neuropathy, diabetes, meta-analysis.
For citation: Meta-analysis of the use of acetyl-L-carnitine with diabetic peripheral neuropathy //RMJ. 2017. № 4. P. 1-1.
Введение.
Периферическая нейропатия — одно из частых осложнений сахарного диабета (СД), распространенность его колеблется от 12 до 50% [1]. Самой частой формой периферической нейропатии при диабете является дистальная периферическая полинейропатия, при этой форме поражаются как чувствительные, так и моторные нервные волокна [1].
Осложнения диабетической нейропатии весьма многочисленны (например, слабость и парестезия на начальных этапах, а на позднейших этапах — язвы и деформация нижних конечностей). Нередко они имеют результатом инвалидизацию и плохое качество жизни [2], что связано прежде всего с болью — типичной жалобой при диабетической нейропатии [1].
Облегчение симптоматики диабетической сенсорной нейропатии представляет собой непростую задачу для врачей, причем терапевтический арсенал ограничивается обычно оптимизацией контроля над уровнем глюкозы и применением обезболивающих препаратов [3, 4]. Справиться с симптомами такими методами зачастую не удается, ведь они не связаны с патогенезом диабетической нейропатии. Хотя этот патогенез полностью не изучен, но, как представляется, один из главных механизмов заключается в сниженной доступности ацетильных остатков, необходимых для синтеза холина [5]. Фактором, запускающим этот механизм, считается дефицит ацетил-L-карнитина (АЛК) и L-карнитина (ЛК) [6], причем было показано, что недостаточное количество АЛК приводит к повреждению миелиновой оболочки [7]. В моделировании на животных обнаружено, что экзогенно вводимый АЛК повышает содержание артемина и усиливает экспрессию фактора роста нервов (ФРН) [8, 9], способствует антиоксидантной активности [10] и проницаемости мелких сосудов для белков [11], индуцирует долговременную увеличивающую регуляцию пресинаптических рецепторов mGlu2 [12]. Таким образом, добавочное количество АЛК оказывает нейропротективное, нейротрофическое и анальгезирующее воздействие на периферическую нервную систему [12, 13].
Что касается людей, то в методических разработках клиники Меио АЛК рассматривается как средство первого уровня при лечении нейропатической боли [14], и недавний метаанализ подтвердил, что прием АЛК смог облегчить болевые ощущения у людей, страдающих периферической нейропатией [15]. Хотя эта работа позволила пополнить наши знания по данной важной теме, но оставались существенные недоработки. Так, авторы рассматривали все виды нейропатии вместе (хотя патогенез у них разный), кроме того, они не исследовали влияние АЛК на показатели электромиографии (ЭМГ), самого распространенного метода для распознавания и оценки выраженности периферической полинейропатии [1].
Формирование метаанализа
Систематический обзор был проведен в соответствии с рекомендациями PRISMA [16] и MOOSE [17] и следовал структурированному, но неопубликованному протоколу. Критериями включения в данный метаанализ были:
- РКИ или исследования с оценками до и после воздействия;
- у больных диабетом, включенных в исследование, нейропатия должна была быть подтверждена ЭМГ;
- изучалось влияние, оказываемое применением карнитина (независимо от пути введения).
- фиксировались характеристики боли (обусловленной нейропатией) и/или параметры ЭМГ.
Исследования исключались, если:
- в них не изучались люди;
- оценивалось влияние карнитина на другие причины нейропатической боли (например, боль в результате химиотерапии);
- среди субъектов исследования были больные диабетом, у которых отсутствовала нейропатия.
Итоговые показатели
Первым результатом, который выявлялся, было изменение в восприятии боли, что оценивалось в динамике с применением общепринятых шкал (таких как визуальная аналоговая шкала (ВАШ)) как у субъектов, получавших АЛК, так и в группе контроля.
Параметры ЭМГ мы обозначили как результаты второго ряда. К ним относились скорость проведения и амплитуда реакции, что конкретно отображалось в виде отличий исходного и итогового показателя (до и после воздействия АЛК) от таких же параметров в группе контроля; в исследованиях, где больным давались только АЛК/ЛК, итоговые данные сравнивались с начальными.
Количественная оценка качества включала адекватность рандомизации (2 балла), обеспечение слепоты исследования (2 балла), описание случаев выхода из исследования (1 балл). Итоговое значение менее 3-х (при максимально возможных 5 баллах) обычно означает низкое качество работы с высоким риском системных ошибок [18]. Качество, оцененное по шкале Jadad [19], указывает на низкий риск систематических ошибок.
Синтез данных и статистический анализ
Все вычисления выполнялись с применением всестороннего метаанализа (СМА) и методики Revman 5.3. Если были известны итоговые показатели хотя бы 2-х исследований, они подвергались метаанализу, если же исследование было единичным, то его данные мы включали в описательную часть результатов. Когда в какой-либо работе проводилось несколько измерений в динамике, то для анализа бралось последнее из них.
При первом анализе пациенты, получавшие АЛК, сравнивались с группой контроля по параметрам шкал боли. Проводилось сравнение группы АЛК и плацебо по разнице средних значений, полученных при наблюдении в динамике, при этом использовалась стандартная разница средних (СРС) с 95% доверительными интервалами (ДИ), применяя модель «случайность - эффект» [20].
Второй анализ (в отношении ЭМГ) проводился по тем же принципам при рассмотрении пациентов, получавших АЛК при РКИ. Что касается исследований, в которых все больные получали АЛК/ЛК, то оценка ЭМГ ограничивалась сравнением итоговых значений с исходными. Для количественной оценки ЭМГ привлекались как РКИ, так и описательные исследования.
Гетерогенность исследований определялась статистическими методами через I2 и Chi2. На случай существенной гетерогенности (I2>50%, p<0,05) и для итоговых показателей из 5 или более исследований мы планировали провести анализ метарегрессии. Но для всех итоговых показателей не удалось собрать соответствующего числа работ.
Систематические ошибки публикаций оценивалась визуальной оценкой воронкообразных распределений и путем вычисления по формуле тенденциозности Egger [21]. Чтобы сделать вывод о систематических ошибках публикации, мы пользовались принципом «стричь и наполнять», согласно которому уровни результатов разных исследований должны распределяться на графике близко к оси воронки. Если же выявляется асимметрия, то проводится проверка на потенциальную значимость неопубликованных данных [21]. Для всех оценок статистически существенным считалось значение p<0,05.
Результаты поиска источников.
Суммарное число статей, выданных поисковыми системами, составило 230 (после исключения дубликатов).
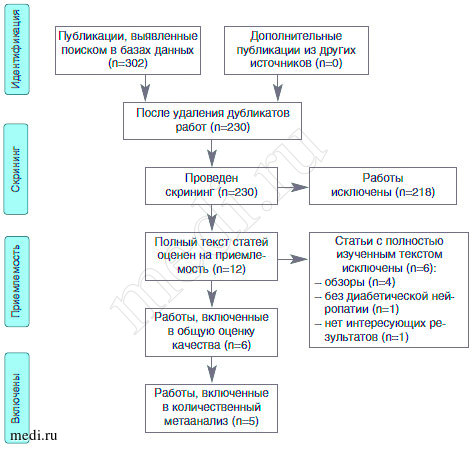
Рис. 1. Поэтапная схема по системе PRISMA
После дальнейшего исключения 218 из них на основании данных в названии или в резюме (главным образом из-за того, что в них не изучались субъекты с диабетической нейропатией), 12 статей были отобраны для ознакомления с полным текстом. В конце концов 6 статей [22-27] были включены в общие оценки по качеству, а 5 [23-27] - в количественный анализ. Из включенных статей 3 содержали описание РКИ [23-25] (рис. 1).
Все исследования включали 711 больных с диабетом, страдавших периферической нейропатией.
Число больных в 3-х РКИ метаанализа составило 658. Из пациентов 3-х РКИ 340 лечились АЛК (средний возраст - 57,8 года), а 318 больных группы контроля (средний возраст - 57,8 года) получали плацебо (n=203) или метилкобаламин (n=115). Все 3 исследования включали больных как с 1-м, так и со 2-м типом СД, которым параллельно проводилось лечение пероральными сахароснижающими препаратами и инсулином. Средний срок отслеживания в динамике составил 48 нед. (разброс - 24-52).
Метаанализ влияния АЛК на боль
В таблице 1 приведены данные о влиянии АЛК на боль у пациентов с диабетической нейропатией. В 2-х исследованиях [23, 25] болевые ощущения оценивались с помощью ВАШ, а в 2-м исследовании [24] применена балльная оценка симптомов нейропатии. В целом АЛК существенно уменьшил болевые ощущения у 340 пациентов, в сравнении с 318 контрольными субъектами,203 из которых получали плацебо, а 115 — метилкобаламин (всего 4 когорты в 3-х РКИ [23-25]; СРС = - 0,45; 95% ДИ: от -0,86 до -0,04; p = 0,03; I2 = 85%).
Хотя данные были гетерогенными, метарегрессивный анализ не представлялся возможным из-за ограниченного числа доступных исследований, в то время как уровень систематических ошибок публикаций был низким (показатель таких ошибок по Egger = 0,78; p = 0,48).
Метаанализ действия АЛК и АЛК/ЛК на электромиографические параметры
Во всех работах (кроме одной [22]) сообщалось о влиянии АЛК/ЛК на показатели ЭМГ.
В таблице 2 приводится метаанализ параметров ЭМГ в 2-х исследованиях, результаты представлены в виде сравнения больных, которые получали АЛК, с группами контроля. Применение АЛК улучшило нервную проводимость по волокнам локтевого нерва - как по чувствительным (СРС = 0,60; 95% ДИ: 0,35 - 0,86, p<0,0001; I2 = 94%), так и по моторным (СРС = 0,67; 95% ДИ: 0,43 - 0,91, p<0,0001; I2 = 0%). Были отмечены такие же положительные сдвиги как для чувствительной, так и для моторной части локтевого нерва после проведения анализа амплитуды реакции как итогового показателя. Кроме того, АЛК увеличил амплитуду реакции моторной части срединного нерва, что отражено в таблице 2. За исключением отдельных случаев, гетерогенность была высокой. Анализ в отношении систематических ошибок публикаций был невозможен по причине малого количества наблюдений для каждого итогового показателя.
Таблица 1. Действие ацетил-L-карнитина (АЛК) на нейропатическую боль в рандомизированных контролируемых исследованиях
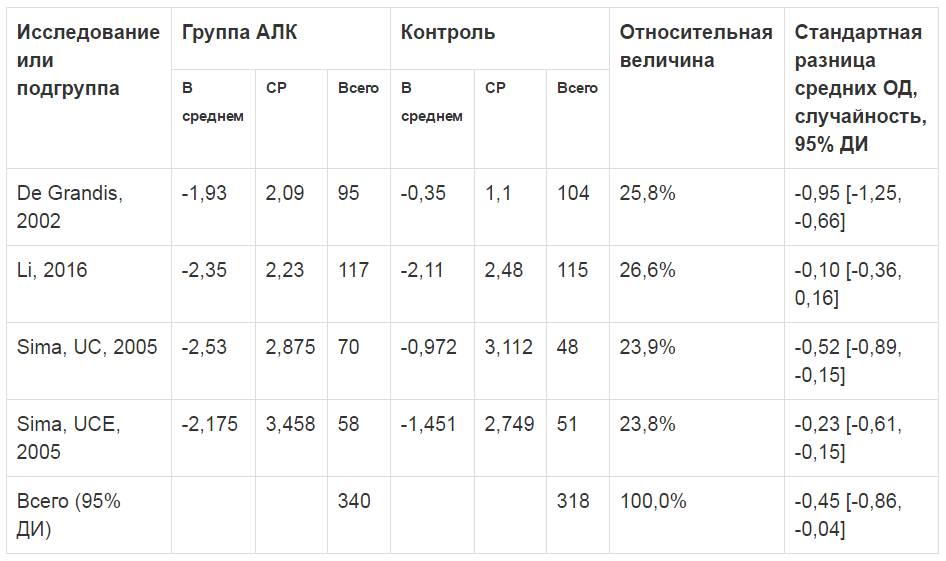
Таблица 2. Данные электромиографии в исследованиях, изучавших роль ацетил-L-карнитина, в сравнении с контролемГетерогенность: Tau2 = 0,15; Chi2 = 19,82, df = 3 (p = 0,0002); I2 = 85%
Тест на общий эффект: Z = 2,15 (p = 0,03)
ДИ — доверительные интервалы, ОД — обратная дисперсия, СР — стандартная разница.
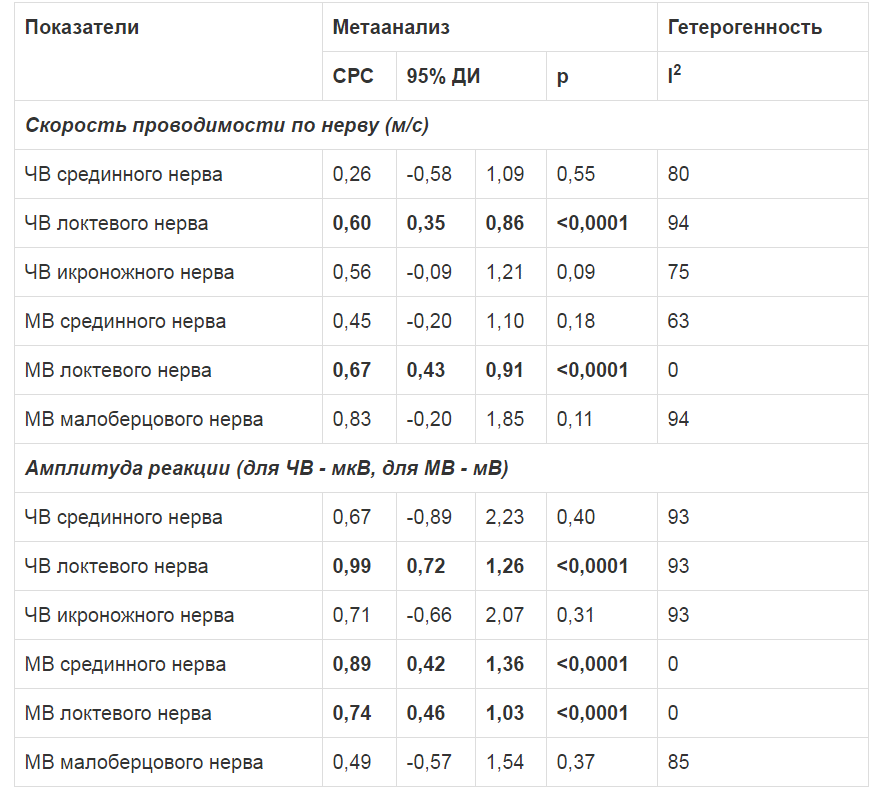
ДИ - доверительный интервал, ЧВ - чувствительные волокна, МВ - моторные волокна.
Жирный шрифт указывает на статистически значимые результаты (значения p<0,05). Все данные взяты из двух исследований [21, 22].
В таблице 3 представлены результаты метаанализа параметров ЭМГ, рассчитанных как разница между исходными значениями и данными наблюдения в динамике после применения АЛК/ЛК. По показателю скорости проведения импульса АЛК/ЛК оказал существенное благотворное влияние на чувствительные волокна всех 3-х изученных нервных стволов, при этом разброс СРС составлял от 0,76 м/с для срединного нерва (95% ДИ: 0,50-,02; 3 исследования, 122 участника) до 1,01 м/с для икроножного нерва (95% ДИ: 0,74—1,29; 3 исследования; 124 участника). Аналогичные данные получены для моторных волокон срединного нерва (СРС = 0,54 м/с; 95% ДИ: 0,25-0,83; 4 исследования, 124 участника) и большеберцового нерва (СРС = 0,49 м/с; 95% ДИ: 0,18-0,79; 3 исследования, 86 участников) (табл. 3).
Для всех этих результатов гетерогенность была низкой (что видно по I2<50%), а системная ошибка публикаций была маловероятной, кроме моторной составляющей локтевого нерва, но процедура «стричь и наполнять» не изменила наши результаты.
Представляется, что действие АЛК/ЛК на амплитуду реакции сравнимо с эффектами в отношении скорости нервной проводимости. АЛК и ЛК оказались способны увеличить амплитуду реакции для всех изученных чувствительных нервов (с разбросом СРС от 0,79 мкВ для икроножного нерва до 1,04 мкВ для срединного нерва) и для всех моторных нервов (СРС от 0,60 мВ для малоберцового до 0,74 мВ для большеберцового нерва), за исключением срединного нерва. Однако после «состригания» результатов одного из исследований слева от средней этот результат также становится статистически существенным (СРС = 1,46 мВ; 95% ДИ: 0,24—2,69) (табл. 3).
По контрасту с данными о скорости проводимости гетерогенность для амплитуды реакции была в целом высокой (I2 >70%) для всех анализируемых результатов.
Наконец, Sima et al. в своем исследовании [25] показали несущественное влияние АЛК на показатели ЭМГ при сравнении с плацебо, но они не представили изменения показателей после применения АЛК в сравнении с исходными. Тем не менее в этом исследовании [25] было обнаружено существенное увеличение числа волокон икроножного нерва наряду с кластерами восстанавливающихся нервных волокон, а также улучшение восприятия вибрации.
Таблица 3. Данные электромиографии из исследований, изучавших изменения под действием ацетил-L-карнитина и L-карнитина относительно исходных значений
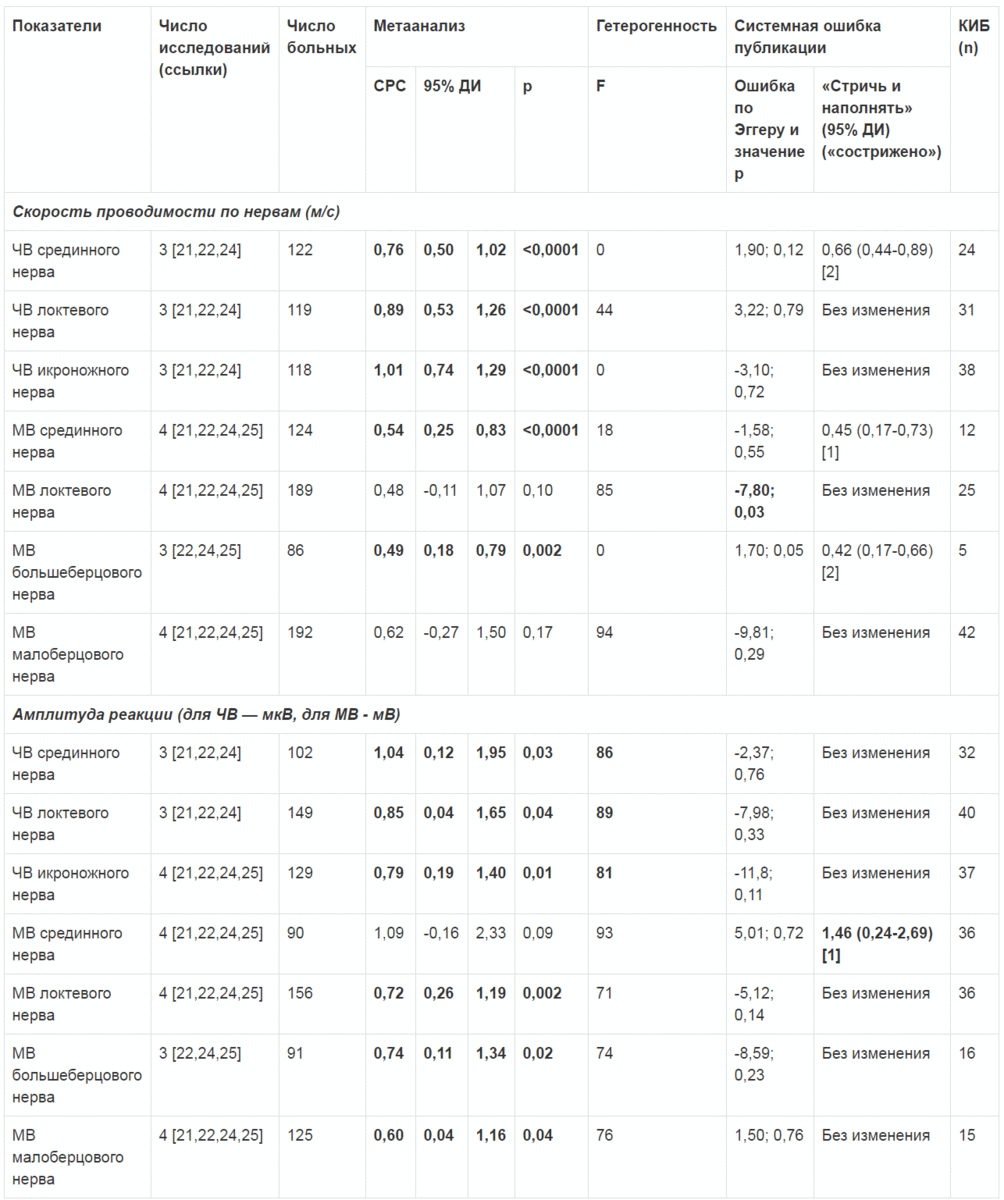
Как показывает дополнительная таблица 3, в РКИ не было отмечено серьезных неблагоприятных явлений (таких как смерть, сердечно-сосудистые нарушения) после лечения АЛК/ЛК. В одном исследовании [25] в группе плацебо чаще, чем в группе АЛК/ЛК, возникали некоторые неврологические симптомы (боль, гиперестезия и парестезия). При этом во всех работах констатировалось, что у пациентов, принимавших АЛК/ЛК, отмечались некоторые незначительные желудочно-кишечные побочные явления, например, рвота или тошнота.ДИ — доверительный интервал, ЧВ — чувствительные волокна, МВ — моторные волокна,; КИБ — классический показатель бесперебойности (число необходимых статей для опровержения систематической ошибки). em>
Жирный шрифт указывает на статистически значимые результаты (значения p <0,05).
Неблагоприятные эффекты
Обсуждение
Проведенный систематический анализ включал 3 РКИ, 3 описательных исследования по боли и 2 исследования по ЭМГ. Общее число больных диабетом, охваченных этими работами, составило 711. Было показано, что АЛК может снижать болевые ощущения и улучшать ЭМГ-параметры у больных диабетом, страдающих периферической нейропатией, по сравнению с контролем. Если проводить сравнение с исходным уровнем, то применение АЛК/ЛК способно улучшать параметры ЭМГ.
Относительно данных групп контроля следует отметить, что применение АЛК приводит к существенному снижению болевых ощущений у пациентов с диабетической нейропатией. Считается, что механизм этого обезболивающего эффекта связан с ацетилированием и активацией транскрипции NF-kB. Промотером данного процесса выступает АЛК, который является донором ацетильных групп [12, 28]. Эта активация имеет отношение к активации экспрессии рецепторов mGlu-2, которые связывают глутамат в синапсах дорсальных рогов, что ведет к снижению болевой гиперчувствительности [12, 28]. Как ранее сообщалось в метаанализе Li et al. [15], влияние АЛК на нейропатическую боль сильнее при диабете, чем при других патологических процессах. Согласно одной из гипотез, влияние глутамата при диабете более выражено, чем при нейропатиях иного происхождения [29, 30]. Этим и объясняется усиленный эффект АЛК.
Описательные исследования показали, что ЛК может улучшить показатели ЭМГ, это подтверждает нейротропный эффект карнитина, который дополняет роль АЛК как донора ацетильных групп. Неясно, почему в отношении одних нервов наблюдается эффект от применения ЛК, в отношении других - нет, и нужны дальнейшие исследования, чтобы разрешить эту проблему.
Метаанализ продемонстрировал также способность АЛК/ЛК существенно повышать скорость нервной проводимости и амплитуду сигнала в нервах верхних и нижних конечностей. При ЭМГ выявляется латентность - время, необходимое для того, чтобы после действия раздражителя возник вызванный потенциал. Это время отражает проводимость по самым быстрым волокнам. Пиковая латентность отражает латентное время для большинства аксонов и измеряется по моменту пиковой активности. Показатели латентности и пиковой латентности зависят от миелинизации нерва [31]. Уменьшение амплитуды реакции обычно отражает потерю аксонов [31]. Скорость проводимости также зависит от состояния миелинизации, и она часто бывает сниженной при болезнях, затрагивающих миелинизацию нервов, хотя некоторое количество миелинизированных аксонов зачастую остается интактным [31]. С молекулярной точки зрения, есть данные, что АЛК усиливает экспрессию ФРН и его рецепторов, способствует восстановлению нервов, уменьшает дегенерацию миелина и в конечном счете улучшает структуру и функцию нерва [8, 14, 32]. Все эти факторы, вероятно, способствуют влиянию АЛК на параметры ЭМГ.
В литературе описано очень мало случаев побочных эффектов от применения АЛК. Во всех 3-х РКИ [23-25] зафиксирована одинаковая частота побочных эффектов в группах АЛК и в контроле, а в единственном описательном исследовании, касавшемся побочных эффектов, только у 2-х участников отмечены такие эффекты, но они не привели к прекращению приема этого дополнительного средства.
Итак, исследование продемонстрировало, что АЛК эффективно снижает боль, обусловленную диабетической нейропатией, по сравнению с группами активного или плацебо-контроля. Более того, получены данные в пользу улучшения параметров ЭМГ под действием АЛК, и это относится как к чувствительным, так и к двигательным волокнам и выявляется при сравнении с группой контроля. Аналогичная зависимость обнаружена для ЛК по сравнению с исходными показателями. Требуются дальнейшие РКИ для подтверждения этих данных, в частности, это касается параметров ЭМГ в сравнении с группами плацебо.
Реферат подготовлен редакцией РМЖ по материалам статьи N. Veronese et aI. Effect of acetyI-I-carnitine in the treatment of diabetic peripheral neuropathy: A systematic review and meta-analysis // Eur Geriatr Med. 2017. Vol. 8(2). P. 117-122.



