Оценка безопасности и эффективности препарата «Элькар» (левокарнитин) у пациентов в остром периоде ишемического инсульта в каротидной системе
Статьи
Опубликовано в РМЖ - Неврология, 2011, 11, с. 3-6
М.К. Бодыхов1'2, Л.В. Стаховская1,2, К.А. Салимов1, И Сун Чер1
1 РГМУ
2 НИИ цереброваскулярной патологии и инсульта ГОУ ВПО РГМУ Росздрава
Введение
Инсульт - заболевание, имеющее огромную социальную и экономическую значимость. Сосудистые заболевания мозга занимают второе место в структуре смертности от болезней системы кровообращения (39%) и в общей смертности населения (23,4%), а также являются лидирующей причиной инвалидизации населения [2] . В связи с этим проблема эффективной и безопасной терапии инсульта является одной из наиболее актуальных в современной неврологии.
Одним из наиболее сложных и многофакторных направлений в лечении инсульта в остром периоде является нейропротекция. Препарат «Элькар» (лево-карнитин) является одним из препаратов, способных замедлить, а возможно, и предотвратить процесс деградации мозга при инсульте.
Наиболее значимыми относительно терапии острого инсульта являются способность левокарнитина и его производных препятствовать развитию апоптоза [6], а также их антиоксидантная активность [1]. Также была выявлена способность производных левокарни-тина уменьшать уровень лактата в очаге ишемии, вероятнее всего, посредством активации цикла трикарбо-новых кислот и ингибирования анаэробного гликолиза [4,7].
Таким образом, левокарнитин обладает экспериментально доказанными и физиологически обоснованными нейропротективными свойствами, что и определило возможность его применения в неврологической практике.
Цель исследования: изучение эффективности и безопасности применения препарата «Элькар» (левокарнитин) у пациентов в остром периоде ишемического инсульта в каротидном бассейне.
Дизайн исследования: открытое параллельное проспективное сравнительное контролируемое рандомизированное исследование.
В качестве контроля использовалась группа пациентов, получавших стандартизированную базисную терапию инсульта. Разделение пациентов на группы проводилось методом простой рандомизации.
Материалы и методы
Обследовано 48 больных с инсультом. Из них 8 пациентов были досрочно исключены из исследования после проведения магнитно-резонансной томографии (МРТ) головного мозга в связи с локализацией ишеми-ческого очага в вертебро-базилярной артериальной системе (5 человек), и наличием геморрагического инсульта (3 человека).
Критериями включения в исследование являлись: возраст от 45 лет включительно, первые 24 часа от начала развития инсульта, ишемический инсульт в каротид-ной системе, не более 2 баллов по модифицированной шкале Ренкина до начала развития нынешнего инсульта (анамнестически), ясное сознание или оглушение (по классификации А.Н. Коновалова и соавт.).
Пациенты были разделены на 3 группы:
• группа контроля - 10 человек,
• группа 1 -15 пациентов, получавших Элькар в дозе 1 г/сут,
• группа 2 - 15 пациентов, получавших Элькар в дозе 3 г/сут.
Пациентам 1 группы в течение 10 дней Элькар вводился внутривенно 2 раза в сутки в дозе 500 мг (5 мл 10% раствора). Затем в течение 10 дней больные принимали Элькар перорально по 1 чайной ложке 20%-го раствора 2 раза в сутки.
Пациенты 2 группы в течение 10 дней получали Элькар внутривенно 2 раза в сутки в дозе 1500 мг (15 мл 10% раствора), в течение последующих 10 дней принимали Элькар перорально по 2 чайные ложки 20%-го раствора 2 раза в сутки.
Оценивалась тяжесть инсульта по шкале NIHSS (шкала оценки тяжести инсульта Национального института здоровья США) в 1, 3, 7, 14 и 21-е сутки заболевания, а также индекс Бартелл (индекс повседневной активности пациента) на 21-е сутки.
Всем пациентам в течение первых двух суток проводилась МРТ головного мозга для подтверждения диагноза ишемического инсульта в каротидном бассейне. Всем больным проводилась ультразвуковая допплеро-графия магистральных артерий головы и шеи (УЗДГ МАГ) и ЭКГ - с целью установления патогенетического типа инсульта согласно критериям TOAST [3].
Все пациенты получали максимально унифицированную терапию в соответствии с рекомендациями Европейской организации по проблемам инсульта [5].
Статистическая обработка полученных данных проводилась с использованием программы SPSS 8.
Результаты
Средний возраст пациентов в группе контроля составил 66 (±13,2), в группе 1 - 70 (±13,8), в группе 2 -75 (±7,9) лет.
В группу контроля вошли 8 мужчин (80%) и 2женщи-ны (20%), в группу 1 - 3 мужчин (20%) и 12 женщин (80%), в группу 2 - 7 мужчин (47%) и 8 женщин (53%).
В группе контроля атеротромботический (АТ) вариант ишемического инсульта по TOAST имел место у 7 пациентов (70%), кардиоэмболический (КЭ) вариант - у 3 пациентов (30%). В группе 1 число пациентов с АТ вариантом составило 8 (53%), с КЭ - 6 человек (40%), еще у одного больного диагностирован ишемический инсульт неизвестной этиологии (НЭ) (7%). В группе 2 количество пациентов с АТ вариантом составило 8 человек (53%), с КЭ - 4 (26%), у 3 пациентов диагностирован ишемический инсульт НЭ (21%).
Статистически значимых различий по значениям АД, ЧСС, ЧД, SpO2, температуре тела, у пациентов группы контроля и групп, получавших терапию Элькаром, не получено на протяжении всего периода наблюдения (1-21-е сутки заболевания).
Результаты оценки тяжести инсульта (по NIHSS) и степени функционального восстановления (индекс Бартелл) у пациентов исследуемыхгрупп представлены в таблице 1.
Таблица 1. Результаты оценки тяжести инсульта (по NIHSS) и степени функционального восстановления (индекс Бартелл)
|
Показатель
|
Группы
|
|
Группа контроля
|
1 Группа 1 (1 г/сут)
|
Группа 2 (3 г/сут)
|
|
Балл по NIHSS в 1-е сутки
|
12,3 (±4,9)
|
1 10,40 (±4,6)
|
11,1 (±5,3)
|
|
Балл по NIHSS на 3-и сутки
|
11,6 (±5,1)
|
8,60 (±4,0)
|
10,0 (±5,0)
|
|
Балл по NIHSS на 7-е сутки
|
11,3 (±4,5)
|
7,33 (±4,0)
|
8,2 (±5,7)
|
|
Балл по NIHSS на 14-е сутки
|
11,1 (±4,7)
|
1 6,73 (±4,0)
|
7,0 (±5,5)
|
|
Балл по NIHSS на 21-е сутки
|
10,8 (±4,6)
|
5,80 (±3,8)
|
6,3 (±5,6)
|
|
Индекс Бартелл
|
45,5 (±33,1)
|
67,7 (±31,4)
|
67,0 (±32,4)
|
Все полученные выборки подчинялись закону нормального распределения (модифицированная статистика Колмогорова-Смирнова для всех выборок была меньше 0,895).
В результате анализа основных характеристик групп исследования выявилась тенденция к включению в группу с большей суточной дозой Элькара более возрастных пациентов (p=0,02), однако достоверных различий в исходной тяжести инсульта, оцененной с помощью NIHSS в 1-е сутки заболевания, между этими группами выявлено не было. Также не было достоверных различий по исходной тяжести инсульта между группой контроля и группами, получавшими Элькар.
Выявлены статистически достоверные различия в выраженности регресса неврологического дефекта у пациентов группы контроля и больных, получавших Элькар. У пациентов 1 группы - начиная с 7-х суток (на 7-е сутки - p=0,03, на 14-е сутки - p=0,02, на 21-е сутки - p<0,01), группы 2 - c 14 суток (на 14-е сутки - p=0,05, на 21-е сутки - p=0,02) (рис. 1). Между группами, получавшими различные суточные дозы Элькара, достоверных различий в динамике тяжести инсульта не выявлено.
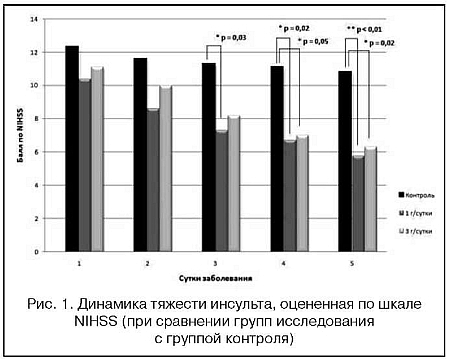
Также необходимо отметить, что у пациентов группы контроля разница между оценкой по шкале NIHSS в 1-е и 21-е сутки (точки начала и завершения исследования у каждого пациента) была недостоверна (p=0,29) и составляла 1,1 (±3,2) балла, тогда как в группах 1 и 2 данные различия были достоверны (p=0,005 и p<0,0001 соответственно) и составляли 4,6 (±3,0) балла и 4,9 (±1,5) балла соответственно.
При оценке функционального восстановления пациентов к 21-м суткам выявлена отчетливая тенденция к увеличению индекса Бартелл в группах, получавших Элькар, по сравнению с группой контроля. Между группами с различным режимом дозирования Элькара каких-либо различий по значению индекса Бартелл не выявлено (рис. 2).
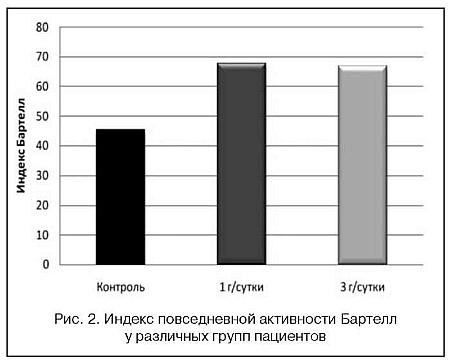
Статистически значимой корреляции между временем от начала заболевания до начала терапии Элькаром и динамикой регресса неврологической симптоматики по шкале NIHSS на 21-е сутки инсульта ни в одной из групп пациентов, получавших Элькар, выявлено не было (для группы 1 -r=0,64, p=0,82, для группы 2- r=-0,125, p=0,657).
Динамика тяжести инсульта и степень функционального восстановления отличались у пациентов с различными патогенетическими вариантами инсульта (табл. 2).
Таблица 2. Результаты оценки тяжести инсульта (по NIHSS) и степени функционального восстановления (индекс Бартелл) у пациентов с различными патогенетическими вариантами инсульта
Показатель | Группы |
Группа контроля | Группа 1 (1 г/сутки) | Группа 2 (3 г/сутки) |
АТ | КЭ | АТ | КЭ | АТ | КЭ |
Балл по NIHSS в 1-е сутки | 13,0 (±4,6) | 10,7 (±6,4) | 12,2 (±4,9) | 8,3 (±6,2) | 11,3 (±6,0) | 10,6 (±3,4) |
Балл по NIHSS на 3-и сутки | 11,6 (±5,4) | 11,7 (±5,7) | 10,8 (±4,9) | 7,8 (±5,3) | 10,4 (±5,6) | 8,5 (±6,4) |
Балл по NIHSS на 7-е сутки Балл по NIHSS на 14-е сутки | 11,4 (±5,1) 10,9 (±5,2) | 11,0 (±3,5) 11,7 (±4,2) | 9.2 (±5,4) 7.3 (±5,5) | 5,5 (±6,6) 5,0 (±5,6) | 8.7 (±6,4) 7.8 (±6,1) | 6,8 (±3,6) 4,8 (±2,2) |
Балл по NIHSS на 21-е сутки | 10,6 (±4,6) | 11,3 (±3,8) | 7,0 (±5,7) | 4,3 (±5,4) | 7,2 (±6,3) | 3,8 (±2,6) |
Индекс Бартелл | 41,4 (±31,2) | 55,0 (±42,7) | 59,1 (±33,2) | 88,8 (±19,3) | 59,0 (±31,6) | 85,0 (±25,5) |
У пациентов с КЭ вариантом инсульта, принимавших Элькар, отмечалась достоверно более значимая положительная динамика по шкале NIHSS, чем у пациентов с АТ вариантом инсульта на 21-е сутки у пациентов 1 груп-пыина14и 21-е сутки в группе 2 (p=0,05, p=0,034, p=0,03 соответственно) (рис. 3 и 4).
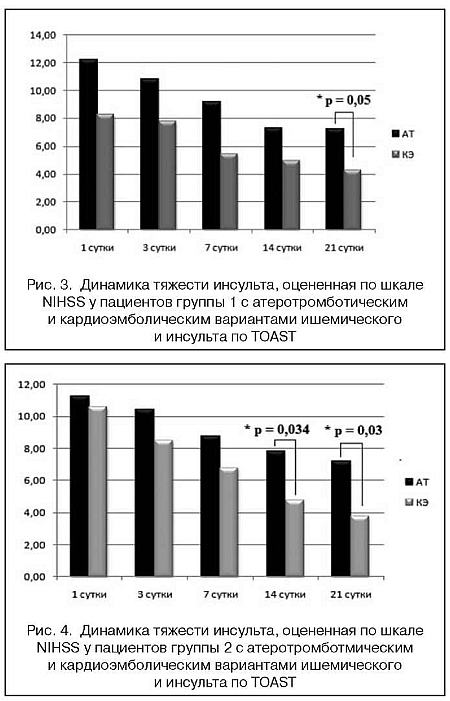
В группе контроля различий между пациентами с КЭ и АТ вариантами ишемического инсульта не выявлено (рис. 5).
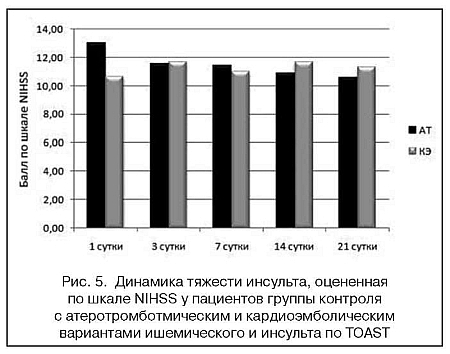
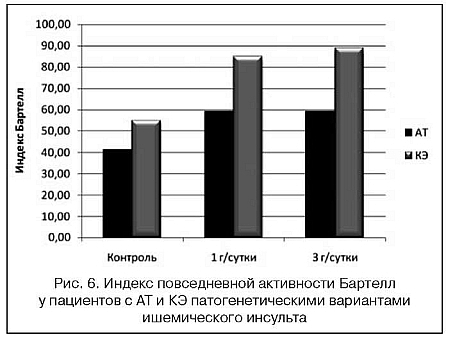
В отношении степени функционального восстановления у пациентов с разными патогенетическими вариантами ишемического инсульта статистически значимых различий не получено, однако имеется сходная тенденция - пациенты, получавшие Элькар и имевшие КЭ вариант инсульта, восстанавливались к 21-м суткам лучше, чем пациенты с АТ вариантом, получавшие Элькар (p=0,16 и p=0,12 для группы 1 и 2 соответственно). В группе контроля по данному показателю различия незначительны (рис. 6).
За весь период проведения исследования не было выявлено ни одного случая развития побочных реакций на Элькар, что позволяет говорить о том, что Элькар (левокарнитин) обладает хорошей переносимостью и не дает каких-либо перекрестных реакций с лекарственными препаратами, направленными на оптимизацию гомеостаза и вторичную профилактику инсульта.
Обсуждение
Таким образом, результаты проведенного исследования показали эффективность и безопасность применения Элькара у пациентов в остром периоде каротидного инсульта - как в отношении тяжести неврологического дефекта, так и в отношении функциональной активности пациентов. Применение Элькара в качестве нейропротектора, начиная с 1-х суток заболевания, позволяет уменьшить сроки восстановления пациентов, а следовательно, способствует более быстрой их активизации и уменьшению количества осложнений, связанных с длительной вынужденной иммобилизацией.
Наиболее выраженный регресс неврологической симптоматики и более полное функциональное восстановление отмечались у пациентов с кардиоэмболиче-ским инсультом. Такое положение вещей, вероятно, связано с тем, что Элькар обладает не только нейропро-тективным, но и выраженным кардиопротективным действием. Улучшая метаболизм миокарда, Элькар способствует поддержанию адекватной системной гемодинамики у пациентов с кардиальной патологией, что, в свою очередь, способствует сохранению жизнеспособности клеток пенумбры. Однако это предположение требует уточнения.
Выбранный способ введения препарата (внутривенное введение в течение первых 10 суток с последующим переходом на прием раствора внутрь) показал достаточную эффективность, однако существенного различия между дозой 1 г/сут и дозой 3 г/сут выявлено не было. Вероятно, это связано с избыточностью дозы 3 г/сут и можно предположить, что 1 г/сут является необходимой и достаточной дозой Элькара (левокарни-тина) для пациентов в остром периоде ишемического инсульта.
Выводы
Элькар обладает хорошей переносимостью и не дает каких-либо перекрестных реакций с лекарственными препаратами, направленными на оптимизацию гомеостаза и вторичную профилактику инсульта.
Применение Элькара (левокарнитина) у пациентов в остром периоде ишемического инсульта в каротидной системе статистически достоверно уменьшает тяжесть течения инсульта, начиная с 7-х суток заболевания.
Имеется выраженная тенденция к увеличению индекса повседневной активности Бартелл у пациентов, принимавших Элькар, по сравнению с группой контроля.
У пациентов с кардиоэмболическим патогенетическим вариантом инсульта, получавших Элькар, тяжесть заболевания уменьшалась достоверно в большей степени, чем у пациентов с атеротромботическим вариантом. В группе контроля таких различий не выявлено.
Имеется выраженная тенденция к увеличению индекса повседневной активности Бартелл у пациентов с кардиоэмболическим вариантом инсульта, принимавших Элькар, по сравнению с пациентами с атеротром-ботическим патогенетическим вариантом. В группе контроля таких различий не выявлено.
Не получено достоверных различий в отношении тяжести течения инсульта и функционального восстановления у пациентов, получавших 1 или 3 г лекарственного препарата в сутки, что позволяет рекомендовать использование Элькара в дозе 1 г/сут.
Литература
1. Гусев Е.И., Кузин В.М., Колесникова Т.Н. и др. Карнитин - ведущий фактор регенерации нервной ткани.//Мед. информац. вестник - 1999 (февраль): 11-23.
2. Гусев Е.И, Скворцова В.И, Стаховская Л.В. Проблема инсульта в Российской Федерации: время активных совместных действий // Журнал неврологии и психиатрии им. С.С.Корсакова 2007; №4:4-10.
3. Adams H, Bendixen B, Kapelle J et al. Classification of subtype of acute ischemic stroke. Definitions for use in a multicenter clinical trial. // Stroke;24; 1:35-40.
4. Bieber L.L. Carnitine. //Ann. Rev. Biochem. 1988; 57:261-283.
5. Guidelines for Management of Ischaemic Stroke and Transient Ischaemic Attack of ESO //2008.
6. G Konyavko M, Adachi S. Regulation of the activity of caspases by L-carnitine and palmitoylcarni-tine. // FEBS Lett. 2000; 478: 19-25.
7. Rosentha R.E, Williams R, Bogaert YE, et al. Prevention of postischemic canine neurological injury through potentiation of brain energy metabolism by acetyl-L-carnitine. // Stroke 1992; 23: 1312-1317
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 pikfarma.ru
pikfarma.ru
 pikfarma.ru
pikfarma.ru
