Уважаемый посетитель!
Эта информация для специалистов здравоохранения
Нажимая «ПРОДОЛЖИТЬ», Вы подтверждаете, что им являетесь
 pikfarma.ru
pikfarma.ru
Элькар® - метаболическое средство пациентов с хронической ишемией мозга и патологией сердца / постинфекционной астенией, далее...
Лечение постинфекционной астении и постковидного синдрома
Эффективность и безопасность применения L-карнитина при хронической сердечной недостаточности: метаанализ рандомизированных контролируемых исследований (реферат)
СтатьиОпубликовано в журнале:
РМЖ, 2017 №20
РЕЗЮМЕ
Введение: до сих пор остается открытым вопрос о целесообразности применения L-карнитина при хронической сердечной недостаточности (ХСН). Для оценки эффектов применения L-карнитина при лечении пациентов с ХСН был проведен метаанализ рандомизированных контролируемых исследований (РКИ).
Материал и методы: в работу были включены результаты исследований, внесенные в следующие базы данных: Pubmed, Ovid Embase, Web of Science, and Cochrane Library, Chinese National Knowledge Infrastructure (CNKI), Wanfang, Chinese Biomedical (CBM) и Chinese Science and Technology Periodicals (VIP) до 30 сентября 2016 г. Исследования, соответствующие критериям включения, оценивались двумя рецензентами независимо друг от друга.
Результаты: в исследование были включены результаты 17 РКИ с участием 1625 пациентов с ХСН. Применение L-карнитина в лечении ХСН ассоциировалось со значительным улучшением общей эффективности (отношение шансов (ОШ) = 3,47, p<0,01), увеличением фракции выброса левого желудочка (ФВ ЛЖ) (взвешенная разность средних (ВРС): 4,14%, p=0,01), ударного объема (УО) (ВРС: 8,21 мл, p=0,01), сердечного выброса (CВ) (ВРС: 0,88 л/мин, p<0,01) и соотношения E/A (ВРС: 0,23, p<0,01). Терапия L-карнитином значительно снизила уровень мозгового натрий уретического пептида (brain natriuretic peptide (BNP)) в крови (ВРС: -124,60 пг/мл, p=0,01), уровень N-терминального мозгового натрийуретического пропептида (NT-proBNP) (ВРС: -510,36 пг/мл, p<0,01), сказалась на уменьшении конечно-систолического размера левого желудочка (КСР ЛЖ) (ВРС: -4,06 мм, p<0,01), конечно-диастолического размера ЛЖ (КДР ЛЖ) (ВРС: -4,79 мм, p<0,01) и конечно-систолического объема ЛЖ (КСО ЛЖ) (ВРС: -20,16 мл, 95% доверительный интервал (ДИ): от -35,65 до -4,67, p<0,01). Тем не менее не было выявлено значительной разницы в общей смертности от различных причин, при прохождении теста 6-минутной ходьбы и в количестве нежелательных явлений между группой пациентов, принимающих L-карнитин, и контрольной группой.
Заключение: терапия L-карнитином пациентов с ХСН эффективна для улучшения клинических симптомов и функций сердца, снижает уровень BNP и NT-proBNP и хорошо переносится пациентами.
Ключевые слова: хроническая сердечная недостаточность, L-карнитин, клинические исследования, BNP.
Для цитирования: Эффективность и безопасность применения L-карнитина при хронической сердечной недостаточности: метаанализ рандомизированных контролируемых исследований (реферат) // РМЖ. 2017. № 20. С. 1471–1480.
Efficacy and Safety of L-Carnitine Treatment for Chronic Heart Failure: A Meta-Analysis of Randomized Controlled Trials (summary)
ABSTRACT
Background: whether additional benefit can be achieved with the use of L-carnitine (L-C) in patients with chronic heart failure (CHF) remains controversial. We therefore performed ameta-analysis of randomized controlled trials (RCTs) to evaluate the effects of L-C treatment in CHF patients.
Material and Methods: Pubmed, Ovid Embase, Web of Science, and Cochrane Library databases, Chinese National Knowledge Infrastructure (CNKI) database, Wanfang database, Chinese Biomedical (CBM) database, and Chinese Science and Technology Periodicals database (VIP) until September 30, 2016, were identified. Studies that met the inclusion criteria were systematically evaluated by two reviewers independently.
Results: 17 RCTs with 1625 CHF patients were included in this analysis. L-C treatment in CHF was associated with considerable improvement in overall efficacy (OR = 3.47, p < 0.01), left ventricular ejection fraction (LVEF) (WMD: 4.14%, p = 0.01), strike volume (SV) (WMD: 8.21ml, p = 0.01), cardiac output (CO) (WMD: 0.88 L/min, p < 0.01), and E/A (WMD: 0.23, p < 0.01). Moreover, treatment with L-C also resulted in significant decrease in serum levels of BNP (WMD: -124.60 pg/ml, p = 0.01), serum levels of NT-proBNP (WMD: -510.36 pg/ml, p < 0.01), LVESD (WMD: -4.06 mm, p < 0.01), LVEDD (WMD: -4.79 mm, p < 0.01), and LVESV (WMD: -20.16ml, 95% CI: -35.65 to -4.67, p < 0.01). However, there were no significant differences in all-cause mortality, 6-minute walk, and adverse events between L-C and control groups.
Conclusions: L-C treatment is effective for CHF patients in improving clinical symptoms and cardiac functions, decreasing serum levels of BNP and NT-proBNP. And it has a good tolerance.
Key words: chronic heart failure, L-carnitine, clinical studies, BNP.
For citation: Efficacy and Safety of L-Carnitine Treatment for Chronic Heart Failure: A Meta-Analysis of Randomized Controlled Trials (summary) // RMJ. 2017. № 20. P. 1471–1480.
Введение
Хроническая сердечная недостаточность (ХСН) – это сложный клинический синдром, характеризующийся снижением сократимости миокарда, нарушением гемодинамики и нейроэндокринной активацией. ХСН является глобальной проблемой, от которой страдают во всем мире около 26 млн человек [1]. В настоящее время нейрогормональные антагонисты (ингибиторы ангиотензинпревращающих ферментов, β-блокаторы, блокаторы ангиотензиновых рецепторов и антагонисты минералокортикоидных рецепторов) являются основными средствами, рекомендованными для лечения ХСН [2, 3]. Тем не менее сердечная недостаточность (СН) по-прежнему остается главной причиной смертности и наиболее распространенным заболеванием во всем мире.
В последнее время растет осознание того факта, что в основе патофизиологии и симптомов СН лежат сложные метаболические процессы [4]. В сущности, сердце при СН является «мотором, у которого закончилось топливо» [5]. L-карнитин – витаминоподобная модифицированная аминокислота, играющая важную роль в поддержке метаболических функций организма. Высокие дозы L-карнитина оказывают положительное влияние при самых разных заболеваниях, например, при ишемической болезни сердца (ИБС), застойной СН, заболеваниях периферических сосудов, сахарном диабете (СД) 2-го типа, дислипидемии и артериальной гипертензии (АГ) [6].
Схемы лечения с применением L-карнитина в разных странах различаются. В Китае L-карнитин признан эффективным у пациентов с ХСН [7]. В США L-карнитин не рекомендован пациентам с симптомами СН при сохранной ФВ ЛЖ в качестве лекарственного средства [3]. В европейских рекомендациях нет упоминания о L-карнитине [2].
Для оценки терапевтических эффектов L-карнитина при вторичной профилактике сердечно-сосудистых заболеваний (ССЗ) было проведено два метаанализа РКИ [8, 9], но метаанализы РКИ при ХСН до сих пор не выполнялись. За несколько последних десятилетий было проведено несколько небольших РКИ, посвященных оценке эффективности терапии L-карнитином пациентов с ХСН. Таким образом, данный метаанализ – единственный в своем роде анализ РКИ по оценке эффективности и переносимости L-карнитина.
Материал и методы
1. Стратегия поиска
Поиск информации проводился по следующим базам данных: Pubmed, Ovid Embase, Web of Science, база данных Кохрановской библиотеки, база данных Китайской национальной инфраструктуры знаний (CNKI), база данных Wanfang, Китайская биомедицинская база (CBM), база данных китайской научной и технической периодики (VIP); поиск проводился по материалам, опубликованным до 30 сентября 2016 г. Были использованы следующие ключевые слова: «L-карнитин», «карнитин», «левокарнитин», «новаин», «L-ксернитин», «Витамин BT», «бикарнезин», «сердечная недостаточность», «сердечная дисфункция», «застойная сердечная недостаточность», «кардиомиопатия» и «дисфункция желудочков». Электронные поиски были дополнены поиском вручную всех обзорных статей, первичных исследований и выдержек из протоколов исследований. Поиск литературы был осуществлен двумя независимыми исследователями (X. Song и Z. Yang), оценивались только исследования, выполненные на человеческих субъектах без языковых ограничений.
2. Отбор исследований
Отбор исследований для включения проводился обоими исследователями независимо друг от друга и далее корректировался в ходе совместного обсуждения. В обзор были включены статьи, соответствующие следующим критериям:
(1) тип исследований – рандомизированное контролируемое;
(2) участники – пациенты с ХСН (возраст – старше 18 лет);
(3) проводимое лечение – L-карнитин в сравнении с плацебо, рутинной или общепринятой терапией;
(4) конечные точки – наличие подходящих данных по одному или более из следующих параметров: смертность от любых причин, сердечно-сосудистые события, классификация Нью-Йоркской сердечной ассоциации (NYHA), общая эффективность, физическая активность (тест 6-минутной ходьбы), изменения в параметрах сердечных функций (ФВ ЛЖ, УО, СВ, Е/А, КСР ЛЖ, КДР ЛЖ, КСО ЛЖ, BNP, NT-proBNP) и нежелательные явления;
(5) доступность полнотекстовых вариантов статей.
Исследования, не использовавшие рандомизацию, были исключены. Исследования, которые включали другие метаболические средства, например, триметазидин, коэнзим Q10, также были исключены. Были исключены фармакокинетические исследования, исследования на животных / лабораторные исследования и общие обзоры. Также не были включены повторяющиеся публикации об одних и тех же группах пациентов.
3. Оценка качества
Методологические характеристики включенных в обзор РКИ оценивались в соответствии с принципами Cochrane Collaboration (Кохрановское сотрудничество), описанными в Руководстве версии 5.1.0 [10]. Оба исследователя оценивали качество независимо друг от друга. В случае возникновения разногласий в качестве арбитра привлекался третий автор обзора (H. Zhou).
4. Обработка данных
Оба исследователя знакомились с полными текстами статей независимо друг от друга и извлекали из них следующую информацию: данные о публикации (имя первого автора, год публикации), характеристики исследования (дизайн, объем выборки, продолжительность последующего наблюдения, критерии включения и конечные точки), клинико-диагностические характеристики пациентов (возраст, пол, класс ХСН по NYHA, данные гистологии сердца и ФВ ЛЖ), протокол лечения (доза L-карнитина) и итоговые данные (смертность от любых причин, общая эффективность, класс ХСН по NYHA, результаты нагрузочного теста 6-минутной ходьбы, изменения эхокардиографических параметров и биомаркеров (ФВ ЛЖ, УО, СВ, Е/А, КСР ЛЖ, КДР ЛЖ, КСО ЛЖ, BNP, NT-proBNP) и нежелательные явления. Если данные были недоступны, для их уточнения исследователи обращались непосредственно к авторам статей по электронной почте.
5. Статистические методы
Данные обрабатывались в соответствии с Кохрановским руководством [10]. Результаты терапии были представлены через коэффициенты вероятностей наступления или ненаступления события (отношение шансов – ОШ) с указанием 95% доверительных интервалов (ДИ) (для дихотомичных данных). Для непрерывных данных результаты были представлены через разность средних значений и 95% ДИ. Статистическая гетерогенность измерялась с использованием I² статистических методов и I² статистики с применением набора значимости при I², превышающей 50% [11].
Впервые для метаанализа была использована статистическая модель постоянных параметров. При наличии гетерогенности использовалась статистическая модель случайных параметров. При отсутствии количественных данных использовался метод описательной статистики. В анализ включались все пациенты, которые хотя бы один раз подверглись процедуре вмешательства (ITT-анализ). Для анализа данных использовалась программа Review Manage (v.5.1; the Cochrane Collaboration).
Результаты
1. Характеристики исследований и пациентов
Для детальной оценки из 2870 публикаций было отобрано 468. В конечном итоге было проанализировано лишь 17 РКИ [12–28], включивших 1625 пациентов. Параметры исследований и пациентов представлены в таблице 1. Дозировка L-карнитина варьировалась от 1,5 до 6 г/сут, а длительность периода последующего наблюдения – от 7 дней до 3 лет.
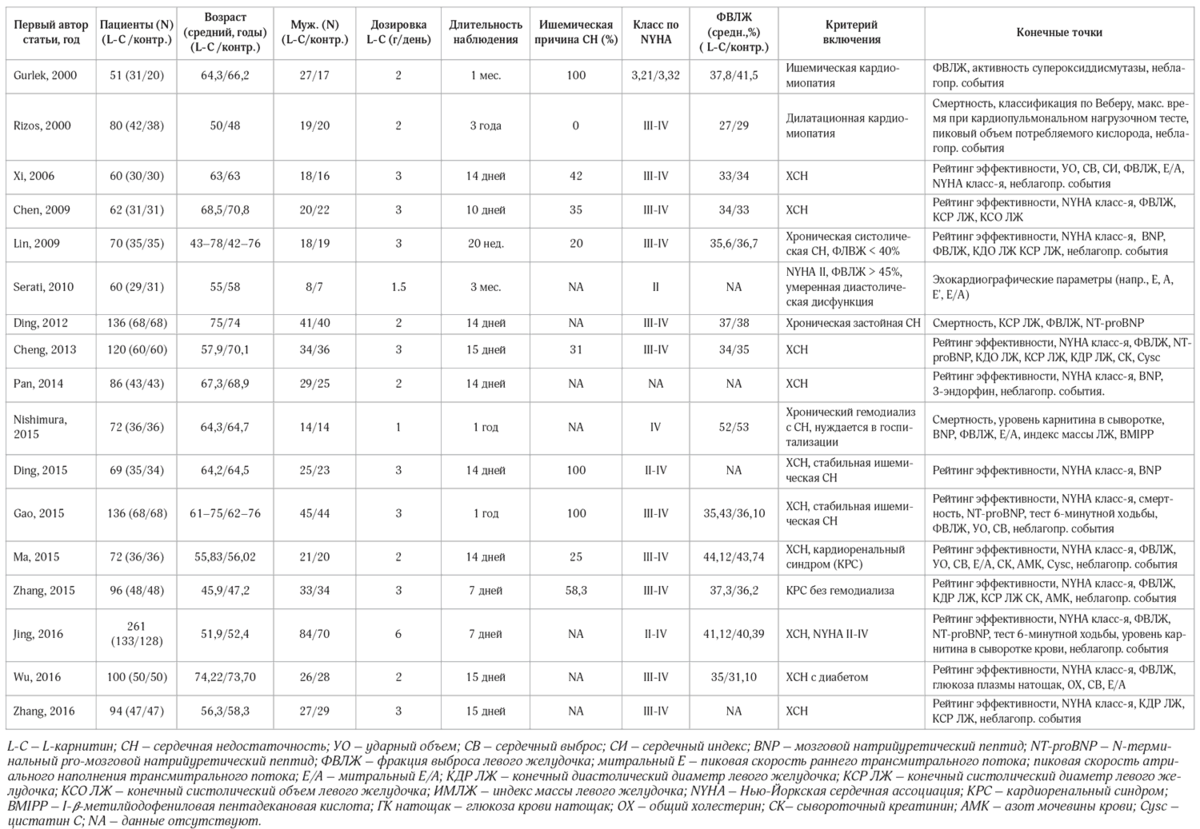
Таблица 1. Базовые характеристики исследований, включенных в метаанализ
2. Оценка качества методологии
Все исследования, включенные в данный метаанализ, являются РКИ. Оценка качества включенных РКИ представлена на рисунке 1. Четыре исследования [12, 13, 21, 26] не предоставили информации о методе рандомизации, тогда как остальные использовали метод последовательных номеров и метод адаптивной рандомизации. Три исследования [13, 17, 26] использовали слепой метод, относительно остальных работ данная информация отсутствовала. В одном из исследований [21] имелась ошибка определения эффективности, поскольку 20% пациентов выбыли из последующего наблюдения. В трех исследованиях [13, 21, 26] результаты были представлены выборочно, поскольку данные ITT-анализа отсутствовали.
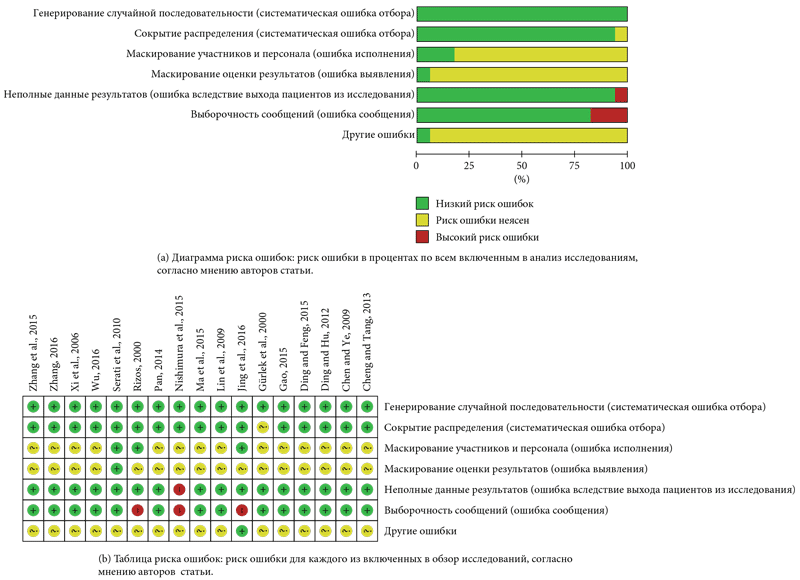
Рис. 1. Оценка риска ошибок
Следует допустить достаточно высокую вероятность присутствия в данных исследованиях различных ошибок. Вопрос о наличии потенциальных ошибок остается открытым. Поскольку большинство из исследований, включенных в обзор, было проведено в Китае, то было сделано предположение, что в метаанализе может присутствовать также ошибка отбора публикаций. Длительность периода терапии могла повлиять на результаты лечения пациентов с ХСН. В 8 исследованиях [14, 18–20, 22, 24, 27, 28] период лечения составил 14–15 дней; тогда как период последующего наблюдения в других исследованиях сильно разнился. Эти исследования были выделены в подгруппу для отдельного анализа.
3. Смертность от любых причин у пациентов с заболеваниями сердца
В четырех исследованиях сообщалось о смерти от любых причин. Как показано на рисунке 2, РР-анализ («per protocol»-анализ, в который включены только пациенты, прошедшие полный курс лечения согласно протоколу), и ITT-анализ («intent-to-treat»-анализ, в который включены все пациенты, даже выбывшие и не получившие полный курс лечения), не обнаружили значительных различий в гетерогенности (I² = 6%, р = 0,36 и I² = 7%, р = 0,36, соответственно). Результаты РР- и ITT-анализов показали наличие тенденции к снижению смертности по любым причинам в группе L-карнитина по сравнению с контрольной группой (ОШ = 0,48, 95% ДИ: 0,21–1,06, р = 0,07 (рис. 2a), ОШ = 0,49, 95% ДИ: 0,22–1,08, р = 0,08 (рис. 2b), соответственно).
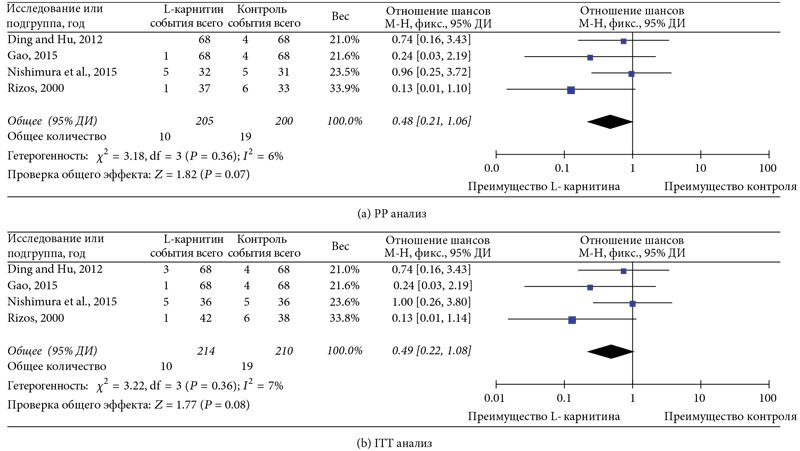
Рис. 2. Графики для смертности от любых причин
4. Оценка функционального состояния
Улучшение сердечной функции (снижение класса по NYHA) было отнесено к параметру оценки общей эффективности. Конечной точкой принято снижение хотя бы на один класс по NYHA; эффективность расценивалась как положительная при снижении на один или два класса или как неэффективная, если класс оставался без изменений. Общая эффективность оценивалась путем суммирования. Двенадцать исследований [14–16, 19, 20, 22–28] продемонстрировали наличие общей эффективности и отсутствие различий в гетерогенности (I² = 0%, р = 0,45). Метаанализ подтвердил значимо большую общую эффективность лечения в группе с L-карнитином по сравнению с группой контроля (ОШ = 3,47, 95% ДИ: 2,49–4,82, р < 0,01 (рис. 3a). Анализ в подгруппе с длительностью терапии 14–15 дней также продемонстрировал, что общая эффективность лечения L-карнитином значимо выше, чем в контрольной группе (ОШ = 5,11, 95% ДИ: 2,87–9,10, р < 0,01 (рис. 3)). С учетом значимой гетерогенности двух исследований [23, 26] метаанализ, выполненный по модели случайных параметров, не выявил в них достоверных межгрупповых различий по результатам нагрузочного теста 6-минутной ходьбы (ВРС: 45,41 мин, 95% ДИ: -14,46–105,29, р = 0,14 (рис. 3b)).
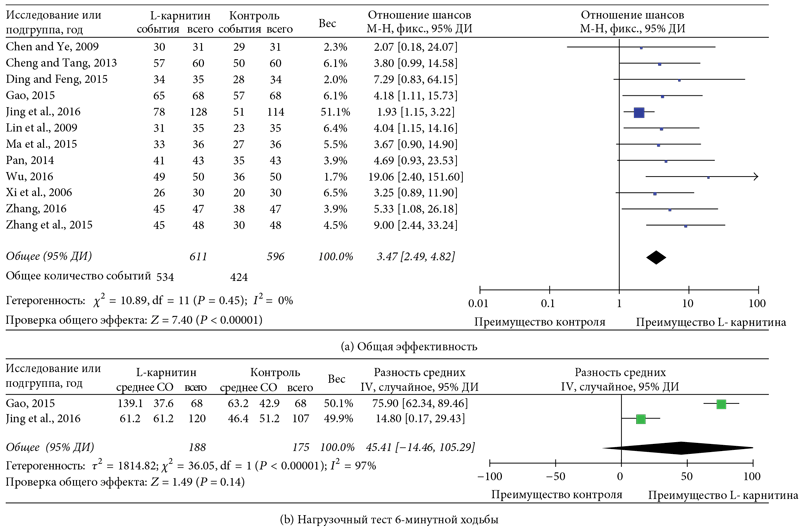
Рис. 3. Графики оценки функциональности
5. Маркеры сыворотки крови
Среди исследований с данными по изменениям в уровнях BNP и NTproBNP в крови [16, 18–23, 26] была выявлена значимая гетерогенность (I² = 97%, р < 0,01 и I² = 99%, р < 0,01, соответственно). При применении модели случайных параметров было установлено, что в группе пациентов, получающих L–карнитин, сывороточные уровни BNP и NT-proBNP существенно снизились по сравнению с таковыми в группе контроля (ВРС: -124,60 пг/мл, 95% ДИ: -220,49-28,71, р = 0,01; ВРС: -510,36 пг/мл, 95% ДИ: -785,42-235,30, р < 0,01, соответственно (рис. 4)). Анализ в подгруппе с продолжительностью терапии 14–15 дней также показал значимое снижение уровня NT-proBNP у пациентов группы L–карни тина (ВРС: -612,44 пг/мл, 95% ДИ: -829,41-395,47, р < 0,01).
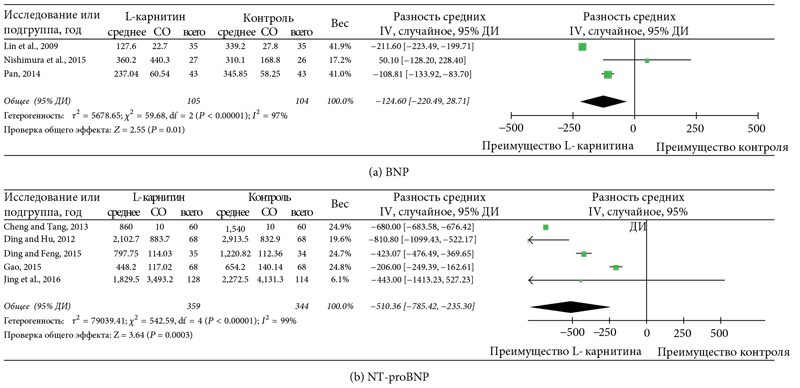
Рис. 4. Графики для сывороточных маркеров
6. Эхокардиографические показатели левого желудочка
Для 12 исследований [12, 14–16, 18, 19, 21, 23–27] с наличием данных по ФВ ЛЖ и значимой гетерогенностью (I² = 70%, р < 0,01) с использованием модели случайных параметров было показано достоверное улучшение ФВ ЛЖ у пациентов, получающих терапию L-карнитином (ВРС: 4,14%, 95% ДИ: 2,34–5,93, р = 0,01 (рис. 5а)). Как показано на рисунках 5b и 5c, значимой разницы по гетерогенности при анализе как УО [14, 23, 24], так и CВ [14, 23, 24, 27] (I² = 0%, p = 0,74, I² = 0%, р = 0,65, соответственно) выявлено не было. УО и СВ были достоверно выше у пациентов группы L-карнитина по сравнению с группой контроля (ВРС: 8,21 мл, 95% ДИ: 6,41–10,01, р = 0,01; ВРС: 0,88 л/мин, 95% ДИ: 0,76–1,01, р < 0,01, соответственно (рис. 5b и 5c)). При сравнении Е/А в исследованиях [14, 17, 21, 24, 27] была обнаружена значимая гетерогенность (I² = 82%, р < 0,01). При использовании модели случайных параметров анализ показал значимое повышение E/A у пациентов, получавших терапию L-карнитином (ВРС: 0,23, 95% ДИ: 0,11–0,35, р < 0,01 (рис. 5d)). Кроме того, терапия L-карнитином коррелировала с достоверным уменьшением КСР ЛЖ [15, 16, 19, 25, 28] и КДР ЛЖ [16, 18, 19, 25, 28] (ВРС: -4,06 мм, 95% ДИ: -6,57-1,55, р < 0,01; ВРС: -4,79 мм, 95% ДИ: -7,08-2,49, p < 0,01, соответственно (рис. 6a и 6b)). Также было показано, что в ответ на терапию L-карнитином достоверно уменьшался КСО ЛЖ [15, 19] (ВРС: -20,16, 95% ДИ: -35,65-4,67, р < 0,01 (рис. 6c)). Анализ в подгруппе с продолжительностью терапии 14–15 дней продемонстрировал статистически значимую корреляцию между ФВ ЛЖ, УО, СВ, E/A, КСР ЛЖ, и КДР ЛЖ (ВРС: 6,63%, 95% ДИ: 4,78–8,47, p < 0,01; ВРС: 9,28 мл, 95% ДИ: 5,90–12,67, p < 0,01; ВРС: 0,90 л/мин, 95% ДИ: 0,78–1,03, p < 0,01; ВРС: 0,31, 95% ДИ: 0,16–0,46, p < 0,01; ВРС: -6,50 мм, 95% ДИ: -8,11-4,89, p < 0,01; ВРС: -3,24 мм, 95% ДИ: -5,93 -0,55, p < 0,01, соответственно).
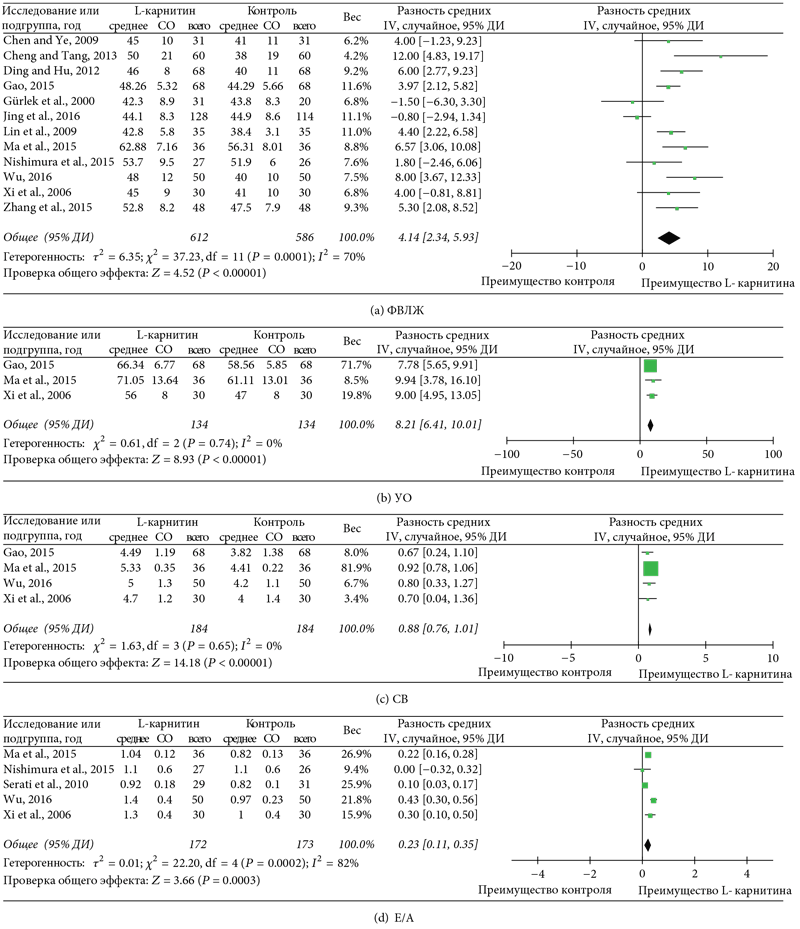
Рис. 5. Графики для эхокардиографических показателей (I)
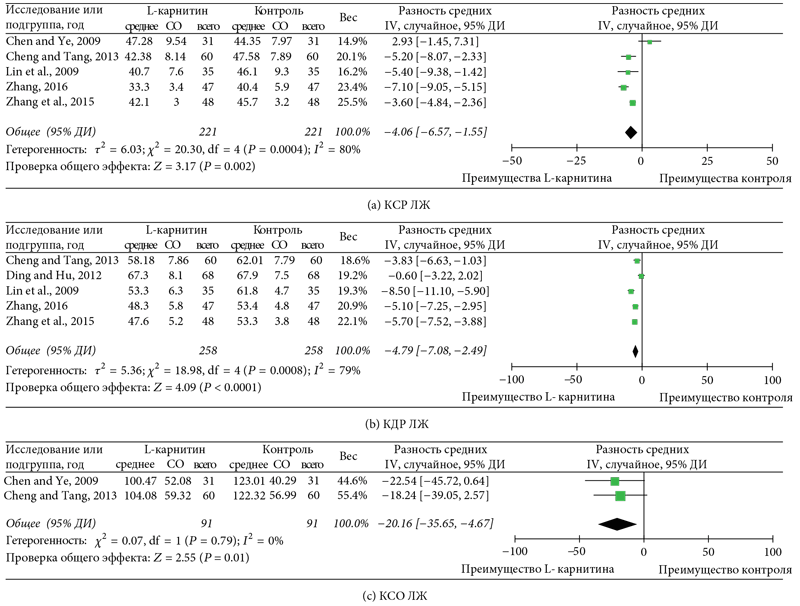
Рис. 6. Графики для эхокардиографических показателей ЛЖ (II)
7. Серьезные нежелательные явления
В 6 исследованиях [12, 14, 16, 24, 25, 28] нежелательные явления, имевшие отношение к L-карнитину, отсутствовали. В 4 исследованиях [13, 20, 23, 26] говорилось о вероятных нежелательных явлениях. В основном пациенты жаловались на сухость во рту и проблемы с желудочнокишечным трактом, также в одном исследовании [20] сообщалось о случаях высыпаний у пациентов обеих групп – контрольной (2/43) и L-карнитина (4/43). Ни один из пациентов не прекратил участия в исследованиях по причине нежелательных явлений. Метаанализ не продемонстрировал разницы в вероятности наступления нежелательных явлений между обеими группами (5,4% против 5,8%, ОШ = 0,92, 95% ДИ: 0,44–1,92, p = 0,83 (рис. 2)).
Оставшиеся 7 исследований не предоставили данных о нежелательных явлениях.
Обсуждение
L.H. Opie отмечал, что «сердце – это больше, чем просто насос». Это орган, нуждающийся в большом количестве энергии. Поэтому идеальная терапия для такого метаболического заболевания, как ишемия – это метаболическая терапия» [29]. ХСН в настоящее время рассматривается как совокупность системных заболеваний многих органов; предполагается, что в основе этого синдрома лежит метаболическая недостаточность. В сущности, больное сердце – не что иное, как «мотор без топлива» [5]. L-карнитин является природным компонентом человеческой клетки и участвует в метаболизме жирных кислот. Он играет важную роль в метаболизме жиров, являясь необходимым кофактором окисления жирных кислот и обеспечивая транспорт длинноцепочечных жирных кислот через митохондриальную мембрану, что необходимо для поступления в клетки миокарда достаточного количества АТФ [30]. Хотя в аннотации к L-карнитину в числе показаний и не стоит СН, данный обзор клинических исследований свидетельствует о существенном улучшении состояния пациентов на фоне терапии L-карнитином.
Проведенный не так давно Di Nicolantonio et al. (2013 г.) [9] метаанализ исследований применения L-карнитина при вторичной профилактике ССЗ показал, что назначение L-карнитина, по сравнению с плацебо, ассоциировалось с 27% снижением общей смертности, 65% уменьшением случаев желудочковой аритмии и 40% уменьшением случаев стенокардии у пациентов с острым инфарктом миокарда (ОИМ). При этом, данный метаанализ применения L-карнитина у пациентов с ХСН показал тенденцию по снижению смертности от любых причин. Доказано, что длительное применение L-карнитина снижает воздействие неблагоприятных факторов, связанных с метаболическим синдромом и ССЗ, например, АГ, уровнем холестерина, нарушением толерантности к глюкозе и резистентностью к инсулину. L-карнитин особенно подходит для лечения пациентов с метаболическим синдромом, страдающих ожирением и АГ с инсулинорезистентностью [31–33]. Результаты одного из включенных в обзор исследований [27] дают основание предположить, что L-карнитин может существенно ослабить неблагоприятное воздействие таких факторов, как повышенный общий холестерин и повышенное содержание глюкозы, положительно повлиять на сердечную функцию и облегчить клинические симптомы пациентов с СН и СД.
Результаты данного метаанализа свидетельствуют о том, что благоприятные эффекты заключались в повышении общей эффективности, ФВ ЛЖ, УО, СВ и отношения Е/А, уменьшении конечного диастолического и систолического размеров ЛЖ, конечного систолического объема ЛЖ и снижении уровней BNP и NT-proBNP в сыворотке крови. Также важно отметить удовлетворительную безопасность применения L-карнитина. В некоторых исследованиях [21, 24, 25] отмечалось, что вероятность улучшения клинической симптоматики, сердечной функции и функции почек у пациентов с ХСН и почечной недостаточностью выше при назначении L-карнитина. Согласно гипотезе «энергетического голода», которая предполагает, что в основе сократительной дисфункции при ХСН лежит недостаточное обеспечение миокарда АТФ [34], кажется обоснованным предположение о положительном влиянии L-карнитина на энергетический метаболизм кардиомиоцитов, что в конечном итоге отражается на механической эффективности и способствует улучшению клинической симптоматики и сердечной функции. Также следует заметить, что L-карнитин оказывает кардиопротективный эффект через альтернативные механизмы, влияя, например, на оксидативный стресс [35], уровень оксида азота (NO) [36], повышенное артериальное давление, воспалительные и фиброзные процессы в сердце [37–39], ремоделирование миокарда [40] и функции эндотелия [41]. Стоит отметить, что L-карнитин сегодня традиционно используется в лечении нарушений энергетического метаболизма и выступает, скорее, в качестве дополнения к уже существующей терапии, чем в качестве ее замещения. ХСН, однако, является заболеванием, требующим разнонаправленной терапии, которая определяется в зависимости от стадии заболевания. Выполненный метаанализ показал, что L-карнитин представляет собой безопасный и эффективный препарат, улучшающий энергетический метаболизм сердца, показатели его систолической и диастолической функций. В этом метаанализе 4 показателя имели относительно высокий уровень гетерогенности: ФВ ЛЖ, BNP, NT-proBNP и тест 6-минутной ходьбы. Следует признать и следующие ограничения – причины, которые могли повлиять на расхождения в данных исследований: (1) различная дозировка L-карнитина, (2) различные стадии заболевания и терапия у пациентов, принимавших участие в РКИ, (3) отсутствие данных по производителям L-карнитина и спецификации препаратов. В заключение нужно заметить, что, во-первых, методологическое качество включенных исследований не являлось основным критерием отбора исследований для метаанализа, поэтому исключить потенциальный риск ошибки невозможно. Во-вторых, в 17 РКИ принимало участие только 1625 пациентов. Возможно, для более точной оценки влияния L–карнитина на пациентов с ХСН стоит дождаться более масштабных исследований. В-третьих, продолжительность периода последующих наблюдений за пациентами варьировалась от 7 дней до 3 лет, что является недостаточным основанием для того, чтобы рекомендовать данный препарат для первой линии терапии, улучшения качества жизни и долговременного результата. Тем не менее, метаанализ продемонстрировал, что применение L-карнитина у пациентов с ХСН улучшает клинические симптомы и функцию сердца, уменьшает уровень BNP, NT-proBNP в сыворотке крови и хорошо переносится пациентами.
Реферат подготовлен к.м.н. Ю.Е. Ефремовой (ФГБУ «НМИЦК» Минздрава России) по материалам статьи Xiaolong Song, Huiyan Qu, Zongguo Yang, Jingfeng Rong, Wan Cai, and Hua Zhou «Efficacy and Safety of L-Carnitine Treatment for Chronic Heart Failure: A Meta-Analysis of Randomized Controlled Trials» // BioMed Research International. 2017. Vol. 2017.
Article ID 6274854, 11 p. doi:10.1155/2017/6274854.
Литература
- Ambrosy A. P., Fonarow G. C., Butler J. et al. The global health and economic burden of hospitalizations for heart failure: lessons learned from hospitalized heart failure registries // Journal of the American College of Cardiology. 2014. Vol. 63(12). P. 1123–1133.
- Spinar J., Hradec J., Spinarovґa L., Vritovec J. Summary of the 2016 ESC Guidelines on the diagnosis and treatment of acute and chronic heart failure. Prepared by the Czech Society of Cardiology // Cor et Vasa. 2016. Vol. 58(5). P. e530–e568.
- Yancy C. W., Jessup M., Bozkurt B. et al. 2013 ACCF/AHA guideline for the management of heart failure: executive summary: a report of the American college of cardiology foundation/American Heart Association task force on practice guidelines // Circulation. 2013. Vol. 128(16). P. 1810–1852.
- Doehner W., Frenneaux M., Anker S.D. Metabolic impairment in heart failure: the myocardial and systemic perspective //Journal of the American College of Cardiology. 2014. Vol. 64. P. 1388–1400.
- Neubauer S. The failing heart — an engine out of fuel // New England Journal of Medicine. 2007. Vol. 356 (11). P. 1140–1151.
- Ferrari R., Merli E., Cicchitelli G. et al. Therapeutic effects of L-carnitine and propionylL-carnitine on cardiovascular diseases: a review // Annals of the New York Academy of Sciences. 2004. Vol. 1033. P. 79–91.
- Chinese Society of Cardiology of Chinese Medical Association, Editorial Board of Chinese Journal of Cardiology. Guidelines for the diagnosis and management of chronic heart failure 2014 // Chinese Journal of Cardiology. 2014. Vol. 42 (2). P. 98–122.
- Shang R., Sun Z., Li H. Effective dosing of l-carnitine in the secondary prevention of cardiovascular disease: a systematic review and meta-analysis // BMC Cardiovascular Disorders. 2014. Vol. 14. P. 88–96.
- DiNicolantonio J.J., Lavie C.J., Fares H. et al. L-carnitine in the secondary prevention of cardiovascular disease: systematic review and meta-analysis // Mayo Clinic Proceedings. 2013. Vol. 88(6). P. 544–551.
- Higgins J.P.T., Green S., eds. Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0, The Cochrane Collaboration. 2011.Электронный ресур handbook.cochrane.org.
- Higgins J.P.T., Thompson S.G. Quantifying heterogeneity in ameta-analysis // Statistics inMedicine. 2002. Vol. 21(11). P. 1539–1558.
- GЁurlek A., Tutar E., Akcёil E. et al. The effects of L-carnitine treatment on left ventricular function and erythrocyte superoxide dismutase activity in patients with ischemic cardiomyopathy // European Journal of Heart Failure. 2000. Vol. 2(2). P. 189–193.
- Rizos I. Three-year survival of patients with heart failure caused by dilated cardiomyopathy and L-carnitine administration // American Heart Journal 2000. Vol. 139(2) P. 120–123.
- Xi H., Liang W., Wu J., Tan Z. Clinical research of L-carnitine treatment on chronic congestive heart failure // Practical Journal of Cardiac Cerebral Pneumal and Vascular Disease. 2006. Vol. 14 (9). P. 714–715.
- Chen L., Ye W. Clinical research of L-carnitine treatment on sixty-two patients with chronic congestive heart failure // China Foreign Medical Treatment. 209. Vol. 22. Article 47.
- Lin C., Li J., Tang J., Yang P. Effects of levocarnitine among patients with chronic heart failure // Zhejiang Practical Medicine. 2009. Vol. 14 (2). P. 109–110.
- Serati A.R., Motamedi M.R., Emami S. et al. R. L-carnitine treatment in patients with mild diastolic heart failure is associated with improvement in diastolic function and symptoms // Cardiology. 2010. Vol. 116(3). P. 178–182.
- Ding C., Hu X. The effectiveness of L-carnitine treatment on senile congestive heart failure //Chinese Journal of Gerontology. 2012. Vol. 32(13). P. 2881–2882.
- Cheng L., Tang X.-F. Influence of levocarnitine on heartfunction and endocrine among patients with heart failure // Chinese Journal of Epidemiology. 2013. Vol. 34(6). P. 630–632.
- Pan X. Clinical research of L-carnitine for elderly patients with chronic congestive heart failure // Zhongguo Ji Ceng Yi Yao. 2014. Vol. 21(23). P. 3550–3552.
- Nishimura M., Tokoro T., Takatani T. et al. Effects of intravenous L-carnitine on myocardial fatty acid imaging in hemodialysis patients: responders or non-responders to Lcarnitine // Springer Plus. 2015. Vol. 4. P. 353–362.
- Ding J., Feng Q. The efficiency assessment of intravenous L-carnitine on elderly patients with heart failure of coronary heart disease // Chinese Journal of Convalescent Medicine. 2015. Vol. 24(7). P. 728–729.
- Gao L. Clinical efficiencies of levocarnitine in the treatment of ischemic cardiomyopathy heart failure and its effect on myocardial cell function // Journal of Bengbu Medical College. 2015. Vol. 40(12). P. 1643–1645.
- Ma J., Zhou X., Li X. The influence of L-carnitine on patients’ cardiac function and renal function with resulting from chronic heart failure // Chinese Journal of Gerontology. 2015. Vol. 35(20). P. 5761–5762.
- Zhang W., Dai Z., Zhou J. et al. Clinical research of L-carnitine treatment on patients of cardiorenal syndrome without hemodialysis // Chinese Journal of Clinical Rational Drug Use. 2015. Vol. 8(8C). P. 61–62.
- Jing Z.-C., Wu B.-X., Peng J.-Q. et al. Effect of intravenous l-carnitine in Chinese patients with chronic heart failure // European Heart Journal, Supplement. 2016. Vol. 18 P. A27–A36.
- Wu W. The clinical effects of intravenous L-carnitine in elderly patients with heart failure of diabetes // Xin Xue Guan Bing Fang Zhi Zhi Shi. 2016. Vol. 6. P. 84–85.
- Zhang K. Clinical effects and safety of intravenous L-carnitine treatment on patients of chronic heart failure // Guide of China Medicine. 2016. Vol. 14(4). P. 153–154.
- Opie L.H. Proof that glucose-insulin-potassium provides metabolic protection of ischaemic myocardium? // Lancet. 1999. Vol. 353(9155). P. 768–769.
- Wong A.P., Niedzwiecki A., Rath M. Myocardial energetics and the role of micronutrients in heart failure: a critical review // American Journal of Cardiovascular Disease. 2016. Vol. 6(3). P. 81–92.
- Bloomgarden Z.T. Obesity, hypertension, and insulin resistance // Diabetes Care. 2002. Vol. 25(11). P. 2088–2097.
- Eckel R.H., Alberti K., Grundy S.M., Zimmet P.Z. The metabolic syndrome // The Lancet. 2010. Vol. 375(9710). P. 181–183.
- De Fronzo R.A. Pathogenesis of type 2 diabetes mellitus // Medical Clinics of North America. 2004. Vol. 88(4). P. 787–835.
- Katz A.M. Is the failing heart energy depleted? // Cardiology Clinics. 1998. Vol. 16(4). P. 633–644.
- Flanagan J. L., Simmons P. A., Vehige J., Willcox M. D., Garrett Q. Role of carnitine in disease // Nutrition and Metabolism. 2010. Vol. 7. Article 30.
- Koc A., Ozkan T., Karabay A. Z. et al. Effect of L-carnitine on the synthesis of nitric oxide in RAW 264 7 murine macrophage cell line // Cell Biochemistry and Function. 2011. Vol. 29(8). P. 679–685.
- Blanca A.J., Ruiz-Armenta M.V., Zambrano S. et al. Inflammatory and fibrotic processes are involved in the cardiotoxic effect of sunitinib: protective role of L-carnitine // Toxicology Letters. 2016. Vol. 241. P. 9–18.
- Zambrano S., Blanca A.J., Ruiz-Armenta M.V. et al. L-carnitine protects against arterial hypertension-related cardiac fibrosis through modulation of PPAR- expression // Biochemical Pharmacology. 2013. Vol. 85(7). P. 937–944.
- Omori Y., Ohtani T., Sakata Y. et al. L-Carnitine prevents the development of ventricular fibrosis and heart failure with preserved ejection fraction in hypertensive heart disease // Journal of Hypertension. 2012. Vol. 30(9). P. 1834–1844.
- Orlandi A., Francesconi A., Ferlosio A. et al. Propionyl-Lcarnitine prevents age-related myocardial remodeling in the rabbit // Journal of Cardiovascular Pharmacology. 2007. Vol. 50(2). P. 168–175.
- Dzugkoev S.G., Mozhaeva I.V., Otiev M.A. et al. Effect of L-carnitine, afobazole and their combination with L-arginine on biochemical and histological indices of endothelial dysfunctions in cobalt intoxication in rats // Patologicheskaia fiziologiia i eksperimental’naia terapiia. 2015. Vol. 59(2). P. 70–75.

