 www.binnopharmgroup.ru
www.binnopharmgroup.ru

Максилак® - это широкая линейка продуктов для взрослых и детей с рождения, для коррекции дисбактериоза и подержания баланса микрофлоры кишечника в любых ситуациях ее нарушения с удобным приемом 1 раз в день.
Максилак® – максимум для микрофлоры с заботой о себе и о семье с первого дня.
Применение синбиотика для коррекции микрофлоры кишечника и лечения пациентов с синдромом раздраженного кишечника
СтатьиК.Н. Халаиджева, В.Н. Дроздов, О.В. Рязанцева, Е.В. Ших
Первый Московский государственный медицинский университет имени И.М. Сеченова (Сеченовский Университет)
Резюме
Введение. Синдром раздраженного кишечника (СРК) - хроническое функциональное заболевание кишечника, при котором боль в животе связана с дефекацией, изменением частоты и характера стула. Высокая социально-медицинская значимость этого заболевания обусловлена большой распространенностью в мире, влиянием на качество жизни и значительными затратами для пациентов, здравоохранения и общества. В настоящее время в качестве одного из провоцирующих заболевание факторов рассматривается состояние кишечной стенки и изменение качественного и количественного состава микрофлоры кишечника. Учитывая роль микробиоты в развитии синдрома раздраженного кишечника, целесообразно применение пробиотических препаратов в качестве терапии СРК.
Цель. Оценить влияние синбиотика Максилак® на микробиоту кишечника и клинические проявления СРК.
Материалы и методы. Исследование проведено у 15 (9 женщин и 6 мужчин) больных СРК с диареей, средний возраст 42,6 ± 3,7 года. Максилак® применяли по 1 капсуле вечером во время еды в течение 21 дня. Всем больным перед началом и по окончании лечения проводили бактериологическое исследование кала и оценивали клинические проявления: частоту стула в течение недели, боль в животе по ВАШ (мм), выраженность метеоризма по ВАШ (мм).
Результаты и обсуждение. Отмечалась положительная динамика изменения микробиоты кишечника: значимое увеличение КОЕ бифидо- и лактобактерий, типичных E.coli и энтерококков. Количество КОЕ гемолитических E.coli, золотистого стафилококка и грибов рода Candida статистически значимо уменьшилось. У больных на фоне приема Максилак® частота дефекаций снизилась с 31 до 16 раз в неделю (р < 0,05); боль в животе с 55 до 35 баллов по ВАШ (р < 0,05); проявления метеоризма с 60 до 40 баллов по ВАШ (р < 0,05).
Выводы. Синбиотик Максилак® является одним из препаратов, который может быть эффективно и безопасно использован в комплексной терапии СРК.
Ключевые слова: функциональные заболевания кишечника, диарея, микробиота кишечника, пребиотик, пробиотик
Для цитирования: Халаиджева К.Н., Дроздов В.Н., Рязанцева О.В., Ших Е.В. Применение синбиотика для коррекции микрофлоры кишечника и лечения пациентов с синдромом раздраженного кишечника. Медицинский совет. 2023;17(6):-. doi.org/10.21518/ms2022-044.
Use of a synbiotic for the correction of gut microbiota and treatment of patients with irritable bowel syndrome
Kseniya N. Khalaidzheva, Vladimir N. Drozdov, О. V. Ryazantseva, Evgenia V. Shik.
Sechenov First Moscow State Medical University (Sechenov University)
Abstract
Introduction. Irritable bowel syndrome (IBS) is a chronic functional bowel disorder that presents with abdominal pain associated with defecation, a change in stool frequency and a change in the appearance of the stool. The high socio-medical significance of this disorder is determined by high global prevalence, impact on quality of life and significant costs for patients, health care and society. Currently, the intestinal wall status, and the qualitative and quantitative changes in gut microbiota are considered as one of the factors provoking the disorder. Given the role of microbiota in the development of irritable bowel syndrome, it is advisable to use probiotics as a therapy for IBS.
Aim. To evaluate the effect of synbiotic Maxilac® on the gut microbiota and clinical signs of IBS.
Materials and methods. A total of 15 (9 women and 6 men, mean age 42,6 ± 3,7 years) patients with diarrhea-predominant IBS (IBS-D) were enrolled in the study. They received Maxilac® at a dose of 1 capsule in the evening with meals for 21 days. Before and after treatment, all patients underwent bacteriological testing of faeces and assessment of clinical signs: stool frequency during the week, abdominal pain measurements using a VAS scale (mm), bloating severity measurements using a VAS scale (mm).
Results and discussion. The study showed positive changes in the intestinal microbiota: a significant growth of bifidobacteria and lactobacilli (CFU), typical E.coli and enterococci. The number of hemolytic E. coli, Staphylococcus aureus and Candida fungi (CFU) was significantly reduced. In the Maxilac® group, the defecation frequency decreased from 31 to 16 times a week (p < 0.05); abdominal pain from 55 to 35 VAS scores (p < 0.05); bloating from 60 to 40 VAS scores (p < 0.05).
Conclusions. The synbiotic Maxilac® is one of the drugs that can be efficiently and safely used as part of combination therapy for IBS.
Keywords: functional bowel disease, diarrhoea, intestinal microbiota, prebiotic, probiotic
For citation: Khalaidzheva K.N., Drozdov V.N., Ryazantseva O.V., Shikh E.V. Use of a synbiotic for the correction of gut microbiota and treatment of patients with irritable bowel syndrome. Meditsinskiy Sovet. 2023;17(6):-. (In Russ.) doi.org/10.21518/ms2022-044.
Введение
Синдром раздраженного кишечника (СРК) - хроническое функциональное заболевание, при котором боль в животе связана с дефекацией, изменением частоты и характера стула [1]. Высокая социально-медицинская значимость этого заболевания обусловлена его распространенностью в мире, которая в среднем составляет около 11%, частота СРК колеблется в зависимости от страны от 1,1 до 45,0% [2]. В метаанализе, проведенном P. Oka et al., была оценена частота СРК в точном соответствии с Римскими критериями III или IV пересмотра: совокупная распространенность СРК, по данным авторов, составила 9,2% при использовании Римских критериев III и 3,8% в исследованиях с использованием критериев IV пересмотра [3]. СРК оказывает существенное влияние на человека и его качество жизни, а также связан со значительными затратами для пациентов, систем здравоохранения и общества [4-8]. Важным является тот факт, что снижение качества жизни происходит у трудоспособной группы населения, ведь средний возраст больных СРК составляет 40 лет [9].
Современная концепция патогенеза СРК основана на генетических и психоэмоциональных факторах, взаимодействие которых формирует висцеральную гиперчувствительность и нарушение моторики кишки. Современные исследования продолжают дополнять патогенез СРК, и в настоящее время в качестве одного из провоцирующих заболевание факторов рассматривается состояние кишечной стенки и изменение качественного и количественного состава микрофлоры кишечника. L. Crouzet, E. Gaultieretal показали, что перенос фекальной микробиоты от пациентов с СРК крысам вызвал развитие симптомов аналогичных тем, что наблюдается у людей с данным диагнозом [10]. Большое количество исследований выявило снижение микробного разнообразия у пациентов с СРК [1118], а также снижение уровня Bifidobacterium, Lactobacillus и Faecalibacterium prausnitzii [19-21]. Показано наличие иммунного взаимодействия между микробиотой и хозяином, которое может вызвать слабовыраженный воспалительный ответ. Авторы указывают на повышенный уровень цитокинов и активность Toll-подобных рецепторов (TLR) на периферии у пациентов с СРК [22, 23].
Одним из провоцирующих факторов являются инфекционные гастроэнтериты. По данным метаанализа 45 исследований, включающих 21 421 человека с энтеритом, общая распространенность СРК через 12 мес. после инфекционного энтерита составляла 10,1% в течение 12 мес. после перенесенного заболевания и увеличивалась до 14,5% при сроке более 12 мес. Риск СРК был в 4,2 раза выше у пациентов, перенесших инфекционный энтерит в течение последних 12 мес. и в 2,3 раза выше у лиц, перенесших инфекционный энтерит более 12 мес. назад, чем у тех, у кого его не было [24]. T. Iacob et al. в исследовании описали, что риск развития постинфекционного СРК (ПИ СРК) после острого инфекционного гастроэнтерита (ОИГЭ) в 4,16 раза выше, чем после острой респираторной вирусной инфекции (группа контроля). Заболеваемость ПИ СРК была самой высокой у пациентов с Campylobacterjejuni по сравнению с другими агентами (в группе наблюдения было 17 больных с Clostridium difficile, 5 больных с Salmonella spp., 2 пациента с Campylobacterjejuni и пациент с ротавирусом, у которых развился ПИ СРК) [25]. Современные исследования показывают, что применение антибиотикотерапии также влияет на риск развития СРК. Увеличение количества функциональных заболеваний кишечника тесно связано с предшествующим приемом антибиотиков [26, 27]. Также в ряде исследований продемонстрирована более высокая распространенность избыточного бактериального роста в тонкой кишке у пациентов с СРК. E. D. Shah et al. в своем метаанализе показали, что дыхательные тесты чаще выявляли отклонения от нормы среди людей с СРК, чем в контрольной группе [28]. Данные еще одного недавнего метаанализа, в который было включено 25 исследований с участием 3192 пациентов с СРК и 3320 человек из контрольной группы, подтвердили более высокую распространенность синдрома избыточного бактериального роста (СИБР) в тонкой кишке у пациентов с СРК в сравнении с контрольной группой [29].
Учитывая роль микробиоты в развитии СРК, применение пробиотических препаратов в качестве терапии СРК является целесообразным. E. Simon et al. подробно описывают механизмы, с помощью которых пребиотики, пробиотики и синбиотики влияют на патофизиологию СРК: модуляцию кишечной микробиоты, улучшение барьерной функции слизистой оболочки кишечника, увеличение слоя слизи и синтеза белков плотных контактов, противовоспалительные эффекты, улучшение иммунитета кишечной стенки, а также влияние на связь между кишечником и мозгом [30]. В исследовании D. Silk, A. Davis et al. показана эффективность применения галактоолигосахарида: применение пребиотика в дозе 3,5 г/сут в сравнении с плацебо эффективно облегчало симптомы пациентов [31]. Еще в одном исследовании с участием 30 пациентов оценивалось влияние синбиотика, содержащего лакто- и бифидобактерии, а также пищевые волокна, на фекальную микробиоту взрослых с СРК с преобладанием запоров. Исследователи пришли к выводу, что ежедневное потребление кисломолочных продуктов с пробиотическими штаммами Lactobacillus acidophilus La-5 (≥6,5 х 109cfu), Bifidobacterium animalis ssp. lactis BB-12 (≥9 x 109cfu) и пищевыми волокнами (90% инулина, 10% олигофруктозы) оказало кратковременное влияние на количество и долю La-5-подобных штаммов и B.animalis ssp. lactis в фекальном микробиоме больных СРК [32]. T. Didari, Sh. Mozaffari также подтверждают способность пробиотиков уменьшать боль и тяжесть симптомов при СРК [33]. В метаанализе Y Wen, J. Li et al. по данным 17 рандомизированных контролируемых испытаний (РКИ) с участием 1 469 взрослых пациентов с СРК с преобладанием запоров сделали вывод, что в целом пробиотики значительно увеличили частоту и улучшили консистенцию стула, а побочные эффекты, связанные с пробиотиками, оказались менее опасными по сравнению со многими другими вариантами лечения, применяемыми в настоящее время. [34]. Данные еще одного метаанализа, куда было включено 53 РКИ с участием 5 545 пациентов, продемонстрировали благотворное влияние на общие симптомы СРК и боль в животе, однако, из-за значительной неоднородности между исследованиями, выделить конкретную комбинацию, виды или штаммы пробиотиков, эффективных при СРК, не представлялось возможным [35]. Использование в исследованиях отдельно или в комбинации различных штаммов бактерий, а также разные сроки лечения, приводят к сильным различиям результатов исследования эффективности данной терапии, что говорит о необходимости дальнейшего изучения видо- и штаммоспецифических эффектов микроорганизмов, входящих в состав пре-, про- и синбиотиков [36].
Одним из современных препаратов данной группы является синбиотик Максилак®, который представляет собой комплекс пробиотических и пребиотических компонентов. В состав препарата входят: бифидобактерии (Bifidobacterium longum Bl-05, Bifidobacterium breve Bb-03, Bifidobacterium bifidum Bb-06), лактобактерии (Lactobacillus acidophilus La-14®, Lactobacillus rhamnosus Lr-32®, Lactobacillus casei Lc-11®, Lactobacillus plantarum Lp-115®), молочнокислые бактерии (Lactococcus lactis Ll-23, Streptococcus thermophilus St-21), а также пребиотический компонент (фруктоолигосахариды). Препарат не содержит казеина, глютена и консервантов, а также для его производства не используется желатин животного происхождения, что позволяет применять его для лиц с непереносимостью лактозы, глютена и склонностью к аллергии. При производстве данного синбиотика используется уникальная технология SFERA® (Surrounded Freeze Release Armour), которая обеспечивает сохранность полезных бактерий при хранении, а также высокую выживаемость при прохождении агрессивных сред желудочно-кишечного тракта: желудочного сока, желчных кислот и пищеварительных ферментов. Кроме того, у синбиотика удобная схема приема - 1 раз в сутки, что способствует повышению комплаентности пациентов.
Синбиотик Максилак® хорошо зарекомендовал себя в реальной клинической практике. Так, в исследовании В.В. Ивановой, Н.В. Болдиной показана эффективность применения данного синбиотика у пациентов с хроническими заболеваниями печени. Были обследованы 60 пациентов в возрасте от 39 до 69 лет. У части пациентов отмечалась диарея, а у другой части - склонность к запорам. В ходе лечения препаратом Максилак® отмечено снижение значений биохимических маркеров, уменьшение симптоматики, а также улучшение качества жизни пациентов [37].
В нашей клинической практике также есть примеры эффективного применения синбиотика Максилак® у больных с СРК.
Целью нашего исследования было оценить влияние синбиотика Максилак® на микробиоту кишечника и клинические проявления СРК.
Материалы и методы
Исследование проведено в группе больных СРК с диарей (СРК-Д). Диагноз устанавливали на основании Римских критериев IV [38]. Под наблюдением находилось 15 больных (9 женщин и 6 мужчин), средний возраст 42,6 ± 3,7 года. Всем больным перед исследованием проводили бактериологическое исследование кала и оценивали основные клинические проявления заболевания: частота стула в течение недели, боль в животе по ВАШ (мм), выраженность метеоризма по ВАШ (мм). Всем пациентам назначали прием Максилак® по 1 капсуле вечером во время еды в течение 21 дня. По окончании исследования повторно проводили бактериологическое исследование кала и оценивали динамику клинических симптомов заболевания.
Результаты и обсуждение
Результаты бактериологического исследования у больных с СРК-Д представлены в табл. Применение синбиотика Максилак® привело к улучшению состава микрофлоры. Отмечалось статистически значимое увеличение КОЕ бифидо- и лактобактерий, типичных E.coli и энтерококков. Количество КОЕ гемолитических E.coli, золотистого стафилококка и грибов рода Candida статистически значимо уменьшалось.
Таблица.
Результаты бактериологического исследования кала у больных с СРК с диарей (медиана LgКОЕ/1 г) на фоне применения синбиотика Максилак®
Table.
Findings of the bacteriological testing of faeces in patients with IBS-D (median LgCFU/1 g) during therapy with synbiotic Maxilac®
| Показатель (норма) | До назначения препарата (n = 15) | Через 1 мес. терапии (п = 15) |
| Бифидобактерии (9-10) | 6,5 | 9* |
| Лактобактерии (7-8) | 3 | 5* |
| Клостридии (0-5) | 3 | 2,5 |
| E.coli типичные (7-8) | 5,5 | 7,5* |
| E.coli лактозонегативные (0-5) | 2,5 | 3,5 |
| E.coli гемолитические (0) | 3,5 | 2,0* |
| Proteus sp. (0-4) | 0 | 0 |
| Providencia sp. (0-4) | 0 | 0 |
| Morganella sp. (0-4) | 0 | 0 |
| Citrobacter sp. (0-4) | 0 | 0 |
| Klebsiella sp. (0-4) | 0,5 | 0 |
| Enterobacter sp. (0-4) | 0,5 | 0,5 |
| Serratia sp. (0-4) | 0 | 0 |
| Неферментирующие бактерии (0-4) | 0,5 | 0,5 |
| Золотистый стафилококк (0) | 1 | 0* |
| Другие стафилококки (0-4) | 0 | 0 |
| Энтерококки (5-8) | 3,5 | 5* |
| Грибы рода Candida (0-4) | 4,5 | 3,0* |
Примечание. *Достоверность разницы по критерию Уилкоксона, р £ 0,05.
Положительная динамика изменения микробиоты кишечника сопровождалась положительной клинической динамикой симптомов СРК-Д (рис.). У больных статистически значимо снизилась частота стула, уменьшились боли и выраженность метеоризма. Нежелательных явлений за время приема препарата в данной группе больных не отмечалось.
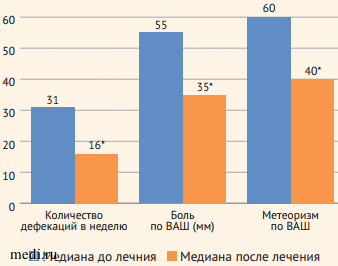 Рисунок. Положительная динамика симптомов СРК: количество дефекаций в неделю, выраженность боли в животе по ВАШ (мм), выраженность метеоризма по ВАШ (мм) на фоне терапии синбиотиком Максилак®
Рисунок. Положительная динамика симптомов СРК: количество дефекаций в неделю, выраженность боли в животе по ВАШ (мм), выраженность метеоризма по ВАШ (мм) на фоне терапии синбиотиком Максилак®Figure. Improvements in IBS symptoms: defecations per week, abdominal pain severity VAS score (mm), bloating severity VAS score (mm) during therapy with synbiotic Maxilac®
Примечание. *Достоверность разницы по критерию Уилкоксона, р £ 0,05.
Выводы
Информация об авторах:
Халаиджева Ксения Николаевна, аспирант кафедры клинической фармакологии и пропедевтики внутренних болезней, Первый Московский государственный медицинский университет имени И.М. Сеченова (Сеченовский Университет);
Дроздов Владимир Николаевич, д.м.н., профессор, профессор кафедры клинической фармакологии и пропедевтики внутренних болезней, Первый Московский государственный медицинский университет имени И.М. Сеченова (Сеченовский Университет);
Рязанцева Ольга Владимировна, к.м.н., доцент, кафедры клинической фармакологии и пропедевтики внутренних болезней, Первый Московский государственный медицинский университет имени И.М. Сеченова (Сеченовский Университет);
Ших Евгения Валерьевна, д.м.н., профессор, заведующая кафедрой клинической фармакологии и пропедевтики внутренних болезней, Первый Московский государственный медицинский университет имени И.М. Сеченова (Сеченовский Университет);
Information about the authors:
Kseniya N. Khalaidzheva, Postgraduate Student of the Department of Clinical Pharmacology and Propaedeutics of Internal Diseases, Sechenov First Moscow State Medical University (Sechenov University);
Vladimir N. Drozdov, Dr. Sci. (Med.), Professor of the Department of Clinical Pharmacology and Propaedeutics of Internal Diseases, Sechenov First Moscow State Medical University (Sechenov University);
Оlga. V. Ryazantseva, Cand. Sci. (Med.), Associate Professor of the Department of Clinical Pharmacology and Propaedeutics of Internal Diseases, Sechenov First Moscow State Medical University (Sechenov University);
Evgenia V. Shikh, Dr. Sci. (Med.), Professor, Head of the Department of Clinical Pharmacology and Propaedeutics of Internal Diseases, Sechenov First Moscow State Medical University (Sechenov University);
ЛСписок литературы / References
1. Ивашкин В.Т., Шелыгин Ю.А., Баранская Е.К., Ачкасов С.И., Белоус С.С., Белоусова Е.А. и др. Синдром раздраженного кишечника. Колопроктология. 2022;21(1):10-25.
Ivashkin V.T., Shelygin Y.A., Baranskaya E.K., Achkasov S.I., Belous S.S., Belousova E.A. et al. Irritable bowel syndrome. Koloproktologia. 2022;21(1):10-25. (In Russ.)
2. Lovell R.M., Ford A.C. Global Prevalence of and Risk Factors for Irritable Bowel Syndrome: A Meta-analysis. Clin Gastroenterol Hepatol. 2012;10(7):712-721.e4. .
3. Oka P, Parr H., Barberio B., Black CJ., Savarino E., Ford A.C. Global prevalence of irritable bowel syndrome according to Rome III or IV criteria: a systematic review and meta-analysis. Lancet Gastroenterol Hepatol. 2020;5(10):908-917.
4. Canavan C., West J., Card T. Review article: The economic impact of the irritable bowel syndrome. Aliment Pharmacol Ther. 2014;40(9):1023-1034.
5. Buono J.L., Carson R.T., Flores N.M. Health-related quality of life, work productivity, and indirect costs among patients with irritable bowel syndrome with diarrhea. Health Qual Life Outcomes. 2017;15(1):35.
6. Frandemark A., Tornblom H.,Jakobsson S., Simren M. Work Productivity and Activity Impairment in Irritable Bowel Syndrome (IBS): A Multifaceted Problem. Am J Gastroenterol. 2018;113(10):1540-1549.
7. Akehurst R.L., Brazier J.E., Mathers N., O’Keefe C., Kaltenthaler E., Morgan A. et al. Health-related quality of life and cost impact of irritable bowel syndrome in a UK primary care setting. Pharmacoeconomics. 2002;20(7):455-462.
8. El-Serag H.B., Olden K., Bjorkman D. Health-related quality of life among persons with irritable bowel syndrome: a systematic review. Aliment Pharmacol Ther. 2002;16(6):1171-1185.
9. Spelber A.D., Dumitrascu D., Fukudo S., Gerson C., Ghoshal U.C., Gwee KA. et al. The global prevalence of IBS in adults remains elusive due to the heterogeneity of studies: a Rome Foundation working team literature review. Gut. 2017;66(6):1075-1082.
10. Crouzet L., Gaultier E., Del’Homme C., Cartier C., Delmas E., Dapoigny M. et al. The hypersensitivity to colonic distension of IBS patients can be transferred to rats through their fecal microbiota. Neurogastroenterol Motil. 2013;25(3):272-282.
11. Maharshak N., Ringel Y., Katibian D., Lundqvist A., Sartor R.B., Carroll I.M. et al. Fecal and Mucosa-Associated Intestinal Microbiota in Patients with Diarrhea-Predominant Irritable Bowel Syndrome. Dig Dis Sci. 2018;63(7):1890-1899.
12. Giamarellos-Bourboulis E., Tang J., Pyleris E., Pistiki A., Barbatzas C., Brown J. et al. Molecular assessment of differences in the duodenal microbiome in subjects with irritable bowel syndrome. Scand J Gastroenterol. 2015;50(9):1076-1087.
13. Ng S.C., Lam E.F.C., Lam T.T.Y., Chan Y., Law W., Tse P.C.H. et al. Effect of probiotic bacteria on the intestinal microbiota in irritable bowel syndrome. J Gastroenterol Hepatol. 2013;28(10):1624-1631.
14. Jeffery I.B., O’Toole P.W., Ohman L., Claesson MJ., Deane J., Quigley E.M.M. et al. An irritable bowel syndrome subtype defined by speciesspecific alterations in faecal microbiota. Gut. 2012;61(7):997-1006.
15. Carroll I.M., Ringel-Kulka T., Siddle J.P., Ringel Y Alterations in composition and diversity of the intestinal microbiota in patients with diarrhea-predominant irritable bowel syndrome. Neurogastroenterol Motil. 2012;24(6):521-530.
16. Codling C., O’Mahony L., Shanahan F., Quigley E.M.M., Marchesi J.R. A molecular analysis of fecal and mucosal bacterial communities in irritable bowel syndrome. Dig Dis Sci. 2010;55(2):392-397.
17. Mei L., Zhou J., Su Y, Mao K., Wu J., Zhu C. et al. Gut microbiota composition and functional prediction in diarrhea-predominant irritable bowel syndrome. BMC Gastroenterol. 2021;21(1):105.
18. Sundin J., Aziz I., Nordlander S., Polster A., Hu Y.O.O., Hugerth L.W. et al. Evidence of altered mucosa-associated and fecal microbiota composition in patients with Irritable Bowel Syndrome. Sci Rep. 2020;10(1):593.
19. Liu H.N., Wu H., Chen Y.Z., Chen Y.J., Shen X.Z., Liu T.T. Altered molecular signature of intestinal microbiota in irritable bowel syndrome patients compared with healthy controls: A systematic review and meta-analysis. Dig Liver Dis. 2017;49(4):331-337.
20. Rajilic-Stojanovic M., Biagi E., Heilig H.G.HJ., Kajander K., Kekkonen R.A., Tims S., Vos W.M. Global and deep molecular analysis of microbiota signatures in fecal samples from patients with irritable bowel syndrome. Gastroenterology. 2011;141(5):1792-1801.
21. Liu H.N., Wu H., Chen Y.Z., Chen Y.J., Shen X.Z., Liu T.T. Altered molecular signature of intestinal microbiota in irritable bowel syndrome patients compared with healthy controls: A systematic review and meta-analysis. Dig Liver Dis. 2017;49(4):331-337.
22. Brint E.K., MacSharry J., Fanning A., Shanahan F., Quigley EMM. Differential expression of toll-like receptors in patients with irritable bowel syndrome. Am J Gastroenterol. 2011;106(2):329-336.
23. McKernan D.P., Gaszner G., Quigley E.M., Cryan J.F., Dinan T.G. Altered peripheral toll-like receptor responses in the irritable bowel syndrome. Aliment Pharmacol Ther. 2011;33(9):1045-1052.
24. Klem F., Wadhwa A., Prokop L.J., Sundt W.J., Farrugia G., Camilleri M. et al. Prevalence, Risk Factors, and Outcomes of Irritable Bowel Syndrome After Infectious Enteritis: A Systematic Review and Meta-analysis. Gastroenterology. 2017;152(5):1042-1054.e1.
25. lacob T., Tatulescu D., Lupse M., Dumitrascu D. Post-infectious irritable bowel syndrome after a laboratory-proven enteritis. Exp Ther Med. 2020;20(4):3517-3522.
26. Maxwell P.R., Rink E., Kumar D., Mendall M.A. Antibiotics increase functional abdominal symptoms. Am J Gastroenterol. 2002;97(1):104-108.
27. Paula H., Grover M., Halder S.L., Locke G.R., Schleck C.D., Zinsmeister A.R., Talley N.J. Non-enteric infections, antibiotic use, and risk of development of functional gastrointestinal disorders. Neurogastroenterol Motil. 2015;27(11):1580-1586.
28. Shah E.D., Basseri R.J., Chong K., Pimentel M. Abnormal breath testing in IBS: a meta-analysis. Dig Dis Sci. 2010;55(9):2441-2449.
29. Shah A., Talley N.J., Jones M., Kendall B.J., Koloski N., Walker M.M. et al. Small Intestinal Bacterial Overgrowth in Irritable Bowel Syndrome: A Systematic Review and Meta-Analysis of Case-Control Studies. Am J Gastroenterol. 2020;115(2):190-201.
30. Simon E., Calinoiu L.F., Mitrea L., Vodnar D.C. Probiotics, Prebiotics, and Synbiotics: Implications and Beneficial Effects against Irritable Bowel Syndrome. Nutrients. 2021;13(6):2112.
31. Silk D.B.A., Davis A., Vulevic J., Tzortzis G., Gibson G.R. Clinical trial: the effects of a trans-galactooligosaccharide prebiotic on faecal microbiota and symptoms in irritable bowel syndrome. Aliment Pharmacol Ther. 2009;29(5):508-518.
32. Bogovic Matijasic B., Obermajer T., Lipoglavsek L., Sernel T., Locatelli I., Kos M. et al. Effects of synbiotic fermented milk containing Lactobacillus acidophilus La-5 and Bifidobacterium animalis ssp. lactis BB-12 on the fecal microbiota of adults with irritable bowel syndrome: A randomized double-blind, placebo-controlled trial. J Dairy Sci. 2016;99(7):5008-5021.
33. Didari T., Mozaffari S., Nikfar S., Abdollahi M. Effectiveness of probiotics in irritable bowel syndrome: Updated systematic review with meta-analysis. World J Gastroenterol. 2015;21(10):3072-3084.
34. Wen Y., Li J., Long Q., Yue C.C, He B., Tang X. The efficacy and safety of probiotics for patients with constipation-predominant irritable bowel syndrome: A systematic review and meta-analysis based on seventeen randomized controlled trials. Int J Surg. 2020;79:111-119.
35. Ford A.C., Harris L.A., Lacy B.E., Quigley E.M.M., Moayyedi P. Systematic review with meta-analysis: the efficacy of prebiotics, probiotics, synbiotics and antibiotics in irritable bowel syndrome. Aliment Pharmacol Ther. 2018;48(10):1044-1060.
36. Harris L.A., Baffy N. Modulation of the gut microbiota: a focus on treatments for irritable bowel syndrome. Postgrad Med. 2017;129(8):872-888.
37. Иванова В.В., Болдина Н.В. Клиническая эффективность препарата Максилак в терапии хронических заболеваний печени. В: Поколение будущего: взгляд молодых ученых: сборник научных статей 9-й Международной молодежной научной конференции. Курск, 12-13 ноября 2020 г. Курск: Юго-Западный государственный университет (Курск); 2020. Т. 3. С. 223-225.
Ivanova V.V., Boldina N.V. Clinical efficacy of the drug Maksilak in the treatment of chronic liver diseases. In: Next generation: a view of young researchers: collection of scholarly articles of the 9th International Young Researchers' Conference. Kursk, November 12-13, 2020, Kursk: Southwest State University (Kursk); 2020. Volume 3. p. 223-225. (In Russ.)
38. Mearin F., Lacy B.E., Chang L., Chey W.D., Lembo AJ., Simren M., Spiller R. Bowel Disorders. Gastroenterology. 2016;S0016-5085(16)00222-5.
