Сравнительное исследование противовоспалительном активности пиритиона цинка на лабораторной модели псориаза
Статьи
Опубликовано в журнале:
Вестник дерматологии и венерологии. 2020; 97 (2): 64-70
Жуков А.С.*, Хайрутдинов В.Р., Самцов А.В.
ФГБВОУ ВО «Военно-медицинская академия им. С. М. Кирова» Министерства обороны Российской Федерации
194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6
Псориаз является хроническим иммуноопосредованным воспалительным заболеванием с преимущественным поражением кожи. Наружная терапия – важное направление лечения таких больных. Нестероидные противовоспалительные средства на основе цинка пиритиона не обладают побочными эффектами, присущими глюкокортикостероидным препаратам, и могут быть им альтернативой. Оценку эффективности действия препаратов не всегда удобно проводить на человеке. Использование лабораторной модели заболевания позволяет изучать изменения клинических, гистологических и иммуногистохимических характеристик кожи при терапии топическими препаратами.
Цель. На лабораторной модели псориаза провести сравнительную оценку противовоспалительной эффективности скин-капа в сравнении с другими препаратами.
Материалы и методы. В эксперименте использовали инбредных мышей Balb/c в количестве 50 особей, рандомизированных на 5 групп. Формирование модели псориаза проводили имиквимодом, после чего мышам I группы выполняли эвтаназию с биопсией кожи. Мышам II группы наносили крем цинк пиритион активированный (скин-кап), III группы – крем пиритион цинка (цинокап), IV группы – крем бетаметазона дипропионат (акридерм) – 2 р/д – 14 дней. V группа находилась под наблюдением без терапии. Ежедневно проводили клиническую оценку по модифицированному индексу PASI (mPASI). На 29-й день исследования мышам II-V групп выполняли эвтаназию и получали биоптаты кожи, которые исследовали гистологическим (толщина эпидермиса, выраженность воспалительного инфильтрата) и иммуногистохимическим методами (Ki-67, CD3). Достоверными считали различия при p<0,05.
Результаты. Исходное значение индекса mPASI было 7,2 [5,2-9,3]. Индекс mPASI в группе, получающей скин-кап, составил 1,8 [1,1-3,2], пиритион цинка – 2,9 [2,1-4,2] и бетаметазона дипропионат – 1,3 [1,0-3,1], что значительно ниже, чем в группе без терапии – 5,8 [5,0-6,8] (p<0,05). При гистологическом исследовании у животных, получавших цинк пиритион активированный, наблюдалось более выраженное снижение толщины эпидермиса (в 2,7 раза), чем при использовании пиритион цинка (в 2 раза) и в то же время отсутствовали явления атрофии кожи, выявляемые при лечении бетаметазона дипропионатом. При иммуногистохимическом анализе показано наиболее значимое снижение пролиферативной активности эпидермиса и количества Т-лимфоцитов при использовании бетаметазона дипропионата и цинка пиритиона активированного.
Выводы. Установлено, что применение препарата скин-кап приводит к подавлению воспалительного процесса в коже, сравнимое по эффективности с сильным топическим глюкокортикостероидом. У скин-капа отсутствует атрофогенный эффект, что позволяет рекомендовать данный препарат в качестве длительно поддерживающего топического средства у больных псориазом при любой локализации высыпаний.
Ключевые слова: псориаз, наружная терапия, скин-кап, цинк пиритион, модель псориаза, имиквимод.
Конфликт интересов: авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Для цитирования: Жуков А.С., Хайрутдинов В.Р., Самцов А.В. Сравнительное исследование противовоспалительной активности пиритиона цинка на лабораторной модели псориаза. 2020; 97 (2): 64-70. doi.org/10.25208/vdv1119
Comparative study of anti-inflammatory activity of zinc pyrition on a psoriasis laboratory model
Alexander S. Zhukov*, Vladislav R. Khairutdinov, Aleksey V. Samtsov
Federal state budgetary educational institution of higher military education “Military Medical Academy named after S.M. Kirov” of the Russian Ministry of Defense
Akademika Lebedeva str., bldg 6, Saint Petersburg, 194044, Russian Federation
Psoriasis is a chronic immune-mediated inflammatory disease with predominant skin lesions. External therapy is an important area of treatment for such patients. Non-steroidal anti-inflammatory drugs based on zinc pyrithione do not have side effects inherent in the glucocorticosteroid drug and can be an alternative to them. Evaluation of the effectiveness of drugs is not always convenient in humans. The use of laboratory models allows us to study changes in the clinical, histological and immunohistochemical characteristics of the skin during topical therapy.
Goal. On laboratory models of psoriasis, conduct a comparative assessment of the anti-inflammatory effectiveness of Skin-cap in comparison with other drugs.
Materials and methods. In the experiment, 50 Balb / c inbred mice were used, randomized to 5 groups. The formation of a model of psoriasis by listening to them, after which I perform euthanasia with a skin biopsy in mice. Group II mice are treated with activated zinc pyrithione cream (Skin-cap), group III – zinc pyrithione cream (Zinocap), group IV – betamethasone dipropionate cream (Akriderm) – 2 p/d – 14 days. Group V was monitored without therapy. The Clinical PASI Index (mPASI) score is given daily. On the 29 day of studies, group II-V mice undergo euthanasia and skin biopsies, which were examined histologically (epidermal thickness, severe inflammatory infiltrate) and immunohistochemical methods (Ki-67, CD3). The differences were considered significant at p<0.05.
Results. The initial mPASI index value was 7.2 [5.2-9.3]. The mPASI index in the Skin-cap group was 1.8 [1.1-3.2], zinc pyrithione 2.9 [2.1-4.2] and betamethasone dipropionate 1.3 [1.0] -3.1], which is significantly lower than in the group without therapy – 5.8 [5.0-6.8] (p <0.05). A histological examination in mice receiving zinc pyrithione-activated showed a more pronounced decrease in the thickness of the epidermis (2.7 times) than with pyrithione zinc (2 times) and, immunohistochemical analysis showed the most significant decrease in the proliferative activity of the epidermis and the number of T-lymphocytes when using betamethasone and zinc pyrithione activated.
Conclusions. It was found that the use of the drug leads to the suppression of the inflammatory process in the skin, comparable in effectiveness with a strong topical glucocorticosteroid. Skin-cap has no atrophogenic effect, which allows us to recommend this drug for the treatment of psoriasis patients with any localization of rashes.
Keywords: psoriasis, external therapy, skin-cap, zinc pyrithione, psoriasis model, imiquimod.
Conflict of interest: the authors states that there is no potential of interest requiring disclosure in this article.
For citation: Alexander S. Zhukov, Vladislav R. Khairutdinov, Aleksey V. Samtsov. Comparative study of anti-inflammatory activity of zinc pyrition on a psoriasis laboratory model. 2020; 97 (2): 64-70. doi.org/10.25208/vdv1119
Псориаз – хроническое мультифакториальное иммуноопосредованное заболевание кожи. Ключевым звеном патогенеза считается дисбаланс про- и противовоспалительных цитокинов, приводящий к развитию хронического воспалительного процесса в эпидермисе и дерме.
Наружная терапия имеет большое значение для больных псориазом. При легкой степени тяжести ее получают больные в качестве монотерапии, а при среднетяжелом и тяжелом течении – как дополнительное лечение [1].
Современные алгоритмы наружной терапии псориаза предполагают использование топических глюкокортикостероидных (ГКС) и других противовоспалительных препаратов. Эффективность и безопасность ГКС хорошо известны, однако возникающие при длительном применении такие нежелательные явления, как развитие вторичной инфекции, атрофии кожи, телеангиэктазии, акнеформной сыпи, гипертрихоза, ограничивают длительность их применения. Кроме того, назначение ГКС препаратов при высыпаниях в области лица, половых органов и крупных складках кожи значительно повышает вероятность появления нежелательных явлений [2].
Приверженность местной терапии является ключевой проблемой при псориазе. Зачастую именно стероидофобия может приводить к снижению комплаентности и отсутствию эффекта от лечения, что сопровождается неудовлетворенностью терапией и низким качеством жизни пациента [3].
В связи с этим нестероидные противовоспалительные средства на основе цинка пиритиона могут быть альтернативой топическим ГКС препаратам в терапии псориаза [4].
Пиритион цинка обладает антибактериальными, противовоспалительными и антипролиферативными свойствами, в то же время на нормально делящиеся клетки не оказывает негативного действия. Установлена также способность цинка ингибировать выделение гистамина тучными клетками и уменьшать зуд кожи [5].
Для оценки эффективности топических препаратов на основе пиритиона цинка, сравнения их силы действия с ГКС и возможности развития нежелательных явлений весомый вклад могут внести экспериментальные работы на лабораторных животных. Они позволяют достаточно быстро моделировать проявления заболевания и в то же время менее строги в этических аспектах [6].
Особый интерес вызывает имиквимод-индуцированная модель, на которую приходится значительная доля исследований псориаза во всем мире. Это объясняется как доступностью условий для формирования модели, так и ее патогенетическим и морфологическим сходством с дерматозом.
Оценка противовоспалительной активности цинка пиритиона активированного и исследование наличия у него атрофогенного действия представляют научный и практический интерес.
Цель исследования. На лабораторной модели псориаза провести сравнительную оценку противовоспалительной эффективности скин-капа в сравнении с другими препаратами.
Материалы и методы исследования
В эксперименте использовали инбредных мышей Balb/c в количестве 50 особей. Формирование псориазиформного воспаления кожи проводили путем ежедневного нанесения препарата имиквимод 1 раз в день в течение 14 дней – острая модель воспаления «Имиквимод индуцированный псориаз у мышей».
После индукции модели мышей рандомизировали на 5 групп по 10 особей (рис. 1). Мышам I группы на 15-й день провели эвтаназию с биопсией кожи. Мышам II группы наносили крем с цинком пиритионом активированным (скин-кап), III группы – крем с пиритионом цинка (цинокап), IV группы – крем с бетаметазоном дипропионатом (акридерм) по 2 раза в день – 14 дней. Контрольная группа мышей (V) находилась под наблюдением без терапии.
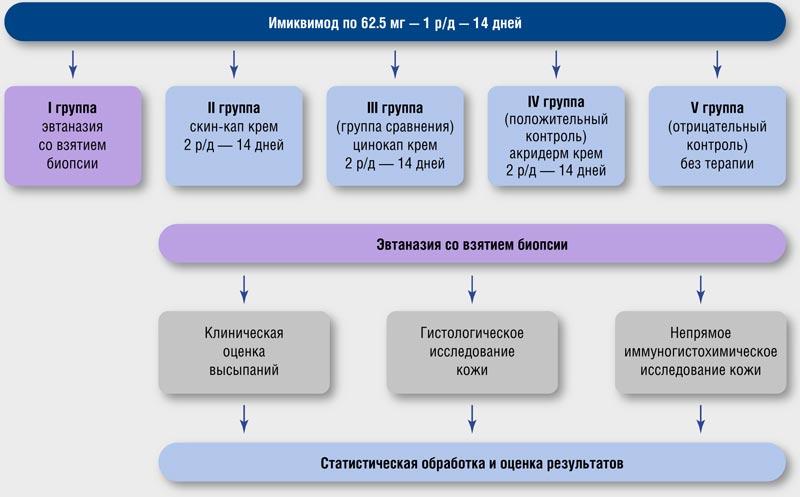 Рис. 1. Дизайн исследования
Рис. 1. Дизайн исследования
Fig. 1. Study design
Ежедневно проводили клиническую оценку тяжести воспаления кожи с помощью PASI-модифицированного индекса (mPASI). Определяли показатели: эритема, индурация, шелушение по пятибалльной шкале от 0 до 4.
На 29-й день исследования мышам II-V групп проводили эвтаназию. С полученными биоптатами кожи выполняли гистологическое (толщина эпидермиса, выраженность акантоза, гиперкератоза и воспалительного инфильтрата) и иммуногистохимическое исследование (пролиферативная активность клеток эпидермиса – маркер Ki-67, содержание лимфоцитов – маркер CD3). Выраженность гистологических изменений оценивали по четырехбалльной шкале («-» – отсутствие признака, «+» – слабо выраженный, «++» – средней выраженности, «+++» – выраженный признак). Для определения количества окрашенных клеток при иммуногистохимическом исследовании анализировали 3 поля зрения при увеличении х200, выбранные с учетом наибольшего количества меченых клеток.
Статистическая обработка данных проводилась с использованием программы «STATISTICA 10.0» (StatSoft, Inc). Для сравнения данных между группами применяли U-критерий Манна-Уитни. Достоверным считали различия при p<0,05.
Результаты исследования
После индукции модели воспаления имиквимодом на коже мышей на 14-й день отмечалось формирование псориазиформных элементов. На 28-й день исследования в V группе клинические изменения были выражены значительно, во II, III – слабо (рис. 2) (табл. 1). В группе II, получающей цинка пиритион активированный, индекс mPASI был ниже, чем в группе III пиритиона цинк. При использовании глюкокортикостероидного препарата наблюдались наименьшие значения индекса mPASI, но статистически значимых различий в группах II (цинк пиритион активированный) и IV (бетаметазона дипропионат) не выявлено (p>0,05).
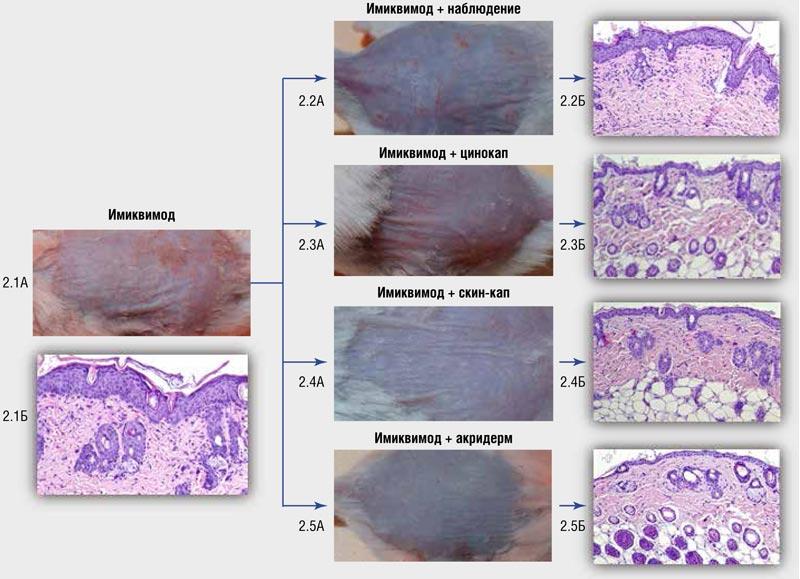 Рис. 2. Данные клинического (А) и гистологического (Б) исследования кожи в группе I – имиквимода (2.1), V – наблюдения (2.2), III – цинокапа (2.3), II – скин-капа (2.4), IV – акридерма (2.5)
Рис. 2. Данные клинического (А) и гистологического (Б) исследования кожи в группе I – имиквимода (2.1), V – наблюдения (2.2), III – цинокапа (2.3), II – скин-капа (2.4), IV – акридерма (2.5)
Fig. 2. Data of clinical (A) and histological (B) studies of the skin in group I – Imiquimod (2.1), V – observation (2.2), III – Cinocap (2.3), II – Skin-cap (2.4), IV – Akriderm (2.5)
Таблица 1. Клиническая оценка тяжести изменения кожи в исследуемых группах
Table 1. Clinical assessment of the severity of skin changes in the study groups
| № | Препарат | Эритема | Индурация | Шелушение | mPASI |
| 1 | Имиквимод (И) | 2,1 [1,5-2,6] | 3,1 [2,1-3,6] | 2 [1,2-2,3] | 7,2 [5,2-9,3] |
| 2 | И+цинка пиритион активированный (скин-кап) | 0,8 [0,5-1,2] | 0,5 [0,3-0,9] | 0,5 [0,2-0,8] | 1,8 [1,1-3,2] |
| 3 | И+пиритион цинка (цинокап) | 1,1 [0,9-1,7] | 1,1 [0,8-1,6] | 0,7 [0,4-0,9] | 2,9 [2,1-4,2] |
| 4 | И+бетаметазона дипропионат (акридерм) | 0,5 [0,3-0,8] | 0,8 [1,0-1,9] | 0 [0-0,2] | 1,3 [1,0-3,1] |
| 5 | И+наблюдение | 1,9 [1,4-2,5] | 2,7 [2,1-3,5] | 1,2 [0,9-1,8] | 5,8 [5,0-6,8] |
При оценке гистологических изменений в I группе (имиквимод) наблюдались характерные для псориаза признаки: в эпидермисе акантоз и паракератоз, в верхних слоях дермы – лимфогистиоцитарный инфильтрат и расширение сосудов (рис. 2). В V группе выявлено частичное уменьшение этих проявлений. При применении бетаметазона дипропионата и цинка пиритиона активированного обнаружено наиболее значимое уменьшение толщины эпидермиса и выраженности лимфогистиоцитарного инфильтрата (табл. 2). В то же время при применении глюкокортикостероидного крема наблюдались начальные проявления стероидной атрофии кожи (гипотрофия клеток эпидермиса и дермы, сглаживание эпидермальных отростков), что не отмечалось в группе, получающей цинк пиритион активированный.
Таблица 2. Гистологические изменения кожи исследуемых групп
Table 2. Histological changes in the skin of the studied groups
| № | Препарат | Толщина эпидермиса, мкм | Акантоз | Гиперкератоз | Лимфогистиоцитарный инфильтрат |
| 1 | Имиквимод (И) | 94 [84-108] | +++ | +++ | +++ |
| 2 | И+цинка пиритион активированный | 23 [16-26] | + | – | – |
| 3 | И+пиритион цинка | 31 [25-37] | + | + | + |
| 4 | И+бетаметазона дипропионат | 17 [14-21] | – | – | – |
| 5 | И+наблюдение | 62 [55-71] | ++ | ++ | ++ |
При иммуногистохимическом анализе проводили оценку площади экспрессии СD3+-клеток (маркер Т-лимфоцитов) и Ki67+-клеток (маркер пролиферации) (табл. 3). Установлено, что в группе I (имиквимод) наблюдалось наиболее выраженное количество CD3+-клеток.
Таблица 3. Уровень экспрессии иммуногистохимических маркеров
Table 3. Expression level of immunohistochemical markers
| № | Группа | CD3+-клетки | Ki67+-клетки |
| 1 | Имиквимод (И) | 45 [39-52] | 92 [82-103] |
| 2 | И+цинка пиритион активированный | 11 [8-16] | 28 [22-34] |
| 3 | И+пиритион цинка | 16 [12-19] | 33 [27-39] |
| 4 | И+бетаметазона дипропионат | 8 [2-13] | 22 [16-29] |
| 5 | И+наблюдение | 35 [30-43] | 63 [56-69] |
На фоне проводимой терапии отмечалось уменьшение количества CD3+-клеток в коже: наименьшее количество обнаружено в группе IV (бетаметазона дипропионат), далее – в нарастающем порядке: в группе II (цинк пиритион активированный) и группе III (пиритион цинка) (рис. 3). Выявлено, что уровень пролиферативной активности клеток кожи в группах, где применяли препараты (II, III, IV), значительно ниже, чем в группах без терапии (I, V) (рис. 4). При сравнении групп, получающих лечение, не обнаружено статистически значимых различий, но отмечено, что наиболее выраженное снижение пролиферативной активности наблюдалось в группе IV (бетаметазона дипропионат), затем – в группе II (цинк пиритион активированный) и наименьшее – в группе III (пиритион цинка) и V (наблюдение).
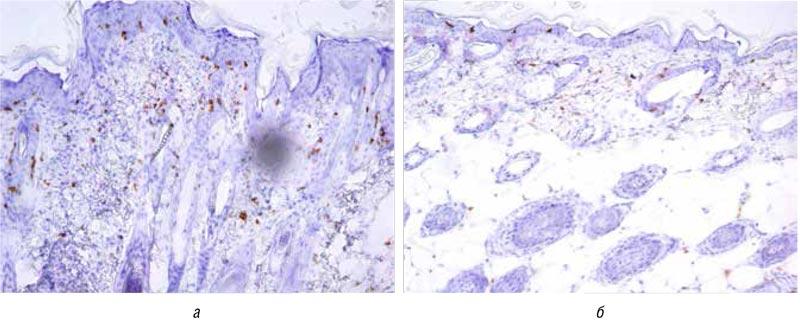 Рис. 3. Непрямое иммуногистохимическое исследование CD3+-клеток в коже на лабораторной модели псориаза до терапии (а), после терапии препаратом скин-кап (б)
Рис. 3. Непрямое иммуногистохимическое исследование CD3+-клеток в коже на лабораторной модели псориаза до терапии (а), после терапии препаратом скин-кап (б)
Fig. 3. Indirect immunohistochemical study of CD3+ cells in the skin on laboratory model of psoriasis before therapy (a), after therapy with Skin-cap (b)
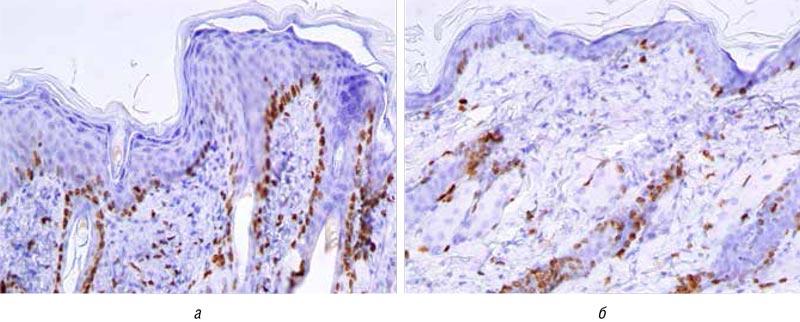 Рис. 4. Непрямое иммуногистохимическое исследование Ki-67+-клеток в коже на лабораторной модели псориаза до терапии (а), после терапии препаратом скин-кап (б)
Рис. 4. Непрямое иммуногистохимическое исследование Ki-67+-клеток в коже на лабораторной модели псориаза до терапии (а), после терапии препаратом скин-кап (б)
Fig. 4. Indirect immunohistochemical study of Ki-67+ cells in the skin on laboratory model of psoriasis before therapy (a), after therapy with Skin-cap (b)
Обсуждение
На лабораторной модели псориаза нам удалось провести клиническую и патоморфологическую оценку противовоспалительного эффекта препарата скин-кап и сравнить его с другими топическими лекарственными средствами.
Экспериментальная модель заболевания позволяет проводить клиническое, гистологическое и иммуногистохимическое исследование динамики изменений, происходящих в эпидермисе и дерме в процессе терапии наружными препаратами [6].
В ходе исследования выявлено, что применение препарата цинка пиритиона активированного приводит к выраженному разрешению высыпаний, проявляющемуся в уменьшении эритемы, шелушения и индурации кожи. Противовоспалительный эффект скин-капа был сопоставим с галогенизированным глюкокортикостероидом, лишь незначительно уступая ему. Другой аналог – пиритиона цинк (цинокап) уступал по противовоспалительной активности.
Гистологическое исследование кожи в изучаемых группах показало, что все препараты вызывают уменьшение толщины кожи за счет значительного разрешения акантоза в эпидермисе. Отмечено, что в группе, получающей скин-кап, на 29-й день исследования гиперкератоз и лимфогистиоцитарный инфильтрат практически не наблюдались, как и в группе, получающей бетаметазона дипропионат. В то же время выявленные при лечении бетаметазона дипропионатом проявления стероидной атрофии кожи (истончение эпидермиса за счет уменьшения размеров кератиноцитов, сглаживание эпидермальных отростков) отсутствовали в группе пациентов, применяющих скин-кап.
Изучение результатов иммуногистохимического анализа кожи показало, что применение противовоспалительных препаратов приводит к нормализации скорости деления клеток эпидермиса. Наиболее выраженный эффект установлен при использовании бетаметазона дипропионата, почти такой же у скин-капа, менее выраженный – у пиритиона цинка (цинокап). Исследование уровня экспрессии маркера СD3-лимфоцитов выявило сходную тенденцию, при использовании скин-капа наблюдалось четырехкратное снижение содержания Т-лимфоцитов в коже.
Применение препарата цинка пиритиона активированного при имиквимод-индуцированном псориазиформном воспалении сопровождается значительным уменьшением количества клеток-эффекторов воспаления, что приводит к снижению уровня воспаления и проявляется клиническим улучшением. При этом гибель клеток происходит по апоптотическому пути, что доказано как in vitro, так и in vivo, и не сопровождается дополнительным выбросом медиаторов воспаления из погибших клеток. Свойство пиритиона цинка активировать апоптоз определяется наличием в нем ионов цинка. Активации апоптоза кератиноцитов пиритионом цинка предшествует выраженное противовоспалительное действие препарата, которое проявляется угнетением синтеза провоспалительных цитокинов лимфоцитами и кератиноцитами [5].
Выводы
В ходе проведенного экспериментального исследования на имиквимод-индуцированной лабораторной модели воспаления установлено, что применение препарата скин-кап приводит к подавлению воспалительного процесса в коже, сравнимое по эффективности с сильным топическим глюкокортикостероидом и превосходящее по силе действия его аналог.
Отсутствие атрофогенного эффекта на лабораторной модели псориаза позволяет предполагать сходные результаты при лечении человека.
Литература/References
- Федеральные клинические рекомендации. Дерматовенерология 2015: Болезни кожи. Инфекции, передаваемые половым путем. 5-е изд., перераб. и доп. М.: Деловой экспресс, 2016. 768 с. [Federal clinical guidelines. Dermatovenerology 2015: Skin diseases. Sexually transmitted infections. 5th ed., Revised. and add. M.: Business Express 2016. 768 p. (Russia).]
- Самцов А. В. Акне и акнеформные дерматозы. Монография. 2-е издание дополненное и переработанное. М.: ООО «ФАРМТЕК», 2014. 352 с. [Samtsov A. V. Acne and acneform dermatoses. Monograph. 2nd edition updated and revised. M.: PHARMTEC LLC, 2014. 352 p. (Russia).]
- Heath M. S., Kolli S. S., Dowling J. R., Cline A., Feldman S. R. Pharmacotherapeutic strategies for standard treatment-resistant psoriasis. Expert Opin Pharmacother. 2019 Mar; 20 (4): 443-454.
- Круглова Л. С., Петрий М. Н., Генслер Е. М. Оценка эффективности применения активированного пиритион цинка в терапии больных псориазом. Клиническая дерматология и венерология. 2019; 18 (5): 616-623. [Kruglova L. S., Petriy M. N., Gensler E. M. Evaluation of the effectiveness of activated zinc pyrithione in the treatment of psoriasis patients. Clinical Dermatology and Venereology. 2019; 18 (5): 616-623 (Russia).]
- Фассахов Р. С. Пиритион цинка в комплексной терапии атопического дерматита: патогенетическое обоснование и результаты исследований. Медицинский совет. 2017; 20: 171-176. [Fassakhov R. S. Zinc pyrithione in the treatment of atopic dermatitis: pathogenetic rationale and research results. Medical advice. 2017; 20: 171-176 (Russia).]
- Жуков А. С., Лавров Н. В., Хайрутдинов В. Р., Самцов А. В. Модели псориаза на лабораторных животных: современное состояние проблемы. Иммунология. 2019; 40 (2): 64-69. [Zhukov A. S., Lavrov N. V., Khayrutdinov V. R., Samtsov A. V. Models of psoriasis in laboratory animals: current status of the problem. Immunology. 2019; 40 (2): 64-69 (Russia).]
Информация об авторах
Жуков Александр Сергеевич – к.м.н., докторант кафедры кожных и венерических болезней
Хайрутдинов Владислав Ринатович – д.м.н., доцент, доцент кафедры кожных и венерических болезней
Самцов Алексей Викторович – д.м.н., профессор, заведующий кафедрой кожных и венерических болезней
Information about the authors
Alexander S. Zhukov – Cand. Sci. (Med.); Doctoral Student of the Department of Skin and Veneral Diseases
Vladislav R. Khairutdinov – Dr. Sci. (Med.); Assoc. Prof.; Assoc. Prof. of the Department of Skin and Veneral Diseases
Alexey V. Samtsov – Dr. Sci. (Med.); Prof.; Head of the Department of Skin and Veneral Diseases
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 invar.ru
invar.ru

 invar.ru
invar.ru
