Особенности течения ко-инфекции COVID-19 и ОРВИ у детей раннего возраста
СтатьиЛ.Н. Мазанкова1, 2, д-р мед. наук, профессор, И.М. Османов1, д-р мед. наук, профессор, Н.А. Драчева3, канд. мед. наук, Э.Р. Самитова1, 2, д-р мед. наук, Е.П. Каурова1, Г.С. Брагина4
1 - ГБУЗ «Детская городская клиническая больница им. З.А. Башляевой Департамента здравоохранения г. Москвы»
2 - ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, г. Москва
3 - ГБУЗ «Детская городская клиническая больница им. Н.Ф. Филатова Департамента здравоохранения г. Москвы»
4 - ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. Н.Ф. Гамалеи» Минздрава России, г. Москва
Ключевые слова: COVID-19, ОРВИ, ко-инфекция, дети раннего возраста, интерферонотерапия
Keywords: COVID-19, acute respiratory viral infections (ARVI), co-infection, young children, interferon therapy
Резюме. В статье представлены современные данные о частоте встречаемости и этиологической структуре коинфекций COVID-19/ОРВИ у детей раннего возраста. Выделены отдельные клинико-диагностические признаки, отличающие COVID-19/ОРВИ от моноварианта коронавирусной инфекции в зависимости от этиологии респираторного вируса.
Summary. The article presents current data on the incidence and etiological structure of COVID-19/ARVI infections in young children. Separate clinical and diagnostic signs have been identified that distinguish COVID-19/ARVI from the monovariant of coronavirus infection, depending on the etiology of the respiratory virus.
Для цитирования: Особенности течения ко-инфекции COVID-19 и ОРВИ у детей раннего возраста / Л.Н. Мазанкова [и др.] // Практика педиатра. 2025. № 1. С. 4-10.
For citation: Features of the course of COVID-19 co-infection and acute respiratory viral infections in young children / L.N. Mazankova [et al.] // Pediatrician's Practice. 2025;(1): 4-10. (In Russ.)
ВВЕДЕНИЕ
В настоящее время ко-инфекции COVID-19 с другими острыми респираторными вирусными инфекциями (ОРВИ) у детей в раннем возрасте представляют проблему в инфектологии в связи с малочисленностью клинических наблюдений по данному вопросу, в том числе по их распространенности и клиническим особенностям течения инфекции и противоречивостью имеющихся данных.
Исследования показывают, что распространенность сочетанных инфекций COVID-19 и ОРВИ сильно варьирует и, по оценкам, составляет от 0,6 до 45% [1]. Частота распространенности респираторных патогенов среди детей раннего возраста была значительно ниже в начале пандемии в 2020 г., чем в 20212023 гг. [2].
Этиологический пейзаж заметно изменялся: во время пандемии 2020-2021 гг. коронавирус SARS-CoV-2 преобладал, вытесняя другие респираторные вирусы, тогда как в 2022-2023 гг. наблюдался рост заболеваемости ОРВИ, в структуре которых лидировали вирусы гриппа, РС-вирусы, риновирусы и другие [3-4].
В ходе исследования Pimenta и соавт., проведенного среди детей в возрасте до 3 лет, SARS-CoV-2 был выявлен в 2,9% случаев всех острых респираторных инфекций [5]. Показатель госпитализации детей раннего возраста с COVID-19 был значительным, многим из которых требовалась интенсивная терапия [4].
Примерно у 10,9% госпитализированных детей с COVID-19 наблюдались сопутствующие инфекции, вызванные преимущественно респираторно-синцитиальным вирусом (РСВ) и энтеровирусом/ринови-русом [6].
Систематический обзор показал, что у 9,3% детей с COVID-19 наблюдались бактериальные, грибковые или респираторно-вирусные сопутствующие инфекции, причем наиболее распространенным вирусным сопатогеном является РСВ [7, 10, 12].
У детей с ко-инфекцией заболевание протекает более тяжело: 38% требовали интенсивной терапии по сравнению с 25,7% у детей с моноинфекцией COVID-19 [6]. Ко-инфекции были связаны с более высокой заболеваемостью и большей потребностью в поддерживающей терапии [8].

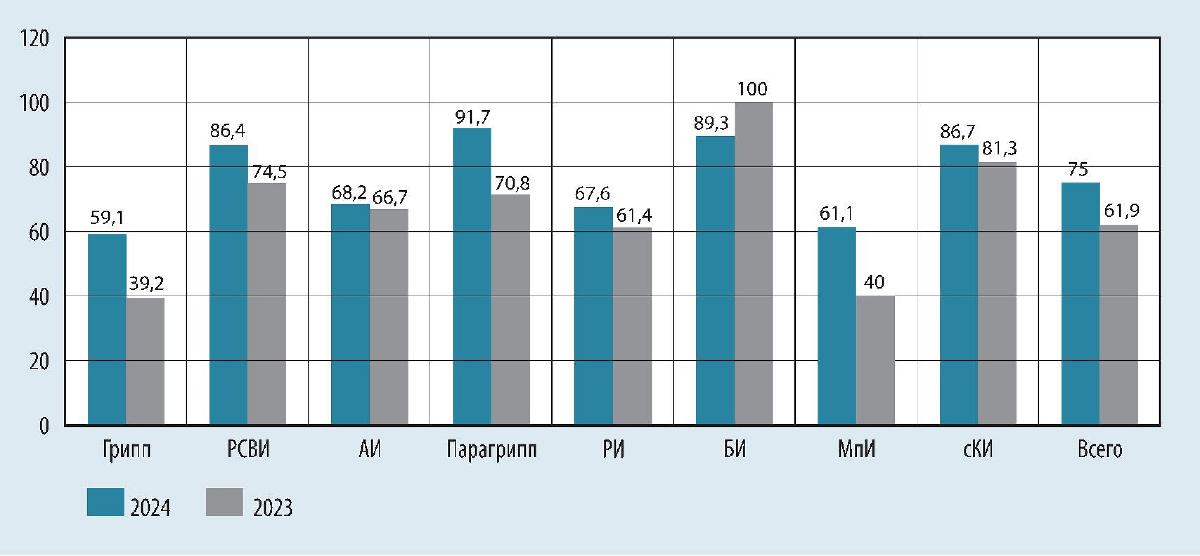
Рис. 1. Распространенность ко-инфекций COVID-19/ОРВИ в 2023-2024 гг. среди детей раннего возраста (от 0 до 3 лет) в зависимости от этиологии ОРВИ, %
Наличие нескольких возбудителей усложняет диагностику COVID-19 [9]. Для точного обнаружения респираторных вирусов рекомендуется мультиплексное ПЦР-тестирование [9]. И наоборот, хотя сопутствующие инфекции связаны с утяжелением заболевания, некоторые исследования показывают, что общая частота сопутствующих инфекций у детей с COVID-19 ниже, чем у взрослых, что указывает на потенциальную разницу в иммунном ответе или характере их воздействия [7].
Таким образом, на данный момент доступны малочисленные, весьма противоречивые исследования, описывающие распространенность, этиологическую структуру и клинические симптомы ко-инфекций COVID-19 и ОРВИ у детей младшего возраста [11, 13, 14]. Это подчеркивает необходимость постоянного мониторинга и исследования частоты встречаемости, клинического метаморфоза ко-инфекций COVID-19 и ОРВИ, что и послужило поводом для проведения нашего исследования.
Цель работы - изучить распространенность и этиологическую структуру ко-инфекций COVID-19 и ОРВИ, а также проанализировать клинико-лабораторные и инструментальные особенности заболевания у детей раннего возраста.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
В исследование были включены дети с лабораторно подтвержденной инфекцией COVID-19 в сочетании с ОРВИ различной этиологии в возрасте от 0 до 3 лет, госпитализированные в инфекционный стационар ГБУЗ «Детская городская клиническая больница имени З.А. Башляевой ДЗМ» в период с 2023 (n = 203 ребенка) по 2024 г. (n = 132 ребенка).
Обнаружение РНК SARS-CoV-2 в мазках из рото-и носоглотки производилось методом полимеразной цепной реакции в режиме реального времени (ОТ-ПЦР). Диагностика респираторных вирусов в назофарингеальном мазке проводилась у всех пациентов методом ОТ-ПЦР с использованием набора реагентов «АмплиСенс® ОРВИ-скрин-FL». Панель включала 13 распространенных сезонных респираторных вирусов: респираторно-синцитиальный вирус (hRSV), метапневмовирус человека (hMPV), аденовирус (hAdV), бокавирус (hBoV), риновирус (hRV), вирусы парагриппа 1-4 (hPiv 1, hPiv 2, hPiv 3, hPiv 4), сезонные коронавирусы (hCoV-229E, hCoV-OC43, hCoV-NL63, hCoV-HKU-1). Вирусная ДНК/РНК была экстрагирована из 100 мкл образца при помощи комплекта реагентов «АмплиТест РИБО-преп».
Для статистической обработки данных применялись t-критерий Стьюдента и непараметрический критерий Манна-Уитни. Достоверными считали результаты при p < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Наиболее часто в 2023 г. регистрировались сочетания SARS-CoV-2 с риновирусами (РИ), аденовирусами (АИ) и респираторно-синцитиальными вирусами (РСВИ), тогда как в 2024 г. наряду с данными патогенами отмечался рост ко-инфекций COVID-19 с бокавирусной инфекцией (БИ) и гриппом (рис. 1).
Наиболее часто ко-инфекция COVID-19/ОРВИ встречалась в зимне-весенний период (с декабря по март). Этиологическая структура сочетанных инфекций у детей раннего возраста в зависимости от месяца в 2023-2024 гг. представлена на рисунке 2.
Сочетания COVID-19/грипп регистрировались с декабря по май в исследуемые годы с максимальным удельным весом среди сочетанных инфекций в декабре 2023 г. и 2024 г. Ко-инфекция COVID-19/ РСВИ в 2023 г. одинаково часто наблюдалась с января по апрель, единичные случаи - в декабре, тогда как в 2024 г. встречалась с февраля по май и с августа по октябрь. В 2024 г. в сравнении с 2023 г. выявлен больший процент сочетаний COVID-19/АИ с мая по декабрь, с максимальным удельным весом в июне и декабре 2024 г. Ко-инфекция COVID-19/РИ встречалась на протяжении всего периода 2023-2024 гг. с пиком заболеваемости с мая по сентябрь. Эпизодически регистрировались ко-инфекции COVID-19 с БИ, МпИ, сКИ без сезонных особенностей.

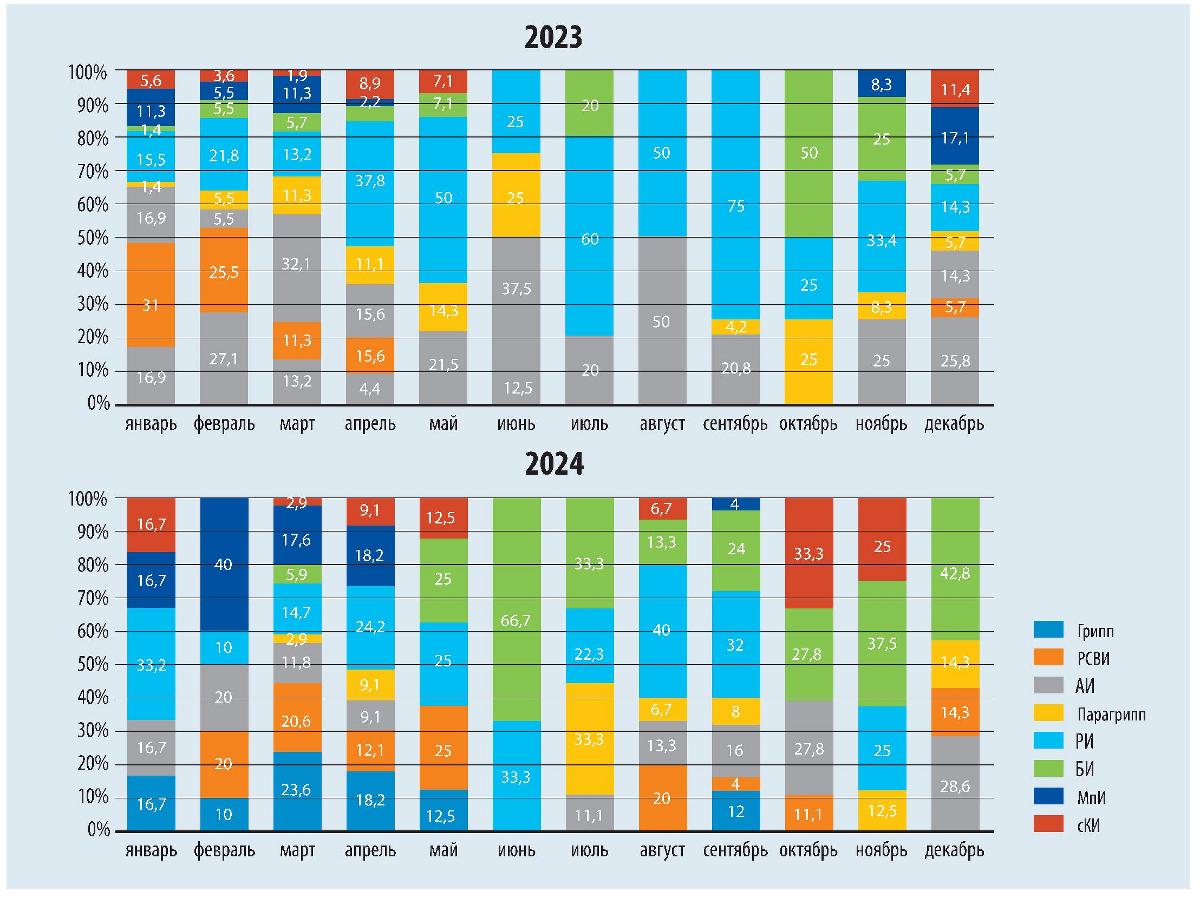
Рис. 2. Сезонная распространенность ко-инфекций COVID-19/ОРВИ, %
В исследуемый период большинство пациентов переносили ко-инфекцию COVID-19/ОРВИ в среднетяжелой форме. Отмечены единичные случаи тяжелого течения заболевания преимущественно среди детей с коморбидной патологией (2023 г. - 1,5% (n = 3), 2024 г. - 3% (n = 4)).
При анализе топики поражения респираторного тракта при ко-инфекциях COVID-19/грипп и COVID-19/МпИ в 2023 г. установлено достоверно частое поражение ВДП и бронхов в сравнении с 2024 г., тогда как обратная ситуация наблюдалась при развитии пневмонии (p < 0,05), что указывает на более легкое течение сочетанной инфекции (табл. 1, 2). Стоит отметить, что катаральные проявления в носо- и ротоглотке отмечены у всех детей независимо от топического варианта поражения респираторного тракта.
При сравнении сочетаний COVID-19/ОРВИ и моноинфекции COVID-19 в 2023 г. установлено, что достоверно реже регистрировались явления рино-фарингита в группах COVID-19/РСВИ, COVID-19/ МпИ, COVID-19/сКИ, тогда как для этих же групп различий в частоте встречаемости пневмонии не было выявлено. При COVID-19 единичными были случаи поражения гортани, трахеи и бронхов, а при сочетаниях COVID-19/РСВИ до 55,3% детей переносят инфекцию с развитием острого бронхита, в том числе с бронхиальной обструкцией; при COVID-19/АИ у 22,5% пациентов отмечены признаки ларинготрахеита и в 10% случаев - острого бронхита; при COVID-19/парагриппе (ПИ) - ларинготрахеит составил 29,4%, острый бронхит - 11,8%; при COVID-19/МпИ обструктивный бронхит зафиксирован у 30% пациентов; при COVID-19/сКИ острый ларинготрахеит отмечен у 23,1%, обструктивный бронхит у 15,4% (p < 0,05). При ко-инфекции COVID-19/грипп в сравнении с COVID-19 развитие острого бронхита выявлено у 11,1% детей, в три раза реже регистрировалась пневмония (11,1% против 33,3% соответственно) (p < 0,05).
Одинаково часто, как и при моно-COVID-19, в группах. COVID-19/РСВИ, COVID-19/РИ, COVID-19/ ПИ, COVID-19/сКИ наблюдались гастроинтестинальные симптомы. В единичных случаях при COVID-19/АИ наблюдалось развитие фарингоконъ-юнктивальной лихорадки.
Таблица 1. Структура топического поражения респираторного тракта при COVID-19/ОРВИ в 2023 г.
|
Топическая форма |
COVID-19 %-абс |
COVID-19 / грипп %-абс |
COVID-19 / РСВИ %-абс |
COVID-19 / РИ %-абс |
COVID-19 / АИ %-абс |
COVID-19 / ПИ %-абс |
COVID-19 / МпИ %-абс |
COVID-19 / БИ %-абс |
COVID-19 / сКИ %-абс |
|
Ринофарингит |
53,4* |
66,7-14 |
7,9-3* |
61,6-25 |
52,5-21 |
58,8-10 |
40-4* |
- |
38,4-5* |
|
Ларинготрахеит |
3,3* |
- |
10,5-4* |
9,6-4* |
22,5-9* |
29,4-5* |
- |
21,4-3* |
23,1-3* |
|
Трахеит |
3,3 |
- |
- |
- |
- |
- |
- |
- |
- |
|
Острый бронхит |
0 |
11,1-2 |
15,8-6 |
4,8-2 |
10-4 |
11,8-2 |
- |
35,9-5 |
- |
|
Бронхиолит |
0 |
- |
- |
- |
- |
- |
- |
- |
- |
|
Обструктивный бронхит |
0 |
- |
39,5-15 |
7,2-3 |
5-2 |
- |
30-3 |
14,2-2 |
15,4-2 |
|
Пневмония |
30 |
11,1-2 |
- |
12-6 |
10-4 |
- |
30-3 |
21,4-3 |
23,1-3 |
|
Пневмония + БОС |
3,3 |
- |
26,3-10 |
4,8-2 |
- |
- |
- |
7,1-1 |
- |
|
Пневмония (всего) |
33,3* |
11,1- 2* |
26,3-10 |
16,8-8* |
10-4* |
- |
30-3 |
28,5-4 |
23,1-3 |
|
Всего: |
100-30 |
18 |
38 |
42 |
40 |
17 |
10 |
14 |
13 |
|
Гастроинтестинальные проявления * p < 0,05 |
16,7 |
5,5-1 |
10,5-4 |
12-6 |
7,5-3 |
17,6-3 |
0 |
0 |
15,4-2 |
Обратная ситуация наблюдалась для соотношения поражения ВДП / пневмонии в 2024 г.: для COVID-19/грипп, COVID-19/МпИ, COVID-19/ПИ по сравнению с COVID-19 отмечен достоверно реже ринофарингит в моноварианте, тогда как по частоте встречаемости пневмонии различий не выявлено (p < 0,05). Топическая характеристика поражения ВДП при ко-инфекциях в 2024 г. повторяет особенности сочетаний COVID-19/ОРВИ в 2023 г. (табл. 1, 2).
В выраженности и продолжительности основных опорных клинических симптомов и лабораторных показателей для ко-инфекций COVID-19/ ОРВИ в сравнении 2023 г. и 2024 г. различий получено не было, в связи с чем дальнейший анализ проводился для двух групп сравнения, где 1-я группа -COVID-19/ОРВИ, 2-я группа - COVID-19.
Таблица 2. Структура топического поражения респираторного тракта при COVID-19/ОРВИ в 2024 г.
Топическая форма | COVID-19 %-абс | COVID-19 / грипп %-абс | COVID-19 / РСВИ %-абс | COVID-19 / РИ %-абс | COVID-19 / АИ %-абс | COVID-19 / ПИ %-абс | COVID-19 / МпИ %-абс | COVID-19 / БИ %-абс | COVID-19 / сКИ %-абс |
Ринофарингит | 53,4* | 38,4-8* | 21,2-4* | 56-14 | 49,4-5 | 18,2-2* | 18,2-2* | 44-11 | 53,8-9 |
Ларинготрахеит | 3,3* | - | 10,5-2* | 20-5* | 13,3-2* | 36,3-4* | 9,1-1 | 32-8* | 15,4-2* |
Трахеит | 3,3* | - | - | - | - | - | 9,1-1 | - | - |
Острый бронхит | 0 | 15,4-2 | 5,2-1 | 8-2 | 12-3 | 18,2-2 | - | 12-3 | - |
Бронхиолит | 0 | - | 10,5-2 | - | - | 9,1-1 | 18,2-2 | - | - |
Обструктивный бронхит | 0 | - | 10,5-2 | 8-2 | 13,3-2 | - | 27,2-3 | - | - |
Пневмония | 30* | 23,1-3 | 31,6-6 | 8-2 | 12-3* | 18,2-2* | 18,2-2* | 12-3* | 15,4-2* |
Пневмония + БОС | 3,3 | - | 10,5-2 | - | - | - | - | - | - |
Пневмония (всего) | 33,3* | 23,1-3 | 42,1-8 | 8-2* | 12-3* | 18,2-2* | 18,2-2* | 12-3* | 15,4-2* |
Всего: | 100 | 13 | 19 | 25 | 15 | 11 | 11 | 25 | 13 |
Гастроинтестинальные проявления * p < 0,05 | 16,7* | 15,4-2 | 15,8-3 | 8-2 | 26,7-4* | 9,1-1 | 18,2-2 | 16-4 | 0 |
КЛИНИКО-ЛАБОРАТОРНЫЕ ОСОБЕННОСТИ СОЧЕТАНИЙ COVID-19/ОРВИ В ЗАВИСИМОСТИ ОТ ЭТИОЛОГИИ РЕСПИРАТОРНОГО ВИРУСА
- COVID-19/аденовирусная инфекция (АИ) (hAdV).
60% детей переносят инфекцию с развитием фебрильной лихорадки, одинаково часто встречается развитие субфебрилитета или гипертермии (до 15% случаев).
Средняя продолжительность лихорадки составляет 3,3 ± 1,2 [2; 6] дня, что почти вдвое меньше, чем при COVID-19 - 6,3 ± 1,3 [4; 9] дня (p = 0,0015). У 90% детей отмечалось наличие сухого или малопродуктивного кашля, прослеживается влияние аденовируса на течение ко-инфекции в виде снижения продолжительности кашля до 4,3 ± 1,3 [2; 8] дней против 7,7 ± 5,2 [4; 9] дней при COVID-19 (p = 0,01). Подобная тенденция отмечена и для ринита. Различий в развитии симптомов интоксикации и их длительности достоверно не было получено.
При исследовании клинического анализа крови (ОАК) у 88% детей отмечались нормальные показатели лейкоцитов и тромбоцитов.
Средние уровни СРБ при ко-инфекции COVID-19/ АИ составили 30,2 ± 12,9 [4; 80,5] мг/л против 23,7 ± 19,4 [3; 23,4] мг/л при COVID-19, D-димера -1090,4 ± 235,3 [343; 2323] нг/л против 930 ± 879 [280; 706] нг/л (p = 0,1).
- COVID-19/бокавирусная инфекция (БИ) (hBoV)
При ко-инфекции COVID-19/БИ у 75% детей отмечается фебрильная лихорадка (p < 0,005).
Длительность течения лихорадки и интоксикационного синдрома была достоверно короче, чем при moho-COVID-19 - 6,3 ± 1,3 [4; 9] дня (р = 0,001).
У всех пациентов с COVID-19/БИ отмечено наличие сухого и малопродуктивного кашля, который сохранялся в среднем 4,0 ± 2,5 [2; 7] дня против 7,7 ± 5,2 [4; 9] дней при COVID-19 (p = 0,02). Стоит отметить, что при COVID-19/БИ в ОАК у 37,5% детей зарегистрирована тромбоцитопения при нормальных показателях лейкоцитов.
Средние показатели СРБ в группах сравнения не различались, при COVID-19/БИ составили 21,2 ± 10,3 [6,4; 30,48] мг/л против 23,7 ± 19,4 [3; 23,4] мг/л при COVID-19 (p = 1), тогда как достоверные отличия отмечены для D-димера - 645,9 ± 78,4 [295; 1188] нг/л против 930 ± 79 [280; 706] нг/л (p < 0,05).
- COVID-19/грипп (тип А, тип В).
При ко-инфекции COVID-19/грипп у 72% детей отмечается гиперпи-ретическая лихорадка. Средняя продолжительность лихорадки составляет 5,2 ± 1,2 [2; 10] дня (p = 0,07).
У всех детей отмечалось развитие сухого или малопродуктивного кашля длительностью в среднем 5,7 ± 2,1 [2; 10] дня против 4,0 ± 2,5 [2; 7] дней при COVID-19 (p > 0,05).
В клиническом анализе крови в группах сравнения не было получено достоверных отличий. При COVID-19/грипп уровень СРБ составил 22,0 ± 9,7 [10,8; 47,7] мг/л против 23,7 ± 9,4 [3; 23,4] мг/л при COVID-19 (р > 0,05), тогда как уровень D-димера был достоверно выше - 1262,7 ± 124,5 [270; 2669] нг/л против 930 ± 879 [280; 706] нг/л (р < 0,05).
- COVID-19/метапневмовирусная инфекция (МпИ) (hMPV).
До 50% пациентов с COVID-19/МпИ переносили заболевание с развитием гиперпирети-ческой лихорадки и интоксикационного синдрома, тогда как при COVID-19 данные симптомы наблюдаются у 6,8% (р < 0,05).
При этом отмечена одинаковая продолжительность данных симптомов в группах исследования: 6,5 ± 1,7 [4; 9] дня против 6,3 ± 1,3 [4; 9] дней соответственно.
Наличие кашля при COVID-19/МпИ зарегистрировано у 75% пациентов, средняя продолжительность составила 7 ± 3,4 [4; 10] дней против 4,0 ± 2,5 [2; 7] дней при COVID-19 (р < 0,05). При этом достоверных различий в клиническом анализе крови, а также в показателях СРБ и D-димера не было выявлено.
- COVID-19/парагрипп (ПИ) (hPiv 1, hPiv 2, hPiv 3, hPiv 4).
Для инфекции COVID-19/ПИ характерны развитие субфебрильной, реже фебрильной лихорадки почти у 90% пациентов без развития интоксикационного синдрома в сравнении с COVID-19 и более быстрое купирование данных симптомов: 3,8 ± 0,5 [2; 6] дня против 6,3 ± 1,3 [4; 9] дней соответственно (р < 0,05).
У всех пациентов с COVID-19/ПИ отмечено наличие ринита и кашля, не различающихся по продолжительности от моно-COVID-19. Значимых различий в показателях ОАК и D-димера в группах исследования не было установлено, при этом для COVID-19/ПИ отмечена тенденция к снижению уровня СРБ - 12,9 ± 7,4 [3,9; 22,4] мг/л против 23,7 ± 19,4 [3; 23,4] мг/л (р = 0,3).
- COVID-19/риновирусная инфекция (РИ) (hRV).
Ко-инфекция COVID-19/РИ характеризуется развитием фебрильной лихорадки у 45,5% пациентов и отсутствием симптомов интоксикации у большинства детей, а также более коротким периодом длительности данных симптомов: 3,2 ± 0,3 [2; 5] дня против 6,3 ± 1,3 [4; 9] дней при COVID-19 (р = 0,012). Достоверных различий в характере и длительности кашля при анализе данных групп не выявлено. Также не выявлено достоверно значимых отличий в показателях ОАК, уровнях СРБ и D-димера.
- COVID-19/респираторно-синцитиальная вирусная инфекция (РСВИ) (hRSV).
Анализируя клиническую картину COVID-19/РСВИ в сравнении с COVID-19, обращает на себя внимание наличие фебрильной и гиперпиретической лихорадки почти у 60% пациентов при отсутствии интоксикационных проявлений, без достоверных различий в их продолжительности.
При этом прослеживается влияние РСВ на длительность кашля при COVID-19/РСВИ, которая составила 6,2 ±1,4 [4,8] дня против 4,0 ± 2,5 [2; 7] дней при COVID-19 (p < 0,05).
При отсутствии значимых отклонений в ОАК при COVID-19/РСВИ реже встречалось повышение показателей СРБ и D-димера, чем при COVID-19: СРБ -11,5 ± 9,7 [0,2; 20,6] мг/л против 23,7 ± 19,4 [3; 23,4] мг/л, D-димер - 490,5 ± 120,2 [150; 990] нг/л против 930 ± 879 [280; 706] нг/л соответственно (p < 0,05).
- COVID-19/сезонная коронавирусная инфекция (сКИ) (hCoV-229E, hCoV-OC43, hCoV-NL63, hCoV-HKU-1).
Для пациентов с COVID-19/сКИ, как и с мо-но-COVID-19, характерна субфебрильная температура тела (до 60%). Обращает на себя внимание почти двукратное уменьшение продолжительности основных опорных клинических симптомов, что, вероятно, обусловлено феноменом интерференции вирусов: длительность лихорадки при COVID-19/сКИ составила 2,0 ± 0,8 [2; 3] дня против 6,3 ± 1,3 [4; 9] дней при COVID-19, кашля и насморка - 1,75 ± 0,4 [2; 3] дня против 4,0 ± 2,5 [2; 7] дней соответственно (p < 0,05). При этом не отмечается достоверных различий при исследовании показателей клинического анализа крови, СРБ и D-димера.
Учитывая ранний возраст пациентов при выборе инструментального метода обследования органов грудной клетки предпочтение отдавалось проведению рентгенографии легких (до 95% исследований). При этом у большинства пациентов с COVID-19/ОРВИ отмечено усиление сосудистого рисунка в проекции бронхиального дерева за счет интерстициального компонента, что аналогично результатам рентгенографии легких при моноинфекции COVID-19. При этом наличие пневмонии при ко-инфекции COVID-19 рентгенологически подтверждалось при наличии инфильтративных изменений, а также неравномерности/снижении пневматизации в легочных тканях, что практически не встречается при коронавирусной пневмонии.
Несмотря на значимые различия в продолжительности и выраженности некоторых клинических симптомов при COVID-19/ОРВИ, длительность стационарного лечения достоверно не отличалась от продолжительности госпитализации при COVID-19.
В стационаре все дети с COVID-19 получали терапию согласно действующему Клиническому протоколу лечения детей с новой коронавирусной инфекцией (COVID-19) (2021 г.) [15].
Учитывая ранний возраст пациентов, в период госпитализации в качестве противовирусной терапии всем детям назначался препарат рекомбинантного интерферона-альфа-2Ь с антиоксидантами (ВИФЕРОН®) в виде ректальных суппозиториев в дозировке 150 000 МЕ 2 раза в сутки курсом 5-7 дней.
Временные методические рекомендации (ВМР) «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19)», версия 18 (2023), содержат указание о том, что «в качестве противовирусной терапии детей с COVID-19 в случаях заболеваний среднетяжелой и легкой степени тяжести рекомендуются препараты ИФН-а, при тяжелой степени тяжести используются внутривенные иммуноглобулины. Интерферон-альфа может снизить вирусную нагрузку на начальных стадиях болезни, облегчить симптомы и уменьшить длительность болезни» [16].
В начале 2023 г. нами был представлен собственный опыт применения препаратов интерферона альфа-2Ь (ВИФЕРОН®) для лечения новой коронавирусной инфекции у детей в условиях стационара в рамках рандомизированного научного исследования, проведенного в 2020-2022 гг. на базе Детской городской клинической больницы им. З.А. Башляевой ДЗМ [17].
В результате было статистически подтверждено, что назначение препаратов «ВИФЕРОН®, суппозитории ректальные с антиоксидантами» в сочетании с «ВИФЕРОН®, гель для наружного и местного применения» способствовало более быстрому купированию основных клинических симптомов COVID-19 и более быстрому формированию противовирусных защитных антител класса IgG, а также сокращало время элиминации SARS-CoV-2 из носоглотки. Не было зарегистрировано побочных эффектов и нежелательных явлений при применении препарата интерферона альфа-2Ь (ВИФЕРОН®).
Также, по данным метаанализа Т.А. Руженцовой [18] и рандомизированных плацебо контролируемых исследований, применение препарата ВИФЕРОН® (рекомбинантного интерферона альфа-2Ь с антиоксидантами) у детей с ОРВИ и гриппом способствовало достоверному сокращению средней продолжительности катаральных явлений (на 1,75 сут.), ринореи (на 1,71 сут.), интоксикации (на 1,18 сут.), лихорадочного синдрома (на 0,8 сут.), общей длительности заболевания (на 4,8 сут.).
Наличие препаратов интерферона в ВМР, данные мета-анализа и собственный клинический опыт послужили основанием для включения препарата ВИФЕРОН® в терапию сочетанных инфекций у исследуемой категории пациентов. Стоит отметить, что все дети этой группы получали ВИФЕРОН® с положительным эффектом.
Таким образом, полученные данные по эффективности и безопасности применения препарата ВИФЕРОН® в виде суппозиториев и топических форм при COVID-19 и ОРВИ у детей раннего возраста позволяют применять интерферонотерапию при сочетанных формах COVID-19/ОРВИ в возрастных дозах.
ЗАКЛЮЧЕНИЕ
Данное клиническое исследование демонстрирует этиологическую структуру, частоту встречаемости и сезонность сочетанных с COVID-19 острых респираторных вирусных инфекций у детей раннего возраста, госпитализированных в инфекционный стационар в 2023-2024 гг.
Представлены различия в топических формах поражения респираторного тракта при COVID-19/ ОРВИ в сравнении с COVID-19, для которых характерно поражение трахеобронхиального дерева с наличием клинических проявлений ларинготрахеита и бронхита с соответствующими рентгенологическими изменениями в легких как результат влияния респираторного ко-патогена на клиническую картину COVID-19 у детей раннего возраста.
Литература
1. Сочетанные формы COVID-19 с острыми респираторными вирусными инфекциями у детей / Л.Н. Мазанкова [и др.] // Детские инфекции. 2022. № 21 (1). С. 16-22. DOI: 10.22627/2072-8107-2022-21-1-16-22.
2. Epidemiological changes in respiratory pathogen transmission among children with acute respiratory infections during the COVID-19 pandemic in Kunming, China / G. Zhang [et al.] // BMC Infectious Diseases. 2024. Vol. 24, No. 826. DOI: 10.1186/ s12879-024-09733-y.
3. О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2023 году : государственный доклад. М. : Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, 2024. 344 с.
4. Xu, D., Chen, Z., & Zhu, G. Change of epidemiological characteristics of four respiratory viral infections in children before and during COVID-19 pandemic // Infectious Diseases Now. 2024. Vol. 54, No. 3. P. 104858. DOI: 10.1016/j.id-now.2024.104858.
5. Polymorphisms in the ACE I/D (rs4646994) and ACE2 G8790A (rs2285666) in Young Children Living in the Amazon Region and SARS-CoV-2 Infection / Y.C. Pimenta [et al.] // Tropical Medicine and Infectious Disease. 2024. Vol. 9, No. 11. P. 270. DOI: 10.3390/tropicalmed9110270.
6. Clinical features and severity of COVID-19 with respiratory virus coinfections versus SARS-CoV-2 monoinfection in hospitalized children: A Canadian national surveillance study / Di Chiara, Costanza & Farrar, Daniel & Bettinger [et al.] // Paediatrics & Child Health. 2024. Vol. 29. P. e19-e20. DOI: 10.1093/pch/pxae067.041.
7. Global Coinfections with Bacteria, Fungi, and Respiratory Viruses in Children with SARS-CoV-2: A Systematic Review and Meta-Analysis / S. Alhumaid [et al.] // Tropical Medicine and Infectious Disease. 2022. Vol. 7, No. 11. P. 380. DOI: 10.3390/ tropicalmed7110380.
8. COVID-19 and Co-infection in Children: The Indian Perspectives / D. Raychaudhuri [et al.] // Journal of Tropical Pediatrics. 2012. Vol. 67, No. 4. fmab073. DOI: 10.1093/tropej/fmab073.
9. Triple Infection of COVID-19, Respiratory Syncytial Virus and Adenovirus in 4-Month-Old Infant / T. Ben Houmich [et al.] // European Journal of Medical and Health Sciences. 2022. Vol. 4, No. 2. P. 18-20. DOI. 10.24018/ejmed.2022.4.2.1304.
10. Respiratory syncytial virus and SARS-CoV-2 coinfections in children / K.C. Halabi [et al.] // Pediatric pulmonology. 2022. Vol. 57, No. 12. P. 3158-3160. DOI: 10.1002/ppul.26127.
11. Comparison of Clinical and Laboratory Characteristics of COVID-19 and Respiratory Diseases of Other Etiology in Hospitalized Children / I.Y. Huseynova, A.Q. Hasanov, F.M. Mam-madova, I.A. Gafarov // American Academy of Pediatrics. 2023. Vol. 9, No. 3. P. 171-179. DOI: 10.11648/j.ajp.20230903.21.
12. Clinical Relevance of RSV and SARS-CoV-2 Coinfections in Infants and Young Children / R. Rodriguez-Fernandez [et al.] // The Pediatric Infectious Disease Journal. 2023. Vol. 42, No. 12. P. e473-e475.
13. Co-infection with COVID-19 and genetic diversity of SARS-CoV-2 in children / D.K. Kamalova [et al.] // Eurasian Journal of Applied Biotechnology. 2023. Vol. 8. P. 15-22. DOI: 10.11134/btp.3.2023.2.
14. Coinfection Characteristics among Children with COVID-19 / I. Villanueva [et al.] // Open Forum Infectious Diseases. 2022. Vol. 9. DOI: 10.1093/ofid/ofac492.335.
15. Клинический протокол лечения детей с новой коронавирусной инфекцией (COVID-19), находящихся на стационарном лечении в медицинских организациях государственной системы здравоохранения города Москвы / И.М. Османов, Е.И. Алексеева, Л.Н. Мазанкова, И.Н. Захарова [и др.] ; под ред. А.И. Хрипуна. М. : ГБУ «НИИОЗММ ДЗМ», 2021. 92 с.
16. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19) : временные методические рекомендации. Версия 18 (26.10.2023) (утв. Минздравом РФ) : [Эл. ресурс]. URL: static-0. minzdrav.gov.ru/system/attachments/attaches/000/064/610/ original/%D0%92%D0%9C%D0%A0_COVID-19_V18.pdf (дата обращения: 24.02.2025).
17. Опыт применения препаратов интерферона альфа-2Ь (Виферон®) для лечения новой коронавирусной инфекции у детей в условиях стационара в рамках рандомизированного научного исследования / И.М. Османов [и др.] // Практика педиатра. 2023. № 2. С. 28-34.
18. Лечение острых респираторных вирусных инфекций и гриппа у детей: результаты метаанализа / Т.А. Руженцова, Д.С. Левицкая // Лечащий врач. 2020. № 3. С. 52-57.

