 vtf.ru
vtf.ru

Разработаны специально для детей
Удобные формы приема и дозирования
Приятный вкус и применение без проблем!
Результаты рандомизированного плацебо-контролируемого исследования клинической эффективности напитка на основе лактулозы, инулина, чернослива и экстракта фенхеля при лечении функциональных запоров у детей
СтатьиОпубликовано в журнале:
« Вопросы практической педиатрии » 2018, том 13, №2, с. 24-31
DOI: 10.20953/1817-7646-2018-2-24-31
Clinical Practice in Pediatrics, 2018, volume 13, No 2, p. 24-31
А.И.Хавкин, О.Н.Комарова
Научно-исследовательский клинический институт педиатрии им. академика Ю.Е.Вельтищева Российского национального исследовательского медицинского университета им. Н.И.Пирогова, Москва, Российская Федерация
Цель. Изучение эффективности применения и переносимости биологически активной добавки на основе лактулозы, инулина, чернослива и экстракта фенхеля «Кидз (Kidz) напиток с черносливом» в комплексной терапии функциональных хронических запоров у детей.
Пациенты и методы. В исследование включены 60 детей разного пола в возрасте 3-14 лет с установленным диагнозом «Функциональный хронический запор в компенсированной стадии». Случайным методом пациенты рандомизированы на 2 группы, по 30 человек в каждой. Всем пациентам даны рекомендации по режиму питанию, дефекации и физической активности. Пациенты основной группы получали «Кидз (Kidz) напиток с черносливом», пациенты контрольной группы - плацебо, имитирующее «Кидз (Kidz) напиток, с черносливом» в течение 30 дней. Детям не назначались другие препараты, обладающие слабительным и/или пре- и пробиотическим действием. Все участники исследования обследованы в стационаре. До начала исследования, далее через 30 и 60 дней проводилась клиническая оценка симптомов: количества дефекаций в неделю, консистенции кала; наличия/отсутствия и выраженности симптомов запора; переносимости препарата и сроков купирования симптомов запора. Также проводилась оценка состояния микробиоценоза кишечника бактериологическим методом. Обработка данных производилась с использованием пакета статистического анализа.
Результаты. На фоне проведения курса терапии с включением «Кидз (Kidz) напитка с черносливом» у большинства детей отмечена нормализация консистенции кала и частоты стула, а также статистически значимая положительная динамика клинической симптоматики в виде уменьшения абдоминальной боли, вздутия живота, чувства неполного и затрудненного опорожнения кишечника, необходимости натуживания, метеоризма. Анализ клинических данных у пациентов контрольной группы, получавших плацебо с маркировкой «Кидз (Kidz) напиток с черносливом», показал отсутствие значимой динамики в изменении формы кала, числа дефекаций, симптомов. Микробный пейзаж кала у пациентов контрольной группы спустя месяц был идентичен первоначальным показателям, тогда как в основной группе по завершении курса приема «Кидз (Kidz) напитка с черносливом» у всех детей отмечен рост числа представителей индигенной микрофлоры, в частности бифидо- и лактобактерий, и подавление роста условно-патогенных представителей микробиоценоза (гемолизирующей E. coli, Citrobacter; рода Klebsiella pneumoniae) до нормальных показателей.
Заключение. Результаты исследования показали клиническую эффективность и безопасность применения биологически активной добавки «Кидз (Kidz) напиток с черносливом» у детей 3-14 лет с хроническим функциональным запором в стадии компенсации - в составе комплексной терапии.
Ключевые слова: запор, лечение, лактулоза, инулин, чернослив, микрофлора
Для цитирования: Хавкин А.И., Комарова ОН. Результаты рандомизированного плацебо-контролируемого исследования клинической эффективности напитка на основе лактулозы, инулина, чернослива и экстракта фенхеля при лечении функциональных запоров у детей. Вопросы практической педиатрии. 2018; 13(2): 24-31. DOI: 10.20953/1817-7646-2018-2-24-31
Results of a randomized placebo-controlled study of the clinical effectiveness of a beverage with lactulose, inulin, prune and fennel extract in treatment of functional constipation in children
А.I.Khavkin, О.N.Komarova
Academician Yu.E.Veltishchev Research and Clinical Institute of Pediatrics at the N.I.Pirogov Russian National Research Medical University, Moscow, Russian Federation
The objective: to study the effectiveness of using and tolerance of a dietary supplement (DS) «KidZ drink with prune» with lactulose, inulin, prune and fennel extract in complex therapy of functional chronic constipation in children.
Patients and methods: the study included 60 children (boys and girls) aged 3-14 years diagnosed with «compensated functional chronic constipation». The patients were randomized into 2 groups, 30 in each. All patients received recommendations about diet regimens, bowel movements and physical activity. Patients from the main group received «KidZ drink with prune», control group received a placebo «KidZ drink with prune» for 30 days. Children received no other medications with laxative and/or pre- and probiotic effects. All participants were examined in inpatient department. Before the study, then after 30 and 60 days, clinical assessment of symptoms was undertaken: number of bowel movements per week, stool consistency; presence/absence and severity of symptoms of constipation; tolerance of the preparation and terms of coping with constipation symptoms. Also, intestinal microbiocenosis was assessed bacteriologically. Data were analysed using a statistical software package.
Results: against the background of therapy with inclusion of «KidZ drink with prune» normalisation of stool consistency and frequency was noted in most children, along with a statistically significant positive dynamics of clinical symptoms, namely, alleviation of abdominal pains, abdominal distention, sensation of incomplete and difficult bowel movement, necessity to strain, meteorism. Analysis of clinical data in patients of the control group who received a placebo labelled «KidZ drink with prune» has shown the absence of a significant dynamics in stool forms, number of bowel movements, dynamics of symptoms. One month afterwards, the landscape of fecal microbiota in patients of the control group was identical with the initial values, whereas in patients of the basic group upon termination of the course of «KidZ drink with prune» a growth of representatives of indigenous flora, in particular, bifidobacteria and lactobacilli and suppression of the growth of conditionally pathogenic representatives of microbiocenosis (haemolysing E. coli, Citrobacter; species Klebsiella pneumoniae) to normal values was found in all children.
Conclusion: the results of the study have demonstrated a clinical effectiveness and safety of the dietary supplement «KidZ drink with prune» in 3-14-year-old children with chronic functional constipation in the compensated stage as part of complex therapy. Key words: constipation, treatment, lactulose, inulin, prune, microbiota
Key words: kids, intestinal infection, probiotic, Hilak forte
For citation: Khavkin A.I., Komarova O.N. Results of a randomized placebo-controlled study of the clinical effectiveness of a beverage with lactulose, inulin, prune and fennel extract in treatment of functional constipation in children. Vopr. prakt. pediatr. (Clinical Practice in Pediatrics). 2018; 13(2): 24-31. (In Russian). DOI: 10.20953/1817-7646-2018-2-24-31
Согласно современным представлениям под запором понимают интегральный комплекс различных симптомов, связанных со стойким или интермиттирующим нарушением опорожнения кишечника (МКБ - К 59.0). В основе патогенеза запора лежат несколько механизмов. Это расстройства моторики, такие как замедление движения каловых масс, слабость внутрибрюшного давления, спастическая дискинезия прямой кишки, гиперсегментация. Совокупность перечисленных причин обусловливает кологенные запоры. Так называемые проктогенные запоры связаны с патологией мышц дна малого таза и нарушением эвакуации кала из прямой кишки [1]. На практике специалисты нередко наблюдают сочетание обоих патогенетических механизмов. Являясь, по сути, синдромом, запор входит в структуру нескольких нозологических форм: синдрома раздраженного кишечника, функционального запора и функционального расстройства дефекации [2]. Кроме того, запор может входить в структуру большого числа патологий нервной, эндокринной, иммунной систем, быть проявлением метаболических расстройств, инфекционных, онкологических и генетически детерминированных заболеваний, врожденных аномалий пищеварительного тракта и др. [3].
Запор является настолько распространенной патологией практически во всех возрастных группах, что можно отнести его к категории «болезней цивилизации». Так, в развитых странах запорами страдают 30-50% взрослого трудоспособного населения.
У детей распространенность запоров, по данным различных исследователей, составляет 7-30%. При этом у 90-95% из них органическая причина запора отсутствует, а лечение слабительными препаратами эффективно лишь у 60% [4-6]. Показано, что значительной части пациентов требуется длительная терапия. Тем не менее, через год лечения запоры рецидивируют более чем у 50% детей, а 25% продолжают страдать от этого состояния и после 5-летнего возраста. Примерно у 30% детей после пубертата сохраняются такие проявления запора, как редкая болезненная дефекация и недержание кала [7]. Более эффективное лечение этой сложной категории пациентов требует разработки новых терапевтических стратегий [8-11].
Учитывая вышесказанное, актуальными являются задачи, связанные с выработкой новых стратегий лечения запоров у детей, внедрением в практику новых средств, оказывающих корригирующее влияние на моторику пищеварительного тракта, облегчающих процесс дефекации.
В этой связи целью настоящего исследования явилось изучение эффективности применения и переносимости биологически активной добавки (БАД) на основе лактулозы, инулина, чернослива и экстракта фенхеля «Кидз (Kidz) напиток с черносливом» при комплексной терапии функциональных хронических запоров у детей.
Для реализации цели исследования были выполнены следующие задачи:
- проведен анализ выраженности клинических симптомов заболевания и их динамики на фоне применения напитка с черносливом и сравнение динамики с контрольной группой;
- оценена переносимость «Кидз (Kidz) напитка с черносливом» (оценка безопасности), проведен анализ частоты развития нежелательных побочных эффектов, ассоциированных с применением данного препарата в условиях амбулаторного приема;
- оценено удобство применения «Кидз (Kidz) напитка с черносливом» в комплексной терапии хронических запоров у детей;
- проанализированы эффективность и удобство применения схемы лечения.
Пациенты и методы
В исследовании приняли участие дети в возрасте 3-14 лет с установленным диагнозом «Функциональный хронический запор в компенсированной стадии». Всего было включено 60 человек: по 30 человек в каждой группе:
- пациенты, получающие «Кидз (Kidz) напиток с черносливом» в дополнение к комплексной терапии;
- пациенты, получающие плацебо «Кидз (Kidz) напиток с черносливом» в дополнение к комплексной терапии.
Объектом исследования была биологически активная добавка к пище «Кидз (Kidz) напиток с черносливом», которая представляет собой порошок для приготовления раствора, расфасованный в саше-пакеты (табл. 1).
Плацебо, имитирующее «Кидз (Kidz) напиток с черносливом», представляло собой порошок для приготовления раствора для приема внутрь, неотличимый по внешнему виду от БАД «Кидз (Kidz) напиток с черносливом», и содержало только инертные вспомогательные компоненты. Пациенты принимали по одному саше (5 г) три раза в день в течение 1 месяца.
Таблица 1. Состав «Кидз (Kidz) напиток с черносливом»

Рандомизация субъектов исследования в группы воздействия осуществлялась случайным методом после получения согласия родителей на участие в исследовании. После беседы и получения согласия на наблюдение и лечение больные были включены в соответствующие группы так, чтобы они были репрезентативны по полу, возрасту и тяжести хронического запора. В исследовании был использован метод фиксированной простой рандомизации. Пациент распределялся в ту или иную группу на основании случайных чисел, сгенерированных с помощью компьютерной программы. Вероятность попадания в основную группу лечения была равна вероятности попадания в группу контроля - 50%.
Контрольные осмотры пациентов, после включения в протокол лечения, проводились на 6, 30 и 60-й день от первичного осмотра. Обследования включали в себя:
- клиническое врачебное исследование с оценками показателей общего состояния здоровья ребенка;
- осмотр гастроэнтеролога, оценку наличия/отсутствия и выраженности симптомов запора по визуально-аналоговой шкале (абдоминальная боль, вздутие живота, затрудненное опорожнение кишечника, чувство его неполного опорожнения, необходимость натуживания, метеоризм), оценку количества дефекаций в неделю, консистенции кала по «Бристольской шкале форм кала»;
- исследование микробиоты кишечника;
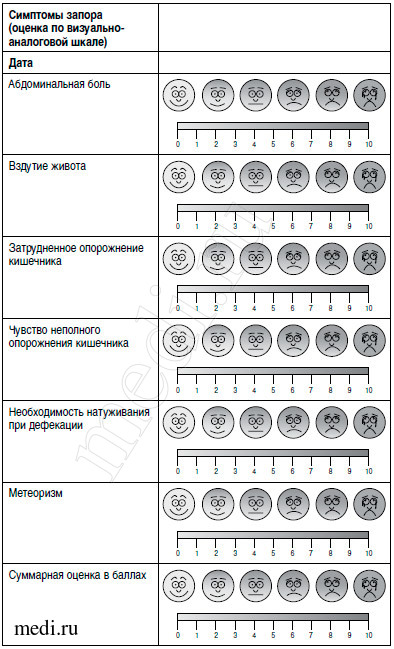
- оценку переносимости препарата по наличию/отсутствию аллергических реакций и других побочных эффектов по 3-балльной шкале (наличие/отсутствие и выраженность других симптомов запора: абдоминальной боли, вздутия живота, затрудненного опорожнения кишечника, чувства его неполного опорожнения, необходимости натуживания, метеоризма оценивались по визуально-аналоговой шкале до начала лечения и на 30-й день терапии самостоятельно пациентами. Визуально-аналоговая шкала представляет собой горизонтальную линию, длиной 10 см, которая отражает интенсивность симптома, где 0 соответствует понятию «отсутствие симптома», 10 - «симптом настолько выражен, насколько можно себе представить». Пациенты отмечали точку на данной линии, соответствующую выраженности симптома (рис.1));
- оценку сроков купирования симптомов запора;
- микробиологическое исследование кала (в динамике: при включении в исследование и после окончания приема «Кидз (Kidz) напитка с черносливом»).
Рис. 1. Визуально-аналоговая шкала оценки симптомов запора.
При установлении факта запора оценивались не только частота стула, но и его характер. Для более объективной оценки была использована «Бристольская шкала форм кала», поскольку именно форма кала, а не частота стула в большей мере соответствует времени кишечного транзита. Эту шкалу используют для детей старше 2-3 лет. Типы 1, 2 и 3, выделяемые в соответствии с ней, означают запор, тип 4 - нормальный стул, типы 5, 6 и 7 - диарею. На практике бывают ситуации, когда у ребенка частота дефекаций укладывается в пределы нормальных значений, но стул плотный, фрагментированный, в скудном количестве. Эти признаки указывают на неполное опорожнение кишечника и должны расцениваться как проявления запора.
На 60-й день от включения в исследование и через 30 дней после окончания приема оценивался отсроченный эффект от приема «Кидз (Kidz) напиток с черносливом».
Медикаментозная терапия. В рамках исследования все больные получали терапию хронического функционального запора, включающую диетотерапию, консультацию по изменению образа жизни и режима дня, по показаниям - спазмолитические препараты. Использовались такие лекарства, прием которых был вызван наличием сопутствующих болезней, при условии, что эти препараты не принадлежали к числу не разрешенных к применению в ходе исследования. В рамках исследования в основной и контрольной группах не использовались другие препараты, обладающие слабительным и/или пребиотическим действием, пробиотики, препараты, замедляющие перистальтику толстого кишечника.
Статистический анализ. Данные, полученные в результате исследования, были подвергнуты статистической обработке на ПЭВМ с использованием пакета статистических программ. Анализ данных выполнялся с использованием пакета статистического анализа. Все статистические тесты проведены для двустороннего 5%-го уровня значимости. Показатели (количественные) описательной статистики представлены количеством наблюдений, средним, медианой, стандартным отклонением, минимальным и максимальным значениями. Для оценки значимости различий средних величин в разных группах использованы двухвыборочный t-критерий Стьюдента или, в случае ненормального распределения, критерий Манна-Уитни. Для определения внутригрупповой динамики использован парный критерий Стьюдента или, в случае ненормального распределения, тест Вилкоксона.
Результаты исследования и их обсуждение
В ходе исследования под наблюдением находились 30 детей основной группы (16 мальчиков и 14 девочек) и 30 - контрольной группы (10 мальчиков и 20 девочек). Дети закончили курс приема «Кидз (Kidz) напитка с черносливом» и плацебо «Кидз (Kidz) напиток с черносливом» через 30 дней (табл. 2).
Таблица 2. Распределение детей по группам исследования, абс.

Таблица 3. Распределение детей по полу и возрасту

Дети основной группы были разделены на две подгруппы. 1-я подгруппа включала 18 пациентов, наблюдавшихся на первом этапе исследования в педиатрическом отделении с гастроэнтерологическими койками и страдающих функциональным компенсированным запором - в рамках основного и сопутствующего диагнозов. 2-я подгруппа из 12 пациентов была сформирована после консультации гастроэнтеролога из пациентов отделений аллергологии и пульмонологии, у которых в качестве сопутствующего диагноза имел место функциональный компенсированный запор. При этом аллергия как причина запора была исключена.
Контрольная группа составила 30 детей, из которых 16 страдали функциональным компенсированным запором в качестве основного заболевания, а 14 (из отделения аллергологии) в качестве сопутствующего (табл. 2). Распределение детей по полу и возрасту представлено в табл. 3.
В соответствии с медико-экономическими стандартами пациенты находились в стационаре 6-7 дней (V0). В этот период проводилось обследование больных, установление диагноза и при выписке назначение терапии. После окончания обследования и подтверждения диагноза «Функциональный компенсированный запор» пациентам назначался напиток с черносливом - по 1 саше три раза в день (V1). Другие препараты, содержащие пищевые волокна, согласно критериям включения не назначались. Также всем пациентам были даны рекомендации по режиму питанию (увеличение потребления жидкости, увеличение квоты овощей в рационе, хлебобулочных и мучных изделий из пшеницы мягких сортов, ограничение потребления жирных сортов мяса, исключение из рациона спреда, кулинарная обработка пищи с учетом ряда особенностей, исключение газосодержащих и газообразующих продуктов), режиму дефекации, физической активности. Пациенты с сопутствующим диагнозом «Функциональный компенсированный запор» получали терапию согласно основному заболеванию, не противоречащую критериям включения. Им также были даны рекомендации, аналогичные тем, которые получили пациенты с запором в качестве основного диагноза.
Таблица 4. Динамика изменения формы кала, абс.

После окончания обследования в стационаре всем детям основной (15 мальчиков и 15 девочек) и контрольной (10 мальчиков и 20 девочек) групп назначался «Кидз (Kidz) напиток с черносливом». В 1-й день приема препарата (V1), а также на 30-й (V2) и 60-й (V3) дни проводились беседы с ребенком или его законным представителем, оценка симптомов, отражающих моторику пищеварительного тракта (частота дефекаций в неделю, форма кала, субъективные жалобы). За истекший период у 4 пациентов имел место незначительный перерыв (2 дня) в приеме препарата по семейным обстоятельствам (родители не осуществляли достаточный контроль за лечением ребенка), 2 пациентам не нравился вкус. Однако эти пациенты не были исключены из исследования, поскольку прием препарата был возобновлен через 2 дня.
В основную группу (n = 30) были включены дети с жалобами на плотный стул: 22 ребенка со стулом 3-го типа, 3 детей - 2-го типа и 5 пациентов со стулом 4-го типа по «Бристольской шкале форм кала». В контрольной группе у 25 детей имел место стул 3-го типа, у 1 - 2-го и у 4 -4-го типа (табл. 4). У всех пациентов основной и контрольной групп, помимо изменения формы кала, отмечался редкий стул: в подгруппе 1 основной группы - 3,6 дефекаций в неделю, в подгруппе 2 - 3,3, контрольной - 3,5 соответственно (табл. 5).
Таблица 5. Динамика изменения среднего числа дефекаций

Как уже было отмечено ранее, 30 детей основной группы закончили курс приема «Кидз (Kidz) напитка с черносливом» (30 дней). На фоне проведения курса терапии (рациона питания и режима дефекации) с включением «Кидз (Kidz) напитка с черносливом» у 18 детей имела место форма кала 4-го типа, у 12 - 3-го типа (табл. 4). Кроме того, отмечено увеличение числа дефекаций в неделю - с 3,6 до 4,9 в подгруппе 1, и с 3,3 до 4,7 в подгруппе 2 (табл. 5). Анализ форм кала как интегративного показателя времени транзита по кишке через 60 дней от начала приема БАД и через 30 дней после окончания приема показал сохраняющиеся позитивные тенденции (табл. 4) у пациентов основной группы и их отсутствие у детей контрольной группы, получавших плацебо.
Анализ клинических данных у пациентов контрольной группы, получавших плацебо с маркировкой «Кидз (Kidz) напиток с черносливом», показал отсутствие значимой динамики в изменении формы кала: у одного ребенка тип формы кала поменялся с 2-го на 3-й, и у одного с 3-го на 4-й. Также у пациентов этой группы не отмечено выраженного изменения количества дефекаций в неделю: 3,5 и 3,8 соответственно. Отсутствие значимой динамики в восстановлении регулярности дефекаций и формы кала у детей контрольной группы, несмотря на рекомендации по режиму дефекаций и рациону питания, можно объяснить низкой комплаентностью детей к рекомендациям, отсутствием должного контроля со стороны родителей (табл. 5).
В то же время погрешности в выполнении рекомендаций (нарушение диеты, питьевого режима и режима дефекации) в основной группе компенсировались ежедневным дополнительным приемом «Кидз (Kidz) напитка с черносливом».
Анализ клинических данных у пациентов основной группы через месяц после прекращения приема «Кидз (Kidz) напитка с черносливом» (60-й день - V3) показал сохранение положительных тенденций в отношении количества дефекаций в неделю - 4,8 в среднем среди детей обеих подгрупп. У детей контрольной группы число дефекаций изменилось незначительно (табл. 5).
До начала лечения акт дефекации сопровождался абдоминальной болью, вздутием живота, затрудненным опорожнением кишечника, чувством его неполного опорожнения, необходимостью натуживания, метеоризмом - как у пациентов контрольной, так и основной групп. Подавляющее большинство детей жаловались на метеоризм, вздутие живота, необходимость натуживания при дефекации (табл. 6).
Таблица 6. Частота симптомов, сопровождающих акт дефекации, у детей в группах, абс.

Наличие/отсутствие и выраженность симптомов оценивались по визуально-аналоговой шкале до начала лечения (V0) и на 30-й день терапии (V2) (табл.7).
Таблица 7. Наличие/отсутствие и выраженность симптомов у детей по визуально-аналоговой шкале до начала лечения (V0) и на 30-й день терапии (V2) (в баллах)
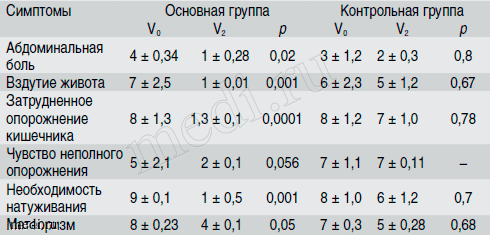
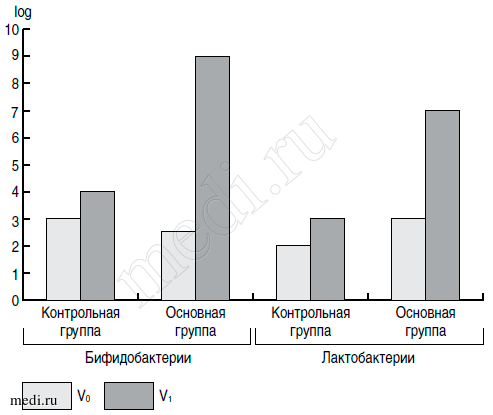
Рис. 2. Динамика роста бифидобактерий и лактобактерий.
Как видно из таблицы, у детей контрольной группы отсутствовала значимая динамика симптомов, тогда как у детей основной группы отмечалась статистически значимая положительная динамика клинической симптоматики в виде уменьшения абдоминальной боли (на 75%), вздутия живота (на 85,7%), чувства неполного и затрудненного опорожнения кишечника (на 83,8 и 60% соответственно), необходимости натуживания (на 88,9%), метеоризма (на 50%).
Исследование микробиоценоза кишечника. Состояние микробиоценоза кишечника бактериологическим методом было проанализировано у всех пациентов до начала исследования, а также через 1 месяц применения плацебо и «Кидз (Kidz) напитка с черносливом» соответственно в контрольной и опытной группах. У пациентов контрольной группы, получавших плацебо с маркировкой «Кидз (Kidz) напиток с черносливом», отмечалось отсутствие значимой динамики в анализах: микробный пейзаж спустя месяц был идентичен первоначальным значениям. В основной группе по завершении курса приема «Кидз (Kidz) напиток с черносливом» (через 30 дней) у всех 30 детей отмечен рост числа представителей индигенной микрофлоры, в частности бифидо- и лактобактерий (рис. 2), который достиг нормальных показателей - 1 х 109 и 1 х 107 КОЕ/мл соответственно (p<0,05). Кроме того, у 5 детей основной группы в начальных анализах определялось повышенное процентное содержание условно-патогенных энтеробактерий (рода Citrobacter у 3 детей; рода Klebsiella pneumoniae у 2 детей; у 5 детей - грибов рода Candida; у 3 - гемолизирующей E. Coli). После окончания применения «Кидз (Kidz) напиток с черносливом» у 5 пациентов определение условно-патогенных представителей микробиоценоза соответствовало нормативным значениям (не превышало 5%), у 2 пациентов с выделенной гемолизирующей E. Coli наблюдалось отсутствие ее выделения, у 1 ребенка - уменьшение выделения с 90 до 20%. Также у двух пациентов сохранялось выделение грибов рода Candida в количестве 1 х 103 и 1 х 104 КОЕ/мл соответственно, что отражало положительную динамику к уменьшению обсемененности кишечника грибами рода Candida (до начала лечения их количество составляло 1 х 104 и 1 х 106 КОЕ/мл соответственно). У пациентов контрольной группы статистически значимых количественных изменений показателей, свидетельствующих о состоянии кишечной микробиоты, выявлено не было.
Заключение
Анализ состояния моторики кишечника у детей основной группы показал наличие выраженной положительной динамики. Этот эффект обусловлен положительным влиянием дополнительного введения в рацион ребенка пребиотиков, способствующих пролиферации сахаролитической микрофлоры и разрыхлению каловых масс, усилению моторики. У детей контрольной группы выраженной динамики в композиции микробиоты, изменении формы кала и количестве дефекаций в неделю не отмечено. На фоне применения «Кидз (Kidz) напитка с черносливом» отмечено увеличение количества дефекаций в неделю на 36-42%, уменьшение тяжести симптомов запора.
Следует подчеркнуть, что проблемы, связанные с состоянием желудочно-кишечного тракта, влияют на формирование хронического психоэмоционального стресса, сопровождающего нарушение нормального акта дефекации. Как известно, существующие долгое время нарушения здоровья, мешающие социальной адаптации, к которым относится и функциональный запор, усугубляют психоневрологические проблемы, замыкая, таким образом, порочный круг патологии. Все это обусловливает еще большую необходимость коррекции при расстройствах дефекации.
Таким образом, результаты исследования клинической эффективности и безопасности препарата «Кидз (Kidz) напиток с черносливом», принимаемого детьми 3-14 лет в комплексной терапии хронического функционального запора в стадии компенсации, показали его клиническую и микробиологическую эффективность. Указанный препарат содержит 3 г нативных пищевых волокон в одном саше, а суточная доза суммарно составляет 9 г. В комплексе с диетой и режимными мероприятиями «Кидз (Kidz) напиток с черносливом» может занять достойное место в ряду средств, используемых для нормализации нерегулярной и затрудненной дефекации вследствие функциональных нарушений кишечника. На фоне его приема отмечено статистически достоверное увеличение частоты дефекаций. Кроме того, анализ форм кала как интегративного показателя времени транзита по кишке показал благотворное влияние на форму и консистенцию, а также сохраняющиеся позитивные тенденции у пациентов основной группы через 30 дней после отмены препарата.
В ходе исследования показаны безопасность и хорошая переносимость препарата (ни у одного ребенка не наблюдалось побочных реакций при приеме «Кидз (Kidz) напитка с черносливом»), отмечено положительное отношение детей к внешнему виду и вкусу препарата. Заявлена эффективность в комплексной терапии хронического функционального запора в стадии компенсации, поскольку прием «Кидз (Kidz) напитка с черносливом» способствовал увеличению числа дефекаций в неделю на 36-42%, уменьшению выраженности симптомов запора: абдоминальной боли на 75%, вздутия живота на 85,7%, затруднений опорожнения кишечника на 83,8%, чувства неполного опорожнения на 60%, необходимости натуживания на 88,9%, метеоризма на 50%. Препарат также оказал положительное влияние на количественный состав кишечной микробиоты: прием «Кидз (Kidz) напитка с черносливом» способствовал росту бифидо- и лактобактерий и достижению нормальных показателей их количества (увеличению на 1 х 104 и 1 х 105 КОЕ/мл соответственно), уменьшению роста условно-патогенной микрофлоры.
Финансирование
Информация отсутствует.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
ЛИТЕРАТУРА
- Drossman DA. Functional gastrointestinal disorders: history, pathophysiology, clinical features and Rome IV. Gastroenterology. 2016 Feb 19. pii: S0016-5085(16)00223-7. DOI: 10.1053/j.gastro.2016.02.032
- Schmulson MJ, Drossman DA. What Is New in Rome IV. J Neurogastroenterol Motil. 2017 Apr 30;23(2):151-163. DOI: 10.5056/jnm16214
- Talley NJ, Stanghellini V, Chan FKL, Gastroduodenal Disorders. In: Drossman DA, Chang LC, W Kellow J, Tack J, Whitehead WE, The Rome IV Committees, eds. Rome IV functional gastrointestinal disorders - disorders of gut-brain interaction. Volume II. Raleigh, NC: The Rome Foundation 2016:903-965.
- Бельмер СВ, Хавкин АИ, Разумовский АЮ, Файзуллина РА. Запоры у детей. М.: ИД «Медпрактика-М», 2016, 312 с.
- Kramer EAH, den Hertog-Kuijl JH, van den Broek LM, van Leengoed E, Bulk AM, Kneepkens CM, Benninga MA. Defecation patterns in infants: a prospective cohort study. Arch Dis Child. 2015 Jun;100(6):533-6. DOI: 10.1136/archdischild-2014-307448
- Keefer L, Drossman DA, Guthrie E, Simren M, Tillisch K, Olden K, Whorwell PJ. Centrally mediated disorders of gastrointestinal pain. Gastroenterology. 2016 Feb 19. pii: S0016-5085(16)00225-0. DOI: 10.1053/j.gastro.2016.02.034
- Хавкин АИ, Файзуллина РА, Бельмер СВ, Горелов АВ, Захарова ИН, Звягин АА, и др. Диагностика и тактика ведения детей с функциональными запорами (Рекомендации общества детских гастроэнтерологов). Вопросы практической педиатрии. 2014;9(5):62-76.
- Tabbers MM, DiLorenzo C, Berger MY, Faure C, Langendam MW, Nurko S, et al. Evaluation and Treatment of Functional Constipation in Infants and Children: Evidence-Based Recommendations From ESPGHAN and NASPGHAN. J Pediatr Gastroenterol Nutr. 2014Feb;58(2):258-74.DOI: 10.1097/MPG.0000000000000266
- Hyams JS, Di Lorenzo C, Saps M, Shulman RJ, Staiano A, van Tilburg M. Childhood Functional Gastrointestinal Disorders: Child/Adolescent. Gastroen-terology. 2016 Feb 15. pii: S0016-5085(16)00181 -5. DOI: 10.1053/j. gastro.2016.02.015
- Gordon M, MacDonald JK, Parker CE, Akobeng AK, Thomas AG. Osmotic and stimulant laxatives for the management of childhood constipation. Cochrane Database Syst Rev. 2016 Aug 17;(8):CD009118. DOI: 10.1002/14651858. CD009118.pub3
- Sperber AD, Gwee KA, Hungin AP, Corazziari E, Fukudo S, Gerson C, et al. Conducting multinational, cross-cultural research in the functional gastrointestinal disorders: issues and recommendations. A Rome Foundation working team report. Aliment Pharmacol Ther. 2014 Nov;40(9):1094-102. DOI: 10.1111/ apt.12942
References
- Drossman DA. Functional gastrointestinal disorders: history, pathophysiology, clinical features and Rome IV. Gastroenterology. 2016 Feb 19. pii: S0016-5085(16)00223-7. DOI: 10.1053/j.gastro.2016.02.032
- Schmulson MJ, Drossman DA. What Is New in Rome IV. J Neurogastroenterol Motil. 2017 Apr 30;23(2):151-163. DOI: 10.5056/jnm16214
- Talley NJ, Stanghellini V, Chan FKL, Gastroduodenal Disorders. In: Drossman DA, Chang LC, W Kellow J, Tack J, Whitehead WE, The Rome IV Committees, eds. Rome IV functional gastrointestinal disorders - disorders of gut-brain interaction. Volume II. Raleigh, NC: The Rome Foundation 2016:903-965.
- Bel'mer SV, Khavkin AI, Razumovskii AYu, Faizullina RA. Zapory u detei. Moscow: «Medpraktika-M» Publ., 2016, 312 p. (In Russian).
- Kramer EAH, den Hertog-Kuijl JH, van den Broek LM, van Leengoed E, Bulk AM, Kneepkens CM, Benninga MA. Defecation patterns in infants: a prospective cohort study. Arch Dis Child. 2015 Jun;100(6):533-6. DOI: 10.1136/archdischild-2014-307448
- Keefer L, Drossman DA, Guthrie E, Simren M, Tillisch K, Olden K, Whorwell PJ. Centrally mediated disorders of gastrointestinal pain. Gastroenterology. 2016 Feb 19. pii: S0016-5085(16)00225-0. DOI: 10.1053/j.gastro.2016.02.034
- Khavkin AI, Fayzullina RA, Belmer SV, Gorelov AV, Zakharova IN, Zvyagin AA, et al. Diagnosis and tactics of treatment of children with functional constipation (Recommendations of the Society of paediatric gastroenterologists). Vopr. prakt. pediatr. (Clinical Practice in Pediatrics). 2014;9(5):62-76. (In Russian).
- Tabbers MM, DiLorenzo C, Berger MY, Faure C, Langendam MW, Nurko S, et al. Evaluation and Treatment of Functional Constipation in Infants and Children: Evidence-Based Recommendations From ESPGHAN and NASPGHAN. J Pediatr Gastroenterol Nutr. 2014Feb;58(2):258-74.DOI: 10.1097/MPG.0000000000000266
- Hyams JS, Di Lorenzo C, Saps M, Shulman RJ, Staiano A, van Tilburg M. Childhood Functional Gastrointestinal Disorders: Child/Adolescent. Gastroente-rology. 2016 Feb 15. pii: S0016-5085(16)00181 -5. DOI: 10.1053/j.gastro. 2016.02.015
- Gordon M, MacDonald JK, Parker CE, Akobeng AK, Thomas AG. Osmotic and stimulant laxatives for the management of childhood constipation. Cochrane Database Syst Rev. 2016 Aug 17;(8):CD009118. DOI: 10.1002/14651858.CD009118.pub3
- Sperber AD, Gwee KA, Hungin AP, Corazziari E, Fukudo S, Gerson C, et al. Conducting multinational, cross-cultural research in the functional gastrointestinal disorders: issues and recommendations. A Rome Foundation working team report. Aliment Pharmacol Ther. 2014 Nov;40(9):1094-102. DOI: 10.1111/apt.12942

