Опыт применения препарата Элькар в практике неонатолога
Статьи
Опубликовано в:
Террамедика 2006 №3
д.м.н. М.Я. Ледяев, к.м.н. Т.Е. Заячникова
Волгоградский Государственный медицинский университет
В последние десятилетия наметилась тенденция к повышению уровня заболеваемости новорожденных [ 1 ]. Это требует от неонатолога поиска современных, эффективных, безопасных, универсальных лекарственных препаратов, соответствующих стандартам перинатальной фармакотерапии.
На базе отделения патологии новорожденных Волгоградского городского перинатального центра проводилось изучение эффективности препарата «Элькар» (20% раствор левокарнитина). Препарат во всех исследованиях назначали в суточной дозе от 50 до 100 мг/ кг в 2-3 приема курсом от 21 до 28 дн. при различной (нередко сочетанной) патологии новорожденных: задержки внутриутробного развития, пренатальной гипотрофии, неона-тальной гипербилирубинемии, транзиторной ишемии миокарда.
Доношенные дети, родившиеся с патологически обусловленной малой массой тела (ММТ), представляют собой гетерогенную группу, объединенную общими проявлениями задержки внутриутробного развития (ЗВУР) и связанными с ней признаками морфофункциональной незрелости.
Исследования последних лет показали хороший анаболический эффект препаратов карнитина в педиатрической практике [2, 3]. Патогенетическим основанием его назначения является развитие «функциональной» карнитиновой недостаточности в отдельные периоды онтогенеза, в том числе у новорожденных с ММТ [3].
Под нашим наблюдением находились 27 новорожденных в возрасте от 4 до 29 дн. жизни, родившихся на сроках гестации 38 — 41 нед. с малой массой тела (пренатальной гипотрофией и ЗВУР), находившихся на лечении в отделении патологии новорожденных. Гипотрофический тип ЗВУР выявлен у 56% новорожденных, гипопластический — у 41%, диспластический — у 3,7%. Все дети наряду со ЗВУР имели клинику пренатальной гипотрофии.
Кроме клинического динамического наблюдения за новорожденными, контролировалась динамика массы и длины тела, производился расчет коэффициента усвоения белка (КУБ) — величины ежедневной прибавки массы на 1 г пищевого белка до начала терапии и на 2-4-й нед. лечения. Все дети
получали комплексную терапию основного заболевания, включавшую парентеральное введение растворов 10 % глюкозы, рибоксина, аскорбиновой кислоты, кокарбоксилазы, пирацетама; энтерального приема витаминов В2, В6, Е, липоевой кислоты, метионина, пищеварительных ферментов, эубиотиков, а также курсы общего массажа и ЛФК.
Все наблюдаемые дети были случайным образом разделены на две группы, сопоставимые по возрасту, антропометрическим данным, факторам антенатального и перинатального риска, патологии неонатального периода: I группа (n= 17) — дети, получавшие дополнительно «Элькар», и II группа (n=10) — контрольная.
Удовлетворительная прибавка массы тела за первый месяц жизни у новорожденных I группы позволила 92% детей выйти из состояния гипотрофии, в то время как во II группе только 30% детей вышли из состояния гипотрофии к моменту окончания курса лечения.
С 1-й недели применения препарата «Элькар» повысились среднесуточные прибавки массы тела (рис.1), ускорились темпы восстановления убыли первоначальной массы тела. На 2-3-й неделях повысился коэффициент усвоения белка, уровень сывороточного белка и гемоглобина крови. Уровень общего белка сыворотки крови у детей I группы достоверно повышался уже на 2-й нед. от начала терапии «Элькаром» по сравнению со II группой.
Необходимо отметить хорошую переносимость препарата у всех пациентов, включенных в исследование, полное отсутствие побочных эффектов и нежелательных реакций, простоту и удобство в применении. Проведенное исследование позволило сделать выводы о том, что препарат «Элькар» способствует повышению суточных прибавок массы тела, улучшению усвоения пищевого белка и повышению уровня сывороточного белка у новорожденных с ММТ.
В последние годы обозначилась тенденция к нарастанию числа затяжных форм непрямой гипербилирубинемии (НГБЕ) с высокими цифрами билирубина в крови, часто не связанных с гемолитической болезнью новорожденных. Хотя причину
НГБЕ не всегда можно определить достоверно, тактика лечения обычно направлена на ускорение процессов элиминации непрямого билирубина и нивелирование факторов риска его нейротоксичности [4]. Существующие на сегодняшний день методы консервативной терапии неонатальных желтух не всегда позволяют добиться быстрого и стойкого купирования НГБЕ, в силу чего проблему лечения неонатальных желтух нельзя считать окончательно решенной.
Известно, что билирубин оказывает действие на обменные процессы в митохондриях путем разобщения окислительного фосфориллирования [4]. Доказано, что одним из важнейших факторов возникновения митохондриальных дисфункций, обусловленных дефицитом транспорта и окисления жирных кислот, является недостаточность карнитина[3].
Нами было проведено динамическое контролируемое исследование в параллельных группах 34 детей в возрасте от 4 до 32 дн. жизни, находившихся на лечении в отделении патологии новорожденных по поводу патологической гипербилирубинемии. Все новорожденные получали комплексную консервативную терапию в виде внутривенной инфузии растворов глюкозы, эсенциале, интрагастральных капельных введений глюкозосолевых растворов, энтерального приема витаминов В2, Е, метионина, фенобарбитала, желчегонных препаратов, энтеросорбентов. В исследование не включались дети, получавшие фототерапию, заменное переливание крови и гемосорбцию.
Препарат «Элькар» дополнительно получали 24 новорожденных. Исходный уровень билирубина в исследуемых группах не отличался. Обратное развитие патологических симптомов заболевания на фоне лечения «Элькаром», по нашим наблюдениям, наступало раньше, чем в группе сравнения. Так, визуальное уменьшение интенсивности желтухи отмечено у детей I группы уже на 2-3-е сут. от начала лечения, а полное исчезновение симптома желтухи — в среднем на 5-6-е сутки, что на 2-4 суток быстрее, чем во II группе.
В I группе новорожденных отмечались более высокие темпы снижения абсолютных значений непрямого билирубина (рис. 2) по сравнению со II группой.
Таким образом, применение препарата «Элькар» в составе комплексной консервативной терапии НЖ способствует более выраженной положительной направленности клинико-биохимических показателей НГБЕ в виде повышения темпов обратного развития симптомов желтухи, снижения уровня непрямого билирубина.
Исследованиями последних лет показана высокая частота (15—40%) транзиторной ишемии миокарда (ТИМ) у новорожденных, перенесших перинатальную гипоксию [7]. Актуальной задачей перинатальной кардиологии является разработка методов коррекции ТИМ у новорожденных, сущностью которой является терапия, направленная на уменьшение зоны дистрофических изменений в сократительном миокарде и проводящей системе сердца [6].
При дефиците карнитина нарушается утилизация длинноцепочечных жирных кислот, что в свою очередь приводит к отложению липидов в мышечной ткани (в том числе — в миокарде), нарушению сократительной способности мышц, окислительного фосфориллирования. С другой стороны, перинатальная гипоксия и родовой стресс приводят к задержке созревания митохондриальных ферментных систем, в том числе карнитиновой [7].
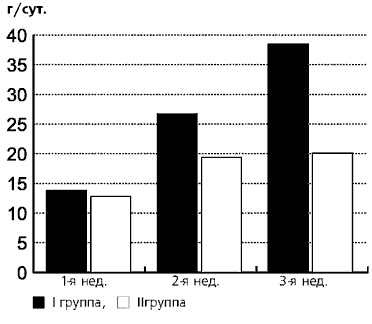
Рис.1. Среднесуточная прибавка массы тела новорожденных с ММТ на фоне терапии препаратом «ЭЛЬКАР».
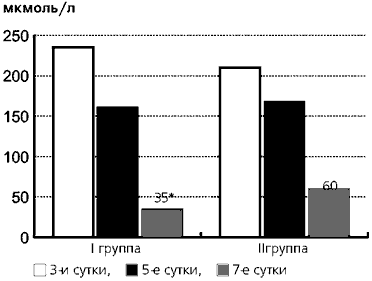
Рис. 2. Динамика уровня непрямого билирубина у новорожденных с непрямой гипербилирубинемией на фоне терапии препаратом «ЭЛЬКАР».
Примечание: *-р<0,05.
Под нашим наблюдением находились 42 новорожденных в возрасте от 7 до 28 дн., родившихся на сроках гестации 37-40 нед., находившихся в отделении патологии новорожденных по поводу гипоксически-ишемического поражения ЦНС и постгипоксической кардиопатии. Все дети получали комплексную терапию в виде в/в инфузий 10% раствора глюкозы, рибоксина, витамина С, трентала, пирацетама. С целью стимуляции метаболических процессов в миокарде часть новорожденных — I группа (п=29) — получала препарат «Элькар».
К ЭКГ- критериям ТИМ относили: деформации желудочкового комплекса QRS, расширение и зазубренность его зубцов, нарушения внутрижелудочковой проводимости, единичные суправентрикулярные экстрасистолы, отклонения сегмента ST от изолинии более чем на 2 мм в 2 и более прекардиальных отведениях, изоэлектричные или интервертированные зубцы Т [7].
В обеих группах новорожденных на фоне проводимого лечения в конце 2-й — начале 3-й нед. отмечена положительная динамика клинических симптомов: уменьшение бледности и цианоза кожи, восстановление звучности сердечных тонов, исчезновение нарушений ритма сердца, сокращение размеров печени, исчезновение отеков. Однако в группе новорожденных, получавших препарат «Элькар», синусовая тахикардия наблюдалась в 2 раза реже, чем в контроле. Частота регистрации других нарушений ритма (брадиаритмии, желудочковые и предсердные экстрасистолии, суправентрикулярные тахикардии) в обеих группах на фоне лечения снижалась одинаково.
В обеих группах отмечено уменьшение деформаций комплекса QRS в динамике, что свидетельствует об отсутствии прогрессирования дистрофических изменений миокарда на фоне лечения. Однако у новорожденных I группы обнаружено более существенное уменьшение отклонений амплитуды зубцов Т, сильнее выраженное в правых грудных отведениях.
На 3-й нед. от начала лечения «Элькаром» у 55 % новорожденных сегмент ST возвратился на изолинию, у 31 % имело место умеренное изменение ST-сегмента в процессе лечения, и только у 14% существенной динамики показателя не отмечено.
Наши исследования подтверждают эффективность коррекции метаболических нарушений при ТИМ у новорожденных препаратом «Элькар». Выявлено существенное улучшение клинической картины и показателей ЭКГ у I группы новорожденных с ТИМ, по сравнению с новорожденными II группы.
Таким образом, наш опыт использования препарата «Элькар» в комплексной терапии различных заболеваний новорожденных показал его полное соответствие требованиям перинатальной фармакологии. Удобство, безопасность, эффективность препарата позволяет рекомендовать его для использования в практической неонатологии.
Список литературы
1. Самсыгина Г.А., Дементьева Г.М., Талалаев А.Г. Здоровье плода и новорожденного: современное состояние и прогноз // Педиатрия. 1999. № 5. С. 4—6.
2. Авакумов В.М., Смирнова Г.И., Клементьева И.В., Кругликова Р.П. Фармакотерапевтические свойства карнитина-хлорида — анаболического препарата нестероидной природы // Химико-фармацевтический журнал. 1988. № 3. Т. 22. С. 379—382.
3. Белозеров Ю.М. Недостаточность карнитина у детей. / Российский вестник перинатологии и педиатрии. 1996. № 4. С. 42 — 47.
4. Макарова И.В., Шабалов Н.П. Клиническая фармакология новорожденных. СПб., 1993. С. 285—301.
5. Симонова Л.В., Котлукова Н.П., Гайдукова Н.В. и др. Постгипоксическая дезадаптация сердечно-сосудистой системы у новорожденных / / Российский вестник перинатологии и педиатрии. 2001. № 2. С. 8—12.
6. Прахов А.В. Коррекция транзиторной постгипоксической ишемии миокарда у новорожденных // Педиатрия. 1998. № 5. С. 38—42.
7. Котлукова Н.П. Дифференциальная диагностика поражений миокарда у детей первого года жизни / / Физиология и патология сердечно-сосудистой системы у детей первого года жизни. М., 2002. СИЗ—125.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)