Уважаемый посетитель!
Эта информация для специалистов здравоохранения
Нажимая «ПРОДОЛЖИТЬ», Вы подтверждаете, что им являетесь
 pikfarma.ru
pikfarma.ru
• Оригинальный ноотропный препарат с противотревожным действием
• Активирует умственную деятельность, улучшает эмоциональное состояние
Применение препарата пантогам актив (D-, L-гопантеновая кислота) в терапии когнитивных и тревожных расстройств у пациентов с артериальной гипертензией
СтатьиОпубликовано в журнале:
« ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ » 12, 2015г.
А.Б. Смулевич1, 2, Б.А. Волель1, 2, Е.С. Терновая1, Ю.М. Никитина1
1ГОУ ВПО «Первый Московский государственный медицинский университет им. И.М. Сеченова», Москва;
2ФГБНУ «Научный центр психического здоровья», Москва
Материал и методы. Наблюдали 80 пациентов кардиологического стационара с верифицированным диагнозом артериальной гипертензии и коморбидными когнитивными и тревожными нарушениями; 50 пациентов составили основную группу, 30 пациентов - группу контроля. Все пациенты получали стандартную кардиотропную гипотензивную терапию. В комплексную терапию пациентов основной группы был включен Пантогам актив в суточной дозе от 600 до 1200 мг. Проводилось психопатологическое и психометрическое обследование с сопоставлением полученных данных с динамикой соматических показателей (ЭКГ, суточное мониторирование артериального давления, биохимический анализ крови). Длительность терапии D-, L-гопантеновой кислотой составила 28 дней.
Результаты. Получены данные о достоверной редукции как когнитивных, так и тревожных нарушений в основной группе по сравнению с контрольной, а также у пациентов, перенесших острое нарушение мозгового кровообращения в анамнезе. Положительная динамика наблюдалась на протяжении всего времени лечения.
Заключение. Подтверждена возможность использования D-, L-гопантеновой кислоты (Пантогам актив) в качестве препарата выбора с бимодальной ноотропной и транквилизирующей активностью для лечения когнитивных и тревожных нарушений у пациентов с артериальной гипертензией. Показано, что в процессе терапии Пантогамом актив происходит быстрая (в течение первой недели терапии) и достоверная редукция тревожных и когнитивных нарушений.
Ключевые слова: соматопсихиатрия, когнитивные нарушения, тревожные расстройства, артериальная гипертензия, лечение.
Pantogam activ (D-, L-hopantenic acid) in the treatment of cognitive and anxiety disorders in patients with arterial hypertension
A.B. Smulevich, B.A. Volel, E.S. Ternovaya, YU.M. Nikitina
Sechenov First Moscow State Medical University, Moscow; Research Center of Mental Health, Moscow
Objective - to evaluate the efficacy and safety of D-, L- hopantenic acid (pantogam active) on cognitive and anxiety disorders in patients with arterial hypertension.
Material and methods. Autors selected 80 inpatients of a cardiology department with the verified diagnosis of hypertension and comorbid cognitive and anxiety disorders (50 patients in the main group, 30 patients in the control one). All patients received standard cardiotropic hypotensive treatment. Patients of the main group received in addition pantogam active in the daily dose from 600 to 1200 mg. Psychopathological and psychometric examinations were conducted, the data were compared with the dynamics of physical parameters (ECG, ambulatory blood pressure monitoring, blood chemistry). The duration of treatment with pantogam activ was 28 days.
Results. There was a significant reduction in both cognitive and anxiety disorders in the main group compared with the controls and in patients with a history of stroke. The positive dynamics was observed during the treatment period.
Conclusions. Authors support the possibility of using D-, L-hopantenic acid (pantogam active) as a drug of choice with bimodal activity (nootropic and tranquilizing) in the treatment of cognitive and anxiety disorders in patients with arterial hypertension. A rapid (in the first week) significant reduction of cognitive and anxiety disorders during the treatment with pantogam activ was noted.
Keywords: somatopsychiatry, cognitive impairment, anxiety disorders, arterial hipertension, treatment.
Когнитивные и тревожные расстройства при артериальной гипертензии (АГ) широко распространены [1-4]. Частота когнитивных нарушений (КН) при АГ превышает таковую в популяции в 10 раз [5]. Субклинические проявления поражения головного мозга наблюдаются по меньшей мере у 44% пациентов с АГ [6]. По данным отечественных исследований [7], нелеченная в течение 5 лет АГ приводит к возникновению КН у 68% пациентов. Таким образом, АГ рассматривается в настоящее время как самый значимый фактор риска развития не только острых нарушений мозгового кровообращения (ОНМК) [8], но и синдрома умеренных КН1 [9, 10].
Прогрессирование АГ способствует нарастанию проявлений КН [14, 15] посредством глубинных нарушений структуры сосудистой стенки, что ведет к увеличению очагов разрежения белого вещества и появлению лакун в головном мозге (феномен «немых» лакун по данным магнитно-резонансной томографии) [16-18].
Актуальность изучения КН, не достигающих степени сосудистой деменции, обусловлена также тем, что их своевременное выявление и адекватное лечение у пациентов с АГ повышает качество жизни больных, позволяя замедлить, а в некоторых случаях и предотвратить наступление тяжелых проявлений когнитивных расстройств (деменция) [19].
Особого внимания заслуживает вопрос о КН у пациентов, перенесших ОНМК/транзиторную ишемическую атаку (ТИА). Согласно данным ряда исследований [20, 21], частота развития недементных КН в постинсультном периоде достигает 40-49%. Умеренные КН в постинсультном периоде приводят к социально-бытовой дезадаптации даже в отсутствие значительных двигательных нарушений, оказывая негативное влияние на качество жизни больных, перенесших инсульт [22]. Существует также тесная корреляция между КН и прогнозом степени инвалидизации пациентов. Среди больных с постинсультной деменцией также выше риск повторного инсульта, что отчасти связано с трудностями проведения вторичной профилактики сосудистой патологии у этой категории пациентов. По некоторым данным, восстановление двигательных функций у больных с более выраженными КН протекает медленнее и обычно бывает менее значительным [23, 24].
Наличие тревожных расстройств имеет высокое прогностическое значение для пациентов с АГ [25]. Частота тревожных нарушений при АГ, по данным литературы [26-28], достигает 42%, что вдвое превышает их распространенность в популяции (без АГ).
В большинстве исследований констатируется факт негативного влияния коморбидных тревожных расстройств на течение АГ (неконтролируемая гипертензия, повышение риска развития кардиоваскулярных осложнений) и поведение пациентов (нарушение комплаенса и формирование кардиоперсонифицированных синдромов)2 [29-31]. Кроме того, тревожные нарушения, амплифицирующие симптом соматической патологии, способствуют ухудшению показателей качества жизни пациентов, усложнению и удорожанию процесса лечения. Так, по данным ряда авторов [32, 33], наличие тревожных расстройств у пациентов кардиологического стационара повышает риск кардиальных осложнений в 2,5-4,9 раза. Тревожные расстройства также коррелируют с увеличением медицинских затрат и длительностью пребывания больного в кардиологическом отделении [34].
Таким образом, тревожные и когнитивные расстройства лидируют по частоте у пациентов с АГ и серьезным образом влияют на течение и прогноз кардиоваскулярной патологии, ухудшают приверженность к терапии и снижают качество жизни больных. Необходимость проведения адекватной купирующей и профилактической терапии этих расстройств, наряду с лечением основного заболевания, не вызывает сомнений.
Современная гипотензивная терапия способствует реализации протективного эффекта при острых сосудистых катастрофах (инсульт), но не обладает профилактическим действием в отношении умеренных когнитивных и тревожных нарушений [35, 36]. Назначаемые кардиологами и терапевтами ноотропные препараты для коррекции КН нередко способствуют повышению уровня тревоги. В свою очередь анксиолитическая терапия (в комбинации с кардиотропными препаратами) значительно улучшает качество жизни больных АГ, однако имеет ряд ограничений. Так, пациенты часто избегают приема противотревожных препаратов (бензодиазепины), опасаясь развития привыкания, поведенческих побочных эффектов (вялость, заторможенность, нарушения внимания, трудности сосредоточения) [37]. Другие же распространенные в нашей стране способы коррекции тревожных нарушений (фитотерапия) у больных с сердечно-сосудистой патологией не оказывают необходимого терапевтического эффекта. С учетом отмеченных проблем в последние годы все чаще возникает потребность в препаратах со сбалансированным транквилизирующим и ноотропным эффектом [38, 39].
Назначение одного препарата, обладающего бимодальной (анксиолитической и ноотропной) активностью, способствует одновременной коррекции как когнитивных, так и тревожных расстройств, позволяет снизить лекарственную нагрузку на пациента, обеспечивает высокие показатели качества жизни пациентов как на стационарном, так и на последующих этапах лечения. По данным литературы, таким препаратом является Пантогам актив (МНН D-, L-гопантеновая кислота, рац-гопантеновая кислота). За счет включения в формулу L-изомера Пантогам актив обладает дополнительным анксиолитическим действием и может применяться длительно без развития привыкания, синдрома отмены или гиперстимуляции у пациентов с сердечно-сосудистыми заболеваниями [40].
Цель настоящего исследования - оценка эффективности и безопасности терапии препаратом Пантогам актив когнитивных и/или тревожных нарушений у пациентов с длительно текущей АГ II-III степени.
Материал и методы
Открытое контролируемое рандомизированное исследование проведено на базе клиники кардиологии Университетской клинической больницы №1 Первого Московского государственного медицинского университета им. И.М. Сеченова. Наблюдали 80 пациентов, находившихся на стационарном лечении с диагнозом АГ (рубрики I10-111 по МКБ-10) и коморбидными когнитивными (легкими и умеренными) и тревожными нарушениями.
Критерии включения больных в исследование были следующие: мужчины и женщины в возрасте от 18 до 75 лет, находящиеся на стационарном лечении с подтвержденным диагнозом АГ II-III стадии по МКБ-10; легкие и умеренные когнитивные (<26 баллов по Монреальской шкале оценки когнитивных функций - MoCA) и тревожные расстройства (F40, F41, F45 по МКБ-10; >30 баллов по шкале самооценки тревоги Шихана); добровольное информированное согласие пациента на участие в исследовании.
Критериями исключения являлись: гиперчувствительность к Пантогаму актив в анамнезе; наличие психической патологии: шизофрения - параноидная (F20.0), гебефреническая (F20.1), кататоническая (F20.2); хронические бредовые расстройства (F22); острые психотические расстройства (F23); шизоаффективные расстройства (F25); биполярное аффективное расстройство (F31); депрессивный эпизод умеренной или тяжелой степени (F32.1, F32.2, F33.3); рекуррентная депрессия, текущий эпизод умеренной или тяжелой степени (F33.1, F33.2, F33.3); злоупотребление анальгетиками (F55.2), злоупотребление стероидами или гормонами (F55.5); зависимость от психоактивных веществ (F10-F19); расстройства влечений (F50-F59); наличие отчетливых суицидальных намерений, суицидальное поведение или суицидальные попытки в анамнезе; наличие соматической патологии - тяжелой печеночной и/или почечной недостаточности, злокачественных новообразований, глаукомы; соматическое заболевание в стадии декомпенсации, не позволяющее провести адекватную клиническую и психометрическую оценку психического состояния пациента.
Методом стратификационной рандомизации с помощью таблиц случайных чисел из пациентов, получавших стандартную кардиотропную гипотензивную терапию в условиях стационара, были сформированы 2 группы. В основную группу вошли 50 пациентов, в комплексную терапию которых был включен Пантогам актив. В контрольную группу вошли 30 пациентов, находившихся на стандартной кардиотропной гипотензивной терапии без применения Пантогама актив. Выделенные группы были сопоставимы по полу, возрасту, проявлениям АГ и психических расстройств. Средний возраст пациентов составил 62,2±6,1 года в основной группе и 58,6±5,4 года в группе контроля. В обеих группах преобладали пациенты женского пола (62,8% в основной и 65,1% в контрольной группах).
Суточная доза Пантогама актив варьировала от 600 до 1200 мг в зависимости от клинических проявлений и выраженности когнитивных и тревожных расстройств. Длительность терапии составила 28 дней. Состояние пациентов оценивалось до начала терапии, через 7, 14 и 28 дней лечения (1-4-й визиты).
Набор больных, скрининговые процедуры, повизитная клиническая диагностика психического состояния и психометрическое тестирование и лечение пациентов обеих групп проводилось врачом-психиатром совместно с кардиологом в условиях кардиологического стационара и на последующем постстационарном этапе.
Терапевтическая эффективность Пантогама актив анализировалась по шкалам оценки когнитивных расстройств МоСА, самооценки тревоги Шихана, самооценки качества жизни EQ-5D.
Шкала самооценки тревоги Шихана состоит из 35 вопросов, описывающих различные симптомы тревожного состояния. Отвечая на каждый вопрос, пациент оценивает наличие и степень их выраженности в течение недели, предшествующей тесту. Исследователь подсчитывает суммарный балл.
MоCA разработана для быстрого скрининга мягких КН и позволяет оценить различные когнитивные функции: внимание и концентрацию, исполнительные функции, память, речь, оптико-пространственную деятельность, концептуальное мышление, счет и ориентированность. При сумме баллов <26 диагностируются КН.
Опросник самооценки качества жизни EQ-5D предназначен для оценки качества жизни и описания состояния здоровья по 5 шкалам. Результаты EQ-5D могут быть представлены в виде индекса здоровья - взвешенного коэффициента, соотнесенного с популяцией, и количественного значения общего состояния здоровья, оцененного по визуальной аналоговой шкале.
В качестве респондеров расценивали больных с более чем 50% снижением первоначальной суммы баллов, частичных респондеров - с более чем 25% снижением.
Безопасность и переносимость препарата оценивались на основании данных клинических и параклинических соматических исследований (биохимический анализ крови, ЭКГ, показатели АД, ЧСС, масса тела, суточное мониторирование АД).
Статистический анализ количественных данных проводили с помощью лицензионного статистического пакета SPSS 13.0 for Windows. Динамика состояния пациентов изучалась при помощи теста Вилкоксона. Уровень значимости принимался p<0,05.
Результаты
Следует сразу отметить, что в процессе терапии Пантогамом актив ни один пациент не был исключен из исследования (ни по причинам неэффективности препарата, ни по причине непереносимости терапии, ни по каким-либо другим причинам). На протяжении всего стационарного и постстационарного этапов терапии пациенты, принимавшие Пантогам актив, демонстрировали высокую приверженность к лечению.
Пантогам актив назначался в стартовой дозе 600 мг/сут. В соответствии с выраженностью клинических проявлений тревожных и КН 20 (40%) пациентов принимали Пантогам актив в суточной дозе 600 мг на протяжении всего курса терапии; у 15 (30%) потребовалось увеличение дозы до 900 мг после 1-й недели терапии; еще в 15 (30%) случаях (пациенты с ОНМК/ТИА в анамнезе) доза была увеличена по усмотрению исследователя до 1200 мг/сут после 2-й недели терапии. Таким образом, средняя суточная доза Пантогама актив в изученной выборке составила 900 мг/сут.
Средняя длительность АГ составила 17,9±9,2 года. В 68% наблюдений диагностирована II стадия АГ, в 32% - III стадия; очень высокий риск сердечно-сосудистых осложнений выявлен в 73% наблюдений. Кардиологическая характеристика пациентов представлена в табл. 1. Следует отметить достаточно высокую частоту осложнений АГ и поражения органов-мишеней, что свидетельствует о необходимости терапии АГ именно в условиях стационара.
Средние баллы по шкале МоСА на момент начала и окончания терапии были следующими: на начало исследования (1-й день) в основной группе 21,5±3,1 балла, на конец исследования (28-й день) - 27,5±1,2 балла, в контрольной группе эти показатели были соответственно 21,7±4,3 и 23,6±2,5 балла. Обращает на себя внимание более выраженное увеличение балльной оценки в основной группе по сравнению с контрольной к моменту окончания терапии.
Когнитивные нарушения
Частота выявленных КН по отдельным параметрам шкалы МоСА представлена в табл. 2. Во всех случаях (100%) встречались нарушения памяти, в большинстве наблюдений - расстройства оптико-пространственной деятельности, абстрактного мышления и внимания.
В соответствии с поставленными задачами исследования в основной группе были выделены пациенты, перенесшие ОНМК/ТИА: 18 человек, 12 женщин и 6 мужчин (средний возраст - 66,2±6,2 года). В контрольной группе также были выделены пациенты с ОНМК/ТИА в анамнезе: 10 человек, 7 женщин и 3 мужчины (средний возраст - 65,9±6,5 года). Средняя длительность постинсультного периода составила 6,07±4,08 года в основной группе и 6,5±3,9 года в контрольной группе. Преобладающим типом перенесенного ОНМК был ишемический инсульт - 16 (88,8%) наблюдений в основной группе, 9 (90%) - в контрольной. В меньшей части наблюдений регистрировался геморрагический инсульт - 2 (11,2%) случая в основной группе и 1 (10%) - в контрольной3. Кардиологическая характеристика пациентов с ОНМК/ТИА в анамнезе представлена в табл. 3. Обращают на себя внимание преобладание кризового течения АГ и большая частота гипертонических кризов в год, а также наличие в 100% наблюдений гиперлипидемии.
Таблица 1. Кардиологическая характеристика выборки на момент включения в исследование
| Показатель | Основная группа (n=50) | Контрольная группа (n=30) | ||
| n | % | n | % | |
| ОНМК/ТИА в анамнезе | 18 | 36 | 10 | 33,3 |
| Средняя длительность постинсультного периода, годы | 6,07±4,08 | - | 6,5±3,9 | - |
| Тип инсульта | ||||
| ишемический | 16 | 88,8 | 9 | 90 |
| геморрагический | 2 | 11,2 | 1 | 10 |
| Течение заболевания | ||||
| кризовое | 23 | 46 | 13 | 43,3 |
| некризовое | 27 | 54 | 17 | 56,7 |
| Среднее число гипертонических кризов в год | 10,4±5,2 | - | 9,9±6,1 | - |
| Факторы риска сердечно-сосудистых осложнений | ||||
| сахарный диабет | 20 | 40 | 13 | 43,3 |
| гиперлипидемия | 43 | 86 | 27 | 90 |
| Осложнения | ||||
| гипертрофия левого желудочка | 27 | 54 | 15 | 50 |
| дилатация левого предсердия | 13 | 26 | 10 | 33,3 |
| хроническая болезнь почек | 5 | 10 | 4 | 13,3 |
| хроническая сердечная недостаточность | 3 | 6 | 1 | 3,3 |
| фибрилляция предсердий | 24 | 48 | 14 | 46,6 |
Таблица 2. Когнитивные нарушения по шкале МоСА в основной и контрольной группах
| Показатель по разделам МоСА | Основная группа (n=50) | Контрольная группа (n=30) | ||
| n | % | n | % | |
| Оптико-пространственная деятельность | 37 | 74 | 21 | 70 |
| Называние предметов | 16 | 32 | 9 | 30 |
| Память | 50 | 100 | 30 | 100 |
| Внимание | 20 | 40 | 11 | 36,6 |
| Речь | 8 | 16 | 3 | 10 |
| Абстрактное мышление | 23 | 46 | 13 | 43,3 |
| Ориентировка | 7 | 14 | 3 | 10 |
Таблица 3. Кардиологическая характеристика пациентов с ОНМК/ТИА в анамнезе основной и контрольной групп на момент включения в исследование
| Показатель | Основная группа (n=50) | Контрольная группа (n=30) | ||
| n | % | n | % | |
| Течение АГ | ||||
| кризовое | 13 | 72,2 | 7 | 70 |
| некризовое | 5 | 27,8 | 3 | 30 |
| средняя частота гипертонических кризов в год | 18,2±4,8 | - | 17,9±4,6 | - |
| Факторы риска сердечно-сосудистых осложнений | ||||
| сахарный диабет | 8 | 44,4 | 4 | 40 |
| гиперлипидемия | 18 | 100 | 10 | 100 |
| Осложнения | ||||
| гипертрофия левого желудочка | 13 | 72,2 | 7 | 70 |
| дилатация левого предсердия | 9 | 50 | 5 | 50 |
| хроническая болезнь почек | 1 | 5,55 | 0 | - |
| хроническая сердечная недостаточность | 2 | 11,1 | 1 | 10 |
| фибрилляция предсердий | 11 | 61,1 | 6 | 60 |
Таблица 4. Когнитивные нарушения по шкале МоСА у пациентов, перенесших ОНМК/ТИА, на момент включения в исследование
| Показатель по разделам МоСА | Основная группа (n=50) | Контрольная группа (n=30) | ||
| n | % | n | % | |
| Оптико-пространственная деятельность | 14 | 77,7 | 8 | 80 |
| Называние предметов | 9 | 50 | 6 | 60 |
| Память | 18 | 100 | 10 | 100 |
| Внимание | 8 | 44,4 | 4 | 40 |
| Речь | 7 | 38,8 | 4 | 40 |
| Абстрактное мышление | 9 | 50 | 5 | 50 |
| Ориентировка | 2 | 11,1 | 1 | 10 |
Средние значения по шкале МоСА составили в данной подгруппе 19,8±2,7 балла. КН по отдельным параметрам МоСА представлены в табл. 4.
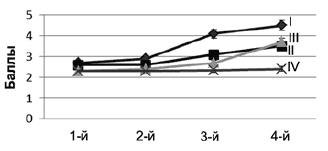
На рис. 1 представлена сравнительная характеристика выраженности КН в основной и контрольной группах, а также у пациентов обеих групп с ОНМК/ТИА в анамнезе. Практически по всем дименсиям КН оценки по шкале MoCA пациентов с ОНМК/ТИА в анамнезе были достоверно ниже (р<0,05) таковых в основной и контрольной группах. Динамика некоторых показателей шкалы MoCA в процессе терапии отражена на рис. 1.
Улучшение по показателю оптико-пространственной деятельности происходило как в основной, так и в контрольной группе, однако при терапии Пантогамом актив положительная динамика была более выражена, а показатели на момент окончания лечения у пациентов, перенесших ОНМК/ТИА в анамнезе, достоверно превышали таковые у больных контрольной группы (p<0,05).
Восстановление когнитивных функций в основной группе происходило достаточно равномерно, с 1-й недели терапии Пантогамом актив, как и в дальнейшем - уже после выписки из стационара. Такая равномерная устойчивая пролонгированная активность в отношении коррекции КН свидетельствует о выраженном положительном эффекте длительного приема Пантогама актив на всех (в том числе постстационарном и реабилитационном) этапах.
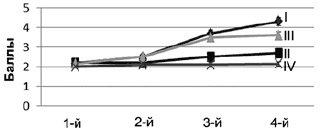
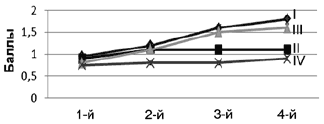
Нарушения внимания и мнестических функций также подверглись редукции, при этом обращает на себя внимание достоверное различие показателей контрольной группы и пациентов с ОНМК/ТИА (р<0,05) к концу терапии (см. рис. 1). На рис.1 представлена также динамика показателей абстрактного мышления в процессе терапии. Несмотря на изначально невысокую клиническую выраженность расстройств, достоверные различия значений на начало и конец исследования отмечены как в основной группе больных АГ, так и у пациентов, перенесших ОНМК/ТИА.
Динамика КН по остальным разделам МоСА (называние, речь, ориентировка) была не столь очевидной, возможно, отчасти и из-за изначальной незначительной выраженности их проявлений. К моменту завершения исследования по шкале когнитивных расстройств МоСА доля пациентов-респондеров по установленным в исследовании критериям составила 78% (39 наблюдений), частичных респондеров - 4% (2). Нонреспондеры составили 18% (9), (рис. 2). Следует отметить, что у нонреспондеров (группа пациентов с ОНМК/ТИА в анамнезе) отмечались наиболее значительные по группе изменения по результатам МРТ.
Тревожные нарушения
Тревожные расстройства, диагностированные у пациентов изученной выборки, в подавляющем числе наблюдений (90%) были представлены нозогенными реакциями (тревожно-фобические и тревожно-диссоциативные по типу «прекрасного равнодушия»). В единичных случаях (по 5% наблюдений) были диагностированы паническое расстройство и генерализованное тревожное расстройство.
Для тревожно-фобических реакций (50% наблюдений) были характерны ипохондрические страхи и опасения по поводу своего здоровья и возможности социальной реабилитации. Пациенты жаловались на ощущение внутреннего напряжения, тревогу за будущее, высказывали опасения инвалидизации или присоединения осложнений. Выявлялись выраженная фиксация на актуальном состоянии сердечно-сосудистой системы (частота и регулярность сердечного ритма, АД), а также разнообразные ипохондрические фобии (кардио-, инсульто-, танатофобия, страх повторения гипертонического криза). Среди соматических (в том числе конверсионных) проявлений тревоги преобладали усиленное сердцебиение или ощущение перебоев в работе сердца, неприятные ощущения или боли в груди кардионевротического характера, колебания АД, предобморочные состояния, приливы жара или холода, потливость, ощущение «кома» в горле или чувство нехватки воздуха, одышка, неравномерность дыхания.
Вторыми по распространенности (40% случаев) среди выявленных тревожных расстройств были тревожно-диссоциативные реакции (по типу «прекрасного равнодушия»). Для данной группы пациентов было характерно демонстративно-пренебрежительное отношение к лечению, прогнозу и исходу заболевания, нарочитое отрицание беспокойства по поводу гипертонии (возникновение подъемов АД связывалось не с каким-либо патологическим процессом, а со случайными, преходящими явлениями: ситуативным стрессом, переутомлением). Однако за фасадом наигранного оптимизма выявлялся страх, связанный с нарушением сердечной деятельности, а также наблюдались массивные проявления соматизированной тревоги (тахикардия, ощущение внутренней дрожи, потливость, нарушения сна по типу ранней инсомнии с тревожными руминациями, неотвязными мыслями о сердечной патологии).
Обращает на себя внимание то, что для перенесших ОНМК/ТИА в анамнезе пациентов были характерны именно тревожно-диссоциативные реакции - 11 (61,1%) пациентов с ОНМК/ТИА в основной группе и 7 (70%) больных в контрольной группе.
Рис. 1. Динамика КН в процессе терапии по отдельным показателям (фрагменты а-г) шкалы МоСА.
а Оптико-пространственная деятельность
 |
б Внимание
 |
в Память
 |
г Абстрактное мышление
 |
 |
|
В единичных наблюдениях тревожные расстройства принимали форму панических атак с витальным страхом и соматовегетативными симптомами (тахикардия, повышение АД, кардиалгии и т.д.) или генерализованного тревожного расстройства. Следует отметить, что данные расстройства, как правило, манифестировали вне связи с АГ и не соотносились с особенностями течения кардиальной патологии. Структура выявленных тревожных нарушений при АГ была следующей: тревожно-фобические реакции - 50%, тревожно-диссоциативные - 40%, паническое расстройство - 5%, генерализованное расстройство - 5%.
Средние значения по шкале самооценки тревоги Шихана в основной группе на момент включения в исследования составили 46,9±11,1 балла, в контрольной - 48±9,1 балла, что соответствует критериям клинически выраженной тревоги.
В основной группе у перенесших ОНМК/ТИА больных средний балл составил 42,3±10,9, в группе контроля у пациентов с ОНМК/ТИА - 42,5±11,1.
Редукция тревожной симптоматики по опроснику самооценки тревоги Шихана в основной группе произошла в 100% наблюдений, при этом доля респондеров составила 88% (44 случая), частичных респондеров - 12% (6) (рис. 3). Динамика тревожных нарушений в процессе терапии приведена на рис. 4.
Сумма баллов по шкале самооценки тревоги Шихана снижалась уже начиная с 1-й недели терапии при каждом последующем визите по сравнению с предыдущим. По мере продолжения терапии отмечалась достоверная редукция как нейровегетативных, соматических (сердцебиение, «ватность» ног, затруднения при вдохе, потливость, боль в области сердца и т.д.), так и психических (озабоченность состоянием здоровья, эпизоды приливов страха) симптомов тревоги (р<0,05).
Редукция тревожной симптоматики происходила при всех выявленных типах тревожных проявлений, однако наиболее выраженная и быстрая динамика отмечалась у пациентов с тревожно-фобическими нозогенными реакциями: купировались ипохондрические фобии, а также нейровегетативные и соматизированные проявления тревоги (тахикардия, эмоциогенные подъемы АД, кардиалгии). У пациентов с тревожно-диссоциативными реакциями также происходила выраженная редукция соматовегетативной тревожной симптоматики. Достоверные различия в выраженности тревожных расстройств получены также у пациентов с ОНМК/ТИА в анамнезе. Следует отметить, что у пациентов с диагностированным паническим расстройством и генерализованным тревожным расстройством также наблюдалось облегчение состояния, но редукция панических атак за время терапии Пантогамом актив не возникала.
Заслуживает внимания то, что в контрольной группе зарегистрировано новое (хотя и незначительное) повышение показателя тревоги после 2-й недели, что может быть связано с выпиской из стационара и страхом возобновления нестабильности АД. В то же время в основной группе и у пациентов с ОНМК/ТИА в анамнезе, принимавших Пантогам актив, наблюдалась положительная и устойчивая динамика редукции тревожных проявлений, возникшая достаточно быстро - в течение 1-й недели терапии, которая сохранялась как на стационарном, так и на постстационарном этапах лечения. Стоит отметить, что пациенты основной группы с изначально высоким уровнем тревоги (более 60 баллов по шкале Шихана) субъективно отмечали существенное снижение тревожных симптомов уже на 2-3-и сутки приема Пантогама актив, что способствовало как стабилизации показателей АД, так и ускорению и упрощению подбора основной - гипотензивной терапии.
Качество жизни
Средние значения по опроснику самооценки качества жизни EQ-5D составили 54,7±14,2 балла в основной группе, 46,1±14,06 балла в подгруппе перенесших ОНМК/ ТИА и 53,5±15,5 балла в контрольной группе.
По шкале EQ-5D доля респондеров в основной группе составила 86% (43 больных), частичных респондеров - 10% (5), нонреспондеров - 4% (2). Динамика показателей шкалы EQ-5D отражена на рис. 5.
У пациентов, принимавших Пантогам актив, имело место достоверное улучшение показателей (р<0,05), что субъективно связывалось больными с редукцией тревожных расстройств и улучшением способности к повседневной деятельности. При этом следует заметить, что если в основной и контрольной группах в целом нарушения были не столь выражены, то достоверные различия (р<0,05) между началом и концом терапии были выявлены у пациентов, перенесших ОНМК/ТИА, в основной группе.
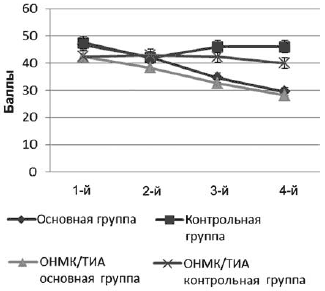
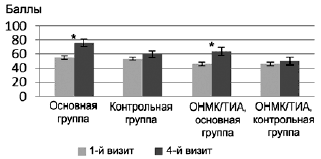
* - достоверные различия на уровне p<0,05.
Было также установлено, что прием Пантогама актив приводит у больных, перенесших ОНМК/ТИА, не только к редукции инсомнии, но и к повышению повседневной активности и энергичности пациентов.
Переносимость и безопасность Пантогама актив
Прием Пантогама актив не оказывал негативного влияния на соматическое состояние пациентов (табл. 5). Кроме того, по некоторым параметрам (АД, ЧСС) отмечены выраженное улучшение и стабилизация показателей соматического статуса. Так, обращает на себя внимание тот факт, что у пациентов с кризовым течением АГ основной группы за все время наблюдения и терапии Пантогамом актив кризы не возникали, в то время как 4 из 13 (30,7%) пациентов с кризовым течением АГ из контрольной группы перенесли по 1 гипертоническому кризу в течение 7-14 дней после выписки из стационара (3-4-й визиты), что потребовало дополнительной коррекции гипотензивной терапии. Таким образом, терапия Пантогамом актив у пациентов с АГ и коморбидными когнитивными и тревожными расстройствами способствовала (вместе с базисной кардиотропной терапией) улучшению динамики кардиоваскулярной патологии.
Нежелательные транзиторные и не требующие отмены препарата явления в виде легкой сонливости после 1-й недели терапии (доза Пантогама актив 600 мг) были отмечены у 2 (4%) пациентов (диагноз - АГ II стадии, без ОНМК/ТИА в анамнезе, изначально выраженные тревожные нарушения - 68 и 72 балла по шкале Шихана). В 2 наблюдениях (диагноз - АГ II стадии, без ОНМК/ ТИА в анамнезе) были зарегистрированы трудности засыпания в течение первых 3 дней терапии (доза Пантогама актив 900 мг).
Обсуждение
В проведенном исследовании была изучена структура когнитивных и тревожных нарушений у пациентов с АГ, находящихся на стационарном лечении. Среди тревожных нарушений преобладали тревожно-фобические реакции (кардио-, инсультофобии, тревожные опасения повторения гипертонических кризов и дестабилизации АД) с массивными проявлениями соматизированной тревоги (сердцебиение, перебои в работе сердца, кардиалгии, ощущение неполноты вдоха, одышка и др.). Кроме того, в 40% наблюдений зарегистрированы тревожно-диссоциативные реакции (по типу «прекрасного равнодушия»). Паническое расстройство и генерализованное тревожное расстройство у пациентов изученной выборки диагностировались лишь в 5% наблюдений каждое.
Применение Пантогама актив приводило к достоверной редукции тревожных проявлений после 1-й недели терапии в 100% наблюдений, при этом субъективное улучшение самочувствия пациенты отмечали уже после 2-3 дней его приема. Доля респондеров при терапии Пантогамом актив составила 88%, частичных респондеров - 12% (подгруппа пациентов с ОНМК/ТИА в анамнезе).
Среди КН, по данным психометрии, преобладали легкие и умеренные формы. Особенно были выражены мнестические расстройства, диагностированные в 100% наблюдений. Кроме того, отмечены также нарушения функций оптико-пространственной деятельности, внимания и абстрактного мышления. Наиболее выраженные КН выявлены у пациентов, перенесших ОНМК/ТИА в анамнезе. На фоне приема Пантогама актив происходило улучшение по всем показателям шкалы МоСА. К моменту завершения исследования по шкале когнитивных расстройств МоСА доля респондеров по установленным в исследовании критериям составила 78%. Обращает на себя внимание также быстрая (в течение 1-й недели) достоверная редукция симптомов КН у пациентов с ОНМК/ ТИА в анамнезе по сравнению с контрольной группой.
Таблица 5. Динамика соматических показателей в процессе терапии Пантогамом актив
| Показатель | Основная группа | Контрольная группа | ||
| 1-й день | 28-й день | 1-й день | 28-й день | |
| Масса тела, кг | 87,8±10,5 | 86,1±8,8 | 88,6±11,1 | 87,6±9,6 |
| ЧСС, уд./мин | 89,5±10,1 | 82,1±6,7 | 88,6±9,7 | 85,3±7,1 |
| АД, мм рт.ст. | 177,8±8,6/96,5±5,5 | 135,2±4,3/85,1±3,8 | 179,1±7,8/96,8±6,3 | 154,1±5,2/90,1±3,3 |
| ЭКГ, n (%), пациенты с депрессией ST | 23(46) | 8(16) | 15(50) | 5(16,6) |
| АСТ, Ед/л | 57,3±12,1 | 38,5±3,9 | 55,1±4,3 | 37,5±3,4 |
| АЛТ, Ед/л | 44,6±5,4 | 35,1±2,3 | 43,6±5,1 | 33,6±3,2 |
| Общий билирубин, мкмоль/л | 17,5±3,4 | 13,6±4,7 | 17,1±3,6 | 13,1±3,8 |
Показатели качества жизни пациентов (уход за собой, повседневная деятельность, тревога/депрессия) на фоне приема Пантогама актив также достоверно улучшались на протяжении всего лечения, начиная с 1-й недели терапии. Особенно выраженное улучшение происходило у пациентов с ОНМК/ТИА в анамнезе. По шкале самооценки качества жизни EQ-5D доля респондеров составила 86%.
Было установлено, что Пантогам актив обладает хорошим профилем переносимости и безопасности у пациентов с АГ как среднего, так и пожилого возраста (старше 65 лет), что находило свое отражение в высокой приверженности больных к терапии на протяжении всего периода наблюдения. Об этом свидетельствует и желание больных продолжать лечения: его выразили 46 (92%) пациентов.
Ни один пациент не выбыл из исследования. Нежелательные явления в виде легкой сонливости или трудности засыпания отмечались чрезвычайно редко (4% наблюдений), возникали, как правило, на 1-й неделе терапии и самостоятельно редуцировались через 3-4 дня без необходимости отмены препарата или снижения дозы. Прием Пантогама актив не приводил к ухудшению соматических показателей (по данным ЭКГ, биохимического анализа крови, суточного мониторирования АД). Кроме того, на фоне его приема наблюдалась стабилизация показателей АД, что облегчало процесс подбора гипотензивной терапии и в некоторых случаях способствовало назначению меньшего числа препаратов. Важным моментом было отсутствие подъемов АД после выписки из стационара у пациентов, принимавших Пантогам актив, в то время как у 30% больных, получавших стандартную гипотензивную терапию, в течение 2 нед после выписки подъем АД отмечался хотя бы один раз.
Полученные результаты свидетельствуют об эффективности и хорошей переносимости Пантогама актив при когнитивных и тревожных расстройствах, наблюдаемых в кардиологической практике (у пациентов с АГ). Данные проведенного исследования подтверждают возможность использования Пантогама актив в качестве препарата с бимодальной ноотранквилизирующей активностью для лечения когнитивных и тревожных нарушений. В процессе терапии Пантогамом актив происходит быстрая (в течение 1-й недели терапии) и достоверная редукция тревожных и когнитивных проявлений. Следует отметить и протективный эффект Пантогама актив в отношении предотвращения прогрессирования КН у пациентов, перенесших ОНМК/ТИА в анамнезе.
Таким образом, терапия Пантогамом актив у пациентов с АГ и коморбидными когнитивными и тревожными расстройствами способствует (вместе с базисной кардио-тропной терапией) улучшению динамических показателей кардиоваскулярной патологии.
Конфликт интересов отсутствует.
1Синдром умеренных КН подразделяется на два основных подтипа - мнестические (нарушения памяти) и немнестические нарушения (трудности концентрации внимания, быстрая утомляемость при умственной нагрузке, нарушения абстрактного мышления). Когнитивное снижение при данном синдроме не приводит к дезадаптации, но существенно влияет на качество жизни пациента и представляет собой промежуточную ступень между нормальной возрастной динамикой когнитивных функций и болезнью Альцгеймера [11 - 13].
2Синдром сердечно-сосудистых заболеваний с неблагоприятным, конгруэнтным невропатической акцентуации течением - невозможность добиться целевых показателей АД связана с психогенной провокацией подъемов АД, а также амплификацией гипертонических кризов симптомами тревожных пароксизмов. Прогрессирование симптомов АГ у больных этой группы связано, прежде всего, с низкой приверженностью к терапии: неадекватная титрация доз чаще в сторону их уменьшения до субтерапевтических, частая смена или отказ от лечения вследствие возникновения «непереносимых» (отеки, крапивница, сухой кашель и др.) побочных эффектов.
3Полученные результаты соотносятся с эпидемиологическими данными. Так, согласно современным исследованиям, ишемический и геморрагический инсульты находятся в соотношении 5:1 [41].
Литература
- Kessler RS, Wittchen HU. Patterns And Correlates Of Generalized Anxiety Disorder In Community Samples. J Clin Psychiatry. 2002;63(8):4-10.
- Kapfhammer HP. The Relationship Between Depression, Anxiety And Heart Disease - A Psychosomatic Challenge. Psychiatr Danub. 2011;23(4):412-424.
- Краснов В.Н., Довженко Т.В., Бобров А.Е. Тревожно-депрессивные расстройства у пациентов первичной медицинской сети. Медицинский вестник. 2010;11(516).
- Андрющенко А.В. Психические и психосоматические расстройства в учреждениях общесоматической сети (клинико-эпидемиологические аспекты, психосоматические соотношения, терапия): Автореф. дис. ... д-ра мед. наук. М. 2011. Доступно по: psychiatry.ru cond/0/diss/2011/186 Ссылка активна на 22.09.15.
- Petersen R, Smith G, Waring S, Ivnik R, Tangalos E, Kokmen E. Mild Cognitive Impairment. Arch Neurol. 1999;56(3):303. doi: 10.1001/archneur.56.3.303.
- Kearney-Schwartz A, Rossignol P, Bracard S, et al. Vascular Structure and Function Is Correlated to Cognitive Performance and White Matter Hyper-intensities in Older Hypertensive Patients With Subjective Memory Complaints. Stroke. 2009;40(4):1229-1236. doi: 10.1161/strokeaha. 108.532853.
- Еремина О.В. Когнитивные нарушения у больных артериальной гипертонией (частота, диагностика, лечение): Автореф. дис. ... канд. мед. наук. Иркутск; 2007. Доступно по: dissercat.com/content kognitivnye-narusheniya-u-bolnykh-arterialnoi-gipertoniei-chastota-diagnostika-lechenie. Ссылка активна на 22.09.15.
- Heart.org. www.heart.org. 2015. Available at: heart.org. Accessed 22.09.2015.
- Reitz C, Tang M, Manly J, Mayeux R, Luchsinger J. Hypertension and the Risk of Mild Cognitive Impairment. Arch Neurol. 2007;64(12):1734. doi: 10.1001/archneur.64.12.1734.
- Sierra C, Domenech M, Camafort M, Coca A. Hypertension and Mild Cognitive Impairment. Curr Hypertens Rep. 2012;14(6):548-555. doi:10.1007/s11906-012-0315-2.
- Grundman M. Mild Cognitive Impairment Can Be Distinguished from Alzheimer's Disease and Normal Aging for Clinical Trials. Arch Neurol. 2004;61(1):59. doi: 10.1001/archneur.61.1.59.
- Obisesan T. Hypertension and Cognitive Function. Clinics in Geriatric Medicine. 2009;25(2):259-288. doi: 10.1016/j.cger.2009.03.002.
- Остроумова О.А. Когнитивные нарушения при артериальной гипертонии и возможности их коррекции. Врач. 2011;14:7-12.
- Reitz C, Tang M, Miller J, Green R, Luchsinger J. Plasma Homocysteine and Risk of Mild Cognitive Impairment. Dementia and Geriatric Cognitive Disorders. 2009;27(1):11-17. doi:10.1159/000182421.
- Морозова Т.Е., Рыкова С.М. Сердечно-сосудистые заболевания и когнитивные нарушения. Consilium Medicum. 2010;9:85-89.
- Fisher C. Lacunar strokes and infarcts: A review. Neurology. 1982;32(8):871. doi:10.1212/wnl.32.8.871.
- Bracco L, Campani D, Baratti E et al. Relation between MRI features and dementia in cerebrovascular disease patients with leukoaraiosis: A longitudinal study. Journal of the Neurological Sciences. 1993;120(2):131-136. doi: 10.1016/0022-510x(93)90263-x.
- Mancia G, Laurent S, Agabiti-Rosei E et al. Reappraisal of European guidelines on hypertension management: a European Society of Hypertension Task Force document. Journal of Hypertension. 2009;27( 11):2121-2158. doi: 10.1097/hjh.0b013e328333146d.
- Повереннова И.Е., Севастьянова Е.В. Особенности когнитивных нарушений при артериальной гипертензии. Саратовский научно-медицинский журнал. 2008;4(1):89-92.
- Madureira S, Guerreiro M, Ferro J. Dementia and cognitive impairment three months after stroke. Eur J Neurol. 2001;8(6):621-627. doi:10.1046/j.1468-1331.2001.00332.x.
- Tham W, Auchus AP, Thong M et al. Progression of cognitive impairment after stroke: one year results from a longitudinal study of Singaporean stroke patients. J Neurol Sci. 2002; 203(4):49-52.
- Путилина М.В. Нейропротекторная терапия хронической ишемии мозга. Врач. 2008; 8:27-29.
- Левин О.С., Усольцева Н.И., Юнищенко Н.А Постинсультные когнитивные нарушения. Трудный пациент. 2007;8:26-29.
- Левин О.С. Диагностика и лечение деменции в клинической практике. М.: Медпресс-информ; 2009.
- Player M, Peterson L. Anxiety Disorders, Hypertension, and Cardiovascular Risk: A Review. The International Journal of Psychiatry in Medicine. 2011;41(4):365-377. doi:10.2190/pm.41.4.f.
- Kubzansky LD, Kawachi I. Going to the heart of the matter: do negative emotions cause coronary heart disease? J Psychosomatic Research. 2000;48:323-337. doi:10.1016/S0022-3999(99)00091-4.
- Johansen A, Holmen J, Stewart R, Bjerkeset O. Anxiety and depression symptoms in arterial hypertension: the influence of antihypertensive treatment. The HUNT study, Norway. Eur J Epidemiol. 2011;27(1):63-72. doi: 10.1007/s10654-011-9641-y.
- Штарик С.Ю., Петрова М.М., Гарганеева Н.П. Некоторые аспекты коморбидности тревожно-депрессивных расстройств и артериальной гипертензии. Сибирский медицинский журнал. 2009;24(4):46-48.
- Волель Б.А., Терновая Е.С., Ермушева А.А., Сыркина Е.А., Ардзинба И.Б. Расстройство личности и сердечно-сосудистые заболевания (на модели артериальной гипертонии и ишемической болезни сердца). Психические расстройства в общей медицине. 2014;1:4-13.
- Hocaoglu C, Yeloglu CH, Polat S. Cardiac Diseases and Anxiety Disorders. INTECH Open Access Publisher; 2011.
- Kong D, Gao H, Lu Y et al. Anxiety disorders are associated with increased plasma adrenomedullin level and left ventricular hypertrophy in patients with hypertension. Clinical and Experimental Hypertension. 2013;36(1):27-31. doi:10.3109/10641963.2013.783049.
- Todaro J, Shen B, Raffa S, Tilkemeier P, Niaura R. Prevalence of anxiety disorders in men and women with established coronary heart disease. Journal of Cardiopulmonary Rehabilitation and Prevention. 2007;27(2):86-91. doi:10.1097/01.hcr.0000265036.24157.e7.
- Vogelzangs N, Seldenrijk A, Beekman A, van Hout H, de Jonge P, Penninx B. Cardiovascular disease in persons with depressive and anxiety disorders. Journal of Affective Disorders. 2010;125(1-3):241-248. doi: 10.1016/j.jad.2010.02.112.
- von Wachter M, Junger S, Renz D, Wollthan S, Sim H, Hendrischke A, Hoff B, Schondube F, Kroger F, Petzold ER. Psychosocial stress and utilization of medical services after coronary bypass operation. Gesundheitswesen. 2000;62(8/9):451-456. doi: 10.1055/s-2000-12614.
- O'Brien J. Cerebrovascular Disease, Cognitive Impairment, and Dementia. London: Martin Dunitz; 2004.
- Bacon S, Campbell T, Arsenault A, Lavoie K. The Impact of Mood and Anxiety Disorders on Incident Hypertension at One Year. International Journal of Hypertension. 2014;2014:1-7. doi: 10.1155/2014/953094.
- Никольская И.Н., Гусева И.А., Близнецов Е.В., Третьякова Т.В. Роль тревожных расстройств при гипертонической болезни и возможности их коррекции. Лечащий врач. 2007;3:89-91.
- Федотова А.В., Миронова О.П., Карпов Ф.А., Федин А.И. Комплексная коррекция артериальной гипертензии и когнитивных нарушений у больных с гипертонической энцефалопатией. Результаты многоцентрового исследования «ЛЕГЕНДА». Атмосфера. Нервные болезни. 2009;4:1-5.
- Захаров В.В., Вахнина Н.В. Инсульт и когнитивные нарушения. Неврология, нейропсихиатрия, психосоматика. 2011;2:8-14.
- Дума С.Н. Оценка клинической эффективности нейропротекторов, влияющих на систему гамма-аминомасляной кислоты, при лечении когнитивных расстройств у пациентов с дисциркуляторной энцефалопатией I-II стадий. Фарматека. 2010;15:96-100.
- Andersen K, Olsen T, Dehlendorff C, Kammersgaard L. Hemorrhagic and ischemic strokes compared: stroke severity, mortality, and risk factors. Stroke. 2009;40(6):2068-2072. doi:10.1161/strokeaha.108.540112.
Комментарии
ПРАКТИКА ПЕДИАТРА

