Уважаемый посетитель!
Эта информация для специалистов здравоохранения
Нажимая «ПРОДОЛЖИТЬ», Вы подтверждаете, что им являетесь
 pikfarma.ru
pikfarma.ru
• Оригинальный ноотропный препарат с противотревожным действием
• Активирует умственную деятельность, улучшает эмоциональное состояние
Аугментация антипсихотической терапии при шизофрении D-, L-гопантеновой кислотой
Статьи Опубликовано в журнале:
« ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ » 8, 2015г. В.Э. Медведев 1, В.И. Фролова 1 , Е.В. Гушанская 1,2 , А.Ю. Тер-Исраелян 1,2
1 Кафедра психиатрии, психотерапии и психосоматической патологии медицинского института Российского университета дружбы народов, Москва;
2Психиатрическая больница №13, Москва
Цель исследования — изучение эффективности D-, L-гопантеновой кислоты (препарат пантогам актив) при лечении больных шизофренией типичными нейролептиками с оценкой скорости наступления клинического ответа и переносимости.
Материал и методы. Обследовали 70 больных шизофренией, которые составили основную (35 человек) и контрольную группы (35 человек). Все пациенты находились на монотерапии одним из типичных антипсихотиков (галоперидол, зуклопентиксол, промазин, перфеназин). Основной группе больных был дополнительно назначен пантогам актив, доза которого колебалась в диапазоне 1200—1800 мг/сут и к концу исследования достигала максимально допустимой (1800 мг в сутки) у 62,9% пациентов.
Результаты и заключение. Было установлено, что включение D-, L-гопантеновой кислоты (препарат пантогам актив) в комплексную терапию шизофрении позволяет в более ранние сроки (на 8-й неделе против 16-й в группе контроля) достичь улучшения состояния, а также значимо уменьшить частоту возникновения и выраженность обусловленных антипсихотической терапией вторичных негативных расстройств. Повышение эффективности комбинированной терапии и ее хорошая переносимость улучшают качество жизни больных, сохраняют их приверженность терапии, что способствует снижению экономических затрат на оказание им помощи.
Ключевые слова: шизофрения, нейролептики, D-, L-гопантеновая кислота, РАЦ-гопантеновая кислота, пантогам актив.
Augmented antipsychotic therapy with pantogam active in patients with schizophrenia
V.E. MEDVEDEV, V.I. FROLOVA, E.V. GUSHANSKAYA, A.U. TER-ISRAELYAN
Medical University, People’s Friendship University of Russia, Moscow; Psychiatric Hospital №13, Moscow
Objective — to study the efficacy of the GABA-ergic drug pantogam active (D-, L-gopantenic acid) in patients with schizophrenia treated with typical neuroleptics and to assess the rate of treatment response and tolerability of the drug.
Material and methods. A sample consisted of 70 patients with schizophrenia stratified into main (n=35) and control (n=35) groups. All patients received one of typical antipsychotics (haloperidol, zuclopenthixol, promazine or perphenazine). Patients of the main group received in addition pantogam active in dose of 1200—1800 mg daily. The maximum allowed dose of 1800 mg daily was used in 62.9% of the patients.
Results and conclusion: The long-term combined therapy with the addition of D-, L-gopantenic acid (pantogam activ) allowed to achieve clinical improvement earlier (on 8th week in the main group versus 16th week in the control group). The frequency and severity of secondary negative symptoms associated with antipsychotic therapy were decreased as well. The high efficacy and tolerability of the combined therapy allow to improve quality of life in patients with schizophrenia and their compliance to treatment as well as to reduce costs of medical care.
Keywords: schizophrenia, antipsychotics, pantogam active.
Высокая распространенность шизофрении и тяжесть ее последствий, включая медицинские, социальные и экономические [1—3], определяют необходимость про¬должения поиска эффективных методов лечения этого заболевания.
Более 60 лет для лечения шизофрении используют антипсихотические препараты (нейролептики) [4—7], эффективность которых в отношении купирования и профилактики экзацербаций психических расстройств подтверждена современными методами доказательной медицины [8—11]. В то же время терапевтические воз¬можности существующих антипсихотических средств ограничены. Результаты масштабных исследований по¬следних лет [12—14] дают основание поставить под со¬мнение превосходство современных атипичных нейролептиков над традиционными препаратами. Более того, некоторые исследователи [15, 16] стали высказывать мне¬ние, что даже при проведении длительной поддерживающей терапии предпочтение должно отдаваться типичным нейролептикам. В связи с накоплением данных о недостаточной эффективности типичных нейролептиков при шизофрении, протекающей с преобладанием негативных, когнитивных расстройств, высокой частоте развития не¬врологических нежелательных явлений, в последние годы в качестве аугметирующих средств наиболее активно ис¬пользуются ноотропные и нейропротекторные препараты.
Сказанное выше определяет актуальность исследований, направленных на оценку возможностей адъювантной терапии в повышении качества поддерживающего лечения шизофрении антипсихотическими препаратами первого поколения [17, 18]. В этом отношении привлекают к себе внимание ГАМК-ергический препарат пантогам актив в аспектах изучения при его применении скорости наступления клинического ответа и его переносимости в дозах до 1800 мг в сутки при лечении больных шизофренией типичными нейролептиками [19—21].
Действующее вещество пантогама актив — D-, L-гопантеновая кислота (рац-гопантеновая кислота — смесь равных количеств D- и L-изомеров гопантеновой кислоты). D-изомер гопантеновой кислоты, взаимодействуя с ГАМК А- и В-рецепторами головного мозга, оказывает на ЦНС ГАМК-ергическое действие. L-изомер гопантеновой кислоты связывается с D2-дофаминовыми рецепторами (этого не отмечено по отношению к D-гопантеновой кислоте). L-изомер придает пантогаму актив свойства, отличающие его от препаратов D-гопантеновой кислоты, а именно — противотревожное и легкое антидепрессивное действия [22].
Цель настоящего исследования — изучение терапевтической эффективности и переносимости адъювантного препарата пантогам актив в дозе до 1800 мг в сутки при длительном лечении больных шизофренией.
Материал и методы
Исследование было натуралистическим сравнительным. Оно было проведено в 2014—2015 гг. на базе кафедры психиатрии, психотерапии и психосоматической патологии факультета повышения квалификации медицинских работников Медицинского института Российского университета дружбы народов.
В исследование включались пациенты обоего пола в возрасте старше 18 лет, обратившиеся за консультацией или госпитализированные в психиатрическую больницу №13 Москвы или ее филиалы, являющиеся клинической базой указанного университета.
Больные не получали антипсихотическую терапию на протяжении предшествующих 6 мес и находились в лекарственной ремиссии. Все они дали информированное согласие на участие в исследовании. С целью снижения вероятности наличия латентной или манифестирующей сопутствующей соматической, неврологической и эндокринологической патологии предельный возраст пациентов был ограничен 45 годами.
Психиатрический диагноз больных, установленный не менее 5 лет назад, соответствовал диагностическим критериям МКБ-10 для шизофрении (F20) и шизотипического расстройства (F21.3—F21.5) с преобладанием негативных расстройств. Критериями включения больных в исследование являлись также результаты скрининговой оценки по психометрическим шкалам: не менее 50 баллов по шкале оценки негативных симптомов BPRS, не более 15 баллов по подшкале позитивных и не менее 21 балла по подшкале негативных расстройств шкалы PANSS, не менее 4 баллов по шкале CGI.
Монотерапия типичными антипсихотиками проводилась у пациентов не менее 4 мес без изменения препарата или его дозы.
Не включались в исследование пациенты с явлениями индивидуальной непереносимости гопантеновой кислоты в анамнезе, страдающие иными, не указанными в изложенных выше критериях включения, психопатологическими расстройствами и заболеваниями, зависимые от психоактивных веществ, а также беременные женщины и в периоде лактации. Не включались в исследование больные с органическим поражением ЦНС (эпилепсия, деменция, новообразования, рассеянный склероз), пролактинзависимыми опухолями гипофиза и молочной железы, феохромоцитомой и другой тяжелой декомпенсированной соматической патологией.
Из включенных в исследование 70 пациентов были сформированы 2 группы — основная и контрольная — по 35 больных (табл. 1). Основную группу составили 21 мужчина и 14 женщин (средний возраст — 31,6±4,9 года), работают 17,1%, временно не работают — 5,7%, инвалиды по психическому заболеванию — 77,2%. Средняя длительность заболевания с момента первого обращения — 9,5±4,2 года, среднее число госпитализаций за время болезни — 5,9±2,2.
Таблица 1.
Психофармакотерапия в исследуемых группах
| Показатель | Галоперидол | Зуклопентиксол | Промазин | Перфеназин |
|---|---|---|---|---|
| Основная группа | ||||
| число пациентов, n (%) | 16 (45,7) | 7 (20,0) | 7 (20,0) | 5 (14,3) |
| диапазон доз, мг в сутки | 2,5—10 | 2—25 | 12,5—50 | 4—16 |
| средняя доза, мг в сутки | 4,8 | 7,5 | 25,0 | 8,9 |
| число пациентов, снижавших дозу из-за нежелательных явлений (НЯ), n (%) | 7 (20) | 0 | 0 | 0 |
| число пациентов, преждевременно выбывших из исследования | 0 | 0 | 0 | 0 |
| Контрольная группа | ||||
| число пациентов, n (%) | 19 (54,3) | 6 (17,1) | 7 (20) | 3 (8,6) |
| диапазон доз, мг в сутки | 2,5—10 | 2—25 | 12,5—50 | 4—16 |
| средняя доза, мг в сутки | 4,8 | 7,3 | 27,5 | 8,0 |
| число пациентов, снижавших дозу из-за НЯ, n (%) | 14 (40,0) | 0 | 0 | 0 |
| число пациентов, преждевременно выбывших из исследования | 7 (20,0) | 0 | 0 | 0 |
В контрольной группе было 19 мужчин и 16 женщин (средний возраст — 33,2±3,7 года), работают 22,9%, временно не работают 2,9%, инвалиды по психическому заболеванию — 74,2%, средняя длительность заболевания — 9,1±3,8 года, среднее число госпитализаций за время болезни — 6,3±1,6.
Сходные социодемографические (пол, средний возраст) и клинико-динамические (длительность заболевания, число госпитализаций) характеристики пациентов обеих групп позволяют рассчитывать на валидность полученных результатов. В основной группе пантогам актив (в максимальной дозе 1800 мг в сутки) назначался в комплексе с одним из типичных антипсихотиков (см. табл. 1). Доза титровалась постепенно с учетом индивидуальной чувствительности и переносимости.
В группе контроля монотерапия шизофрении осуществлялась типичными антипсихотиками без назначения пантогама актив. При возникновении экстрапирамидных расстройств предусматривалось дополнительное, не более чем 7-дневное назначение корректора (бипериден до 6 мг в сутки). При сохранении экстрапирамидных расстройств предполагалось снижение дозы антипсихотика до индивидуально переносимой вплоть до смены антипсихотической терапии и исключения больного из исследования.
Эффективность терапии оценивалась при плановых визитах: Н (неделя) 0, Н2, Н4, Н8, H12, H16, H20, H24. Инструментами сравнения и основными критериями эффективности препарата в отношении психопатологических расстройств, наряду с клинической оценкой, являлась редукция симптоматики по сравнению с исходными балльными оценками по шкалам PANSS, CGI, BPRS. Для определения динамики когнитивных нарушений использовались тест беглости речевых ответов, тест Струпа. Для оценки влияния препарата на динамику вторичных негативных расстройств применялись шкалы HDRS-21 (для выявления нейролептической депрессии), ESRS (для выявления нейролептической заторможенности и паркинсонизма).
Оценка качества жизни больных проводилась по общей шкале функционирования (GAF) и опроснику SF-36.
Безопасность и переносимость терапии оценивались на основании спонтанных жалоб больных, шкалы побочных эффектов (UKU) и данных клинических и параклинических соматических исследований, включавших регистрацию ЧСС, систолического и диастолического АД в положении сидя, ортостатическую пробу, клинический и биохимический анализы крови, ЭКГ в покое.
Дополнительно результаты исследования оценивались с точки зрения возможного влияния на фармакоэкономические аспекты терапии. В ходе наблюдения фиксировались такие показатели, как длительность пребывания в стационаре, частота регоспитализаций 1, число случаев отмены или смены терапии (выбывание из исследования), назначения корректоров.
Полученный материал обрабатывался с помощью программы Statistica («StatSoft Inc.», США). Достоверность различий рассчитывалась при помощи теста Колмогорова—Смирнова. 1Регоспитализация не являлась критерием исключения из исследования, если происходила по социальным показаниям и не сопровождалась изменением терапии.
Результаты и обсуждение
Доза пантогама актив в основной группе колебалась в диапазоне 1200—1800 мг в сутки и к концу исследования достигала максимально допустимой 1800 мг в сутки у 22 (62,9%) пациентов.
Согласно шкале CGI, статистически достоверное (рЧисло больных в тяжелом состоянии в основной группе к окончанию исследования снизилось достоверно более значимо, чем в контрольной группе (на 93,8% против 58,1%, рСогласно шкале CGI, в динамике самого начала терапии в основной и контрольной группах отмечались разнонаправленные тенденции: в основной группе у больных уже с первых недель регистрировалось «небольшое улучшение», в то время как в контрольной группе, напротив, первые 4—8 нед у части больных (n=11 на Н4 и n=3 на Н8) отмечалось «небольшое ухудшение» состояния, по всей видимости, обусловленное нарастанием выраженности НЯ антипсихотической терапии.
Общая редукция балльной оценки по шкале PANSS в основной группе была статистически более значима, чем в контрольной группе (на 25% против 6%, р Таблица 2.
Динамика состояния пациентов по шкале PANSS на разных этапах исследования
| Показатель, баллы | Средний балл | Достоверность на последнем визите (H24) | |||
|---|---|---|---|---|---|
| основная группа | контрольная группа | ||||
| Н0 | Н24 | Н0 | Н24 | ||
| Подшкала продуктивной симптоматики | 14,6 | 11,0 | 14,5 | 12,4 | |
| Подшкала негативной симптоматики | 35,0 | 26,0 | 32,5 | 32,5 | |
| Подшкала общей психопатологической симптоматики | 47,7 | 36,0 | 47,8 | 44,2 | |
| Общий | 97,3 | 73,0 | 94,8 | 89,1 | |
Наибольшая положительная динамика, достоверно превосходящая таковую в контрольной группе, наблюдалась в основной группе по подшкале негативных расстройств (на 25,7% против 0, р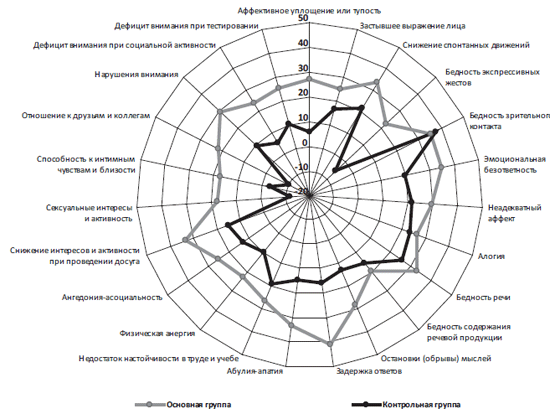
Рис. 1. Влияние комплексной терапии, включающей пантогам актив,
на эффективность редуцирования (%) психопатологических расстройств по шкале BPRS.
В контрольной группе снижение общего балла по рассматриваемой шкале достигало достоверных значений только к 20-й неделе терапии. К моменту окончания исследования достоверно значительнее, чем в основной группе, уменьшалась только оценка «ослабления контроля импульсивности (агрессивность)».
При сравнении данных обследования пациентов обеих групп обратила на себя внимание разнонаправленность динамики таких психопатологических симптомов/синдромов, как эмоциональная отгороженность, малоконтактность, нарушение внимания, стереотипность и нарушение абстрактного мышления, соматическая озабоченность, чувство вины, напряженность, депрессия, моторная заторможенность, уменьшающиеся к концу исследования в основной группе, и, напротив, увеличивающиеся в контрольной. Последнее можно объяснить как динамикой эндогенного заболевания, так и развитием более выраженных НЯ антипсихотической терапии. Последнее предположение подтверждается психометрической оценкой переносимости терапии.
Аналогичные данные получены при анализе результатов оценки состояния пациентов по шкале BPRS (рис. 1). В большинстве случаев фиксируются статистически достоверные различия между основной и контрольной группами, указывающие на преимущество комбинированной терапии.
Динамика когнитивных функций у пациентов обеих групп свидетельствует о более выраженном положительном эффекте терапии с применением пантогама актив (табл. 3). Монотерапия типичными антипсихотиками на уровне тенденции ухудшала когнитивные функции.
Таблица 3.
Динамика состояния когнитивных функций пациентов на фоне разных схем терапии
| Тест | Основная группа | Контрольная группа | ||
|---|---|---|---|---|
| визиты | ||||
| Н0 | Н24 | Н0 | Н24 | |
| Беглость речевых ответов | ||||
| правильные слова (категорийная часть), число | 11 | 15 | 9 | 10 |
| правильные слова (буквенная часть), число | 7 | 9 | 7 | 7 |
| повторяющиеся слова (категорийная часть), число | 3 | 4 | 3 | 4 |
| повторяющиеся слова (буквенная часть), число | 2 | 1 | 1 | 2 |
| искажения (категорийная часть), число | 3 | 1 | 4 | 1 |
| искажения (буквенная часть), число | 2 | 2 | 2 | 2 |
| Тест Струпа | ||||
| время выполнения 1-й части, с | 82 | 73 | 85 | 91 |
| время выполнения 2-й части, с | 98 | 82 | 101 | 103 |
| число ошибок | 9 | 5 | 8 | 9 |
Таким образом, добавление пантогама актив к антипсихотической терапии не только потенцирует терапевтическое влияние нейролептиков на проявления продуктивных, первичных негативных и общих психопатологических синдромов, но и позволяет предупредить и/или уменьшить частоту возникновения и выраженность симптомов вторичных негативных расстройств (нейролептическая депрессия, когнитивные нарушения) (рис. 2).
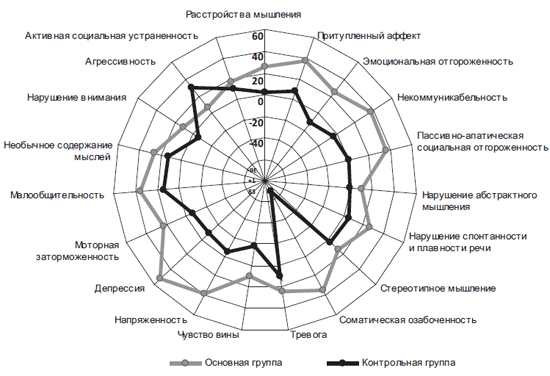
Рис. 2. Влияние комплексной терапии, включающей пантогам актив, на эффективность редуцирования (%) психопатологических расстройств по PANSS.
Представлены пункты шкалы с достоверной разницей между группами.
Важным свидетельством положительного влияния пантогама актив на переносимость нейролептической терапии является тот факт, что в основной группе все пациенты полностью завершили исследование, а в контрольной — 7 (20%) больных выбыли из исследования в связи с развитием субъективно непереносимых НЯ (паркинсонизм, дискинезия, чрезмерная седация).
Кроме того, число пациентов, которым в ходе исследования была снижена доза нейролептика, в основной группе составило 7 (20%), в контрольной группе — в 2 раза больше — 14 (40%). В основной группе больных на разных этапах терапии дополнительное краткосрочное назначение холинолитического корректора бипиридена потребовалось 10 (28,6%) пациентам, в контрольной — 21 (60%).
В ходе исследования получены также достоверные данные о способности пантогама актив купировать/предупреждать развитие и нивелировать симптомы нейролептической депрессии: средний балл по шкале HDRS в основной группе достоверно уменьшился, начиная с 8-й недели терапии, на 44,3% к моменту завершающей оценки, против увеличения на 6,5% в контрольной группе (рВключение пантогама актив в схему терапии шизофрении типичными нейролептиками позволяет достоверно снизить и выраженность развивающихся экстрапирамидных расстройств: по шкале ESRS c 0,8 до 0,3 балла в основной группе против увеличения с 0,9 до 1,1 балла в контрольной (pСпектр НЯ в обеих группах группах оказался сходным (рис. 3), но выраженность их в основной группе на всем протяжении исследования и на момент его окончания была достоверно меньшей.
Соматическое состояние и основные гемодинамические показатели пациентов были стабильными (табл. 4), однако к концу лечения в основной группе наметилась тенденция к меньшему влиянию терапии в основной группе на индекс массы тела (ИМТ), уровень глюкозы и печеночных трансаминаз.
Оценка качества повседневного функционирования больного со стороны врача (шкала GAF) и самооценка качества жизни пациента (опросник SF-36, рис. 4) достоверно свидетельствуют о превосходстве комбинированной терапии типичными антипсихотиками с пантогамом актив над монотерапией нейролептиками на момент завершения исследования. Так, повседневное функционирование пациентов в основной группе улучшилось на 60,5% от исходного против 40,7% в контрольной группе (р 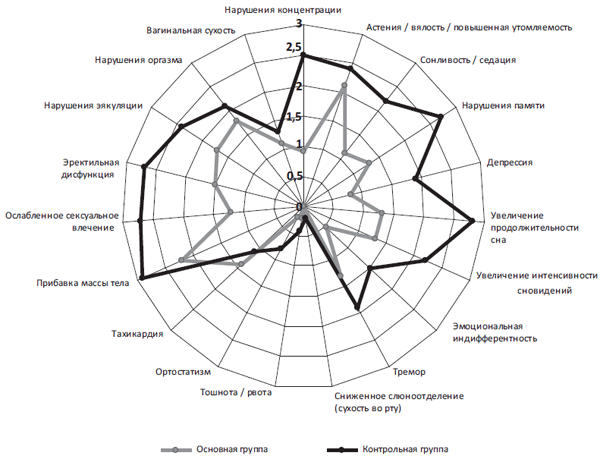
Рис. 3. Спектр и выраженность основных НЯ на момент окончания исследования по шкале UKU (средний балл).
Таблица 4.
Динамика соматического состояния больных
| Показатель | Основная группа | Контрольная группа | Достоверность на последнем визите (H24) | ||||
|---|---|---|---|---|---|---|---|
| Н0 | Н24 | динамика показателя, % | Н0 | Н24 | динамика показателя, % | ||
| ИМТ | 24,3 | 26,9 | 10,7 | 24,1 | 28,6 | 18,7 | |
| АД, мм рт.ст. | 126,5/74,6 | 127,1/76,7 | 0,5/2,8 | 125,9/72,4 | 126,2/77,1 | 0,2/6,5 | Н.д. |
| Глюкоза в крови, моль/л | 4,9 | 5,4 | 10,2 | 4,9 | 6,1 | 24,5 | |
| АЛТ, ед. | 34,8 | 37,9 | 8,9 | 32,9 | 39,1 | 18,8 | |
| АСТ, ед. | 18,9 | 22,6 | 19,6 | 19,8 | 23,2 | 17,2 | Н.д. |
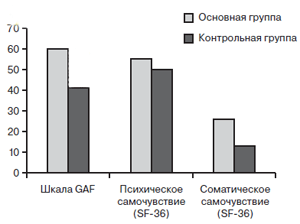
Рис. 4. Динамика качества жизни и повседневного функционирования пациентов к моменту завершения исследования (достоверность различий между группами была отмечена на Н24 при p
Cогласно полученным данным, прием пантогама актив достоверно уменьшает значение каждого из включенных в фармакоэкономический анализ показателей на фоне базовой терапии нейролептиком (табл. 5).
Таблица 5.
Сравнение показателей фармакоэкономической эффективности терапии пациентов в группах
| Показатель | Основная группа | Контрольная группа | р |
|---|---|---|---|
| Длительность пребывания в стационаре, сутки | 68,4 | 89,6 | |
| Необходимость отмены терапии, назначение корректоров, число наблюдений | 10 | 28 | |
| Частота регоспитализаций за время исследования | 0,9 | 1,8 |
Таким образом, в ходе настоящего исследования было установлено, что включение пантогама актив в длительную комплексную (наряду с типичными антипсихотиками) терапию шизофрении позволяет повысить эффективность и переносимость лечения.
Статистически достоверно в более ранние сроки (на 8-й неделе против 16-й в группе контроля) улучшается клиническое состояние больных, уменьшается тяжесть психопатологических расстройств (негативные и общие). Значимо уменьшается частота возникновения и выраженность вторичных негативных расстройств, обусловленных НЯ антипсихотической терапии (экстрапирамидные расстройства, нейролептическая депрессия), по шкале HDRS средний балл в основной группе достоверно уменьшается, начиная с 8-й недели терапии, на 44,3% к моменту завершающей оценки, против увеличения на 6,5% в контрольной группе (рПовышение эффективности и переносимости комбинированной терапии позволяет достичь достоверно более значимого улучшения качества жизни больных шизофренией как с точки зрения врача, так и самооценки пациентов и сохранить приверженность пациентов к терапии, способствует снижению экономических затрат на смену терапии, регоспитализацию больных.
Пантогам актив в средней дозе 1200—1800 мг в сутки может быть рекомендован двукратный прием в первой половине дня в качестве дополнительного препарата для длительной (не менее 24 нед) терапии шизофрении типичными нейролептиками.
ЛИТЕРАТУРА
1. Bhugra D. The global prevalence of schizophrenia. PLoS Medicine. 2006;2(5):372-373. doi: 10.1371/journal.pmed.0020151.
2. Harrison PJ, Weinberger DR. Schizophrenia genes, gene expression and neuropathology on the matter of their convergence. Mol Psychiatry. 2005;10(suppl 3):40-68. doi:10.1038/sj.mp.4001558.
3. Rossler W, Salize HJ, van Os J, Riecher-Rossler A. Size of burden of schizo phrenia and psychotic disorders. Еuropean Neuropsychopharmacology. 2005;15:399-409. doi: dx.doi.org/10.1016/j.euroneuro.2005.04.009.
4. McGlashan T, Walsh B, Woods S. The psychosis-risk syndrome. Handbook for diagnosis and follow-up. New York: Oxford University Press; 2010. doi.org/10.1017/S0033291711000687.
5. Mrazek PJ, Haggerty RJ. eds. Reducing risks for mental disorders: frontiers for preventive intervention research. Washington: National Academy Press; 1995. doi: 10.1002/hpm.4740100216/
6. Stahl S. Essenctial psychopharmacology. Cambrige. 2013.
7. Stip E. Cognition, schizophrenia and the effect of antipsychotics. Encephale. 2006;32(3 Pt 1):341-350. doi:10.1016/S0013-7006(06)76162-0.
8. Мазаева Н.А. Риски и преимущества применения атипичных антип-сихотиков в психиатрии (по данным зарубежных публикаций последних лет). Психиатрия и психофармакотерапия. 2006;5: 4-11.
9. Мосолов С.Н. Современная антипсихотическая фармакотерапия шизофрении. Русский медицинский журнал. 2004;10: 6.
10. Baldessarini RJ, Tarazi FI. Drugs and the treatment of psychiatric disorders: Antipsychotic and antimanic agents. In: Hardman J.G., Limbird L.E., Gilman A.G. eds. Goodman and Gilman’s the pharmacological basis of therapeutics. 10thed. N.-Y.: McGraw-Hill Press; 2001:485-528. doi: 10.1021/jm020026w.
11. Dossenbach M, Pecenak J, Szulc A, Irimia V, Anders M, Logozar-Perkovic D, Peciukaitiene D, Kotler M, West TM, Lowry AJ, Treuer T. Long-term antipsychotic monotherapy for schizophrenia: disease burden and compar ative outcomes for patients treated with olanzapine, quetiapine, risperi- done, or haloperidol monotherapy in a pan-continental observational study. J Clin Psychiatry. 2008;69(12):1901-1915. doi: 10.4088/jcp.v69n1208.
12. Сыропятов О.Г. Современное лечение шизофрении. Нейронауки (UA). 2007;2.
13. Harrow M, Jobe TH. Factors involved in outcome and recovery in schizophrenia patients not on antipsychotic medications: a 15-year multifollow-up study. Journal of Nervous and Mental Disease. 2007;195(5):404-406.
14. Lieberman JA, Stroup TS, McEvoy JP, Swartz MS, Rosenheck RA, Perkins DO, Keefe RSE, Davis SM, Davis CE, Lebowitz BD, Severe J, Hsiao JK. Effectiveness of antipsychotic drugs in patients with chronic schizophrenia. N Engl J Med. 2005;353(12):1209-1223. doi: 10.1056/nejmoa051688.
15. Дэвис ДжМ. Шизофрения: выбор антипсихотической терапии. Социальная и клиническая психиатрия. 2006;3:77-80.
16. Цыганков Б.Д., Агасарян Э.Т. Анализ эффективности и безопасности современных и классических антипсихотических препаратов. Журнал неврологии и психиатрии им. С.С. Корсакова. 2010;9:64-70.
17. Андрусенко М.П., Морозова М.А. Комбинированное использование антидепрессантов и нейролептиков при аффективных расстройствах и шизофрении: показания к назначению, побочные эффекты и осложнения. Психиатрия и психофармакотерапия. 2001;1:9.
18. Попов М.Ю. Адъювантная терапия параноидной шизофрении: оптимизация клинического действия галоперидола: Дис. ... д-ра мед. наук. СПб. 2012. https: //medi.rucal-diss.com/medicina/adyuvantnaya-terapiya-obostreniya-paranoidnoy-shizofrenii.
19. Джуга Н.П., Козловский В.Л., Попов М.Ю. Влияние гопантеновой кислоты и глицина на эффективность галоперидола при терапии пациентов с параноидной шизофренией. Психиатрия и психофармакотерапия. 2012;2:23-29.
20. Катунина Е.А., Малыхина Е.А., Аванесова О.В., Макарова А.А., Аб-дурахманова Е.К., Гридякин В.И. Применение пантогама актив в комплексном лечение дистонических гиперкинезов. Неврология и психиатрии. 2010;11:2:57-61.
21. Медведев В.Э., Исраелян А.Ю., Гушанская Е.В., Фролова В.И. Оптимизация терапии негативных расстройств при шизофрении рацематом гопантеновой кислоты. Психиатрия и психофармакотерапия. 2013;6:30-37.
22. Ковалев Г.И., Старикова Н.А. Пантогам актив: механизм фармакологического действия. РМЖ. 2010;21:2-4.

