Уважаемый посетитель!
Эта информация для специалистов здравоохранения
Нажимая «ПРОДОЛЖИТЬ», Вы подтверждаете, что им являетесь
 pikfarma.ru
pikfarma.ru
• Оригинальный ноотропный препарат с противотревожным действием
• Активирует умственную деятельность, улучшает эмоциональное состояние
Дифференцированный подход к усовершенствованию методов предупреждения и коррекции нейролептических побочных экстрапирамидных расстройств препаратом пантогам актив у больных шизофренией
СтатьиА.С. Тиганов, Г.П. Пантелеева*, Л.И. Абрамова**, П.В. Бологов, П.С. Кананович, М.А. Омельченко, И.Ю. Никифорова
ФГБНУ «Научный центр психического здоровья», Москва, Россия
Опубликовано в журнале: Неврология и психиатрия им. С.С.Корсакова. № 2.2017.с. 72-80
Цель исследования. Оценка эффективности и безопасности применения пантогама актив (ПА) в коррекции и предупреждении неврологических побочных эффектов при курсовой нейролептической терапии острых эндогенных психозов.
Материал и методы. Обследованы 80 больных обоего пола с острыми психотическими состояниями при шизофрении. Их средний возраст — 33 года. Все больные проходили 28-дневную курсовую терапию типичными и атипичными нейролептиками. Исследование проводилось в двух группах больных по 40 человек: получающих в качестве корректора тригексифенидил (ТГФ) в дозе 0,002—0,012 мг — 1-я группа, и при сочетании ТГФ с ежедневной постоянной суточной дозой 0,9 ПА — 2-я группа. Использовались методы клинического наблюдения психометрические (с помощью оценочных шкал PANSS, CGI-S, UKU) с оценкой результатов в 0-й, 1-й, 3-й, 7-й, 14-й, 21-й и 28-й дни.
Результаты. Установлено, что ПА при сочетанном применении с ТГФ способствует лучшей переносимости нейролептической терапии в целом и оказывает лучшее, чем монотерапия ТГФ, корригирующее воздействие на нейролептические экстрапирамидные расстройства (ЭПР). ПА в схеме корригирующего лечения в 1,5 раза сокращал число больных с ЭПР в ходе курсовой терапии, и в 3 раза чаще полностью предупреждал у больных их развитие. На монотерапии ТГФ в 1,7 раза чаще, чем при приеме ПА, наблюдались иные, помимо ЭПР, нежелательные побочные явления (НЯ), а сумма симптомов НЯ была в 2,5 раза больше (131 против 50). При сочетанном применении ТГФ и ПА чаще выявлялось корригирующее и профилактическое их действие на клинически более тяжелые симптомы ЭПР (акатизия, мышечная дистония) у больных, получающих типичные нейролептики. При сочетании с ПА для купирования ЭПР в сумме требовалось в 1,2 раза меньшее количество ТГФ.
Заключение. ПА в комплексном лечении неврологических побочных эффектов нейролептиков обнаруживает отчетливое нейропротекторное влияние на их формирование, частоту и клинические проявления. Этот препарат может быть рекомендован как препарат выбора для коррекции и профилактики побочных эффектов нейролептиков, способствует их лучшей переносимости и улучшает качество жизни пациентов на курсовом лечении.
Ключевые слова: побочные экстрапирамидные расстройства, типичные и атипичные нейролептики, тригексифенидил, пантогам актив, нейропротекторное действие.
A differential approach to the improvement of prevention and correction of neuroleptic side extrapyramidal disorders with pantogam activ in patients with schizophrenia
A.S. Tiganov, G.P. Panteleeva, L.I. Abramova, P.V. Bologov, P.S. Kananovich, M.A. Omelchenko, I.YU. Nikiforova
Mental Health Research Center, Moscow, Russia
Objective: To assess the efficacy and safety of pantogam active (PA) in prevention and correction of neurological side-effects during the course neuroleptic treatment of acute endogenous psychoses.
Material and methods: Eighty schizophrenic patients (mean age 33 years) with acute psychosis were examined. All patients received 28-day course treatment with typical and atypical neuroleptics. Two equal groups were studied: patients of the first group were treated with trihexyphenidyl (THP) in dose of 0,002—0,012 mg and patients of the second group received in addition PA in dose 0,9 mg/day. Clinical-observation, psychometric scales (PANSS, CGI-S, UKU) were administered at baseline and in 1 st,3rd,7th, 14th, 21st, 28st day.
Results: PA in the combination with THP improved tolerability to neuroleptic therapy in whole and exerted the better correction effect on neuroleptic extrapyramidal disorders (EPD) compared to THP monotherapy. The number of patients with ERD was reduced by 1.5 times and prevention of EPD was observed 3 times more frequent in the group treated with PA. In the THP group, other adverse effects (AE) were 1,7 times more frequent and the total AE score was 2,5 times greater compared to the PA group (131 vs 50). Correction and preventive effects of the combined treatment on the clinically severe symptoms of EPD (akathisia, muscle dystonia) were more frequent in patients treated with typical neuroleptics. A less amount of THP (by 1,2 times) was used to stop EPD in the PA group. Conclusion: PA in the combination with THP has demonstrated the clear neuroprotective effect on the development, frequency and clinical presentations of neurological side-effects. The РА can be recommended as a drug of choice for correction and prevention of neuroleptic side-effects, it promotes their tolerability and improves quality of life during the course treatment.
Keywords: side extrapyramidal disorders, typical and atypical neuroleptics, trihexyphenidyl, pantogam active, neuroprotective action.
Широкое внедрение психофармакологических средств в медицинскую практику расширило возможность оптимизации лечения психических заболеваний, но в 50—60% случаев применение таких средств приводит к развитию побочных эффектов, которые существенно нарушают качество жизни пациентов. Поэтому поиск и усовершенствование методов коррекции нежелательных явлений (НЯ) психофармакотерапии за весь период ее истории вплоть до настоящего времени не теряет своей актуальности и составляет предмет научных исследований. Это особенно касается лечения нейролептиками, назначение которых сопровождается развитием тяжелых неврологических нарушений в виде экстрапирамидных расстройств (ЭПР) вплоть до поздней дискинезии. Их возникновение связывают с нарушением аксонального транспорта и синаптической передачи нейротрансмиттеров (дофамин, ацетилхолин, норадреналин, ГАМК и др.). Исходя из предположения о нарушении функционирования ГАМК-ергической системы, которая регулирует активность дофаминовой системы, при разработке корригирующей терапии нейролептических ЭПР более 40 лет назад выбор пал на препараты ноотропного ряда. Было установлено, что первый и основной представитель этого класса соединений ноотропил, будучи близким по химической структуре к ГАМК, усиливает синтез дофамина, увеличивает плотность холинергических рецепторов и за счет активизации корково-подкорковых связей повышает устойчивость тканей головного мозга к токсическим воздействиям (в том числе нейролептиков), что обусловило его применение при плохой переносимости психотропных средств. Уже первые клинические исследования ноотропила показали, что введение его в схему терапии психических заболеваний значительно улучшает переносимость психотропных средств, позволяет избежать их побочных эффектов и осложнений (от соматовегетативных до неврологических и психических), обеспечивает профилактику непереносимости психофармакологических препаратов. Была обнаружена эффективность аналога ноотропила пирацетама как вспомогательного средства при лечении стойких неврологических (экстрапирамидных) нарушений вплоть до их полного купирования в период лечения различными нейролептическими средствами эндогенных психозов [1, 2]. Не случайно устранение неврологических осложнений нейролептических средств и их плохой переносимости внесено в показания к применению ноотропила [3].
В последующем аналогичные фармакотерапевтические свойства были обнаружены у отечественного ноотропного препарата пантогам. По химической структуре активное вещество пантогама представляет собой кальция гопантенат (кальциевая соль D-пантоил-гамма-аминомасляной кислоты) и имеет сходство фармакологических эффектов с ГАМК и пантотеновой кислотой. Это обосновывало показания к его применению в качестве лечебного и профилактического средства при подкорковых гиперкинезах, лекарственном паркинсонизме, треморе и нейролептическом синдроме с ЭПР [1, 4, 5].
В поисках новых ноотропных средств купирования нежелательных побочных действий антипсихотических нейролептиков внимание исследователей было привлечено к отечественному инновационному препарату пантогам актив, действующим веществом которого является рац-гопантеновая кислота — смесь равных количеств D- и L-стереоизомеров гопатеновой кислоты. Благодаря наличию в своем составе L-изомера гопантеновой кислоты, рац-гопантеновая кислота не только взаимодействует с ГАМК-В рецепторами, но и обладает большим сродством к небензодиазепиновым ГАМК-А рецепторам, а также уникальной способностью взаимодействовать с D2-дофаминовыми рецепторами [6, 7]. Это обеспечивает рац-гопантеновой кислоте качественную новизну фармакологических свойств и способность повышать устойчивость ЦНС к воздействию токсических веществ, тем самым снижая частоту побочных эффектов нейролептиков.
Проведенные к настоящему времени клинические исследования позволили установить нейровегетотропное и легкое анксиолитическое свойства рац-гопантеновой кислоты, ее способность улучшать интегративные показатели когнитивных функций [8, 9]. Также было изучено клиническим и психометрическим методами действие рац-гопантеновой кислоты в качестве корректора побочных эффектов антипсихотической терапии у больных шизофренией (дистонических гиперкинезов, мышечных дискинезий, экстрапирамидной симптоматики), что показало ее способность в 4 раза сокращать частоту и выраженность нежелательных явлений нейролептической терапии [10, 11]. Эти данные определили выбор рац-гопантеновой кислоты (препарат пантогам актив) в качестве протектора и/или корректора побочных экстрапирамидных расстройств при активной нейролептической терапии психотических состояний у больных шизофренией и аргументировали его дальнейшее изучение в этом направлении.
Цель исследования — определить эффективность и безопасность применения ПА как нейропротективного средства для профилактики и купирования побочных ЭПР при нейролептической терапии острых психотических состояний у больных шизофренией.
Материал и методы
Исследование проводилось в Отделе по изучению эндогенных психических расстройств и аффективных состояний (зав. — акад. РАН А.С. Тиганов) Научного центра психического здоровья.
В соответствии с протоколом исследования полный курс терапии прошли 80 больных, 33 мужчины и 47 женщин, в возрасте от 18 до 51 года (средний — 33 года).
Все больные обследовались в стационаре в период острого психотического состояния с картиной параноидного, кататоно-галлюцинаторно-бредового, аффективнобредового (маниакально-бредового или депрессивно-бредового) психозов в рамках приступообразной шизофрении (28 пациентов), экзацербации непрерывно текущей параноидной шизофрении (23) и шизоаффективного психоза (29). По МКБ-10 их диагноз соответствовал рубрикам F20.х(1-2); F20.х0 и F25.(0-1-2). Средний суммарный балл по шкале PANSS у одного больного, включенного в исследование, составил 82,4, что соответствовало средней степени тяжести острого психотического состояния.
В период исследования все больные получали основную терапию нейролептиками разных поколений в адекватных суточных дозах, назначаемую в соответствии с особенностями психотического состояния. У 20 (25%) больных это были типичные нейролептики (ТН) — галоперидол, зуклопентиксол, трифлуоперазин, труксал, хлорпротиксен, хлорпромазин, проперициазин, модитен; у 31 (30,7%) — атипичные нейролептики (АТН) — оланзапин, рисперидон, азенапин, клозапин, арипипразол, кветиапин, сердолект, амисульприд; 29 (36,3%) пациентов получали ТН в сочетании с АТН. В качестве дополнительной к нейролептикам и сопутствующей терапии допускалось (по показаниям) назначение нормотимиков (кроме карбамазепина), антидепрессантов и соматического лечения. Исключался прием других, кроме ПА, ноотропов и других, кроме тригексифенидила (ТГФ), корректоров, бензодиазепиновых транквилизаторов и гипнотиков, барбитуратов. Обязательным было получение информированного согласия пациента на участие в исследовании.
В качестве инструментов исследования использовались методы клинического наблюдения, международная оценочная шкала PANSS с оценкой в 0-й, 14-й и 28-й дни лечения, шкала побочных эффектов UKU и шкала CGI-S для оценки тяжести ЭПР. Все результаты оценки состояния больных фиксировались в индивидуальной карте больного.
Каждого из больных наблюдали 28 дней (4 нед). Всем больным с первого дня включения в протокол исследования одновременно с назначением нейролептиков с профилактической для ЭПР целью назначался корректор ТГФ в дозе 0,002 мг. При развитии ЭПР его суточную дозу ежедневно повышали и доводили до активной купирующей (максимально до 0,012 мг), величина ее определялась клиническими показаниями. Оценка ЭПР осуществлялась в 0-, 3-, 7-, 10-, 14-, 21- и 28-й дни (с первого дня их появления в статусе больного до полной редукции).
Исследование проводилось как проспективное натуралистическое сравнительное и осуществлялось в двух группах больных по 40 человек. Эти группы были сформированы в зависимости от введения в схему нейролептической терапии корригирующих ЭПР средств — только ТГФ или его сочетания с ПА. 1-я группа (n=40) — больные с первого дня исследования и до его окончания в качестве дополнительной к нейролептикам терапии получали в качестве корректоров для профилактики и коррекции побочных ЭПР только ТГФ, начиная с суточной дозы 0,002 мг в 1 день лечения с постепенным повышением ее в случае развития ЭПР до оптимальной купирующей (максимально до 0,012 мг). 2-я группа (n=40) — все больные в период проводимой нейролептической терапии, начиная с первого дня лечения, также получали для профилактики побочных ЭПР корректор ТГФ в суточной дозе 0,002, но в сочетании с 0,9 мг ПА ежедневно. При развитии ЭПР, как и в 1-й группе, доза ТГФ повышалась вплоть до купирующей, тогда как суточная доза ПА оставалась постоянной, независимо от изменений суточных доз ТГФ в процессе экспериментального курсового лечения.
В сформированных группах больных не установлено статистически значимых различий по таким показателям, как пол, средний возраст больных, диагноз заболевания, суммарный балл оценки по PANSS. В ходе проведения исследования и оценки его результатов все клинические и психометрические показатели в их динамике в 1-й и 2-й группах больных сравнивались между собой. Достоверность различий между полученными показателями (р) определялась по критерию Стьюдента t.
Результаты и обсуждение
При лечении острых психотических состояний у больных шизофренией нейролептиками разных поколений клиническое улучшение с выходом в ремиссию к 28му дню лечения отмечалось в обеих группах. Динамика психотических расстройств по оценке PANSS в 0-, 14- и 28-й дни лечения по показателям среднего суммарного балла их выраженности в 1-й и 2-й группах больных была примерно одинаковой и статистически не различалась: средний суммарный балл PANSS у одного больного от 0 до 28 дней оценки соответственно изменялся от 80 до 58,5 и от 84,7 до 63,8.
В процессе лечения нейролептические ЭПР развились у 76,25% больных, при этом в 1-й группе, получавших с корригирующей целью только ТГФ, ЭПР имели место у 35 (у 87,5%) больных из 40, во 2-й группе, где ТГФ назначался в сочетании с 0,9 ПА ежедневно, ЭПР развивались реже — у 25 (у 65%) из 40 пациентов (различия достоверны, р=0,05). Кроме того, в 1-й группе в процессе лечения у 40% больных имели место повторные эпизоды ЭПР, во 2-й группе повторные эпизоды ЭПР наблюдались также реже — у 30,8% больных. Важно отметить, что в процессе нейролептической и корригирующей терапии побочные ЭПР не развились у 12,5 и 35% больных 1-й и 2-й групп соответственно, т.е. почти в 3 раза чаще они отсутствовали у больных 2-й группы, получавших ТГФ в сочетании с 0,9 ПА ежедневно.
Установленные особенности развития и коррекции нейролептических ЭПР согласуются с результатами их оценки по шкале CGI-S: суммарное число больных с ЭПР, наблюдаемых во все дни терапии, в 1-й группе составило 109, во 2-й группе — 82. Соответственно показатель среднего числа пациентов с ЭПР на один день терапии в 1-й и 2-й группах был равен 3,9 и 2,9 человек, т.е. указанные показатели во 2-й группе больных также почти в 1,5 раза были меньше, чем в 1-й группе.
По данным шкалы CGI при коррекционной монотерапии ТГФ (1-я группа) в первый день оценки число больных с ЭПР более чем в 1,5 раза превышало показатели пациентов 2-й группы, получавших ТГФ в сочетании с ПА (12,5 и 7,5% соответственно), В последующем частота больных с ЭПР в 1-й группе последовательно нарастала и к 3-му и 7-му дням оценки становилась более чем в 5,5 раза выше по сравнению с 1-м днем (до 70%), а затем медленно снижалась к 28-му дню, но оставалась на большем, чем в первый день, уровне — 22,5%. Во 2-й группе число больных с ЭПР, начиная с 3-го дня оценки, также неуклонно увеличивалось, но с меньшими показателями частоты, чем в 1-й группе; максимальной частоты они достигали к 21-му дню лечения (до 57,5%), и по показателям на этот день приравнивались к показателям 1-й группы больных. Однако после 21-го дня частота больных с ЭПР во 2-й группе резко снижалась к 28-му дню оценки (до 10%), а практически уже с 25-го дня терапии признаков ЭПР у больных 2-й группы не наблюдалось совсем (различия по дням оценки достоверны на 5,0 и 0,1% уровнях) (см. рис. 1).
Рис. 1. Динамика частоты (в % к общему числу больных) ЭПР у больных 1-й и 2-й групп при нейролептической терапии по CGI.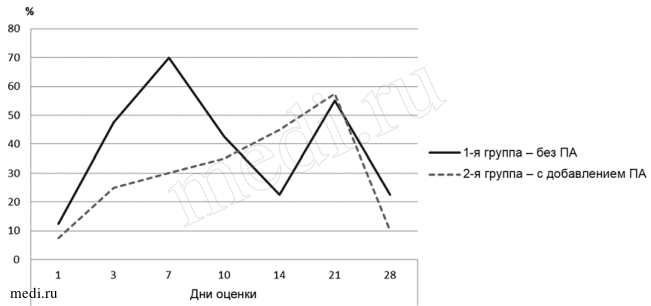
Различия во времени формирования и обратного развития ЭПР в обеих группах больных правомерно было связать с разной величиной суточной дозы получаемых нейролептиков: в 1-й группе больных при использовании только ТГФ ЭПР развивались чаще уже в 1-й день назначения еще минимальных начальных суточных доз нейролептиков, тогда как во 2-й группе больных, получавших ТГФ в сочетании с ПА, более позднее (с 3-го дня лечения) развитие ЭПР происходило в условиях приема уже более высоких суточных доз антипсихотиков и их наращивания в последующие дни. Согласно схеме нейролептической терапии, они повышались в период 1—7-го дней от минимальных до оптимальных терапевтических (или соответственно редуцировались на этапе 21—28-го дней курсового лечения). Установлено, что в 1-й группе больных повышение или понижение суточных доз нейролептиков в указанные периоды имело место соответственно в 81 и 43,1% случаев, во 2-й группе — в 75,4 и 33,3%. Эти тенденции больше представлены у больных, леченных ТН, по сравнению с получавшими АТН (статистически достоверных различий между показателями в группах не было).
В 1-й группе больных за весь период курсового лечения в сумме обнаружено 150 признаков ЭПР, а в среднем на 1 больного приходилось по 4,3 симптома ЭПР; во 2-й группе эти показатели соответственно составляли 74 и 2,8 симптомов, т.е. были в 2 и 1,5 раза меньше. В 1-й группе больных частота признаков ЭПР в 1-й день курсовой терапии почти в 5 раз превышала таковую во 2-й группе (12% против 2,7% признаков), в дальнейшем она нарастала к 7-му дню терапии и начинала снижаться лишь с 10-го дня лечения. Во 2-й группе наибольшая частота симптомов ЭПР наблюдалась только в период с 3-го к 7—10-му дням оценки, но уступала на 7-й день в 1,5 раза более высоким показателям в 1-й группе (24,7% против 16,2% симптомов), и оставалась относительно стабильной на этом уровне вплоть до 10-го дня. При оценке на 28-й день лечения частота признаков ЭПР в 1-й группе более чем в 2 раза превышала показатели во 2-й группе, при этом во 2-й группе, как уже отмечалось выше, с 25-го дня курсового лечения ЭПР не наблюдались вовсе (табл. 1).
Таблица 1.
Динамика частоты признаков ЭПР при курсовой терапии нейролептиками разных поколений в 1-й и 2-й группах больных
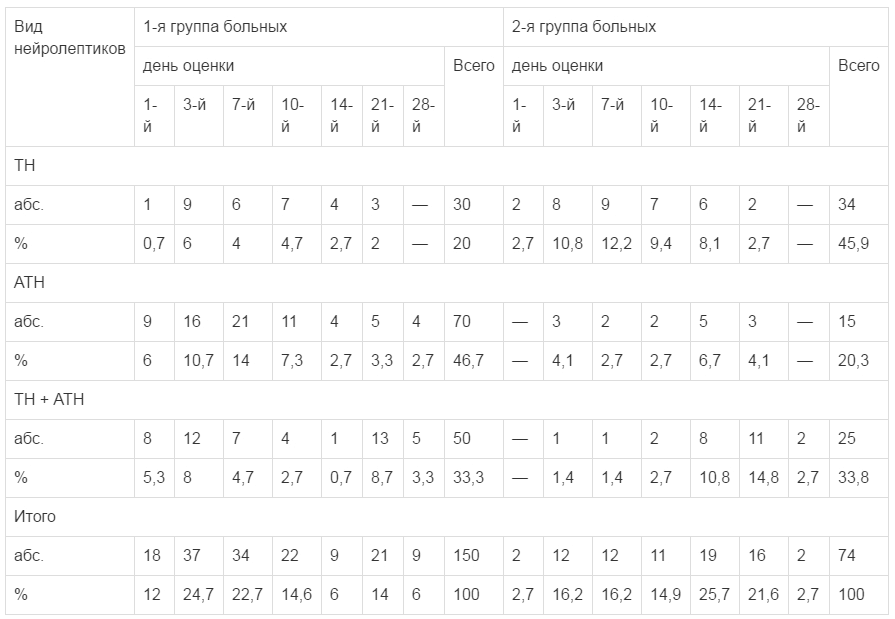
Среди подвидов нейролептических ЭПР на курсовой терапии наблюдались акатизия, тремор, гипо- и гиперкинезия, мышечная ригидность, дистония мышц. Обнаруживалась тенденция к большей частоте клинически более тяжелых признаков ЭПР во 2-й группе наблюдений — акатизии — 31,1% (р=0,05), мышечной дистонии — 12,2%. Но терапевтическая динамика симптомов акатизии и мышечной дистонии во 2-й группе больных была более благоприятной, чем в 1-й. Частота симптома акатизии среди других признаков ЭПР во 2-й группе больных при лечении ТГФ и ПА от 1-го до 21-го дня курсовой терапии снижалась с 50 до 25%, а к 28-му дню лечения уже отсутствовал полностью. В 1-й группе частота акатизии, хотя изначально была менее выраженной, чем во 2-й группе, от 1-го до 28-го дня лечения неуклонно возрастала от 16,7 до 33,4%. Кроме того, у больных 2-й группы симптом мышечной дистонии был наиболее представлен среди всех признаков ЭПР на 3-й день курсового лечения (41,7%), но к 7-му и 10-му дням терапии заметно редуцировался до 33,3 и 9,1% соответственно, а в 14—28-й дни уже не регистрировался вовсе. В 1-й группе симптом мышечной дистонии среди других признаков ЭПР в 1-й день лечения имел незначительную частоту — 5,6%, хотя в последующие дни оценки частота его увеличивалась до 11,1% и сохранялась на этом уровне вплоть до 28-го дня терапии.
Во 2-й группе больных тяжесть побочных явлений в целом, определяемая по шкале UKU, также была выше, чем в 1-й группе: средний балл тяжести одного признака ЭПР соответственно был 1,5 и 1,2 балла. При этом следует учесть, что 46% больных 2-й группы находились на монотерапии ТН, которые в большей степени, чем АТН, склонны к развитию неврологических побочных эффектов. Из всего количества симптомов ЭПР в 1-й группе 46,7% развивалась при приеме АТН, почти в 2 раза чаще, чем у больных 2-й группы (20,3%), а при лечении ТН признаки ЭПР в 1-й группе наблюдались в 2,3 раза реже, чем во 2-й группе (в 20% против 45,9% соответственно; p<0,01). К тому же обнаруживалась установленная ранее зависимость показателей тяжести ЭПР от динамики величины суточной дозы нейролептиков в схеме назначаемого курсового лечения (рис. 2).
Рис. 2. Динамика тяжести ЭПР при нейролептической терапии у больных 1-й и 2-й групп (по среднему баллу UKU).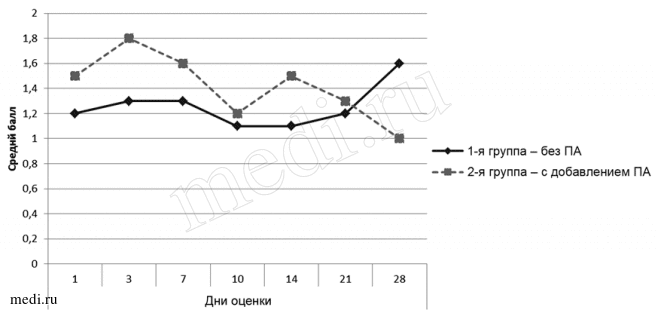
Имелись различия по числу больных, у которых не развились ЭПР при лечении разными поколениями нейролептиков: в 1-й группе ЭПР отсутствовали у 28,6% больных, получавших АТН, и у 5,6% при лечении ТН + АТН. Во 2-й группе среди больных, получавших АТН и ТН + АТН, ЭПР не наблюдались одинаково часто, соответственно в 41,2 и 45,5%. К тому же только во 2-й группе не имели ЭПР 16,7% больных при лечении ТН. Обращает внимание тот факт, что среди леченных ТН больных 1-й группы у всех развивались ЭПР (р=0,01 только для АТН). Таким образом, только во 2-й группе больных профилактическое действие ТГФ в сочетании с ПА в отношении ЭПР чаще проявлялось в условиях назначения ТН, обладающих, как известно, более выраженным развитием побочных эффектов, чем АТН.
Как видно из табл. 1, в зависимости от вида получаемой нейролептической терапии, в динамике частоты признаков ЭПР выявились различия. Несмотря на то что больные 1-й группы в преобладающем большинстве случаев получали АТН как в виде монотерапии, так и в сочетании с ТН, частота симптомов ЭПР у них была выше, чем во 2-й группе, где чаще назначались ТН как в виде монотерапии, так и в сочетании с АТН (различия по дням от 3-го к 14-му высоко достоверны, р=0,05; 0,01; 0,001). Эти данные показывают, что ПА, введенный в схему лечения, усиливает корригирующие свойства ТГФ, особенно при воздействии на более тяжелые ЭПР, свойственные ТН (рис. 3).
Рис. 3. Частота ЭПР в 1-й и 2-й группах больных при лечении нейролептиками разных поколений.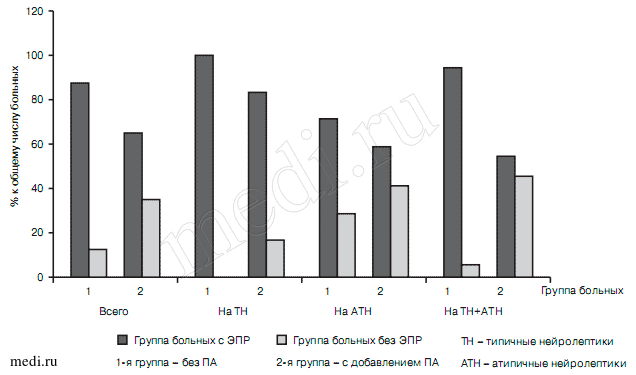
Показатели средней длительности одного признака ЭПР от его возникновения до полного купирования в обеих группах практически совпадали и равнялись 2,01 и 2,05 дня в 1-й и 2-й группах соответственно, однако диапазон количества дней, необходимых для купирования ЭПР, в 1-й группе варьировал от 1,5 до 3,6, а во 2-й группе — от 1 до 3, т.е. коррекция ЭПР достигалась быстрее.
На всех этапах лечения в 1-й группе для купирования ЭПР были использованы более высокие средние суточные дозы ТГФ, чем во 2-й группе: диапазон их величин соответственно был 4,7—6,9 и 4—6,2 мг в разные дни терапии. Купирующий ЭПР эффект ТГФ в сочетании с ПА во 2-й группе в каждый из дней оценки достигался в целом при меньшем, чем в 1-й группе, увеличении той средней суточной дозы ТГФ, на которой изначально развивались ЭПР как в каждый из дней терапии, так и в суммарном их выражении за весь период лечения. В 1-й группе наблюдений купирующая доза ТГФ по сравнению с начальной при развитии ЭПР увеличивалась на 89,3%, во 2-й группе меньше — на 77,4%. Во 2-й группе для купирования ЭПР требовалось не только меньше, чем в 1-й группе, дней (2,1 дня против 2,2 дня соответственно), но и меньшее по величине наращивание дозы ТГФ (p=0,001). Доля начальной суммарной дозы ТГФ, при которой развивались ЭПР, по отношению к купирующей ЭПР суммарной дозе в 1-й группе была меньше, чем во 2-й, и составляла 52,6% против 56,1%. Для коррекции нейролептических ЭПР в 1-й группе требовалась средняя суточная доза ТГФ для одного больного 4,9 мг, во 2-й группе, получавших ТГФ в сочетании с ПА, — 4 мг, т.е. в 1,2 раза меньше. Исходя из этих данных установлено, что суммарное количество ТГФ, израсходованное за все время курсового лечения, у больных ЭПР в 1-й группе было больше, чем во 2-й группе (4786 мг против 2942 мг). В среднем на одного пациента 1-й группы требовалось на 28-дневный курс комплексного лечения 136,7 мг ТГФ (68,4 таблетки по 2 мг), во 2-й группе — 113,2 мг (56,6 таблеток по 0,002 мг).
В обеих группах в процессе лечения нейролептиками наблюдались и иные, кроме неврологических, НЯ, характеризующие в целом переносимость нейролептической терапии. Они имели место у 27 (в 67,5%) больных 1-й группы и у 16 (40%) пациентов 2-й группы. По данным шкалы UKU в 1-й и 2-й группах в сумме было зарегистрировано соответственно 131 и 50 симптомов НЯ, а в среднем на одного больного приходилось по 4,9 и 3,1 НЯ, т.е. более чем в 1,5 раза меньше НЯ развивалось при сочетанном применении ТГФ с ПА у пациентов 2-й группы. По частоте в разных сферах НЯ статистических различий между группами обнаружено не было, хотя в 1-й группе преобладали психические НЯ (66,4% против 58%) и другие НЯ (2,3% против 0%), а вегетативные НЯ больше были представлены во 2-й группе (42% против 31,3%). По набору признаков в сферах психических и вегетативных НЯ 1-я и 2-я группы также мало различались, но частота их была неодинаковой. В целом в 1-й группе больных по частоте и длительности доминировали симптомы астении и седации, во 2-й группе среди НЯ лидировали такие симптомы, как бессонница и внутреннее беспокойство. Только у больных 1-й группы обнаруживались единичные другие НЯ — кожная сыпь, кожный зуд (1 балл тяжести), прибавка массы тела у больной с ожирением (2 балла), наблюдаемые соответственно в 3-, 7- и 21-й дни оценки (табл. 2).
Таблица 2.
Частота НЯ, возникших при нейролептической терапии в 1-й и 2-й группах больных по UKU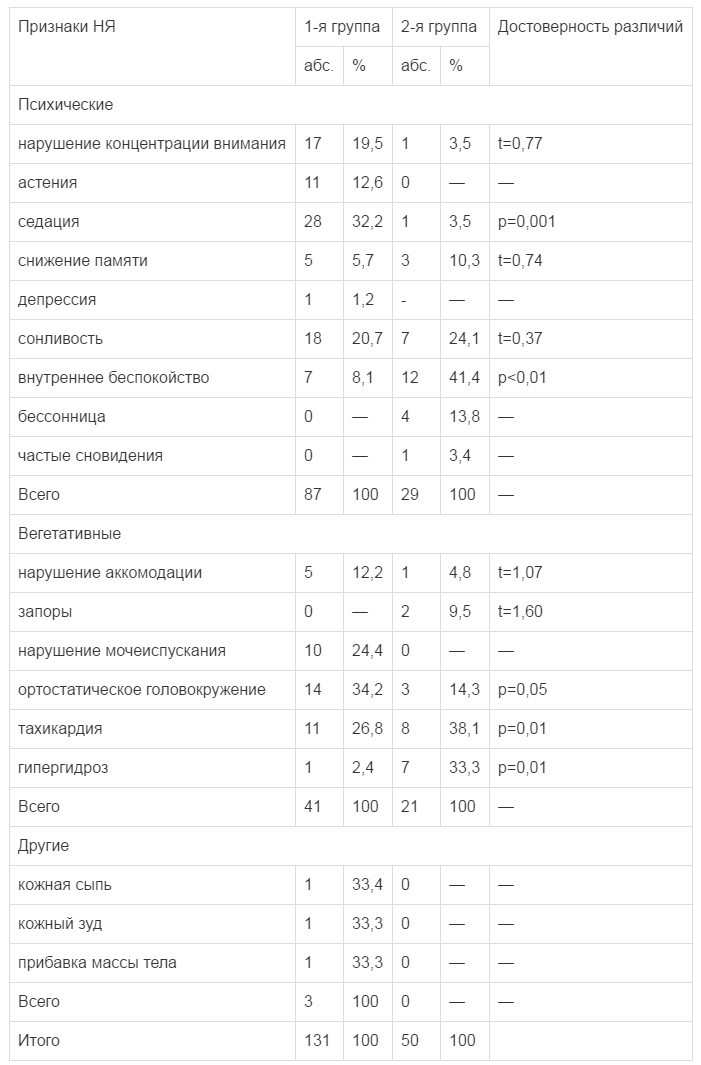
Тяжесть НЯ в обеих группах оценивалась преимущественно как легкая по UKU — от 1 до 1,4 балла. В этом диапазоне НЯ во 2 группе в целом были тяжелее, чем в 1-й, на всех этапах курсового лечения нейролептиками, по тяжести среди них преобладали психические НЯ (на уровне 1,4—1,7 баллов), что также можно связать с преобладанием типичных нейролептиков при курсовом лечении больных 2-й группы.Динамика развития НЯ в обеих группах имела тенденцию к наибольшей их частоте к 3-му дню курсового лечения (до 44,3 и 34% симптомов в 1-й и 2-й группах соответственно), но дальнейшая их редукция с 10-го дня терапии более интенсивно происходила в 1-й группе: к 28-му дню в 1-й группе частота НЯ становилась минимальной, во 2-й группе, несмотря на изначально меньшую частоту НЯ, редукция их после 7-го дня оценки была в целом не столь интенсивной, а частота НЯ держалась на относительно постоянном и большем, чем в 1-й группе, уровне вплоть до 28-го дня.
Таким образом, проведенное исследование позволило установить, что введение 0,9 мг ПА в схему корригирующего лечения ТГФ неврологических побочных эффектов нейролептической терапии по сравнению с монотерапией ТГФ позволило в 1,5 раза сократить частоту развития нейролептических ЭПР у больных острыми шизофреническими психозами, в 3 раза чаще полностью избежать их развития и в целом значительно улучшить общую переносимость приема нейролептиков (табл. 3).
Таблица 3.
Особенности формирования нейролептических ЭПР на корригирующем лечении больных 1-й и 2-й групп при терапии ТН и АТН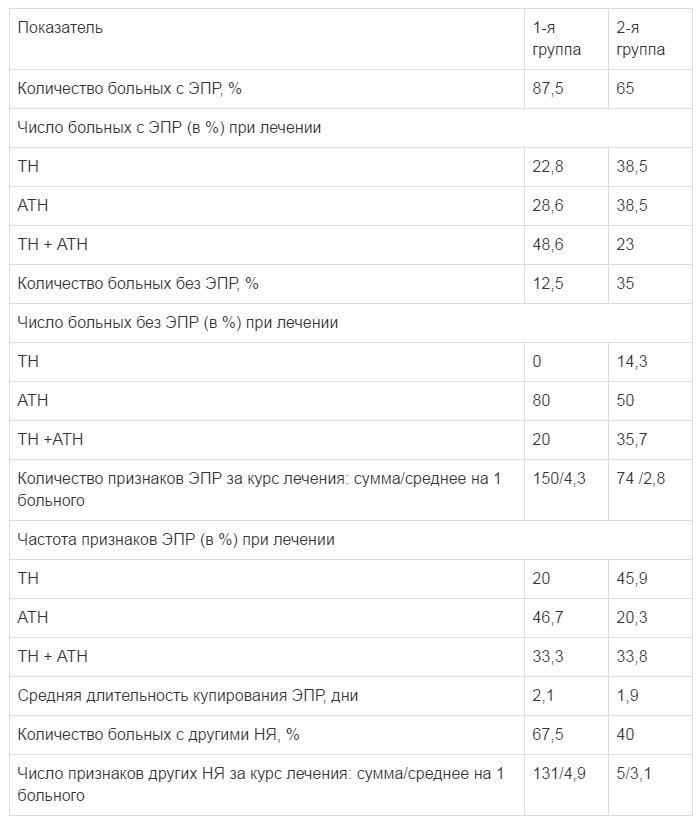
ПА, введенный в схему корригирующего лечения, позволил значительно улучшить и общую переносимость нейролептической терапии по показателям частоты иных, кроме неврологических, НЯ. По оценке шкалы UKU на монотерапии ТГФ НЯ наблюдались в 1,7 раза чаще, чем у больных, получающих ТГФ в сочетании с ПА. При монотерапии ТГФ у больных в сумме зарегистрирован 131 симптом НЯ, а на ТГФ с применением ПА более чем в 2,5 раза меньше. К тому же, хотя по частоте и «набору» признаков психические и автономные НЯ в обеих группах больных были представлены примерно одинаково, однако в 1-й группе больных, на монотерапии ТГФ, достоверно чаще обнаруживались такие симптомы НЯ, как астения, седация, вегетативные нарушения, а во 2-й группе больных, при сочетании ТГФ с ПА, достоверно более частыми и более постоянными были симптомы внутреннего беспокойства и бессонницы.При введении ПА в схему лечения общее число симптомов ЭПР, развивающихся за весь период курсового лечения нейролептиками, сократилось в 2 раза, а среднее количество признаков ЭПР у одного больного за один день уменьшилось более чем в 1,5 раза. Установлено также, что у больных, получающих с первого дня курсовой терапии дополнительно к ТГФ ПА, развитие ЭПР фиксировалось впервые в более поздние сроки курсового лечения нейролептиками и только после наращивания величины суточной дозы нейролептика от минимальной в 1-й день лечения до оптимально более высоких, терапевтических доз в последующие 3—7-й дни терапии, тогда как на монотерапии ТГФ ЭПР обнаруживались не только чаще в фиксированные дни оценки, но и развивались уже с 1-го дня лечения при приеме минимальных суточных доз нейролептиков. Также при снижении суточных доз нейролептиков к концу курсовой терапии (21—28-й дни оценки) во 2-й группе больных, получающих ТГФ в сочетании с ПА, развития ЭПР не наблюдалось уже с 25-го дня лечения, а на монотерапии ТГФ в 1-й группе больных, несмотря на уменьшение суточных доз нейролептиков, ЭПР обнаруживались вплоть до 28-го дня лечения и с большей частотой, чем в 1-й день приема нейролептиков.
Установленные приоритетные корригирующие свойства ПА при сочетанном применении с ТГФ выявлялись более чем в 2 раза чаще у больных, принимающих типичные нейролептики, которые, как известно, в большей степени, чем АТН, обладают свойством к развитию неврологических побочных эффектов, в том числе наиболее выраженных. Правомерно полагать, что по этой причине показатели тяжести симптомов ЭПР в ходе курсовой терапии нейролептиками в группе больных, получающих ТГФ в сочетании с ПА, в 1,3 раза превышали по степени выраженности показатели тяжести ЭПР у больных на «чистом» ТГФ. У больных, получающих ПА, также чаще наблюдались более тяжелые по клиническим проявлениям виды ЭПР, такие как акатизия, мышечная дистония. Однако, следует заметить, что 50% пациентов без ЭПР, получавших ПА, лечились ТН в качестве монотерапии или при их сочетании с АТН, тогда как в группе пациентов, лечившихся только ТГФ, при монотерапии типичными нейролептиками случаев без ЭПР не было.
При лечении преимущественно ТН в группе больных, получающих ПА, величина начальной суточной дозы ТГФ, на которой впервые развивались ЭПР, была выше, чем на монотерапии ТГФ (3,1 и 2,8 мг соответственно). Но по своей длительности эпизоды ЭПР от начала их появления и до дня их купирования у больных, получающих ПА, были в абсолютных величинах почти в 1,5 раза короче по сравнению с теми, кто получал только ТГФ. Хотя в среднем купирующие ЭПР дозы тригексифенидила в обеих группах больных почти не различались (5,3 и 5,5 мг), но у больных, получающих ПА, купирующий ЭПР эффект достигался при количественно меньшем увеличении купирующей дозы ТГФ. В целом при введении в схему корригирующего лечения ПА для купирования ЭПР требовалось в 1,2 раза меньшее количество ТГФ, что обеспечивало экономический эффект апробированного метода коррекции ЭПР.
Сказанное выше позволяет сделать вывод, что ПА, назначаемый ежедневно в суточной дозе 0,9 мг дополнительно к ТГФ при корригирующем лечении нейролептических побочных неврологических эффектов, возникающих при терапии острых эндогенных психотических состояний, способствует лучшей переносимости нейролептической терапии в целом. При сочетанном применении с ТГФ ПА оказывает большее, чем ТГФ, корригирующее воздействие на нейролептические ЭПР, снижает их частоту и длительность, сокращает суточную потребность в традиционном корректоре. ПА оказывает большее нейропротекторное действие на побочные ЭПР, способствуя предупреждению и профилактике развития их симптомов, в том числе и наиболее тяжелых, обусловленных приемом ТН.
Полученные данные позволяют рассматривать ПА как эффективное средство корригирующего воздействия на неврологические побочные эффекты нейролептической терапии, обладающее выраженным нейропротекторным влиянием на их формирование и клинические проявления, и может быть рекомендован как препарат выбора на пути оптимизации и усовершенствования методов коррекции и профилактики побочных эффектов нейролептиков, способствуя их лучшей переносимости в ходе курсового лечения и улучшению качества жизни пациентов.
ЛИТЕРАТУРА
1. Пантелеева Г.П., Цуцульковская М.Я., Мазурский М.Б., Беляев Б.С., Морозов П.В. Применение пирацетама при шизофрении (в качестве лечебного средства и корректора осложнений нейролептической терапии). Клиническое значение препарата ноотропил. Материалы советско-бельгийского симпозиума. М., 15.12.1976;59-70.
2. Руденко Г.М., Звездин А.В., Врублевский А.Г., Остапенко О.В. Применение препарата пирацетам при непереносимости нейролептиков и других психотропных средств. Клиническое значение препарата ноотропил. Материалы советско-бельгийского симпозиума. М., 15.12.1976;71-78.
3. Машковский М.Д. Лекарственные средства. Изд. 13-е новое. Харьков. 1997;I:109-111, 114-115.
4. Пантелеева Г.П., Макеева В.Л. Место ноотропных препаратов в терапии нейролептического паркинсонизма. Материалы симпозиума «Патогенез, клиника и лечение паркинсонизма». Тезисы докладов. М. 1978;243-246.
5. Концевой В.А., Ротштейн В.Г., Богдан М.Н., Ряховский В.В. Пантогам в повседневной психиатрической практике. Журнал неврологии и психиатрии им. С.С. Корсакова. 2007;107(12):34-40.
6. Ковалев В.М. Пантогам актив — инновационный препарат на основе рацемата гомопантотеновой кислоты с ноотропным, нейропротекторным и противосудорожным действием. В кн.: Пантогам и Пантогам актив. Клиническое применение и фундаментальные исследования. Под ред. Копелевича В.М. М.: Триада-фарм; 96-103.
7. Ковалев Г.И., Старикова Н.А. Пантогам актив: механизм фармакологического действия. РМЖ. Неврология, психиатрия. 2010;26:1538.
8. Катунина Е.В., Малыхина Е.А., Аванесова О.В., Макарова А.А., Абдурахманова Е.К., Гридякин В.И. Применение пантогама актив в комплексном лечении дистонических гиперкинезов. Журнал неврологии и психиатрии им. С.С. Корсакова. 2010;110:11(2):57-61.
9. Канаева Л.С., Вазагаева Т.С., Ястребова В.В. Перспективы применения препарата Пантогам актив у больных с астеническими расстройствами. Журнал неврологии и психиатрии им. С.С.Корсакова, 2010; 11:6:34-39.
10. Медведев В.Э., Исраелян А.Ю., Гушанская Е.В., Фролова В.И. Оптимизация терапии негативных расстройств при шизофрении рацематом гопантеновой кислоты. Психиатрия и психофармакотерапия им. П.Б. Ганнушкина. 2013;15(6):30-37.
11. Медведев В.Э., Фролова В.И., Исраелян А.Ю. Аугментация терапии шизофрении рацематом гопантеновой кислоты. Журнал Неврология и психиатрия им. С.С. Корсакова, 2015;8.

