Эффективность и безопасность применения лекарственного средства Галавит® в форме суппозиториев в лечении коронавирусной инфекции среднетяжелой формы у детей в возрасте от 6 до 12 лет
СтатьиЛ.Н. Мазанкова1, 2 д-р мед. наук, профессор, И.М. Османов1, д-р мед. наук, профессор, Э.Р. Самитова1, 2, д-р мед. наук, Е.П. Каурова1, Н.А. Драчева3, канд. мед. наук
1 ГБУЗ «Детская городская клиническая больница им. З.А. Башляевой Департамента здравоохранения г. Москвы»
2 ФГБОУ ДПО «Российская медицинская академия непрерывного последипломного образования» Минздрава России, г. Москва
3 ГБУЗ «Детская городская клиническая больница им. Н.Ф. Филатова Департамента здравоохранения г. Москвы»
Ключевые слова: новая коронавирусная инфекция, COVID-19, осложненная форма, пациенты-дети, иммунотерапия, аминодигидрофталазиндион натрия, Галавит®
Keywords: new coronavirus infection, COVID-19, complicated form, pediatric patients, immunotherapy, aminodihydroftalazindion sodium, Galavit®
Резюме. Предметом исследования является эффективность и безопасность применения иммуномодулирующего препарата Галавит® (аминодигидрофталазиндион натрия) в форме суппозиториев для лечения среднетяжелой формы COVID-19 у детей в возрасте 6-12 лет. Цель работы - оценить влияние препарата на сроки выздоровления, частоту осложнений и иммунологические показатели. Методология включала проспективное сравнительное нерандомизированное исследование с участием 80 детей, разделенных на основную группу (50 пациентов, получавших Галавит®) и контрольную группу (30 пациентов). Оценивались клинические и иммунологические параметры на 10-й день наблюдения. Результаты показали, что применение Галавита® сократило длительность заболевания (5,75 ± 0,771 суток против 6,56 ± 1,366 в контроле, p = 0,004), способствовало нормализации иммунологических показателей (повышение уровней IgM, цитотоксических Т-лимфоцитов, NK-клеток и В-лимфоцитов) и не вызвало нежелательных явлений. Осложнения в обеих группах отсутствовали. Полученные данные подтверждают целесообразность включения Галавита® в комплексную терапию COVID-19 у детей для ускорения выздоровления и модуляции иммунного ответа. Результаты могут быть применены в педиатрической практике для лечения респираторных инфекций. Выводы: Галавит® демонстрирует эффективность и безопасность в лечении среднетяжелого COVID-19 у детей, оказывая иммунокорригирующее действие.
Summary. The subject of the study is the efficacy and safety of the use of the immunomodulatory drug Galavit® (ami-nodihydroftalazindion sodium) in the form of suppositories for the treatment of moderate COVlD-19 in children aged 6-12 years. The purpose of the work is to assess the effect of the drug on the timing of recovery, the frequency of complications and immunological indicators. The methodology included a prospective comparative non-randomized study involving 80 children divided into the main group (50 patients treated with Galavit®) and the control group (30 patients). Clinical and immunological parameters were evaluated at Day 10 of follow-up. The results showed that the use of Galavit® reduced the duration of the disease (5,75 ± 0,771 days versus 6,56 ± 1,366 in the control, p = 0,004), contributed to the normalization of immunological parameters (increased levels of IgM, cytotoxic T-lymphocytes, NK-cells and B-lymphocytes) and did not cause adverse events. There were no complications in both groups. The data obtained confirm the feasibility of including Galavit® in the complex therapy of COVID-19 in children to accelerate recovery and modulate the immune response. The results can be applied in pediatric practice to treat respiratory infections. Conclusions: Galavit® demonstrates efficacy and safety in the treatment of moderate COVID-19 in children, having an immunocorrective effect. Further research could expand its scope in other infections.
Для цитирования: Эффективность и безопасность применения лекарственного средства Галавит® в лечении новой коронавирусной инфекции среднетяжелой формы у детей в возрасте от 6 до 12 лет / Л.Н. Мазанкова, И.М. Османов [и др.] // Практика педиатра. 2025. № 3. С. 4–10.
For citation: Mazankova L.N., Osmanov I.M. etc. Efficacy and safety of Galavit® in the treatment of moderate coronavirus infection in children aged 6 to 12 years // Pediatrician's Practice. 2025;(3): 4–10. (In Russ.)
ВВЕДЕНИЕ
С момента своего появления в конце 2019 г. вирус SARS-CoV-2 претерпел значительную эволюцию, пройдя путь от нового, неизученного патогена до сезонного респираторного вируса, циркулирующего наряду с другими возбудителями ОРВИ [1]. По данным ВОЗ, в 2024 г. COVID-19 демонстрировал четкую сезонность с пиками заболеваемости в осенне-зимний период, что характерно для других коронавирусов человека [2]. Однако в отличие от традиционных сезонных ОРВИ SARS-CoV-2 сохраняет ряд уникальных особенностей, делающих его по-прежнему опасным для определенных групп пациентов, включая детей [3].
Важную проблему в педиатрической практике представляют микст-инфекции. В 35-45% случаев COVID-19 у детей протекает в ассоциации с другими респираторными вирусами (грипп, респираторно-синцитиальные вирусы, аденовирусы), что значительно утяжеляет клиническую картину и затрудняет диагностику [4]. При сочетанных инфекциях у детей чаще развиваются бронхиолиты, пневмонии и требуются госпитализации [5].
Главной отличительной чертой SARS-CoV-2 остается его исключительно высокая мутагенность. По данным исследований, частота мутаций у этого вируса в 2-4 раза выше, чем у других коронавирусов [6]. В 2024 г. продолжали циркулировать штаммы линии Омикрон, среди которых доминируют субварианты JN.1 и KP.2, демонстрирующие повышенную контагиозность и способность частично избегать нейтрализации существующими антителами, уклоняясь от иммунного ответа, сформированного как после перенесенного заболевания, так и после вакцинации [7]. Согласно данным Всемирной организации здравоохранения и Центра по контролю и профилактике заболеваний США (CDC) в 2025 г. ожидается продолжение циркуляции сезонных респираторных инфекций, включая грипп (с потенциальным доминированием штаммов A/H3N2, A/H1N1pdm09 и линий B/Victoria/Yamagata), респираторно-синцитиальный вирус, а также риновирусы и аденовирусы. COVID-19, вероятно, сохранит свое присутствие в структуре ОРВИ, но будет проявляться менее тяжелыми формами благодаря сформировавшемуся популяционному иммунитету. Основными факторами, влияющими на эпидемиологическую ситуацию, останутся сезонность, уровень вакцинации и возможное появление новых антигенных вариантов вирусов. Что касается эволюции SARS-CoV-2, наиболее вероятным сценарием считается его переход в эндемическую фазу с периодическими волнами, обусловленными новыми подвариантами Omicron. Эти штаммы могут демонстрировать повышенную контагиозность, но, скорее всего, будут вызывать менее тяжелое течение болезни благодаря накопленному иммунитету. Однако риск возникновения более патогенных вариантов, способных ускользать от иммунной защиты, полностью исключать нельзя. В долгосрочной перспективе коронавирусная инфекция, вероятно, интегрируется в группу сезонных респираторных заболеваний, подобно гриппу, требуя регулярного обновления вакцин и постоянного эпидемиологического мониторинга.
Особую озабоченность у педиатров вызывает способность SARS-CoV-2 вызывать иммуносупрессию. Вирус оказывает комплексное воздействие на иммунную систему:
1. Снижает количество и функциональную активность Т-лимфоцитов, а именно CD3+ - зрелых Т-лимфоцитов (основные клетки клеточного иммунитета), CD4+ - Т-хелперов (координируют работу других иммунных клеток), CD8+ - цитотоксических Т-лимфоцитов («киллеры», уничтожают зараженные вирусом клетки).
2. Угнетает активность натуральных киллеров (NK-клеток).
3. Нарушает процесс антителообразования В-лимфоцитами (CD19+) (важнейшие клетки иммунной системы, отвечающие за гуморальный иммунитет (выработку антител) [8].
Эти нарушения создают благоприятные условия для развития вторичных бактериальных инфекций и затяжного течения заболевания. У детей 6-12 лет, чья иммунная система находится в стадии активного развития, COVID-19 часто протекает в среднетяжелой форме, сопровождаясь стойкой лихорадкой, выраженными респираторными симптомами и риском серьезных осложнений [9]. В этой возрастной группе сохраняется риск развития мультисистемного воспалительного синдрома (МВС), а также формирования постковидных астенических состояний, проявляющихся снижением когнитивных функций и физической выносливости [5].
Склонность к легкому течению COVID-19 у детей также тесно связана с отличительными чертами их иммунной системы по сравнению со взрослыми. Во-первых, у детей лучше функционирует лимфоэпителиальное кольцо, благодаря чему большое количество SARS-CoV-2 нейтрализуется в верхних дыхательных путях. Во-вторых, у детей на ранних стадиях заболевания активно пролиферируют натуральные киллеры, которые вырабатывают интерлейкин 17А, предотвращающий поражение нижних дыхательных путей и развитие пневмонии. У пациентов с МВС выявляется пониженное количество натуральных киллеров. SARS-CoV-2 способен вызвать лимфопению, у детей она ассоциируется с тяжестью заболевания. В-третьих, у детей продукция антител происходит в первые три недели заболевания, а иммуноглобулины G появляются уже на первой неделе. Теоретически иммуномодуляция у детей должна дополнительно уменьшить сроки лечения, число осложнений и переходов в тяжелые формы COVID-19 [10-14].
В сложившейся эпидемиологической ситуации особую актуальность приобретает поиск эффективных и безопасных иммуномодулирующих препаратов, способных:
• сократить продолжительность заболевания,
• снизить частоту осложнений,
• восстановить нарушенный иммунный ответ,
• минимизировать риск развития постковидных состояний.
При этом терапия должна соответствовать строгим критериям безопасности, предъявляемым к препаратам в педиатрической практике, особенно в возрастной группе 6-12 лет, когда идет активное формирование иммунной системы.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Оценка эффективности и безопасности применения лекарственного средства Галавит® в форме суппозиториев ректальных в лечении коронавирусной инфекции среднетяжелой формы у детей в возрасте от 6 до 12 лет.
ЗАДАЧИ ИССЛЕДОВАНИЯ
Задачами исследования были следующие:
• оценить частоту осложнений коронавирусной инфекции среднетяжелой формы в группах исследования;
• оценить сроки купирования коронавирусной инфекции среднетяжелой формы в группах исследования;
• оценить безопасность применения Галавит®.
ДИЗАЙН ИССЛЕДОВАНИЯ
Проспективное сравнительное нерандомизированное одноцентровое наблюдательное исследование для оценки эффективности применения лекарственного препарата Галавит® в форме суппозиториев ректальных в лечении коронавирусной инфекции среднетяжелой формы у детей в возрасте от 6 до 12 лет. Препарат Галавит® относится к группе иммуномодулирующих и противовоспалительных средств. К настоящему времени проведены доклинические исследования препарата Галавит®, а также клинические исследования с участием пациентов. Результаты, полученные в ходе исследований, позволили заключить, что препарат Галавит® эффективен в комплексной терапии различных заболеваний, в том числе часто рецидивирующих заболеваний дыхательных путей и ЛОР-органов бактериальной и вирусной этиологии, в том числе у детей. Препарат обладает хорошей переносимостью. Препарат Галавит® одобрен Министерством здравоохранения Российской Федерации для применения в широкой практике.
Назначение препарата Галавит® производилось врачом-исследователем в стационаре в соответствии с действующими клиническими рекомендациями, с учетом инструкции по применению и индивидуальных особенностей пациента.
В случае отказа родителей (представителей) пациента от назначения препарата Галавит® им предлагалось участие в исследовании в контрольной группе.
Таким образом, в исследовании сформировано две группы пациентов для наблюдения:
• группа 1 - пациенты, получающие Галавит® для иммунопрофилактики по одному суппозиторию 50 мг ежедневно в течение 5 дней в стационаре, затем по 1 суппозиторию 50 мг ежедневно в течение 5 дней амбулаторно;
• группа 2 - пациенты, не получающие Галавит® для иммунопрофилактики (контрольная группа).
Наблюдение за участником исследования происходило в течение 90 дней, во время которых собирались необходимые данные.
При включении пациента в исследование проводилось лабораторное обследование, повторяемое впоследствии на 10-й день лечения - общий (клинический) анализ крови с оценкой лейкоцитарной формулы (лейкоциты, нейтрофилы, лимфоциты), иммунологический анализ крови, включавший определение уровней иммуноглобулинов A, G, M, E (IgA, IgG, IgM, IgE), Т-лимфоцитов (CD3+CD19-) - зрелых Т-лимфоциты, основных клеток клеточного иммунитета, отвечающих за распознавание и уничтожение вирус-инфицированных клеток; Т-цитотоксических клеток (CD3+CD8+CD45+) - специализированных иммунных клеток, играющих ключевую роль в противовирусной защите, NKT-клетки (CD3+CD56+CD45+) - естественные киллерные Т-лимфоциты, редкая популяция Т-клеток, обладающая свойствами как Т-лимфоцитов (CD3+), так и NK-клеток (CD56+); NK-киллеров (CD3-CD56+CD45+) - важного компонента врожденного иммунитета, соотношения Т-хелперы/Т-цитотоксические клетки (CD3+CD4+ / CD3+CD8+) - важного иммунологического показателя, отражающего баланс между регуляцией и эффекторной функцией иммунитета, интестинальных интраэпителиальных лимфоцитов (CD3-CD8+CD45+) - специализированной популяции лимфоцитов, постоянно находящихся в эпителии кишечника, В-лимфоцитов (CD19+CD3- (основные продуценты антител IgM, IgG, IgA); CD3+CD19+ (переходные формы в процессе дифференцировки).
Пациенты включались в исследование, если они соответствовали следующим критериям:
1) дети возрастом от 6 до 12 лет;
2) находящиеся на стационарном лечении в исследовательском центре с лабораторно подтвержденным методом полимеразной цепной реакции диагнозом коронавирусной инфекции среднетяжелой формы [15], в том числе полиморбидные пациенты с легким или умеренным течением сопутствующей патологии, не являющейся ограничением участия ребенка в исследовании по мнению врача-исследователя;
3) обратились за медицинской помощью не позднее 72 часов с момента заболевания;
4) родители / законные представители пациента подписали форму информированного согласия.
Пациенты не включались в исследование, если они соответствовали следующим критериям:
1) принимают или принимали в предшествующие три месяца другие лекарственные средства с иммуномодулирующим эффектом;
2) имеют противопоказания для назначения Галавит® согласно утвержденной инструкции по медицинскому применению;
3) имеют на момент включения в исследование осложнения коронавирусной инфекции;
4) имеют на момент включения в исследование коронавирусной инфекции тяжелой или критической формы [15].
В исследование включено 80 пациентов: 50 - в основной группе, 30 - в контрольной.
Первичная переменная:
• количество пациентов, у которых развились осложнения ОРВИ группы COVID-19 с момента начала приема Галавит® в основной группе и с момента включения в исследование в контрольной группе на 5, 10, 90 день периода наблюдения или при внеплановом визите.
Вторичные переменные:
• сроки клинического купирования проявлений коронавирусной инфекции (измеряемые в сутках с момента начала лечения);
• количество пациентов с нежелательными явлениями (НЯ) и серьезными нежелательными явлениями (СНЯ) в группах исследования;
• иммунологические показатели пациентов основной и контрольной групп до начала лечения и на 10-е сутки терапии.
Количественные переменные представлены 95% ДИ для среднего, медианой, межквартильным диапазоном, минимальным и максимальным значением. Оценка распределения производилась по критерию Шапиро - Уилка. С учетом выявленного отсутствия нормальности распределения всех количественных переменных, а также размера доступной выборки пациентов (50 - в основной (опытной) группе, 30 - в контрольной), статистический анализ количественных переменных производился с использованием критерия Манна - Уитни. Критический уровень статистической значимости (р) - 0,05 (двусторонняя р).
РЕЗУЛЬТАТЫ
Медианный возраст пациентов в основной группе составил 9 (95% ДИ 8,12-9,37) лет, в контрольной -9 (95% ДИ 6,78-11,22) лет. Распределение по полу: в контрольной группе - 13 мальчиков (43,3%) и 17 девочек (56,7%), в опытной группе - 26 девочек (52,0%) и 24 мальчика (48,0%), статистически незначимые различия (p = 0,686).При сравнении групп до исследования статистически значимые различия выявлены для концентрации иммуноглобулинов Е (IgE) (p = 0,007, выше в контрольной группе), концентрации CD3+CD56+CD45+ (p = 0,044, выше в основной группе), доли (%) в лейкоцитарной формуле CD3-CD8+CD45+ (р = 0,002, выше в основной группе), доли (%) в лейкоцитарной формуле нейтрофилов (p < 0,001, выше в основной группе).
У пациентов проведен анализ различий в сроках купирования клинических проявлений новой коронавирусной инфекции. Выявлены статистически значимые различия с меньшими сроками купирования новой коронавирусной инфекции в основной группе (5,75 ± 0,771 и 6,56 ± 1,366, сут. для контрольной группы, р = 0,004).
У пациентов основной группы для всех изучаемых показателей, за исключением концентрации IgE (p = 0,415), достигнуты статистически достоверные изменения на фоне проводимой терапии (р < 0,05) (рис. 1).
 Рис. 1. Динамика концентрации иммуноглобулина Е (IgE) у пациентов основной группы по результатам 10 дней лечения
Рис. 1. Динамика концентрации иммуноглобулина Е (IgE) у пациентов основной группы по результатам 10 дней лечения
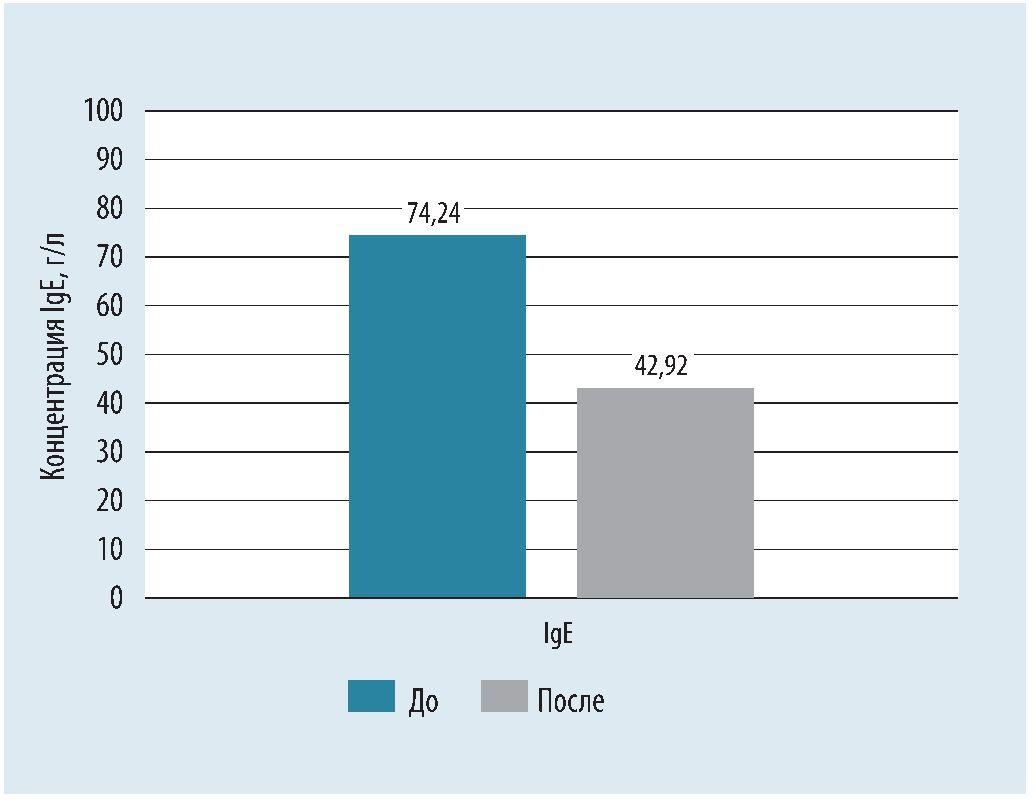
Примечание: * - уровень достоверности р < 0,05 на основании критерия Уилкоксона; Ig - иммуноглобулин.
Увеличение (рост) показателей выявлено для: концентрации IgA; концентрации IgG; концентрации IgM (рис. 2); концентрации Т-лимфоцитов (CD3+CD19-), Т-цитотоксических клеток (CD3+CD8+CD45+), NK-киллеров (CD3-CD56+CD45+), интестинальных интраэпителиальных лимфоцитов (CD3-CD8+CD45+), В-лимфоцитов (CD19+CD3-); доли (%) в формуле клеток CD3+CD8+CD45+, CD3+CD56+CD45+, CD3-CD56+CD45+, CD3-CD8+CD45+, CD19+CD3-; соотношения Т-хелперы/Т-цитотоксические клетки (CD3+CD4+/CD3+CD8+); концентрации лимфоцитов и их доли (%) в формуле (рис. 3).
Рис. 2. Динамика концентрации иммуноглобулинов у пациентов основной группы по результатам 10 дней лечения.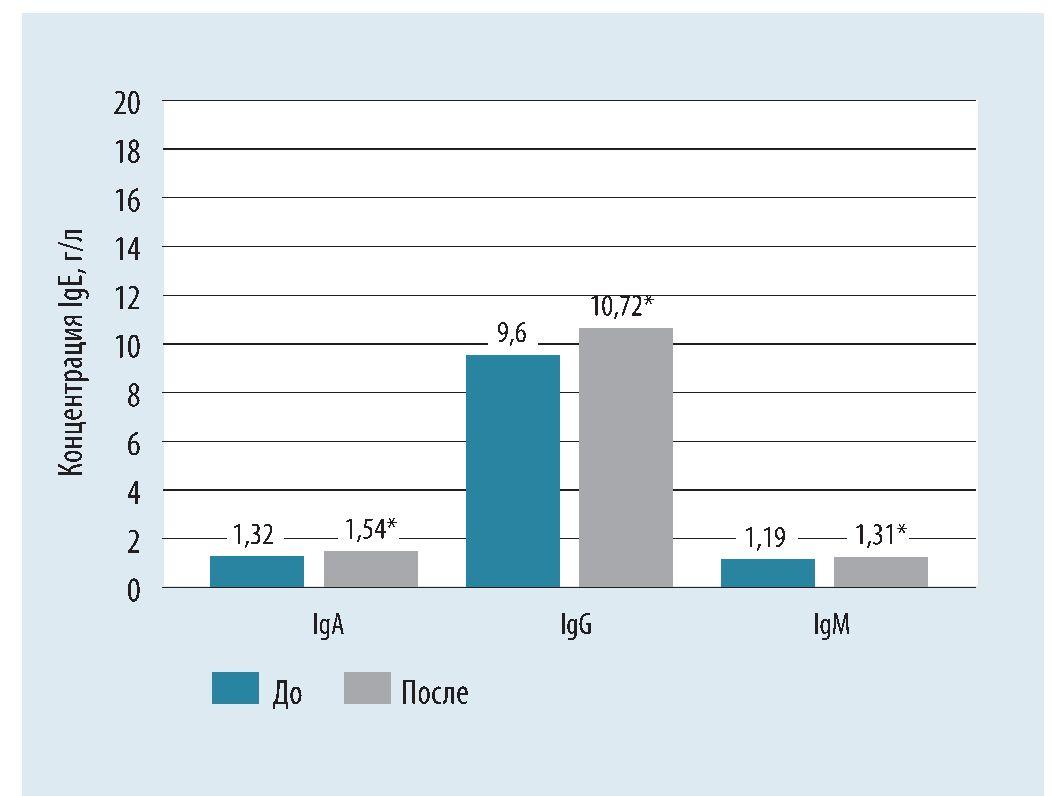
Примечание: * - уровень достоверности р < 0,05 на основании критерия Уилкоксона; Ig - иммуноглобулин.
Снижение показателей выявлено для: доли (%) Т-лимфоцитов (CD3+CD19-); нейтрофилов; концентрации лейкоцитов, нейтрофилов (рис. 3).
Рис. 3. Динамика иммунологических показателей у пациентов основной группы по результатам 10 дней лечения.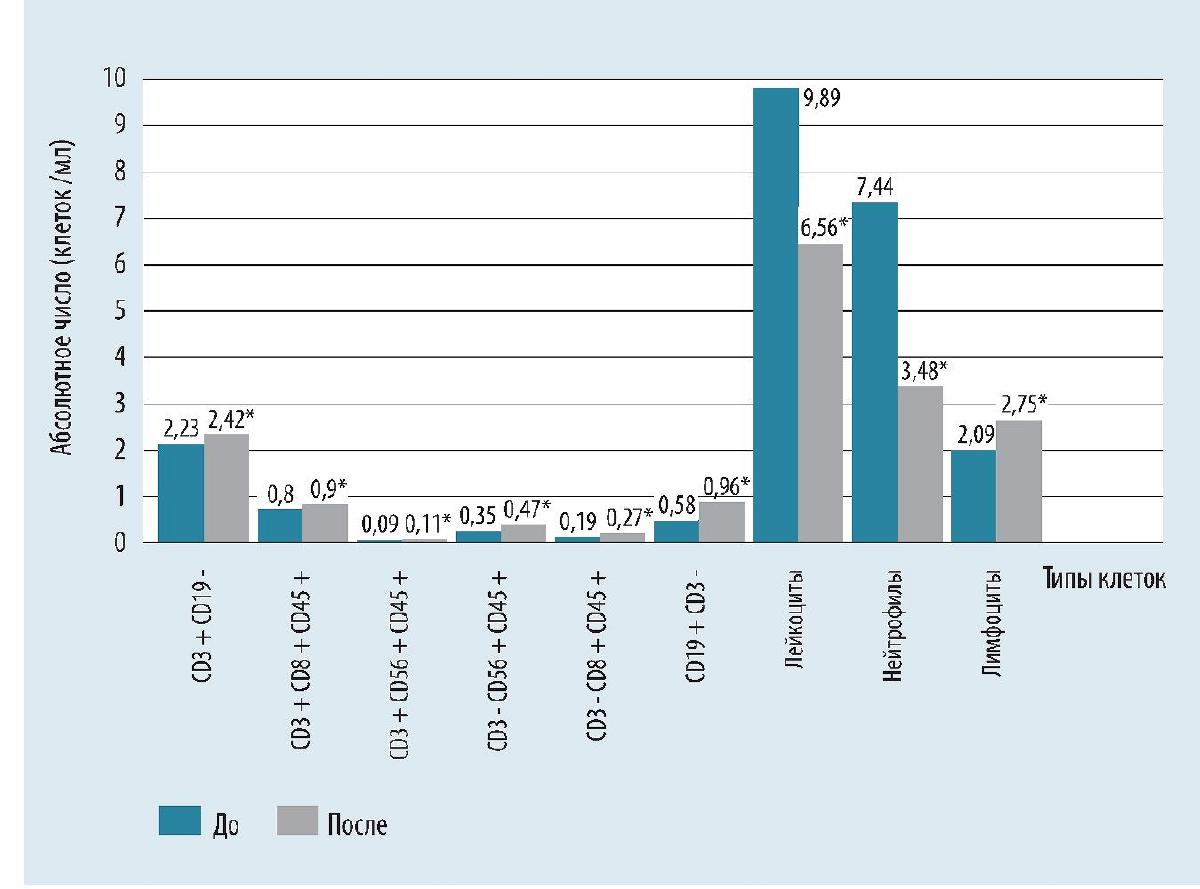
Примечание: * - уровень достоверности р < 0,05 на основании критерия Уилкоксона; Т-лимфоциты (CD3+CD19-); Т-цитотоксические клетки (CD3+CD8+CD45+); NKT-клетки (CD3+CD56+CD45+); NK-киллеров (CD3-CD56+CD45+); интестинальные интраэпителиальные лимфоциты (CD3-CD8+CD45+); В-лимфоциты (CD19+CD3-).
У пациентов контрольной группы для ряда изучаемых показателей достигнута статистически достоверная (р < 0,05) динамика. Увеличение (рост) показателей выявлено для доли (%) Т-цитотоксических клеток (CD3+CD8+CD45+), а также концентрации клеток и доли (%) NK-киллеров (CD3+CD56+CD45+). Снижение показателей выявлено для: соотношения Т-хелперы/Т-цитотоксические клетки (CD3+CD4+/ CD3+CD8+); доли (%) Т-лимфоцитов (CD3-CD19+) и нейтрофилов.
Учитывая сопоставимость групп исследования, была получена возможность сравнения количественных переменных по результатам 10 дней периода лечения и 90 дней периода наблюдения. Статистически значимые различия по итогам 10 дней лечения выявлены для ряда показателей: концентрация иммуноглобулинов М (IgM, p = 0,018, выше в основной группе), концентрация иммуноглобулинов Е (IgE, p = 0,011, выше в контрольной группе) (рис. 4, 5), концентрация В-лимфоцитов CD3+CD19+ (p = 0,015, выше в основной группе), концентрация клеток CD3+CD8+CD45+ (р = 0,005, выше в основной группе), концентрация клеток CD3+CD56+CD45+ (p = 0,009, выше в основной группе), концентрация клеток CD3-CD56+CD45+ (p = 0,001, выше в основной группе), концентрация клеток CD3-CD8+CD45+ (p < 0,001, выше в основной группе) и их доля в лейкоцитарной формуле (р = 0,039, выше в основной группе), концентрация и доля в лейкоцитарной формуле В-лимфоцитов CD19+CD3-(p < 0,001, выше в основной группе) (рис. 6).
Рис. 4. Динамика концентрации иммуноглобулинов у пациентов основной группы по результатам 10 дней лечения.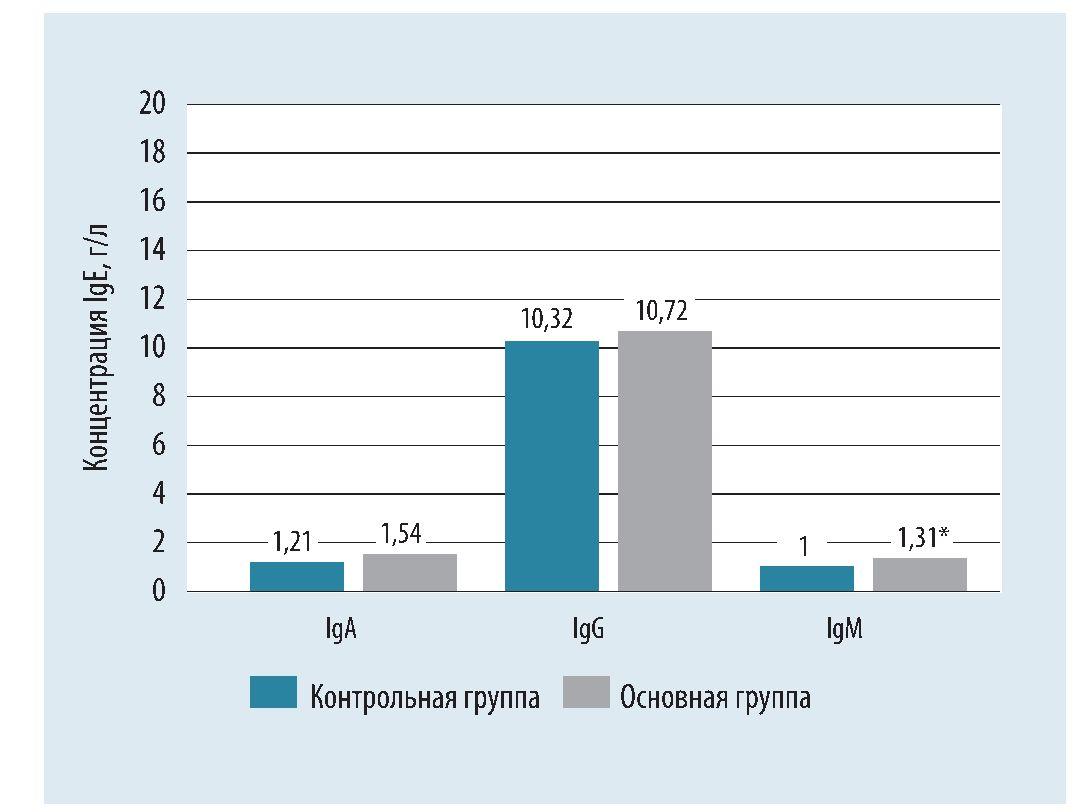
Примечание: * - уровень достоверности р < 0,05 на основании критерия Манна - Уитни; Ig - иммуноглобулин.
Рис. 5. Динамика концентрации иммуноглобулина Е (IgE) у пациентов основной группы по результатам 10 дней лечения.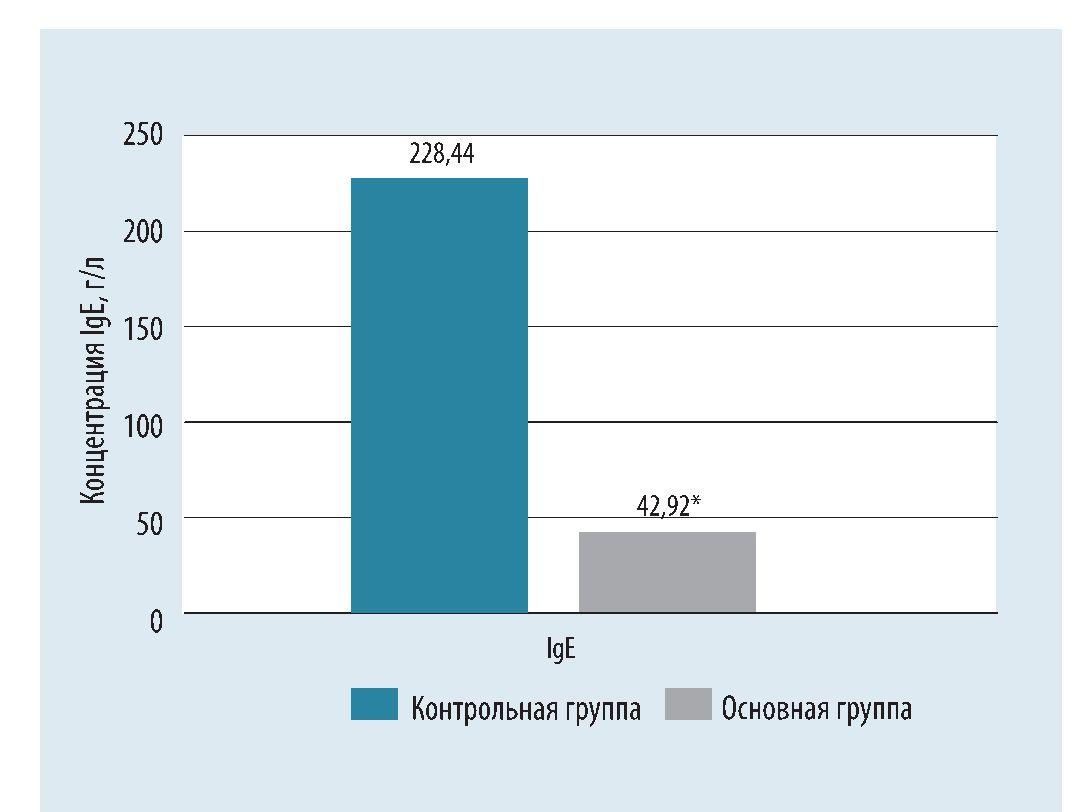
Примечание: * - уровень достоверности р < 0,05 на основании критерия Манна - Уитни; Ig - иммуноглобулин.
Рис. 6. Изменение иммунологических показателей у пациентов контрольной и основной группы по итогам 10 дней лечения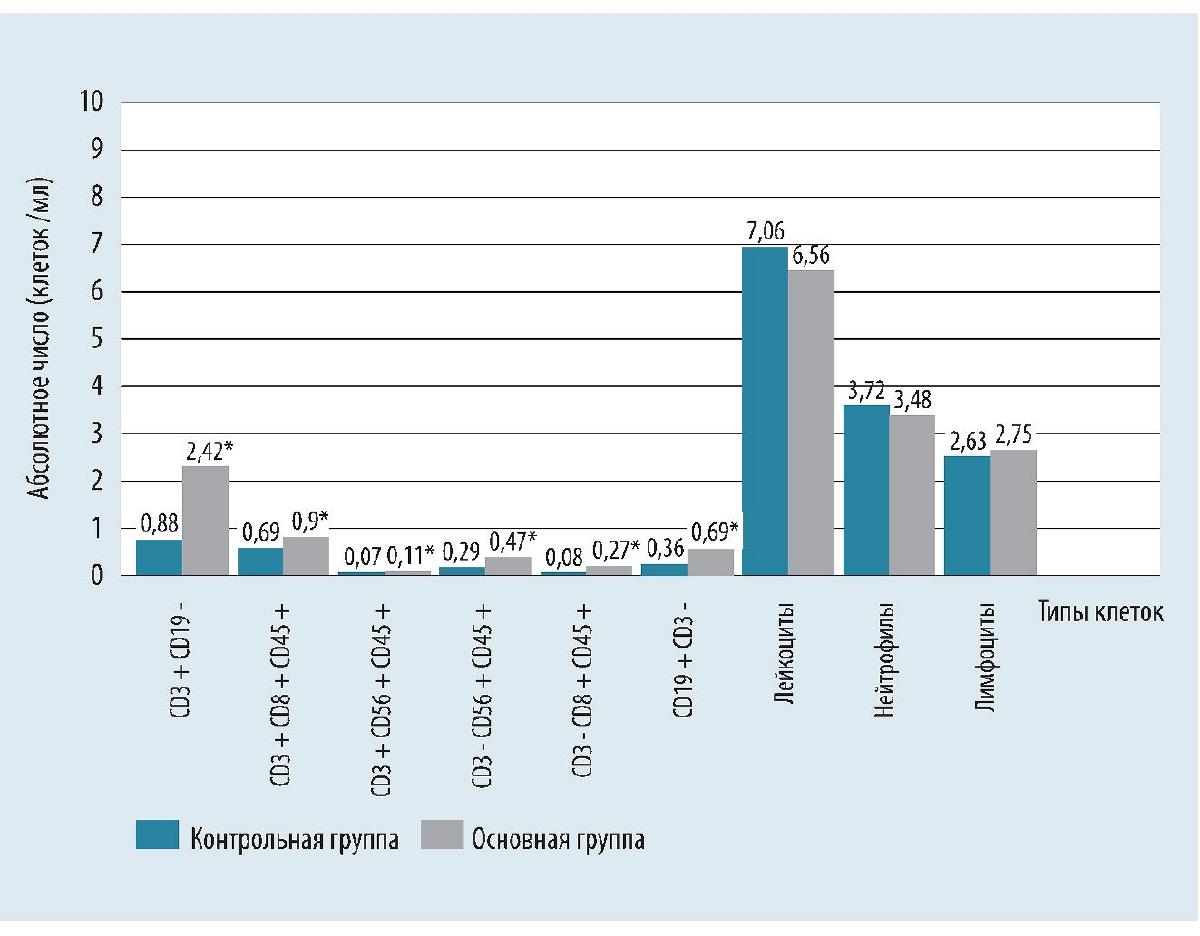
Примечание: * - уровень достоверности р < 0,05 на основании критерия Манна - Уитни; Т-лимфоциты (CD3+CD19-); Т-цитотоксические клетки (CD3+CD8+CD45+); NKT-клетки (CD3+CD56+CD45+); NK-киллеров (CD3-CD56+CD45+); интестинальные интраэпителиальные лимфоциты (CD3-CD8+CD45+); В-лимфоциты (CD19+CD3-).
Осложнения не были зарегистрированы (0%) ни в одной из групп сравнения, по данной причине статистическое сравнение их частоты невозможно. Данный исход не противоречит оценке исследуемого препарата как безопасного.
Нежелательных явлений в процессе приема препарата Галавит® в течение 10 дней лечения и 90 дней наблюдения не отмечалось.
ОБСУЖДЕНИЕ
SARS-CoV-2 оказывает комплексное иммуносупрессивное действие, включая снижение функциональной активности Т-лимфоцитов, NK-клеток и нарушение антителообразования В-лимфоцитами. Эти изменения способствуют затяжному течению инфекции и повышают риск вторичных бактериальных осложнений.
Галавит® (аминодигидрофталазиндион натрия) обладает селективным иммуномодулирующим действием, направленным на восстановление баланса между провоспалительными и противовоспалительными цитокинами [16]. Его механизм включает:
• регуляцию фагоцитарной активности макрофагов и нейтрофилов, что способствует завершенному фагоцитозу и элиминации вируса;
• ингибирование гиперпродукции ИЛ-1, ИЛ-6, TNF-a, что снижает риск цитокинового шторма;
• стимуляцию выработки эндогенных интерферонов (IFN-a, IFN-y) без провоспалительных побочных эффектов, характерных для экзогенных интерферонов;
• антиоксидантный эффект за счет подавления активных форм кислорода, что минимизирует повреждение тканей.
Механизм действия препарата связан со способностью избирательно регулировать (повышая или понижая в зависимости от исходных значений) функционально-метаболическую активность клеток врожденного и адаптивного иммунитета (макрофагов, нейтрофилов, натуральных киллеров и др.). Усиливая фагоцитарную активность макрофагов и моноцитов, бактерицидную активность нейтрофилов и цитотоксическую активность NK-клеток при ее исходном дефиците, препарат повышает неспецифическую резистентность организма к инфекционным заболеваниям бактериальной, вирусной и грибковой этиологии, способствует более быстрой элиминации возбудителя из организма, сокращает частоту, выраженность и длительность инфекций.
Препарат аминодигидрофталазиндион натрия (Галавит®) производства ООО Сэлвим (Россия), существующий на рынке с 1997 г. Галавит® выпускается в нескольких формах, одна из них Галавит® суппозитории ректальные 50 мг и в соответствии с утвержденной инструкцией по медицинскому применению (РУ ЛСР-002796/10) может применяться в качестве иммуномодулирующего и противовоспалительного средства в комплексной терапии у детей в возрасте от 6 до 12 лет с частыми рецидивирующими заболеваниями дыхательных путей и ЛОР-органов бактериальной и вирусной этиологии (частые ОРВИ, бронхит, пневмония, хронический тонзиллит, отит и аденоидит). Также препарат Галавит® используется для профилактики гриппа и ОРВИ.
В проспективном сравнительном исследовании применение Галавита® у детей 6-12 лет со среднетяжелым COVID-19 привело к:
1. Сокращению длительности заболевания (5,75 ± 0,771 сут. vs. 6,56 ± 1,366 сут. в контроле, p = 0,004).
2. Нормализации иммунологических параметров:
• повышение уровней IgM (p = 0,018), что указывает на усиление первичного гуморального ответа;
• более низкий уровень IgE у пациентов, получавших Галавит® (p = 0,011, выше в контрольной группе), может свидетельствовать о снижении избыточного иммунного ответа, что важно при COVID-19, где «гипервоспаление» (включая цитокиновый шторм) ухудшает течение болезни. Это согласуется с противовоспалительным действием препарата, которое модулирует иммунный ответ без избыточной активации ^2-зависимых реакций (связанных с аллергией и IgE);
• рост CD3+CD8+CD45+ цитотоксических Т-лимфоцитов (p=0,005) и NK-клеток (CD3-CD56+CD45+, p = 0,001), критичных для элиминации инфицированных клеток;
• увеличение В-лимфоцитов (CD19+CD3-, p < 0,001), что коррелирует с долгосрочным иммунитетом;
• изменение уровня нейтрофилов, лимфоцитов и лейкоцитов, описанное в исследовании, можно интерпретировать как положительное влияние препарата Галавит® на иммунный ответ у детей со среднетяжелой формой COVID-19. Нейтрофилы играют важную роль в воспалительном ответе, но их избыточная активность может способствовать повреждению тканей и усилению воспаления. Снижение уровня нейтрофилов может указывать на уменьшение воспалительного процесса, что соответствует противовоспалительному действию Галавита®. Это особенно важно при COVID-19, где «гипервоспаление» (например, цитокиновый шторм) является одним из ключевых патологических механизмов. Лейкоцитоз часто наблюдается при инфекционных заболеваниях как реакция на воспаление. Нормализация уровня лейкоцитов может свидетельствовать о снижении общей воспалительной нагрузки и улучшении контроля над инфекцией.
3. Отсутствию осложнений и нежелательных явлений, подтверждающему благоприятный профиль безопасности.
Препарат Галавит® эффективен для профилактики осложнений и лечения среднетяжелых форм COVID-19 при применении в составе комплексной терапии в сравнении со стандартной схемой терапии.
Учитывая тот факт, что в контрольной группе значимые изменения выявлены лишь для некоторых показателей, в то время как в основной - у всех, за исключением концентрации IgE. Данное обстоятельство может указывать на выраженное иммуномодулирующее влияние препарата аминодигидрофталазиндиона натрия.
Выявлено благоприятное модулирующее влияние аминодигидрофталазиндиона натрия на иммунный ответ при лечении коронавирусной инфекции (с увеличением концентрации отдельных видов Т- и В-лимфоцитов, а также иммуноглобулинов М). Суммарно данные факторы косвенно указывают на иммуномодулирующее воздействие аминодигидрофталазиндиона натрия.
Препарат Галавит® безопасен для иммуномодуляции у пациентов-детей с коронавирусной инфекцией.
ЗАКЛЮЧЕНИЕ
 Препарат Галавит® обладает многонаправленным (многоцелевым) фармакологическим механизмом действия, включающим модуляцию иммунной системы, противовоспалительное и антиоксидантное действие и регенеративный эффект. Его включение в комплексную терапию COVID-19 у детей позволяет сократить сроки болезни, снизить риск осложнений и минимизировать фармакологическую нагрузку.
Препарат Галавит® обладает многонаправленным (многоцелевым) фармакологическим механизмом действия, включающим модуляцию иммунной системы, противовоспалительное и антиоксидантное действие и регенеративный эффект. Его включение в комплексную терапию COVID-19 у детей позволяет сократить сроки болезни, снизить риск осложнений и минимизировать фармакологическую нагрузку.
Проведенное исследование продемонстрировало, что включение иммуномодулирующего препарата Галавит® в форме суппозиториев ректальных в состав комплексной терапии детей в возрасте 6-12 лет со среднетяжелой формой COVID-19 способствует повышению эффективности проводимого лечения за счет значительного сокращения длительности заболевания (5,75 ± 0,771 суток в основной группе против 6,56 ± 1,366 суток в контрольной группе, p = 0,004), а также нормализации ключевых иммунологических показателей, включая повышение уровней IgM, цитотоксических Т-лимфоцитов, NK-клеток и В-лимфоцитов. Это свидетельствует о положительном влиянии препарата на гуморальный и клеточный иммунный ответ при коронавирусной инфекции COVID-19.
Важно отметить, что в ходе исследования не было зарегистрировано нежелательных явлений или осложнений, что подтверждает благоприятный профиль безопасности Галавита®. Полученные данные обосновывают целесообразность включения препарата в комплексную терапию COVID-19 у детей для ускорения выздоровления.
Таким образом, Галавит® представляет собой перспективное средство для иммунокоррекции при среднетяжелых формах коронавирусной инфекции у детей. Дальнейшие исследования могут расширить область его применения при других респираторных инфекциях, что особенно актуально в условиях продолжающейся циркуляции SARS-CoV-2 и других патогенов.
Литература
1. WHO. Statement on the antigen composition of COVID-19 vaccines. 2024. [Электронный ресурс]. URL: www. who.int/news/item/18-05-2024-statement-on-the-antigen-composition-of-covid-19-vaccines
2. CDC. COVID-19 and Children: Trends in Hospitalizations. 2024. [Электронный ресурс]. URL: cdc.gov coronavirus/2019-ncov/science/science-briefs/children-hos-pitals.html
3. Brodin P. Immune modulation by SARS-CoV-2 in children // Nature Reviews Immunology. 2023. Vol. 2, No. 5. P. 289-301.
4. Respiratory viral co-infections in patients with COVID-19 and associated outcomes: A systematic review and meta-analysis / H. Krumbein [et al.] // Reviews in Medical Virology. 2023. Vol. 33, No. 1.
5. Мазанкова Л.Н., Горелов А.В., Нестеренко В.Г. Клиникоиммунологические особенности COVID-19 у детей школьного возраста // Педиатрия. Журнал им. Г.Н. Сперанского. 2023. Т. 102, № 3. С. 45-52.
6. A SARS-CoV-2 vaccine candidate would likely match all currently circulating variants / B. Dearlove [et al.] // Proceedings of the National Academy of Sciences. 2020. Vol. 117, No. 38. P. 23652-23662.
7. Antibody evasion by SARS-CoV-2 Omicron subvariants JN.1 and KP.2 / Wu Qian [et al.] // New England Journal of Medicine. 2024. Vol. 390, No. 12. P. 1123-1135.
8. Immune responses to SARS-CoV-2 infection in hospitalized pediatric and adult patients / C.A. Pierce [et al.] // Science Translational Medicine. 2020. Vol. 12, No. 564.
9. Мазанкова Л.Н., Горелов А.В., Нестеренко В.Г. Клинико-иммунологические особенности COVID-19 у детей школьного возраста // Педиатрия. Журнал им. Г.Н. Сперанского. 2023. Т. 102, № 3. С. 45-52.
10. Multisystem Inflammatory Syndrome in U.S. Children and Adolescents / L.R. Feldstein [et al.] // New England Journal of Medicine. 2020. Vol. 383, No. 4. P. 334-346.
11. Filippatos F., Tatsi E.B., Michos A. Immune response to SARS-CoV-2 in children: A review of the current knowledge // Pediatric Investing. 2021. Aug 17. Vol. 5, No. 3.
12. Mucosal immunity in COVID-19: A neglected but critical aspect of SARS-CoV-2 infection / M.W. Russell, Z. Moldo-veanu, P.L. Ogra, J. Mestecky // Frontiers in Immunology. 2020. Vol. 11. P. 611337.
13. Mapping systemic inflammation and antibody responses in multisystem inflammatory syndrome in children (MIS-C) / C.N. Gruber [et al.] // Cell. 2020. Vol. 183. P. 982-995.
14. Protective humoral immunity in SARS-CoV-2 infected pedi-atricpatients / Y. Zhang [et al.] // Cellular and Molecular Immunology. 2020. Vol. 17. P. 768-770.
15. Особенности клинических проявлений и лечения заболевания, вызванного новой коронавирусной инфекции (COVID-19) у детей, версия 2. 2020:73 : методические рекомендации // Министерство здравоохранения Российской Федерации. М., 2020.
16. Мазанкова Л.Н., Самитова Э.Р. Возможности использования многоцелевой терапии в лечении инфекционновоспалительных заболеваний в педиатрии // Практика педиатра. 2025. № 1. С. 45-51.

