Сравнительный анализ применения различных анестетиков и их комбинаций при спинномозговой анестезии
СтатьиОпубликовано в журнале:
Вестник интенсивной терапии »» N3 / 2000 А.А. Дроздов, С.В. Шахов, В.И. Дразнин, О.Н. Майоров, М.Н. Дроздова
Городская клиническая больница N 2 им. Н.А. Семашко. Медико-санитарная часть N 4. Самара
Со времени первоначального описания в 1899 году Августом Биром спинномозговая анестезия (СА) испытала и периоды популярности, и забвения. Популярность связана с несомненными достоинствами метода: простотой и доступностью, способностью надежно блокировать болевую импульсацию, обеспечением релаксации, предотвращением развития многих нейровегетативных реакций, сохраненным сознанием больного.
Учитывая вышеперечисленное, широкое применение находит СА как местноанестезирующими препаратами (МА), так и в сочетании с наркотическими анальгетиками (НА). Однако оба варианта не лишены недостатков: в первом случае - это короткий период анестезии, во втором - возможные осложнения и побочные реакции (Ф.Ф. Белоусов, 1977; А.В. Максимов, В.Х. Хейфед, Schuring, 1993). Осложнения и побочные эффекты при СА лидокаином, тримекаином, либо лидокаином в сочетании с НА морфинового ряда имеют место у 36,7% больных, причем у пятой части пациентов отмечается 2-3 осложнения одновременно на различных этапах лечения (А.А. Семенихин, В.Б. Шуматов, 1991). Поэтому повышение эффективности и безопасности СА является одной из основных проблем регионарного обезболивания.
Цель и задачи исследования
1. Изучить характер и течение СА, осложнения и побочные эффекты при использовании спинальных форм бупивакаина (Маркаин спинал и Маркаин спинал хэви).
2. Провести сравнительный анализ течения СА при использовании Маркаина с другими препаратами и их комбинациями при сходных методах проведения обезболивания.
Материалы и методы
Контрольную группу составили 68 больных урологического профиля, которым проводили СА:
- 1 подгруппа - 5% р-р тримекаина (100-120 мг);
- 2 подгруппа - 5% р-р тримекаина (100 мг) + Морадол 0,005 мкг/кг;
- 3 подгруппа - 5% р-р тримекаина (100 мг) + промедол 0,15 мг/кг;
- 4 подгруппа - 5% р-р тримекаина (100 мг) + фентанил 0,7 мкг/кг;
- 5 подгруппа - 5% тримекаин (100 мг) + морфин 10-14 мкг/кг;
- 6 подгруппа - 2% р-р лидокаина (100 мг).
Исследуемую группу составили 42 больных в возрасте от 18 до 77 лет (средний возраст в группе урологических больных составил 69,2+/-4,1 лет, в группах гинекологических и хирургических больных - 49,6+/-4,2 лет). Урологические и проктологические операции произведены у 26,4%; гинекологические (ампутация и экстирпация матки, пластические операции) - у 23,8% больных; хирургические операции (венэктомии, ампутации, операции на костях и суставах) составили 49,8%. В этой группе СА проводилась спинальными формами бупивакаина - Маркаином спинал и Маркаином спинал хэви, производимыми фирмой "Astra-Zeneca" (0,5% изобарическим раствором у 10 больных, 0,5% гипербарическим раствором - у 32 больных).
Условия подготовки больных, техника и обеспечение СА были идентичными во всех группах. Накануне производилась стандартная премедикация с использованием атарактиков и антигистаминпых препаратов. За 30 мин до операции осуществлялось введение седуксена (0,07-0,15 мг/кг). В операционной начиналась инфузия кристаллоидных препаратов 10-15 мл/кг (до начала введения анестетика инфузия составляла 700-1000 мл). За 15-20 мин до пункции в/м вводилось 0,5 мг атропина. В положении на правом боку пунктировалось субарахноидальное пространство на уровне L2-3-4-5 при помощи "стандартной" иглы типа Квинке-Бебкока G 20-22 длиной 80 мм срединным доступом по общим правилам. При поступлении ликвора в павильон иглы производилось ее вращение на 360° для подтверждения правильного местонахождения. Если ликвор не поступал из всех квадрантов, то это расценивалось как нахождение иглы рядом с дуральной муфтой и от введения анестетика отказывались, во избежание травмы и неадекватной блокады. Маркаин вводили в течение 1-2 мин, не смешивая с ликвором, в дозе 10-15 мг при операциях на нижних конечностях и 15-20 мг при полостных операциях. При использовании гипербарических растворов больному придавалось положение Фовлера под контролем уровня блока. После введения изобарического раствора больной находился в горизонтальном положении. Блок оценивали, исходя из правила дифференциальной блокады: уровень симпатической блокады находится выше уровня сенсорной, которая в свою очередь выше уровня моторной (разница приблизительно 2 сегмента). Сенсорный блок оценивали тестом с помощью иглы, моторный - по шкале Бромэджа. Мониторинг особенно тщательно осуществляли каждые 3 мин в течении первых 20 мин, учитывая факт постепенной фиксации МА структурами спинного мозга (Duthie, 1987; B.G. Covino, 1989). Производилось измерение АД, пульса и SpO2 (пульсоксиметр "ЭЛОКС 01С") выборочно-математический анализ ритма сердца с оценкой активности элементов вегетативной нервной системы на ритмкардиомониторе "ЭЛОН-001" (P.M. Баевский, Л.И. Калакутский, Э.С. Манелис; 1998).
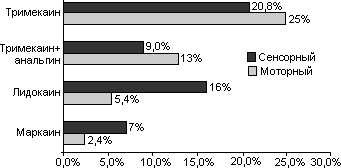
Рис. 1. Число случаев (в %) недостаточной силы блока
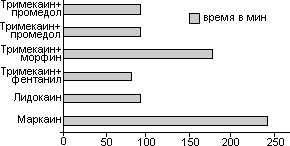
Рис. 2. Длительность блока
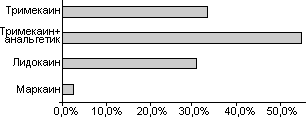
Pис. 3. Подключение вазопрессоров (% случаев)
Результаты и их обсуждение
В исследуемой группе в большинстве случаев блок развивался за 3-5 мин (в единичных наблюдениях 10-15 мин). В контрольной группе блок наступал за 5-7 мин.
Уровень блока при использовании Маркаина в дозе до 15 мг чаще находился на уровне пупка, либо на середине расстояния между пупком и лонным сочленением. При дозе выше 15 мг сенсорный блок развивался до уровня линии, соединяющей соски и выше на 1-3 см. В контрольной же группе при использовании тримекаина блок развивался до уровня реберной дуги, при СА другими комбинациями препаратов - до V ребра, при комбинации с морфином - до III ребра. Уровень сенсорного блока не имел четкой зависимости от уровня пункции. При СА Маркаином отмечался центральный седативный эффект примерно в 50% наблюдений.
Моторный блок в исследуемой группе оценивался как адекватный в 97,6% (++++), за исключением одного больного (2,4%). Сенсорный блок считался недостаточным когда по уровню не соответствовал ожидаемому, либо когда возникала необходимость в/в введения НА, кетамина и др. Сравнительные данные по группам приведены на рис. 1.
Эффективность блока в исследуемой группе подтвердили результаты математического анализа ритма сердца: ИНБ = 11+/-2,3; СИМ = 2+/-0,9; ПАР = 2,4+/-2,3; МО = 780+/-8,6; АМО = 11+/-1,1; АХ = 352+/-4,3 (все показатели достоверно не отличались от контрольных величин).
Длительность блока (рис. 2.) при СА Маркаином составила 3,5-4 ч, тримекаином - 50-55 мин, лидокаином -1,5 ч, в комбинациях тримекаин + промедол или Морадол - 85 мин, тримекаин + фентанил - 80 мин, тримекаин + морфин - 2,5-3 ч соответственно.
В контрольной группе чаще имели место эпизоды нестабильной гемодинамики: снижение АД на 50-60 мм рт.ст. и урежение ЧСС могло произойти на любом этапе операции и ближайшего послеоперационного периода. Особенно это отмечено в группах с применением опиоидов (АД снижалось на 60-70 мм рт.ст).
В связи с этим больным контрольной группы проводилась инфузия коллоидов, а приблизительно половине - коррекция выраженной брадикардии атропином.
В исследуемой группе изменения гемодинамики носили более мягкий и управляемый характер: АД снижалось в первые 20 мин, после чего относительно стабилизировалось, а введение атропина потребовалось не более чем в 20% случаев. Анестезия Маркаином характеризовалась мягкостью и предсказуемостью: коллоиды применялись в 2 случаях по поводу кровотечения, вазопрессоры - всего в 1 случае (рис. 3.).
В контрольной группе отмечено 3 случая депрессии дыхания (при введении морфина), в то время как в исследуемой группе нарушения дыхания не отмечено.
К осложнениям мы отнесли выраженную гипотонию до 60 мм рт.ст и ниже (в контрольной группе 20,6%, в исследуемой - 2,4%). Некоторые осложнения наблюдали только у больных контрольной группы: раннюю и позднюю респираторную депрессию (2,9% больных), позднюю гипотонию (2,9%), дезориентацию и нарушение сознания (5,9%). К побочным эффектам были отнесены постпункционные головные боли (ПГБ), тошнота, рвота, транзиторные расстройства мочеиспускания, кожный зуд. Побочные эффекты тоже были более выражены в контрольной группе. В исследуемой группе (Маркаин) не отмечались ПГБ, наблюдался один случай мышечной дрожи (купировался введением сульфата магния), один случай непроизвольного мочеиспускания у женщины через 12 ч после ампутации матки, не потребовавший терапии.
Выводы
1. Маркаин (спинальные формы - Маркаин спинал и Маркаин спинал хэви) показал себя как адекватный и безопасный анестетик для эффективной длительной моноанестезии.
2. При использрвании у перечисленных нозологических единиц он не требует дополнительной пролонгации, комбинации с анальгетиками и уменьшения дозы в связи с токсичностью.
3. Данные приведенного клинического исследования обосновывают необходимость более широкого применения спинальных форм Маркаина и замены ими ранее применявшихся препаратов для спинальной анестезии.
