Лактофильтрум в комплексной терапии атопического дерматита взрослых: двойное слепое плацебо-контролируемое рандомизированное сравнительное исследование
Статьи Опубликовано в журнале:
« СОВРЕМЕННЫЕ ПРОБЛЕМЫ ДЕРМАТОВЕНЕРОЛОГИИ,
ИММУНОЛОГИИ И ВРАЧЕБНОЙ КОСМЕТОЛОГИИ », №6, 2010г.
Перламутров Ю. Н., Ольховская К. Б., Аматуни Э. А., Дукова Е. Л., Московский Государственный Медико-стоматологический Университет
Дворников А. С., Круглова Л. С. , Кожно-венерологический клинический диспансер № 1 Департамента здравоохранения г. Москвы
Целью исследования являлось изучение эффективности и безопасности применения лактофильтрум в комплексном лечении атопического дерматита у взрослых. Обследовано 89 больных атопическим дерматитом со средне тяжелым и тяжелым течением (30 женщин и 59 мужчин, средний возраст 25,69 ± 5,86 лет), разделенных на две сопоставимые группы в соответствии с получаемой терапией. В 1 группе больные получали стандартное лечение в сочетании с лактофильтрум, во второй — стандартное лечение и плацебо.
Оценивались тяжесть течения заболевания, распространенность поражения кожи, интенсивность зуда, качество жизни больных до начала лечения, после трех недель лечения и через месяц после окончания лечения.
В результате двойного слепого, плацебо контролируемого, рандомизированного исследования показано, что применение препарата лактофильтрум в комплексной терапии атопического дерматита способствует повышению эффективности лечения. Выраженное клиническое улучшение, отмеченное у больных в 56,7% случаев, сопровождалось депрессией средних значений индекса SCORAD на 71,94%, устранением дневного и ночного зуда у пациентов в 50% случаев и улучшение качества жизни на 76,41%, что было значительно выше, чем во 2 группе больных. Сделан вывод о целесообразности применения лактофильтрум в комплексной терапии больных атопическим дерматитом.
Ключевые слова: атопический дерматит, лечение, применение лактофильтрум.
Введение
Согласно современным представлениям, атопический дерматит — это генетически обусловленное, хроническое, рецидивирующее заболевание кожи [1]. Реализации генетической предрасположенности способствуют различные триггерные факторы как аллергенной, так и неаллергенной природы: нерациональное питание, хронические заболевания желудочно-кишечного тракта, патология ЛОР-органов и наличие других очагов инфекции, контакт с аэроаллергенами, высокая обсеменённость кожи золотистым стафилококком и дрожжеподобными грибами [2]. В целом, у детей раннего возраста (до 3 – 5 лет) наиболее вероятно наличие пищевой аллергии, в то время как внешнесредовые аэроаллергены, очевидно, вносят наибольший вклад в развитие атопического дерматита у детей старшего возраста (от 5 до 12 лет), а факторы инфекционной природы — у подростков и взрослых [3 – 5].
На сегодняшний в день основным в базисной терапии атопического дерматита помимо увлажнения кожи является элиминация причинно-значимых аллергенов преимущественно с помощью энтеросорбции и назначением пробиотиков [6,7].
Энтеросорбция является неинвазивным методом связывания и выведения из организма аллергенов, медиаторов, продуктов аллергической реакции, метаболитов, токсинов, активных перекисных соединений, условно-патогенной флоры и вирусов [8]. Энтеросорбция осуществляется введением в кишечный тракт различных твердых или жидких соединений естественного или искусственного происхождения, обеспечивающих поглощение, связывание и удаление экзогенных и эндогенных токсинов, и направлена на детоксикацию организма и восстановление его реактивности. При этом используются как прямые (непосредственные), так и опосредованные эффекты энтеросорбции [9].
Прямые эффекты энтеросорбции обеспечиваются различными физико-химическими механизмами (адсорбции, абсорбции и хемосорбции, ионообмена и комплексирования), протекающими на активной поверхности различных пористых систем при движении энтеросорбента в просвете кишки. При этом молекулы небольшого размера сорбируются преимущественно в микропорах с радиусом менее 1,5 нм, молекулы средней и высокой массы поглощаются мезопорами с радиусом от 1,5 до 200 нм, а субклеточные надмолекулярные структуры и клетки сорбируются в макропорах с радиусом более 200 нм [10,11].
Опосредованные эффекты энтеросорбентов обеспечиваются за счёт ослабления и предотвращения аллергического воспаления, профилактики эндо-и экзотоксикозов, уменьшения метаболической нагрузки на выделительную систему, коррекции обменных процессов и иммунного статуса больного, восстановление целостности и проницаемости слизистых оболочек, улучшение функционального состояния кишечника [12 – 14]. В свою очередь в многочисленных исследованиях была доказана эффективность комплексной терапии атопического дерматита с использованием пробиотиков [15 – 17]. Использование этих препаратов приводит к нормализации микробиоты кишечника, что в свою очередь оказывает положительное влияние иммунную реактивность организма, улучшая прогноз течения АД [18 – 20].
В таблетки лактофильтрум входят в качестве активных веществ 355 мг лигнина гидролизного и 120 мг лактулозы; вспомогательные вещества — натрия кроскармеллоза, магния стеарат. Фармакологическое действие препарата обусловлено свойствами, входящих в его состав активных компонентов. Лигнин гидролизный — природный энтеросорбент, состоящий из продуктов гидролиза компонентов древесины, обладает высокой сорбирующей активностью и неспецифическим дезинтоксикационным действием. Связывает в кишечнике и выводит из организма патогенные бактерии и бактериальные токсины, лекарственные препараты, соли тяжёлых металлов, алкоголь, аллергены а также избыток некоторых продуктов обмена веществ, в том числе билирубин, холестерин, гистамин, серотонин, мочевину, иные метаболиты, ответственные за развитие эндогенного токсикоза. Не токсичен, не всасывается, полностью выводится из кишечника в течение 24 ч. Лактулоза — синтетический дисахарид, молекула которого состоит из остатков галактозы и фруктозы. В желудке и верхних отделах кишечника не всасывается и не гидролизуется. Высвобождающаяся из таблеток в толстом кишечнике в качестве субстрата ферментируется нормальной микрофлорой кишечника, стимулируя рост бифидобактерий и лактобацилл. В результате гидролиза лактулозы в толстом кишечнике образуются молочная, уксусная и муравьиная органические кислоты, подавляющие рост патогенных микроорганизмов и уменьшающие продукцию азотсодержащих токсических веществ. Описанный процесс приводит к увеличению осмотического давления в просвете толстого кишечника и стимулированию перистальтики. Комплексное действие препарата направлено на нормализацию микробиоценоза толстого кишечника и снижение интенсивности эндогенных токсических состояний.
Целью исследования являлось изучение эффективности и безопасности применения лактофильтрум в комплексном лечении атопического дерматита у взрослых.
Материал и методы исследования
В результате скринингового обследования в исследование вошло 89 больных атопическим дерматитом со среднетяжёлым и тяжёлым течением (30 женщин (33,71%) и 59 мужчин (66,29%)). Средний возраст пациентов составил 25,69±5,86 лет, при этом средний возраст женщин равнялся 26,17±5,82, мужчин — 25,28±6,05, что свидетельствовало о соответствии групп мужчин и женщин по возрасту.
Все больные были рандомизированы на две группы в зависимости от проводимого лечения (табл. 1).
Таблица 1.
Распределение больных по группам
| I группа n=44 | II группа n=45 |
|---|---|
| Пациенты, получающие стандартную терапию (антигистаминные, десенсибилизирующие препараты, наружные средства, содержащие ГКС) в комплексе с препаратом Лактофильтрум® (по 2 таб. 3 раза в день, в течение 21 дня | Пациенты, получающие cтандартную терапию (антигистаминные, десенсибилизирующие препараты, наружные средства, содержащие ГКС) в комплексе с плацебо (по 2 табл. 3 раза в день, в течение 21 дня) |
Критерии включения пациента в исследование:
- возраст от 18 до 60 лет с установленным диагнозом атопический дерматит в фазе обострения средней или тяжёлой степени;
- индекс SCORAD >25 (среднее и тяжёлое течение);
- наличие подписанного и датированного информированного согласия пациента на участие в исследовании.
- любые тяжёлые, декомпенсированные или нестабильные соматические заболевания или состояния, которые, угрожают жизни больного или ухудшают прогноз заболевания (анемия, сахарный диабет);
- другие сопутствующие заболевания, которые требуют назначения системных кортикостероидов, цитостатиков, иммуносупрессантов, антиметаболитов, антицитокиновых препаратов и / или местной терапии в ходе исследования: паразитарные заболевания, диффузные заболевания соединительной ткани, лимфомы кожи, лимфогранулематоз, чесотка, красный плоский лишай, псориаз;
- беременность и кормление грудью;
- гиперчувствительность к препарату Лактофильтрум®;
- одновременный приём менее чем за 2 недели до включения пациента в исследование сорбентов, пре- и пробиотиков;
- одновременный приём, как сопутствующей терапии менее чем за 2 недели до включения пациента в исследование нейролептиков и транквилизаторов;
- острая психотическая продуктивная симптоматика (галлюцинация, бред);
- профессиональная деятельность пациента, связанная с частыми травмами кожи, переохлаждением, инсоляцией, воздействием ультрафиолетового излучения;
- участие в другом клиническом исследовании в последние 30 дней.
Распространённость поражения кожи оценивалась по правилу «девятки», где за единицу принята площадь ладонной поверхности кисти. Общая сумма округляется с точностью до 5 баллов. Общая сумма может составить от 0 баллов (отсутствие кожных поражений) до 96 – 100 баллов при тотальном поражении кожи. Каждый субъективный симптом оценивался в диапазоне от 0 до 10 баллов; баллы суммировались. Сумма баллов субъективных симптомов может колебаться от 0 до 20.
Индекс SCORAD рассчитывался по формуле:
SCORAD=А / 5+7В / 2+С,
где А — распространённость поражения кожи, В — сумма уровней интенсивности клинических симптомов атопического дерматита, С — сумма оценок субъективных нарушений по визуальной аналоговой шкале.
Значения индекса могут варьироваться от 0 — нет заболевания до 103 — максимально тяжёлое течение атопического дерматита. Через месяц от начала исследования проводилась оценка терапевтического эффекта, пользуясь категориями приведённой ниже 6-балльной шкалы (табл. 2.).
Индекс терапевтического эффекта (ИТЭ) на каждого пациента выражался в процентах и оценивался в баллах. Расчёты производились по следующей формуле: 100 х (базовое общее число элементов — конечное общее число элементов): базовое число элементов. Лечебным эффектом считалось полное исчезновение или уменьшение индекса SCORAD на 50% и больше, т. е. согласно приведенной выше шкале только 1, 2 и 3 балла.
В связи с тем, что зуд является основным симптомом атопического дерматита, всем пациентам на каждом визите проводилась оценка интенсивности зуда при помощи 5-балльной шкалы BRS (Behavioral rating scores.)?, которая учитывает степень дискомфорта в дневное и ночное время.
Оценка качества жизни больных проводилась при помощи специального анамнестического анкетного средства — ДИКЖ [22]. Данный индекс применяется дерматологами для оценки степени негативного влияния кожного заболевания на различные аспекты жизни больного, характеризующие в целом его качество жизни. ДИКЖ может быть использован как один из критериев оценки эффективности терапии кожного заболевания у конкретного больного.
Цифровой индекс, получаемый в результате ответов на все вопросы анкеты, отражает степень негативного влияния симптомов болезни на качество жизни больного: чем выше индекс, тем сильнее болезнь «ухудшает» качество жизни.
Максимальный индекс равен 30.
Таблица 2.
Оценка терапевтического эффекта
| Балл | Описание |
|---|---|
| 1 | Чисто (полное исчезновение признаков и симптомов заболевания по сравнению с исходным уровнем) |
| 2 | Отличное улучшение (уменьшение на 75% и более признаков и симптомов заболевания по сравнению с исходным уровнем) |
| 3 | Хорошее улучшение (уменьшение на 50 – 75% признаков и симптомов заболевания по сравнению с исходным уровнем) |
| 4 | Умеренное улучшение (уменьшение на 50% признаков и симптомов заболевания по сравнению с исходным уровнем) |
| 5 | Без улучшения (отсутствие уменьшения признаков и симптомов заболевания по сравнению с исходным уровнем) |
| 6 | Ухудшение (ухудшение признаков и симптомов заболевания по сравнению с исходным уровнем) |
Для оценки безопасности исследуемого препарата проводились лабораторные исследования крови и мочи, которые оценивались как нежелательные явления в том случае, если они являлись клинически значимыми. Также в исследовании фиксировались все нежелательные явления, которые происходили с пациентом после приёма первой дозы исследуемого препарата и до окончания исследования.
Статистический анализ полученных данных был проведен с учетом (intention-to-treat) и без учета преждевременно выбывших испытуемых. Был выполнен описательный анализ количественных и порядковых данных с расчётом значений среднего арифметического (M), стандартного отклонения (SD), 95% доверительного интервала (ДИ) для среднего, медианы (Med) и интерквартильного размаха (IQR) для всех экспериментальных групп. Распределение качественных переменных представлено в виде значений выборочной доли (W), её стандартной ошибки (SE) и 95% ДИ для доли.
Статистический анализ полученных данных выполнен с использованием программных пакетов SPSS 17.0.
Дизайн исследования: двойное слепое, плацебо контролируемое, рандомизированное, сравнительное исследование IV фазы в параллельных группах у пациентов. Исследование включало три периода, общей продолжительностью 54±3 дня: период скрининго-вого обследования (0 – 3 дня), период активного лечения исследуемым препаратом (21±3 дня), период последующего наблюдения (30±3 дня) (рис. 1).
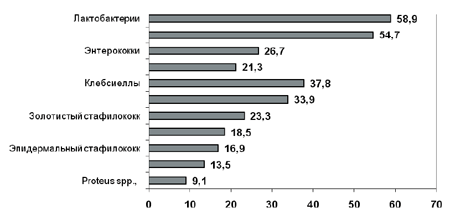
Рис. 1. Дизайн исследования
Результаты исследования и их обсуждение
При проведении скринингового обследования все больные перед включением в исследование находились в стадии обострения атопического дерматита и предъявляли жалобы на зуд различной интенсивности и высыпания. Нарушение сна вследствие наличия ночного зуда отмечали 76 больных, а сухость кожи — 47 пациентов.
Исходные значения SCORAD у всех пациентов в среднем составили 45,03±11,43 (среднетяжёлое течение) при этом средние значения SCORAD у мужчин составили 46,08±11,23, у женщин — 42,96±11,73. При анализе течения атопического дерматита тяжёлое течение АД (SCORAD > 40 баллов) регистрировалось у 54 больных (60,67%), а среднетяжёлое (SCORAD от 15 до 40 баллов) — у 35 пациентов (39,33%).
При оценке степени нарушения качества жизни у пациентов было установлено, что средние значения индекса ДИКЖ составили 11,17±6,65 баллов, что отражало средний уровень снижения социальной адаптации вследствие наличия дерматоза.
Всем пациентам в каждой группе, для оценки результатов лечения, в период активного наблюдения (визит 1 — начало исследования, визит 2 — через 10±3 дня от начала лечения, визит 3 — через 11±3 дней от второго визита) и в период продолженного наблюдения (визит 4 — через 30±3 дня после окончания курса лечения (визита 3) производили оценку индекса SCORAD и интенсивности зуда. Во время 3 визита также производилась оценка терапевтического эффекта. Результаты изучения динамики клинических проявлений представлены в таблице 3.
Таблица 3.
Динамика средних значений индекса SCORAD у больных в результате лечения
| Визит | I группа | II группа |
|---|---|---|
| 1 | 42,23+11,36 | 35,94+11,39 |
| 3 | 11,85+5,56#* | 20,55+7,77* |
| 4 | 4,31+1,58#* | 13,10+6,34* |
| * — различия достоверны между группами по t-критерию при р # - различия достоверны в группе больных в результате лечения по t-критерию при р | ||
Таким образом, в первой группе больных у большинства пациентов (56,75%) наблюдалось разрешение и снижение интенсивности высыпаний более чем на 75%, а отсутствие пациентов, имеющих либо слабый положительный ответ, либо ухудшение в результате проводимого лечения, свидетельствовало о высокой эффективности комплексной терапии АД с использованием препарата лактофильтрум.
Оценка терапевтического эффекта во второй группе больных, которым был назначен стандартный курс терапии, показала среднюю эффективность (рис. 3).
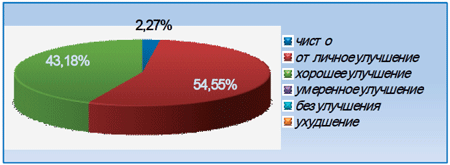
Рис. 2. Оценка результатов лечения у больных первой группы
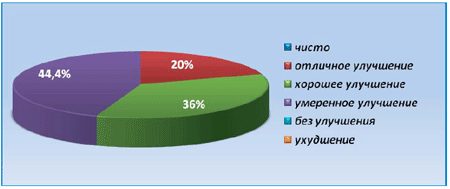
Рис. 3. Оценка результатов лечения у больных второй группы
Как видно из рисунка, разрешение кожного процесса до полного отсутствия высыпаний не наблюдалось ни у одного больного, отличное улучшение зарегистрировано у 9 пациентов (20%), хорошее улучшение — у 16 (35,56%), у остальных 20 больных (44,44%)) — отмечено умеренное улучшение.
Анализ динамики индекса SCORAD в первой группе больных показали, что проведение комплексной терапии способствовало достоверному снижению индекса в среднем с 42,23±11,36 до 11,85±5,56 баллов (рПри оценке терапевтического эффекта в первой группе больных очищение кожных покровов от высыпаний в результате применения препарата Лактофильтрум отмечалось у 1 больного (2,27%), отличное улучшение — у 24 (54,55%), хорошее улучшение — у 19 (43,18%) больных; умеренное улучшение, отсутствие улучшения и ухудшение — в этой группе больных не зарегистрировано (рис. 2).
Отсутствие улучшения и ухудшение не наблюдалось ни у одного больного. Динамика интенсивности зуда в соответствии со шкалой BRS приведена в таблице 4.
Таблица 4.
Динамика средних значений интенсивности зудау больных в результате лечения
| Визит | I группа | II группа | ||
|---|---|---|---|---|
| Интенсивность дневного зуда | Интенсивность ночного зуда | Интенсивность дневного зуда | Интенсивность ночного зуда | |
| 1 | 2,72+0,63 | 1,35+0,90 | 2,93+0,65 | 1,69+0,11 |
| 2 | 1,44+0,13#* | 0,44+0,15#* | 2,13+0,72 | 1,13+0,12 |
| 3 | 0,53+0,05#* | 0,05+0,01#* | 1,35+0,83 | 0,58+0,10# |
| 4 | 0,12+0,05#* | 0,05+0,003#* | 1,18+0,86# | 0,35+0,090 |
| * — различия достоверны между группами по t-критерию при р #- различия достоверны в группе больных в результате лечения по t-критерию при р | ||||
Как следует из таблицы, снижение интенсивности зуда в первой группе больных происходило быстрее, чем в группе сравнения. Уже на 10 сутки терапии с использованием препарата лактофильтрум в первой группе больных отмечалось достоверное уменьшение и дневного (с 2,72±0,63 до 1,44±0,13 баллов (рПереносимость лечения в обеих группах была хорошей, отрицательной динамики в результатах лабораторных тестов (клинический анализ крови и мочи) не зарегистрировано, аллергических реакций и других нежелательных явлений не отмечено.
Снижение качества жизни прослеживается у большинства больных с дерматозами. Наиболее выраженное нарушение социальной адаптации и сексуальной жизни отмечается среди больных, у которых имеются дерматозы, сопровождающиеся зудом и высыпаниями на открытых участках кожи. Субъективная оценка больными влияния атопического дерматита на жизнедеятельность проводилась в настоящем исследовании с помощью соответствующего вопросника и определения дерматологического индекса качества жизни (ДИКЖ) (табл. 5).
Таблица 5.
Динамика средних значений ДИКЖ у больных в результате лечения
| Визит | Группа 1 | Группа 2 |
|---|---|---|
| 1 | 9,37+5,89 | 12,89+6,95 |
| 2 | 5,65+4,59* | 11,07+7,86 |
| 3 | 2,21+1,03#* | 8,20+6,87 |
| 4 | 0,93+0,04#* | 6,49+6,28 |
| * — различия достоверны между группами по t-критерию при р #- различия достоверны в группе больных в результате лечения по t-критерию при р | ||
Аналогично данным о динамике индекса SCORAD и BRS наиболее выраженное снижение ДИКЖ было зарегистрировано в группе больных, получавших комплексное лечение с использованием препарата лактофильтрум. Уже через 10 дней от начала исследования в этой группе было отмечено достоверное улучшение качества жизни пациентов на 39,5%, а к концу проводимой терапии — на 76,41%. В группе сравнения, где применяли плацебо, снижение ДИКЖ к концу лечения составило только 36,4%. В период наблюдения на фоне положительной динамики клинических проявлений атопического дерматита также регистрировалось и снижение индекса ДИКЖ в обеих группах, однако, в группе сравнения через месяц после окончания лечения индекс был достоверно выше, чем в группе, где применялся лактофильтрум.
Заключение
В результате исследования выявлено, что течение атопического дерматита у взрослых характеризуется тяжёлым и среднетяжёлым течением дерматоза, при этом у мужчин отмечается сравнительно более тяжёлое течение.
Основными жалобами больных при этом заболевании являлись ночной и дневной зуд, а также сухость кожи, что существенно отражается на качестве жизни пациентов (ДИКЖ — 11,17±6,65 баллов — средний уровень снижения социальной адаптации).
Показано, что применение препарата лактофиль-трум в комплексной терапии атопического дерматита способствует повышению эффективности лечения. Выраженное клиническое улучшение, отмеченное у больных в 56,7% случаев, сопровождалось депрессией средних значений индекса SCORAD на 71,94%, устранением дневного и ночного зуда у пациентов в 50%случаев и улучшение качества жизни на 76,41%. В группе больных, где проводилась комплексная терапия с использованием плацебо, выраженное клиническое улучшение отмечено только в 20% случаев, индекс SCORAD, в среднем, снизился на 56,98%, устранением зуда отмечено в 15,5% случаев, качество жизни улучшилось на 36,38%.
Быстрое и стойкое устранение клинических симптомов атопического дерматита, а также безопасность проводимого лечения позволяют считать целесообразным проведение комплексной терапии данной категории больных с использованием препарата лактофильтрум. Литература 1. Hanifi n J. M., Rajka G. Diagnostic features of atopic dermatitis. Acta Derm. Venereol. (Stockh). 1980; 92 (Suppl.) 44 – 47.
2. Crossen J. R. Psychological assessment and treatment of patients with atopic dermatitis. Dermatol. Therapy 1996;1: 94 – 103.
3. Sicherer S. H., Sampson H. A. Food hypersensitivity and atop-ic dermatitis: Pathophysiology, epidemiology, diagnosis, and management. J. Allergy Clin. Immunol. 1999; 104: 114 – 122.
4. Clark R. A. F., Adinoff A. D. The relationship between positive aeroallergen patch test reaction and aeroallergen exacerbations of atopic dermatitis. Clin. Immunol. Immunopathol. 1989; 53 (Suppl): 132 – 140.
5. Ohnishi Y., Okino N., Ito M. et al. Ceramidase activity in bacterial skin fl ora as a possible cause of ceramide defi -ciency in atopic dermatitis. Clin. Diagn. Lab. Immunol. 1999;6:101 – 104.
6. Сергеев Ю. В., Иванов О. Л., Новиков Д. К. Атопический дерматит: современная диагностика и лечение. Иммунопатол., аллергол., инфектол. 2001; 4: 28 - 48.
7. Аряев Н. Л., Клименко В. А. Атопический дерматит у детей. Киев; 2006.
8. Нагорная Н В., Лимаренко М. П., Логвиненко Н Г. и соавт. Одновременное проведение энтеросорбции и коррекции дисбиоза кишечника у детей с атопическим дерматитом препаратом «Лактофильтрум». In: Використання методу ентеросорбції у лікувальній практиці. Збірник постмаркетингових клінічних досліджень препарату «Лактофільтрум». Киiв; 2008: 29 - 31.
9. Беляков Н. А., Соломенников А. В., Журавлева И. Н. Энтеросорбция - механизмы лечебного действия. Эфферент. терап. 1997; 3 (2): 20 - 26.
10. Маркелов Д. А., Ницак О. В., Геращенко И. И. Сравнительное изучение адсорбционной активности медицинских сорбентов. Химико-фармацевт. журнал 2008; 42 (7): 30 – 33.
11. Беляков Н. А., Соломенников А. В. Энтеросорбция — механизм лечебного действия. Эфферент. терапия 1998;4 (2):10 – 16.
12. Хотимченко Ю. С., Кропотов А. В. Энтеросорбция в медицине. Медико-фармацевт. вестн. Приморья 1998;4: 99 – 107.
13. Хотимченко Ю. С., Кропотов А. В. Применение энтеро-сорбентов в медицине. Тихоокеан. мед. журн. 1999;2: 84 – 89.
14. Aoyama I., Shimokata K., Niwa T. An oral adsorbent down-regulates renal expression of genes that promote interstitial infl ammation and fi brosis in diabetic rats. Nephron. 2002; 92 (3): 635 – 651.
15. Weston S., Halbert H., Richmond P. et al. Eff ects of probi-otics on atopic dermatitis: a randomised controlled trial. Arch. Dis. Child. 2005; 90: 892 – 897.
16. Viljanen M., Savilahti E., Haahtela T. et al. Probiotics in the treatment of atopic eczema / dermatitis syndrome in infants: a double-blind placebo-controlled trial. Allergy 2005; 60: 494 – 500.
17. Rosenfeldt V., Benfeldt E., Nielsen S. D. et al. Eff ect of probi-otic Lactobacillus strains in children with atopic dermatitis. J. Allergy Clin. Immunol. 2003; 111: 389 – 395.
18. Helin T., Haahtela S., Haahtela T. No eff ect of oral treatment with an intestinal bacterial strain, Lactobacillus rhamnosus (ATCC 53103), on birch-pollen allergy: a placebo-controlled doubleblind study. Allergy 200; 57: 243 – 246.
19. Ishida Y., Nakamura F., Kanzato H. et al. Clinical eff ects of Lactobacillus acidophilus strain L-92 on perennial allergic rhinitis: a double-blind, placebo-controlled study. J. Dairy Sci. 2005; 88: 527 – 533.
20. Galdeano C. M., Perdigton G. The probiotic bacterium Lactobacillus casei induces activation of the gut mucosal immune system through innate immunity. Clin. Vacc. Immunol. 2006; 13: 219 – 226.
21. Severity scoring of atopic dermatitis: SCORAD Index (Consensus report of the European Task Force on atopic dermatitis). Dermatology 1993; 186: 23 – 31.
22. Finlay A. Y., Khan C. K. Dermatology Life Qualiti Index (DLQI) — a simple practical measure for routine clinical use Text. Clin. Exp. Dermatol. 1994; 19: 210 – 216.
