Лактофильтрум в терапии атопического дерматита
Статьи Опубликовано в журнале:
« СОВРЕМЕННЫЕ ПРОБЛЕМЫ ДЕРМАТОВЕНЕРОЛОГИИ,
ИММУНОЛОГИИ И ВРАЧЕБНОЙ КОСМЕТОЛОГИИ » №2, 2011г.
Снарская Е. С., Первый МГМУ им. И. М. Сеченова
Устойчивая тенденция роста частоты и тяжести течения атопического дерматита (АД), развитие сочетанных форм с аллергическим контактным дерматитом (АКД), бронхиальной астмой (дерматореспираторный синдром), аллергическим ринитом и др., а также резистентность к традиционной терапии обуславливают необходимость поиска возможных путей коррекции основных лечебно-диагностических мероприятий при этой патологии [1 – 3].
Одной из очевидных причин тяжелого варианта течения АД является быстрое присоединение вторичной бактериальной и грибковой инфекции, среди возбудителей которой преобладают токсигенные штаммы стафилококка, дрожжеподобных грибов рода Candida, Malassesia furfur и мицелиарных дерматофитов [4]. В качестве фактора, индуцирующего формирование сочетанных форм АД и тяжелого варианта его течения, может являться эндотоксин грамотрицательных бактерий пищеварительного тракта, имеющий высокую степень токсичности для человека [2]. Продукты метаболизма бактерий, грибов или вирусных белков представляют собой суперантигены, вызывающие неспецифическую активацию Т-клеток. Число Т-клеток, взаимодействующих с суперантигенами, почти в 100 раз превосходит число Т-клеток, взаимодействующих с обычным антигеном; при этом CD4+ Т-клетки выделяют большое число цитокинов, способных оказать токсическое действие на организм хозяина [5].
В последние годы в качестве универсального патогенетического механизма развития АД многие ученые считают повышение уровня эдотоксина, приводящее к «эндотоксиновой агрессии» и развитию синдрома эндогенной интоксикации (СЭИ), который не только сопровождает течение заболевания, но и выступает поддерживающим, усугубляющим моментом его развития, оказывая повреждающее действие на ткани и определяя прогноз и исход АД [3; 6 – 8]. В связи с этим проводится целый ряд углубленных исследований уровня токсинов (энтеротоксинов В и С, дельта-гемолизина) [9], микробной флоры кожи с определением степени ее патогенности [4], уровня маркеров системной эндотоксемии и оценка степени напряженности антиэндотоксинового иммунитета [2], состояния бронхолегочного барьера, показателей перекисного окисления липидов, уровня общей антирадикальной активности организма больного с атопическим дерматитом [10].
Степень эндогенной интоксикации организма можно оценить по уровню молекул средней массы в плазме эритроцитов, показателю перекисного окисления липидов, количеству первичных и вторичных продуктов в плазме и эритроцитах, степени сорбционной емкости эритроцитов и количеству циркулирующих иммунных комплексов (ЦИК) в плазме [11; 12].
Эндотоксин является биологически активным соединением, содержание которого может использоваться для оценки состояния антиэндотоксинового иммунитета при АД. Так, по данным исследователей [6], повышение уровня эндотоксина в 8 раз было отмечено у IgE-зависимых пациентов и в 12 раз — у IgE-независимых (уровень эндотоксина составил 1,69 и 2,43 EU / ml соответственно при норме 0,19 EU / ml). При этом авторы отмечали достоверное снижение показателей антиэндотоксинового иммунитета в обеих группах больных, особенно у IgE-независимых пациентов.
Полученные данные авторы расценивают как трансформацию физиологической «эндотоксинемии» в патологический процесс — «эндотоксиновую агрессию», значительно усугубляющую течение атопического дерматита. Увеличение уровня эндотоксина также может наблюдаться при снижении функции печени, нарушениях пристеночного пищеварения, повышенной кишечной проницаемости, дисбактериозе и любом патологическом процессе, приводящем к недостаточности эндотоксинэлиминирующих и эндотоксинсвязывающих функций организма [6]. Токсичные продукты, проникая в неизмененные, относительно интактные клетки, вызывают в них нарушение метаболизма, что сопровождается массивным высвобождением внутриклеточных биологически активных веществ, распределение которых в тканях на фоне прогрессирующего увеличения в организме токсичных метаболитов способно привести к глубоким расстройствам регуляции и повреждению биологических барьеров и процесса всасывания в ЖКТ, что в результате ведет к значительной дезинтеграции деятельности организма.
По степени выраженности СЭИ можно судить о тяжести основного заболевания, в частности атопи-ческого дерматита, и прогнозировать его течение. При СЭИ развивается также иммуносупрессия, чему способствуют следующие факторы:
- накопление молекул средней массы;
- накопление продуктов перекисного окисления липидов;
- усиление транслокации эндотоксинов и микрофлоры из кишечника в кровь, приводящее к увеличению в крови концентрации липополисахаридов грамотрицательных микроорганизмов и бактериемии;
- нарушение обмена нуклеиновых кислот в клетках иммунной системы (диснуклеотидоз);
- нарушение цитокинового статуса (существенное преобладание провоспалительных цитокинов).
При СЭИ формируется комплекс метаболических расстройств, которые приводят не только к уменьшению объемов органов иммунной системы (инволюция тимико-лимфатического аппарата) и увеличению проницаемости естественных барьеров, но и к нарушению взаимодействия отдельных ее эффекторных звеньев. Все это создает патогенетическую основу для формирования клинических проявления иммуносупрессии и формирования вторичной иммунной недостаточности.
Параллельное исследование этих показателей с иммунологическим обследованием позволит судить не только о выраженности СЭИ при АД, но и степени формирующейся иммуносупрессии. Кроме того, эндоинтоксикация, наблюдающаяся у больных АД в 60 – 80% случаев, способствует фармакологической резистентности, что приводит к снижению эффективности любых методов терапии и требует ее коррекции [13].
Таким образом, наличие СЭИ у больных с АД различной степени тяжести свидетельствует о патогенетической необходимости на ранних этапах лечения адекватной комбинации базисной терапии АД и препаратов со свойствами энтеросорбентов, что приведет к повышению эффективности лечения за счет как активной дезинтоксикации, так и повышения фармакочувствительности [11; 12]. При назначении энтеросорбентов устраняются интоксикация веществами с иммунотоксическими свойствами, явления провоспалительной гиперцитокинемии, усиливается антитоксический потенциал печени и микрофлоры кишечника, уменьшается процесс транслокации микробного содержимого кишечника, нормализуются процессы перекисного окисления липидов. В целом ряде исследований по применению детоксицирующих средств и энтеросорбентов в терапии аллергодерматозов у детей демонстрируется высокий уровень ремиссии процесса (до 86,6%) при снижении SCORAD в 2,5 раза, уменьшении частоты обострений в 4 раза, продолжительности ремиссии в 3,5 раза [8; 9; 11].
Исходя из изложенного, большой интерес представляет российский препарат лактофильтрум («АВВА Рус»). Фармакологическое действие препарата обусловлено уникальными свойствами его активных компонентов — энтеросорбента и пребиотика. В качестве энтеросорбента — лигнин гидролизный с высоким потенциалом сорбционной активности, что позволяет связывать и выводить из организма широкий спектр высокотоксичных бактериальных токсинов, аллергены, медиаторы воспаления, патогенную микрофлору и избыток продуктов обмена в 2500 раз сильнее активированного угля. В качестве пребиотика используется лактулоза — синтетический дисахарид, способный избирательно стимулировать рост бифидо- и лактобактерий, не претерпевая изменений в агрессивной среде желудочного содержимого, ингибировать рост патогенной микрофлоры, уменьшая продукцию токсических веществ и активируя перистальтику кишечника. За счет уникального состава лактофильтрум восстанавливает защитную бактерицидную функцию кожи [14], повышая местный иммунитет, что приводит к быстрому регрессу клинических проявлений АД [15]. Применение лактофильтрума позволяет повысить эффективность стандартной терапии АД на 25 – 50%, а при легкой и средней степени тяжести течения АД препарат лактофильтрум эффективен даже в качестве монотерапии [15].
Учитывая позитивный клинический опыт, мы применили лактофильтрум в комплексной терапии АД у 15 больных в возрасте от 17 до 23 лет, со средним и среднетяжелым течением патологического процесса. Группа сравнения состояла из 10 пациентов в возрасте от 18 до 26 лет со средним и среднетяжелым течением процесса, получавших терапию, предусмотренную стандартом. Лактофильтрум назначался по 3 таблетки 3 раза в день за час до еды и приема других лекарственных препаратов. Курс лечения составлял 3 недели. В процессе терапии на фоне приема лактофильтрума отмечалось купирование клинических проявлений АД (зуд, отек, экскориации, гиперемия) в более короткие сроки (7 – 10 дней против 15 – 20 при стандартной терапии) (рис. 1 а, б).
Динамика индекса SCORAD была интенсивнее в 1,5 раза в группе пациентов, принимающих лактофильтрум, особенно при средней форме тяжести АД. Пациенты отмечали удобство применения препарата, отсутствие побочных эффектов и неприятных ощущений. Применение лактофильтрума позволяет значительно повысить эффективность терапии АД, при средней и среднетяжелой степени тяжести течения процесса, снизить сроки пребывания пациентов в стационаре, повысить качество жизни пациентов. Препарат обладает хорошей переносимостью и комплаентностью и может быть рекомендован для применения и в амбулаторных условиях с целью увеличения сроков ремиссии и коррекции эндотоксемии при АД.
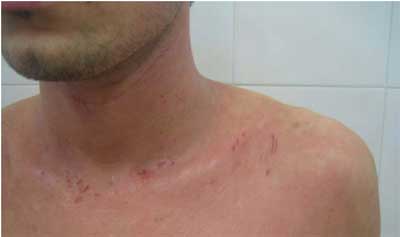
Рис. 1а.
Больной В., 25 лет, Атопический дерматит средне-тяжелое течение. До лечения
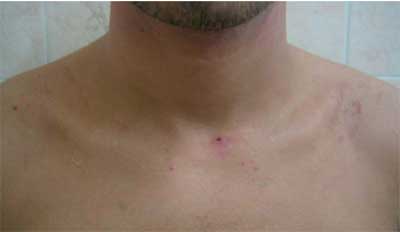
Рис. 1б. Литература 1. Землякова С. С., Иванов О. Л., Львов А. Н. и д р. / / Рос . журн. кож. и вен. бол. — 2010. — № 4. — С. 47 – 50.
Тот же больной после лечения
2. Шамов Б. А., Газиев А. Р., Шамова А. Г. // Рос. журн. кож. и вен. бол. — 2006. — № 6. — С. 16 – 20.
3. Darsow V., Ring J. // Allergy Clin. Immunol. Int. — 2002. — Vol. 14. — P. 170 – 173.
4. Белоусова Т. А., Фи липпова В. А., Горячкина М. В. / / Дерматология. Приложение к Consilium medicum. — 2002. — № 2. — С. 34 – 38.
5. Бурместер Г. Р. Наглядная иммунология / Пер. с англ., под ред. Л. В. Козлова. — М.: Бином, 2007.
6. Васенова В. Ю., Федорова Ю. С., Бутов Ю. С. // ХI Всерос. съезд дерматовенерологов и косметологов. Тезисы научных работ. — Екатеринбург, 2010. — С. 44.
7. Короткий Н. Г., Тихомиров А. А., Белова А. В. // Педиатрия. — 2003. — № 6. — С. 55 – 58.
8. Трофимова И. Б., Мишурина Л. А., Гевондян В. С. и др. // Вестн. дерматол. и венерол. — 2001. — № 2. — С. 9 – 13.
9. Батыршина С. В., Хаертдинова Л. А., Сабынина Е. Е. / / ХI Всерос. съезд дерматовенерологов и косметологов. Тезисы научных работ. — Екатеринбург; 2010. — С. 39.
10. Дубняк Н. С., Юцковский А. Д., Палагина М. В. и др. // Р о с . журн. кож. и вен. бол. — 2010. — № 4. — С. 30 – 32.
11. Химкина Л. Н., Пантелеева Г. А., Копытова Т. В. Пособие для врачей. — Н. Новгород, 2000. — С. 11.
12. Химкина Л. Н., Пантелеева Г. А. и др. // Эксперим. и клин. дерматокосметол. — 2005. — № 6. — С. 61 – 64.
13. Сидельникова В. И., Лифщиц В. М. // Клин. лаб. диагностика. — 1998. — № 8. — С. 3 – 7.
14. Молочков В. А., Кара улов А. В. Николаева С. А. // Эффективная фармакотер. в дерматол. и дерматокосме-тол. — 2010. — № 1. — С. 12 – 16.
15. Смирнова Г. И. // Леч. врач. — 2009. — № 1. — С. 23 – 26.
