 invar.ru
invar.ru

ЛИНИЯ СРЕДСТВ ДЛЯ ЖЕНСКОГО ИНТИМНОГО ЗДОРОВЬЯ ЭПИГЕН ИНТИМ
На основе активированной глицирризиновой кислоты
(экстракт корня солодки).
Опыт применения активированной глицирризиновой кислоты в монотерапии воспалительных заболеваний шейки матки
СтатьиЖ.А. Мандрыкина, Л.В. Сапрыкина, М.Р. Нариманова
ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, Москва, Россия
Резюме
Причинами воспалительных заболеваний шейки матки (N72 по МКБ-10 - воспалительная болезнь шейки матки - ВБШМ) могут быть не только специфические или неспецифические микроорганизмы, но и различные механические и химические факторы (спринцевания, использование барьерной контрацепции и т.д.), которые приводят к повреждению эпителия ШМ, нарушениям локального иммунитета. В этих случаях ВБШМ может персистировать, несмотря на повторные курсы антимикробной терапии. Особенно, риск повышен у молодых женщин и подростков, вследствие незрелости шейки матки, физиологической эктопии эпителия эндоцервикса и повышенной его чувствительностью к внешним воздействиям, в т.ч. к инфекциям, передаваемым половым путем (ИППП), вирусу папилломы человека (ВПЧ).
Цель исследования: оценить эффективность и безопасность применения активированной глицирризиновой кислоты (АГК) в монотерапии воспалительных заболеваний ШМ.
Материал и методы: в пилотное исследование были включены 24 пациентки репродуктивного и перименопаузального возраста (средний возраст 41,8±8,2 г.) с воспалительными заболеваниями ШМ. Основные жалобы – дискомфорт, зуд, жжение в области половых органов. У всех женщин при выполнении полимеразной цепной реакции в режиме реального времени и культуральном исследовании не было выявлено ИППП и УПМ в диагностически значимых титрах. Все пациентки интравагинально использовали АГК в качестве монотерапии. Эффективность терапии оценивали по: уменьшению/нивелированию жалоб, положительной динамике при кольпоскопии. Для оценки демографических и клинических данных использовали описательную статистику.
Результаты исследования: при контрольном визите через 14 дней 100% (n=24) пациенток не предъявляли жалоб на дискомфорт, зуд и жжение в области половых органов. Побочных эффектов препарата у пациенток зарегистрировано не было. По данным расширенной кольпоскопии было отмечено сокращение границ эктопированного участка у 100% пациенток, а также более равномерное окрашивание раствором Люголя.
Заключение: локальное применение АГК у пациенток с воспалительными заболеваниями ШМ в отсутствии ИППП и диагностически значимых титров УПМ является эффективным и безопасным методом лечения. Использование АГК в качестве монотерапии способствует нивелированию симптомов данного заболевания уже к 7 дню от начала лечения. При этом отмечается улучшение результатов кольпоскопии.
Ключевые слова: цервицит; воспалительная болезнь шейки матки; активированная глицирризиновая кислота; репродуктивный возраст; перименопаузальный возраст; лечение; диагностика; кольпоскопия; условно-патогенные микроорганизмы; инфекции, передаваемые половым путем; иммуностимулирующая активность; монотерапия.
Цитирование: Мандрыкина, Ж. А. Опыт применения активированной глицирризиновой кислоты в монотерапии воспалительных заболеваний шейки матки / Ж. А. Мандрыкина, Л. В. Сапрыкина, М. Р. Нариманова // РМЖ. Мать и дитя. – 2019. – Т. 2, № 3. – С. 249-253. – DOI 10.32364/2618-8430-2019-2-3-249-253. – EDN ALUXGA.
(1) Введение
Причинами воспалительных заболеваний шейки матки (N72 по МКБ-10 - воспалительная болезнь шейки матки - ВБШМ) могут быть не только специфические или неспецифические микроорганизмы, но и различные механические и химические факторы (спринцевания, использование барьерной контрацепции и т.д.), которые приводят к повреждению эпителия ШМ, нарушениям локального иммунитета. В этих случаях ВБШМ может персистировать, несмотря на повторные курсы антимикробной терапии. Особенно, риск повышен у молодых женщин и подростков, вследствие незрелости шейки матки, физиологической эктопии эпителия эндоцервикса и повышенной его чувствительностью к внешним воздействиям.
Наличие воспалительного процесса вызывает, с одной стороны, реактивные клеточные нарушения, которые выражаются в изменении ядра и ядерно-цитоплазматического соотношения в эпителии шейки матки (ШМ). С другой – снижение общего и локального иммунитета, снижение резерва бактерицидной и вирусоцидной функции нейтрофилов повышает восприимчивость ШМ к ИППП, а также к папилломавирусной инфекции в условиях ВБШМ. В дальнейшем, в случае хронизации процесса, особенно при присоединении папилломавирусной инфекции, изменения эпителия являются ко-факторами плоскоклеточных интраэпителиальных поражений.
Клинически ВБШМ характеризуется наличием слизисто-гнойных выделений из цервикального канала и других признаков воспаления, таких как контактное кровотечение (после полового акта, во время гинекологического осмотра). В ряде стран в качестве диагностического критерия используется окраска мазка из цервикального канала по Граму (включена в стандарт обследования больных с ВБШМ в Российской Федерации в соответствии с приказом Министерства Здравоохранения № 572н). Количество лейкоцитов, обнаруживаемых при микроскопии в мазке, в качестве диагностического критерия ВБШМ варьирует от ≥10 (в соответствии с руководством CDC [США]) до ≥30) лейкоцитов в поле зрения.
К диагностическим мероприятиям, выполняемым в Российской Федерации также относится цитология мазков (РАР-тест), молекулярно-биологическое исследование отделяемого женских половых органов (полимеразная цепная реакция (ПЦР) на определение ИППП). Такое тестирование может быть выполнено либо на образцах материала, полученного из цервикального канала, влагалища или моче. Кроме того, выполняется бактериологическое исследование отделяемого женских половых органов на аэробные и факультативно-анаэробные микроорганизмы и чувствительность к антибиотикам, кольпоскопия. При этом диагностическая точность результатов полученных исследований для диагностики ВБШМ может меняться. Необходимо помнить, что при ВБШМ высока вероятность наличия неадекватной кольпоскопической картины из-за проявлений воспаления, контактных кровотечений и т.д. Кроме того, при кольпоскопии наблюдается неадекватная реакция на тесты, манифестация признаков цервикальной интраэпителиальной неоплазии без ее наличия.
Лечение ВБШМ зависит от результатов анализов. При выявлении микробного/вирусного агента проводят этиотропную терапию. В состав комплексного лечения ВБШМ, вызванной вирусом простого герпеса или осложненной наличием ВПЧ-инфекции целесообразно включить препарат Эпиген Интим (Хемигруп Франс С.А., Франция). Только Эпиген Интим содержит активированную глицирризиновую кислоту (АГК), получаемую путем экстракции из корня солодки. АГК обладает комплексным действием: противовирусным, иммуностимулирующим (индуцирует выработку собственных интерферонов), противозудным, а также противовоспалительным и регенерирующим. Особенно актуально применение АГК при сомнительных результатах кольпоскопии, связанных с ВБШМ.
Применение АГК у молодых женщин с персистирующей ВПЧ-инфекцией приводит к снижению числа пациенток с клиническими проявлениями ВБШМ в 2 раза, улучшению показателей Pap-теста до нормы у 29% женщин, снижению количества атипических изменений при кольпоскопии с 40 до 16%.
У пациенток с повышенным риском C. trachomatis и N. gonorrhoeae лечение противомикробными препаратами может быть начато до получения результатов анализов (например, в возрасте <25 лет, при наличии нового полового партнера, при наличии нескольких половых партнеров, если у полового партнера есть ИППП), особенно если последующее наблюдение не может быть обеспечено, или если тестирование с помощью ПЦР невозможно.
У женщин с более низким риском наличия ИППП можно отложить лечение до получения результатов диагностических тестов. Если лечение отложено, и ПЦР по отношению к C. trachomatis и N. gonorrhoeae отрицательны, можно рассмотреть возможность наблюдения с констатацией разрешения ВБШМ. У такой категории пациенток возможно применение препарата Эпиген Интим в монорежиме с целью уменьшения симптомов ВБШМ, нивелирования воспалительных изменений на ШМ.
(1) Собственные результаты
В данное пилотное исследование первоначально было включено 78 пациенток, которые обратились на прием с жалобами на выделения из половых путей, дискомфорт, зуд в области половых органов.
Проводился сбор жалоб, оценка данных анамнеза. У всех пациенток уточняли время начала половой жизни, использование методов контрацепции. Диагноз ВБШМ устанавливался на основании данных осмотра в зеркалах (гиперемия ШМ, наличие гнойных, слизисто-гнойных выделений в области наружного зева, травматизация эпителия ШМ, кровоточивость при осмотре и взятии биоматериала и т.д.), микроскопии мазка (количество лейкоцитов более 30 [в соответствии с референсными значениями лаборатории] в поле зрения). Кроме того, всем пациенткам бактериологическим методом, методом ПЦР в режиме реального времени (ПЦР-РТ) выполняли определение УПМ и степени обсемененности и выявление ИППП. Проводили взятие материала для выполнения жидкостной онкоцитологии. Выполняли кольпоскопию, при необходимости - ультразвуковое исследование органов малого таза.
Еще до получения результатов бактериологического исследования и ПЦР-РТ 38,46% (n=30) пациенток начали использование препарата Эпиген Интим для уменьшения неприятных ощущений, зуда в области половых органов. Препарат назначали в соответствии с инструкцией - интравагинально с помощью специальной насадки: при явлениях дискомфорта в области половых органов, сопровождающихся зудом, жжением и сухостью слизистых оболочек: 2 раза в день (утром и вечером) в течение 2-3 нед.
В дальнейшее исследование из первоначальной когорты было включено 24 пациентки (средний возраст 41,8±8,2 год), у которых после культурального исследования и ПЦР-РТ не было выявлено ни ИППП, ни диагностически значимых титров УПМ, которым еще до получения результатов анализов назначали Эпиген Интим.
В наше наблюдение не вошли пациентки, имеющие: иммуносупрессию, включая ВИЧ-инфекцию; беременность; сахарный диабет; ИППП; УПМ в диагностически значимых титрах; прием антибиотиков в течение месяца до включения в исследование.
Длительность наблюдения составила 14 дней от начала лечения. Эффективность терапии оценивали по: уменьшению/нивелированию жалоб, положительной динамике в результатах кольпоскопии.
Для анализа полученных данных применяли методы описательной статистики с вычислением средней арифметической (M) и ее стандартной ошибки (m).
При сборе анамнеза было выявлено, что 79,17% (n=19) пациенток, живущих половой жизнью, не использовали методы контрацепции (в т.ч. барьерные), что соответствует данным об этиологии и патогенезе ВБШМ, с одной стороны. С другой стороны, возможными причинами ВБШМ в условиях отсутствия инфектанта может быть аллергия на латекс, спермициды, использования влагалищной диафрагмы, что следует учитывать при ведении такой категории пациенток [1].
После выполнения ПЦР-РТ были получены следующие данные о микробиоте влагалища (табл. 1).
Таблица 1.
Видовой состав вагинальной микробиоты
Table 1.
Composition of vaginal microbiota
| Микроорганизмы Microbes |
Пациенты |
|
Gardnerella vaginalis (%, n) |
29.17% (7) |
|
Candida spp. (%, n) |
25% (6) |
|
Ureaplasma spp. (%, n) |
20.83% (5) |
|
Mycoplasma hominis (%, n) |
16.7% (4) |
|
Аэробная микрофлора (%, n) |
25% (6) |
При ПЦР-РТ и культуральном исследовании у 62.5% (n=15) пациенток выявлялись УПМ. Диагностически значимых титров УПМ выявлено не было.
В нашем исследовании ни у одной из пациенток не было зарегистрировано предраковых поражений ШМ.
При кольпоскопии визуализировались расплывчатые, нечеткие красноватые пятна, образованные в результате расширения капилляров. После обработки уксусной кислотой пятна сокращались и становились беловатыми. При пробе Шиллера поверхность слизистой оболочки окрашивалась неравномерно, пестро, с характерной крапчатостью йодопозитивных и йодонегативных участков (симптом «манной крупы»). У 70,83% (n=17) пациенток при кольпоскопии была выявлена эктопия ШМ или эктропион. У одной пациентки (4,17%) была выявлена лейкоплакия ШМ.
Все пациентки, получавшие лечение, хорошо переносили терапию и завершили двухнедельный курс лечения.
При контрольном визите через 14 дней от начала терапии у пациенток были зафиксированы изменения жалоб и кольпоскопической картины.
На фоне использования Спрея Эпиген Интим у 100% пациенток было отмечено купирование симптомов дискомфорта, зуда и жжения на 4–7-й день от начала применения (в среднем 5,17±0,34). Побочных эффектов препарата у пациенток зарегистрировано не было.
При контрольной кольпоскопии было отмечено сокращение границ эктопированного участка, а также более равномерное окрашивание раствором Люголя. Данные изменения можно объяснить следствием выраженного противовоспалительного иммуномодулирующего эффекта АГК, в результате которого уровни ключевых провоспалительных цитокинов IL-1, IL-6, TNF-α и IFN-γ снижаются до контрольных значений, уровни противовоспалительных цитокинов IL-4, IL-10 - повышаются [7].
(1) Клинические примеры
Клинический случай 1. Пациентка Я., 40 лет. Обратилась с жалобами на жжение в области влагалища, слизисто-гнойные выделения. Из анамнеза: считает себя больной в течение месяца. Развитие заболевания ни с чем не связывает. В настоящее время – 1 половой партнер, контрацепция – прерванный половой акт.
При осмотре в зеркалах: ШМ ярко-розового цвета с бело-серым налетом, который легко удаляется марлевым тампоном. Эпителий влагалища – розовый, чистый.
При бимануальном исследовании: матка и область придатков без особенностей, шейка матки – чувствительная. Своды влагалища – глубокие, параметрий не инфильтрирован.
При микроскопии отделяемого из цервикального канала – количество лейкоцитов до 60 в поле зрения. При ПЦР-РТ - Gardnerella vaginalis (102 КОЕ). Мазок на онкоцитологию – NILM (negative for intraepithelial lesion or malignancy – отсутствие интраэпителиальных изменений и злокачественных процессов).
При проведении расширенной кольпоскопии выявлен эктропион ШМ по передней губе в виде прямоугольника, размером 5х3 мм (рис. 1 а,в).
Установлен диагноз: ВБШМ. Эктропион ШМ.
Учитывая отсутствие диагностически значимых титров УПМ, дискомфорт в области половых органов, пациентке рекомендована АГК по схеме, описанной выше.
При контрольной явке через 14 дней - жалобы отсутствовали. При осмотре в зеркалах – ШМ бледно-розового цвета, выделения – слизистые. При кольпоскопии – уменьшение размеров эктропиона, изменение его формы. При пробе Шиллера – более равномерное окрашивание (рис. 1 c, d).
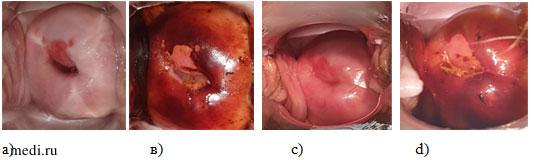 Рис. 1. Расширенная кольпоскопия. а) проба с уксусной кислотой до лечения, в) проба Шиллера до лечения проба, с) проба с уксусной кислотой после лечения, d) проба Шиллера после лечения.
Рис. 1. Расширенная кольпоскопия. а) проба с уксусной кислотой до лечения, в) проба Шиллера до лечения проба, с) проба с уксусной кислотой после лечения, d) проба Шиллера после лечения.
Fig. 1. Colposcopy. a) acetic acid test before the treatment, в) Shiller’s test before the treatment, c) acetic acid test after the treatment, d) Shiller’s test after the treatment.
Клинический случай 2. Пациентка Н., 52 лет, обратилась с жалобами на жжение во влагалище и обильные выделения из половых путей. Из анамнеза: считает себя больной в течение 3 недель. Развитие заболевания связывает со сменой геля для интимной гигиены. В настоящее время – половая жизнь отсутствует. Последняя менструация – 2 месяца назад.
При осмотре в зеркалах выявлено: эпителий влагалища – розовый, ШМ - гиперемирована. Вокруг цервикального канала определяется участок белого налета, который не снимался ватным шариком. При лабораторных обследованиях выявлена смешанная микрофлора (Gardnerella vaginalis, Ureaplasma parvum – 103 КОЕ), лейкоциты - до 40-50 в поле зрения. Мазок на онкоцитологию – цитограмма соответствует воспалительным процессам слизистой оболочки с реактивными изменениями эпителия, клетки с явлением гипер- и паракератоза.
При расширенной кольпоскопии визуализируется участок вокруг цервикального канала, который при обработке 3% уксусной кислотой имеет вид ацетобелого эпителия, и открытая железа с грубым валиком. При обработке раствором Люголя – йоднегативное окрашивание яркое, с четкими контурами в виде «крыльев бабочки», с наибольшими размерами по боковым стенкам шейки матки 5х3 мм, а по передней и задней губе с наименьшим 2х3 мм (рис. 2 а, в).
Установлен диагноз: лейкоплакия ШМ, ВБШМ.
Через 14 дней жалобы отсутствовали.
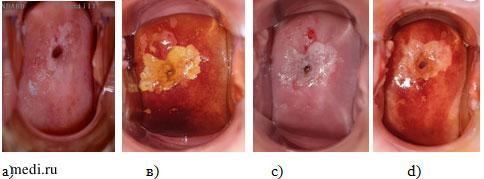 Рис. 2. Расширенная кольпоскопия. а) проба с уксусной кислотой до лечения, в) проба Шиллера до лечения, с) проба с уксусной кислотой после лечения, d) проба Шиллера после лечения.
Рис. 2. Расширенная кольпоскопия. а) проба с уксусной кислотой до лечения, в) проба Шиллера до лечения, с) проба с уксусной кислотой после лечения, d) проба Шиллера после лечения.
Fig. 2. Colposcopy. a) acetic acid test before the treatment, в) Shiller’s test before the treatment, с) acetic acid test after the treatment, d) Shiller’s test after the treatment.
При физикальном осмотре: стенки влагалища и слизистая ШМ бледно-розовые, чистые, выделения слизистые. При проведении расширенной кольпоскопии – участок ацетобелого эпителия сократился и стал менее ярким и четким, исчез грубый ободок вокруг открытой железы. Форма и размер йоднегативной зоны сократился и стал менее ярким (рис. 2 с,d).
(1) Заключение
Т.о. частота отсутствия ИППП и диагностически значимых титров УПМ в нашем исследовании у пациенток с ВБШМ составила 30,77%. Поэтому оправдана выжидательная тактика (до получения результатом анализов) в отношении антибактериальной терапии у больных с низким риском ИППП. На данном этапе возможно локальное использование Спрея Эпиген Интим в качестве монотерапии, что будет способствовать нивелированию таких симптомов заболевания как дискомфорт в области половых органов, зуд и жжение уже к 7 дню от начала лечения. Интравагинальное применение АГК в случае отсутствия ИППП и диагностически значимых титров УПМ хорошо переносится больными, не вызывает побочных эффектов, является эффективным и безопасным. При этом отмечается улучшение результатов кольпоскопии: уменьшение площади эктопированного участка, более равномерное окрашивание раствором Люголя.
Сведения об авторах:
Мандрыкина Жанна Анатольевна, кандидат медицинских наук, ассистент кафедры;
Сапрыкина Людмила Витальевна, кандидат медицинских наук, ассистент кафедры;
Нариманова Метанат Рафиговна, кандидат медицинских наук, ассистент кафедры;
ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России. 117997, Россия, Москва, ул. Островитянова, 1.
Литература/References
1. Workowski KA, Bolan GA; Centers for Disease Control and Prevention. Sexually transmitted diseases treatment guidelines, 2015. MMWR Recomm Rep. 2015;64(RR-03):1-137.
2. Gorgos L.M., Sycuro L.K, Srinivasan S. Relationship of Specific Bacteria in the Cervical and Vaginal Microbiotas with Cervicitis. Sex Transm Dis. 2015; 42(9): 475–481.
3. Taylor S.N., Lensing S., Schwebke J. et al. Prevalence and treatment outcome of cervicitis of unknown etiology. Sex Transm Dis 2013;40:379–85.
4. Ye H., Song T., Zeng X. et. al. Association between genital mycoplasmas infection and human papillomavirus infection, abnormal cervical cytopathology, and cervical cancer: a systematic review and meta-analysis. Arch. Gynecol. Obstet. 2018; 297(6): 1377–87.
5. Papp J.R., Schachter J., Gaydos C. et al. Recommendations for the laboratory-based detection of Chlamydia trachomatis and Neisseria gonorrhoeae–2014. MMWR Recomm Rep. 2014; 63(0): 1–19.
6. Доброхотова Ю.Э., Сапрыкина Л.В., Сапрыкина О.А. ВПЧ-ассоциированные поражения кожи и слизистых оболочек женских половых органов. Возможности локальной терапии. РМЖ. Мать и дитя 2018; 1 (1): 57-61. [Dobrokhotova Yu.E., Saprykina L.V., Saprykina O.A. Lesions of skin and mucous membranes of female genital organs associated with human papillomavirus. Local treatment options. Russian journal of Woman and Child Health. 2018;1(1):57–61. (in Russ)].
7. Зароченцева Н.В., Белая Ю.М. Современный взгляд на остроконечные кондиломы. Возможности лечения и профилактики. Российский вестник акушера-гинеколога. 2017;17(1):109-112. [Zarochentseva N.V., Belaya Yu.M. Present views on genital warts: possibilities for treatment and prevention. Russian bulletin of obstetrician-gynecologist. 2017; 17 (1): 109-112. (in Russ)].
