Эффективность применения мирамистина у детей раннего и дошкольного возраста с гипертрофией миндалин лимфоидного глоточного кольца, с рецидивирующими острыми респираторными инфекциями и сенсибилизацией к streptococcus pyogenes
СтатьиОпубликовано в журнале:
« Педиатрия » № 6 Том 94, 2015
Е.В. Шабалдина1, С.В. Рязанцев2, А.В. Шабалдин1,3
1ГБОУ ВПО «Кемеровская государственная медицинская академия» МЗ РФ,
2ФГБУ «Санкт-Петербургский НИИ уха горла носа и речи» МЗ РФ,
3ФГБНУ «НИИ Комплексных проблем сердечно-сосудистых заболеваний», г. Кемерово, РФ
Лекарственный препарат Мирамистин® (бензилдиметил[3-(миристоиламино)пропил]аммоний хлорид моногидрат) является катионным антисептиком и обладает антибактериальным, противогрибковым и противовирусным действием. Мирамистин® разрешен для топического лечения острого фарингита, ларингита и обострений хронического тонзиллита, в т.ч. у детей. Препарат усиливает функциональную активность иммунных клеток за счет активации поглотительной и переваривающей функции фагоцитов, потенцирует активность моноцитарно-макрофагальной системы. Целью исследования была оценка эффективности применения препарата Мирамистин® в комплексной иммунореабилитации детей раннего и дошкольного возраста с гипертрофией миндалин лимфоидного глоточного кольца, рецидивирующими острыми респираторными инфекциями (ОРИ) и сенсибилизацией к антигенам Streptococcus pyogenes. Проведено обследование и лечение 306 детей в возрастном интервале 3-7 лет с рецидивирующими ОРИ (более 4 раз в год), гипертрофией миндалин лимфоидного глоточного кольца и сенсибилизацией по IgG типу к антигенам Streptococcus pyogenes. Все дети были рандомизированы на две подгруппы, получавших Мирамистин в составе базисной терапии (основная группа, n=154) и получавших только базисную терапию (группа сравнения, n=152). Базисная терапия включала препараты с противовоспалительным, антигистаминным, муколитическим и ирригационным эффектами. После базисной терапии проводили 6-месячный курс иммунореабилитации с помощью мукозальных вакцин. У всех детей выполнены исследования концентраций провоспалительных и проаллергических интерлейкинов в назофарингеальном смыве, а также иммуноаллергологическое и микробиологические исследования. Проведение курса иммунореабилитации с включением препарата Мирамистин®, по сравнению с пациентами, не получавшими Мирамистин®, показало снижение частоты ОРИ, степени гипертрофии миндалин лимфоидного глоточного кольца, уровня локального TNFα и системных антистрептококковых антител, а также степени колонизации слизистых оболочек носа и глотки Streptococcus pyogenes.
Ключевые слова: Мирамистин, рецидивирующие острые респираторные инфекции, гипертрофия глоточной и нёбных миндалин, Streptococcus pyogenes, часто болеющие дети, иммунореабилитация.
Miramistin effectiveness in infants and preschool children with tonsils pharyngeal lymphoid ring hypertrophy, with recurrent acute respiratory infections and sensitization for streptococcus pyogenes
E.V. Shabaldina1, S.V. Ryazantsev2, A.V. Shabaldin1,3
1 Kemerovo State Medical Academy;
2St. Petersburg Research Institute of Ear, Throat, Nose and Speech;
3Scientific Research Institute of Complex Issues of Cardiovascular Deseases
Medicament Miramistin (benzildimethyl[3(miristoilamine)propilammonium chloride monohodrate) is a cationic antiseptic with antibacterial, antifungal and antiviral effect. Miramistinis approved for topical treatment of acute pharyngitis, laryngitis and acute exacerbation of chronic tonsillitis in children. The drug increases functional activity of immune cells by activating the absorption and digestive functions of phagocytes, potentiates the activity of monocytemacrophage system. The aim of the study was to evaluate the effectiveness of Miramistin in complex immunorehabilitation of infants and preschool children withtonsils pharyngeal lymphoid ring hypertrophy, recurrent acute respiratory infections (ARI) and sensitization to Streptococcus pyogenes antigens. The study included examination and treatment of 306 children aged 3-7 years with recurrent acute respiratory infections (more than 4 times per year), tonsillar pharyngeal lymphoid ring hypertrophy and IgG type sensitization to Streptococcus pyogenes antigens. All children were randomized into two groups: receiving Miramistin as part of basic therapy (study group, n=154) and basic therapy alone (control group, n=152). Basic therapy included medication with anti-inflammatory, antihistamine, mucolytic and irrigation effects. After basic treatment followed 6-month course of immunorehabilitation via mucosal vaccines. Concentrations of inflammatory and allergic interleukins in nasopharyngeal washings were studied in all children, immuno-allergological and microbiological studies were performed. Patients of immunorehabilitation course with Miramistin, compared to patients not receiving Miramistin, showed reduction of ARI, degree of tonsils pharyngeal lymphoid ring hypertrophy, level of local and systemic TNFα and systemic antistreptococcal antibodies, as well as degree of Streptococcus pyogenes colonization of nose and throatmucous membranes.
Keywords: Miramistin, recurrent acute respiratory infections, hypertrophy of pharyngeal and palatine tonsils. Streptococcus pyogenes, sickly children, immunorehabilitation.
Неоднократно показано, что уровень обсеменения условно-патогенной (УПМ) и патогенной микрофлорой слизистых оболочек носа и глотки у детей раннего и дошкольного возраста с рецидивирующими острыми респираторными инфекциями (ОРИ), а также с гипертрофией миндалин лимфоидного глоточного кольца очень высок [1]. Одним из наиболее вирулентных представителей этого микробного сообщества является Streptococcus pyogenes (Фила В13: Firmicutes, Порядок: Lactobacillales, Семейство: Streptococcaceae) [2]. По классификации Р. Лендсфилда (1933) этот микроорганизм относится к серологической группе «А». Streptococcus pyogenes имеет выраженные гемолитические свойства, поэтому по классификации Брауна (1919) он относится к (ß-формам (полный ß-гемолиз в питательной среде с кровью барана) и в литературе нередко обозначается как ß-гемолитический стрептококк группы А (БГСА). Показано, что БГСА относится к видам стрептококков, которые могут самостоятельно вызвать инфекционный процесс и по этому качеству их относят к III группе патогенности, согласно МКБ10 [3, 4]. Данный микроорганизм определяет этиологию не только инфекционных заболеваний респираторного, кишечного трактов, кожи и подкожной клетчатки, но является причиной постинфекционных заболеваний - ревматической болезни и острого постстрептококкового гломерулонефрита [5].
Показано, что первичным источником БГСА может быть материнское микроокружение [6]. Персистенция БГСА у детей с гипертрофией миндалин лимфоидного глоточного кольца приводит к срыву толерантности к его антигенам с последующей индукцией антител класса IgG к ним. Этот процесс ассоциирован с развитием дополнительных гуморальных иммунопатологических реакций, таких как увеличение в периферической крови циркулирующих иммунных комплексов (ЦИК), С-реактивного белка (СРБ), ревматоидного фактора (РФ), а также антистрептолизина О (ACЛO) и антистрептогиалуронидазы (АСГ) [1, 7]. Пролонгация и доминирование вышеуказанных реакций в конечном итоге могут приводить к формированию ревматической патологии у ребенка. С этих позиций выявление у часто и длительно болеющих детей (ЧБД) с гипертрофией миндалин лимфоидного глоточного кольца дополнительно антител класса IgG к Streptococcus pyogenes может быть скрининговым маркером развивающихся ревматических болезней.
Проведенное исследование также показало, что дети, имеющие иммунный ответ к антигенам Streptococcus pyogenes и высевающие его со слизистых оболочек носа и глотки, имеют микст-инфицирование глоточного биотопа такими микроорганизмами, как Streptococcus pneumoniae, Streptococcus mutans, Staphylococcus epidermidis, Haemophilus influenzae [1]. Эти данные указывают, что стойкие дисбиотические нарушения слизистых оболочек верхних отделов респираторного тракта способствуют пролонгации локального воспалительного процесса.
Учитывая полученные результаты, детей с гипертрофией миндалин лимфоидного глоточного кольца и с нарушенной толерантностью к антигенам Streptococcus pyogenes можно отнести к группе риска по формированию БГСА-ассоциированной патологии, и с этих позиций, им необходимо проводить дополнительное эффективное локальное санирования слизистых оболочек носа и глотки. Для этой процедуры необходим топический антибактериальный препарат с широким спектром действия (включая противогрибковый эффект) и топическим иммуномодулирующим эффектом для активации подавленного врожденного иммунитета.
С середины 80-х годов прошлого века в рамках программы «Космические биотехнологии» начал разрабатываться топический антисептический препарат для космонавтов «орбитальных станций». Основные требования к этому медицинскому изделию были следующие: он должен эффективно бороться с различными видами бактерий, вирусов и грибов и при этом оставаться безопасным для человека, в т.ч. не вызывать аллергических реакций при длительном многократном применении [8]. Этими свойствами обладало химическое соединение бензилдиметил[3- (миристоиламино)пропил]аммоний хлорид моногидрат, которое в дальнейшем получило фирменное название «Мирамистин» [9].
Доказано, что Мирамистин обладает антимикробным действием и при местном применении не всасывается через слизистые оболочки, кожу. Мирамистин имеет свойства катионного детергента. Он взаимодействует с липидным слоем мембран микроорганизмов, вызывая их разрушение и увеличивая проницаемость, что индуцирует цитолиз. Препарат обладает выраженным бактерицидным действием в отношении анаэробных и аэробных бактерий, грамположительных (Staphylococcus spp., Streptococcus spp., Streptococcus pneumoniae, Bacillus subtilis, Bacillus anthracoides), грамотрицательных (Neisseria spp., Shigella spp., Pseudomonas aeruginosa, Escherichia coli, Klebsiella spp., Salmonella spp., Vibrio spp.), как в виде монокультур, так и в виде ассоциаций (синегнойная палочка и стафилококк, эшерихии и стафилококки), включая госпитальные штаммы, обладающие полирезистентностью к антибиотикам [9].
Свойства катионного детергента определяют и противогрибковое действие Мирамистина. Препарат активен в отношении рода Aspergillus, рода Penicillium, дрожжевых (Rhodotorula rubra, Torulopsis gabrata и др.) и дрожжеподобных грибов (Candida albicans, Candida tropicalis, Candida krusei, Pityrosporum orbiculare (Malassezia furfur) и др.), а также дерматофитов (Trichophyton rubrum, Trichophyton mentagrophytes, Trichophyton verrucosum, Trichophyton schoenleini, Trichophyton violacent, Epidermophyton Kaufman-Wolf, Epidermophyton floccosum, Microsporum gypseum, Microsporum canis и др.). Мирамистин эффективно подавляет рост других патогенных грибов, как в виде монокультур, так и микробных ассоциаций, включая грибковую микрофлору с резистентностью к химиотерапевтическим препаратам [10].
Следует также отметить, что Мирамистин обладает противовирусным действием. Он активен в отношении сложноустроенных вирусов (вирусы герпеса, вирус иммунодефицита человека и др.) и действует на возбудителей заболеваний, передающихся половым путем (Chlamydia spp., Treponema spp., Trichomonas vaginalis, Neisseria gonorrhoeae).
Препарат усиливает функциональную активность иммунных клеток за счет активации поглотительной и переваривающей функции фагоцитов, потенцирует активность моноцитарно-макрофагальной системы. Обладает выраженной гиперосмолярной активностью, вследствие чего купирует раневое и перифокальное воспаление, абсорбирует гнойный экссудат, способствуя формированию сухого струпа. Не повреждает грануляции и жизнеспособные клетки кожи, не угнетает краевую эпителизацию.
С 1992 г. Мирамистин применяется в оториноларингологии при воспалительных заболеваниях околоносовых пазух, уха, гортани, глотки, миндалин лимфоидного глоточного кольца. В настоящее время препарат выпускается во флаконе (150 мл) с насадкой-распылителем, что позволяет наносить его на нёбные миндалины и слизистую оболочку носа и глотки. Мирамистин разрешен для лечения острого фарингита, ларингита и обострений хронического тонзиллита у детей с 3-летнего возраста [11]. Этими характеристиками Мирамистин выгодно отличается от своего ближайшего аналога по своим антисептическим свойствам - хлоргексидина.
Целью настоящего исследования была оценка эффективности применения препарата Мирамистин в комплексной иммунореабилитации детей раннего и дошкольного возраста с гипертрофией миндалин лимфоидного глоточного кольца, с рецидивирующими ОРИ и с сенсибилизацией к антигенам Streptococcus pyogenes.
Материалы и методы исследования
Для выполнения поставленной задачи было проведено обследование 306 детей в возрастном интервале 3-7 лет, проходивших лечение на клинических базах Кемеровской государственной медицинской академии МЗ РФ у врачей - оториноларинголога и клинического иммунолога, по поводу рецидивирующих ОРИ и гипертрофии миндалин лимфоидного глоточного кольца. Все дети были отнесены к группе ЧБД по рекомендациям В.Ю. Альбицкого (1986), а также имели гипертрофию более II степени глоточной и/или нёбных миндалин.
Основным критерием, по которому формировали выборку детей, был иммунный ответ по IgG-типу к антигенам Streptococcus pyogenes. Считали, что серологическое обследование наиболее четко отражает срыв иммунной толерантности к данному микроорганизму и тем самым указывает на декомпенсацию дисбиоза слизистых оболочек БГСА-этиологии.
Обследование верхних дыхательных путей выполняли на специализированном ЛOP-месте «Азимут-ЗЧ»: проводили осмотр полости носа и носоглотки жесткими эндоскопами с полями зрения 45° и 90° и диаметром 2,4 и 4 мм. Повторное клиническое обследование проводили через 7 дней после проведенного лечения (или 17 дней от начала лечения), а ТЭ.КЖ6 через 6 месяцев от начала лечения. В конечной точке обследования учитывали степень гипертрофии миндалин лимфоидного глоточного кольца и частоту ОРИ за 6 месяцев (данные по частоте ОРИ экстраполировали на 1 год жизни).
У всех детей выполнено исследования концентраций интерлейкина 1ß (IL1ß), рецепторного антагониста интерлейкина 1 (ILIRα), интерлейкина 4 (IL4), фактора некроза опухоли α (TNFα) и интерферона α (INFα) в назофарингеальном смыве (НФС). Исследование проводили методом твердофазного ИФА на коммерческих наборах ООО «Цитокин» (г. Санкт-Петербурга, Россия), согласно прилагаемым инструкциям, до начала лечения, через 17 дней от начала лечения, а также через 6 месяцев от начала лечения. НФС получали методом промывания носоглотки через носовые ходы 3 мл физиологического раствора. В литературе неоднократно вставал вопрос о трактовке концентраций того или иного аналита в секретах. Один из предлагаемых способов выравнивания концентраций связан с пересчетом количества анализируемого вещества на грамм белка, содержащегося в исследуемом секрете. Учитывая возможность различного разведения НФС, провели исследования в каждой пробе общего белка колориметрическим методом с использованием красителя пирогаллолового красного. Получили концентрацию общего белка 0,5 г/л в каждой пробе, и эта величина была постоянной. Исходя из того, что соответствующий коэффициент пересчета концентраций цитокинов на грамм белка также получался постоянным, отказались от данного способа выравнивания и в дальнейшем концентрацию цитокинов, полученную в ИФА, анализировали в пг/мл.
Иммуноаллергологическое исследование проводили с помощью твердофазного ИФА на наборах фирмы ООО «Иммунотекс» (г. Ставрополь, Россия). Анализируемая панель включала антигены к следующим микроорганизмам: Streptococcus (Str.) pyogenes, Str. pneumoniae, Str. mutans, Staphylococcus (S.) aureus, S. epidermidis, Escherichia (E.) coli, Pseudomonas (P.) aeruginosa, Proteus (Prot.) vulgaris, Klebsiella (Kl.) pneumoniae, Branchamella (Br.) catarrhalis, Haemophilus (H.) influenzae. Уровень сенсибилизации учитывали классами: 0 класс - антитела класса Е (ATE) или антитела класса G (ATG) ниже 1 нг/мл, I класс - ATE или ATG в пределах 1-2,5 нг/ мл, II класс - ATE или ATG в пределах 2,6-50 нг/мл, III класс - ATE или ATG в пределах 5,1-10 нг/мл, IV класс - ATE или ATG свыше 10 нг/мл. При выявлении поливалентной аллергии с очень высокой концентрацией аллергенспецифических антител класса Е проводили повторные исследования на глистную инвазию. Исследования проводили только до начала лечения с целью характеристики спектра иммунных ответов к условно-патогенным и патогенным микроорганизмам.
Для изучения остро фазовых проявлений иммунопатологических реакций исследовали уровень ACЛ-0, АСГ, СРВ и РФ. Данные исследования проводили в реакциях латексной агглютинации на наборах фирмы ООО «Оливекс», Россия, согласно прилагаемым инструкциям, до начала лечения, через 17 дней от начала лечения, а также через 6 месяцев от начала лечения.
У всех обследованных детей проводили посев на питательные среды отделяемого носа и ротоглотки с последующей идентификацией выделенной чистой культуры микроорганизмов. Учитывали количественное содержание микроорганизмов, рассчитанное в КОЕ/тампон, по методике, изложенной в приказе МЗ РФ № 535 от 22.04.85 г. Данное исследование проводили в бактериологической лаборатории МУЗ ДГКБ № 5 (директор д.м.н. М.И. Ликстанов). Кроме того, проводили исследования молекулярных маркеров цитомегаловируса (ЦМВ) и вируса Эпштейна-Барра (ВЭБ) в клеточном соскобе со слизистых оболочек задней стенки глотки и нёбных миндалин методом полимеразной цепной реакции в реальном времени. Количество ампликонов оценивали копий на мл. Для оценки степени инфицирования глоточного биотопа детей условно-патогенными и патогенными микроорганизмами, а также наличия вирусных геномов их количественное содержание у индивидуума отражали в среднем логарифмическом титре. Исследование микробиоты глоточного биотопа и вирусных молекулярных маркеров проводили до начала лечения, через 17 дней от начала лечения, а также через 6 месяцев от начала лечения.
Все дети были рандомизированы на две подгруппы, получавших Мирамистин в составе базисной терапии (основная группа, n=154) и получавших только базисную терапию (группа сравнения, n=152). Рандомизацию проводили по дню недели: в четный день недели назначали Мирамистин, в нечетный - не назначали. Применяли орошение Мирамистином глотки через насадку-распылитель в объеме 5 мл (однократное нажатие на головку насадки-распылителя) 3 раза в день в течение 10 дней.
Базисная терапия включала в себя применение системных препаратов с противовоспалительным и муколитическим эффектами [12], антигистаминных средств в возрастных дозировках, а также ирригационной терапии физиологическими растворами морской соли. Для нанесения жидких лекарственных препаратов на слизистую оболочку носа и глотки применяли распылитель для жидких лекарственных средств и отсос, входящих в состав ЛOP-места «Азимут-ЗЧ». Курс лечения составлял 10 дней. После базисной терапии проводили 6-месячный курс иммунореабилитации с помощью мукозальных вакцин, содержащих рибосомальные антигены Klebsiella pneumoniae, Streptococcus pneumonia, Streptococcus pyogenes, Haemophilus influenzae, а также протеогликаны мембранной части Klebsiella pneumoniae согласно прилагаемым инструкциям [13].
Анализ данных проводили с помощью стандартных медико-статистических методов, используя пакет прикладных программ «Statistica for Windows, 6.0». Непараметрические количественные показатели сравнивали с помощью критерия Манна-Уитни, а параметрические - с помощью критерия Стьюдента. Результаты считали достоверными при ошибке менее 5%, что соответствует медико-биологическим исследованиям.
Результаты и их обсуждение
Проведенное исследование показало, что в группе детей, имеющих иммунный ответ по IgG-типу к Streptococcus pyogenes, средняя частота ОРИ за один год составила Ме=4,35 случаев/год (LQ=3,91; UQ=4,71), а средняя степень гипертрофии миндалин лимфоидного глоточного кольца - Ме=2,81 степени (LQ=2,51; UQ=3,03). Во всей обследованной группе наследственная отягощенность по аллергическим заболеваниям встречалась в 97,38%, фетоплацентарная недостаточность и гипоксия плода (при беременности данным ребенком) - в 89,86%, кожные проявления пищевой аллергии на первом году жизни - в 98,36% и тимомегалия в анамнезе - в 27,45% случаев. Эти данные показывают, что у детей с сенсибилизацией к Streptococcus pyogenes имели место как предрасположенность к иммунопатологическим реакциям, так и несостоятельность фетоплацентарного обмена антигенами (в т.ч. инфекционными) между матерью и плодом. Необходимо отметить, что микробиота плода и в дальнейшем ребенка формируется в перинатальный период под воздействием материнского микроокружения. С этих позиций первичная колонизация Streptococcus pyogenes слизистых оболочек плода и новорожденного ребенка также была связана с материнской микроэкологией [6, 14]. В целом, эти две составляющие (генетическая и микроэкологическая) могли быть ведущими в этиологии и патогенезе формирующихся после рождения аутоиммунных и аллергических заболеваний у этих детей.
Исследование цитокинового статуса в иммунной системе, ассоциированной со слизистыми оболочками носа и глотки, характера иммунных реакций на антигены стрептококка (АСЛО, АСГ) и на Fc-фрагмент IgG (РФ), а также уровня системного воспаления, отраженного в концентрациях ЦИК И СРБ в периферической крови, показало отклонение от межквартильных интервалов, выведенных на выборке здоровых детей (рис. 1). Прежде всего это касалось СРБ, АСГ, РФ и АСЛО, для которых было показано значительное увеличение их концентрации в периферической крови. Из цитокинов НФС только TNFα был выше нормальных значений. Представленные данные показывают, что сенсибилизация к Streptococcus pyogenes протекает на фоне иммунопатологических реакций, направленных не только на антигены стрептококка, но и на аутоантигены организма. В частности, у этих детей повышены гуморальные иммунные реакции. Повышенный локальный синтез TNFα доказывает наличие воспалительного процесса на слизистых оболочках носа и глотки.
Рис. 1. Особенности системных гуморальных реакций и локального синтеза цитокинов (НФС) у детей, сенсибилизированных к Streptococcus pyogenes.
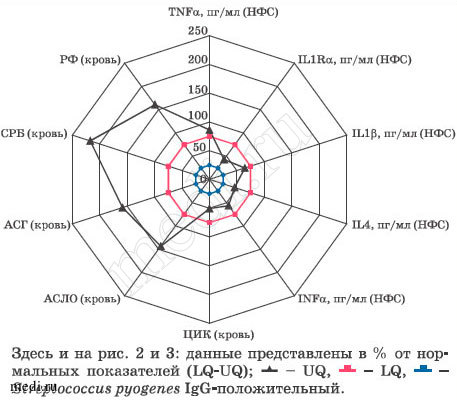
Оценка особенностей микробного пейзажа носоглоточного биотопа у детей, имеющих иммунный ответ по IgG-типу к Streptococcus pyogenes, показало следующее (рис. 2).
Рис. 2. Особенности микробного и вирусного пейзажа глоточного биотопа у детей, сенсибилизированных к Streptococcus pyogenes.
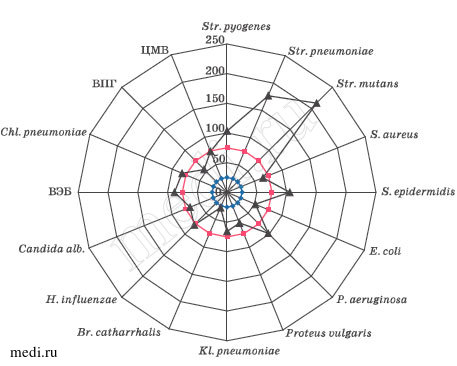
Превышение верхнего квартиля было показано не только для Streptococcus pyogenes, но и для Str. pneumoniae, Str. mutans, S. epidemidis и P. aeruginosa. Причем доминантным микроорганизмами были Str. mutans и Str. pneumoniae. Из вирусных геномов наиболее экспрессированным был ВЭБ. Учитывая тот факт, что у этих детей в НФС был повышен TNFα, можно говорить о декомпенсации у них дисбиоза слизистых оболочек верхних дыхательных путей с преимущественной активацией патогенных стрептококков и синегнойной палочки.
При исследовании в периферической крови антител класса G и Е к антигенам условно-патогенной и патогенной микрофлоры наиболее выраженные изменения были выявлены для атопических иммунных ответов (рис. 3). Обнаружено, что, помимо антител класса G, на антигены Streptococcus pyogenes синтезировались антитела класса Е. Атопический иммунный ответ у этих детей формировался к Str. pneumoniae, S. aureus, Proteus vulgaris, Kl. pneumoniae.
Рис. 3. Особенности атопического иммунного ответа по IgE-типу к УПМ глоточного биотопа у детей, сенсибилизированных к Streptococcus pyogenes.
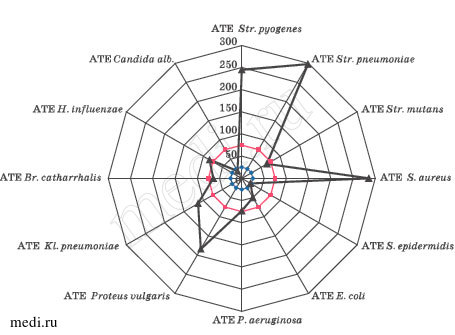
Развитие атопических иммунных реакций на условно-патогенную и патогенную микрофлору слизистых оболочек респираторного и желудочно-кишечного трактов пролонгирует локальное воспаление, снижает защитные функции мукозального иммунитета, повышает риск развития пищевой аллергии.
Тем самым представленные данные показали, что дети с рецидивирующими ОРИ, гипертрофией миндалин лимфоидного глоточного кольца и с сенсибилизацией к антигенам Streptococcus pyogenes относятся к группе высокого риска по формированию аллергических (прежде всего бронхиальной астмы) и аутоиммунных (прежде всего ревматическая патология) заболеваний. Эти дети имеют признаки декомпенсации дисбиоза слизистых оболочек носа и глотки (преимущественно стрептококковой этиологии) с проявлениями локального воспаления и активацией системных стрептококк-ассоциированных иммунопатологических реакций. С этих позиций для этих детей особую значимость имеет эффективная санации носоглоточного биотопа в острый период заболевания с последующим закреплением эффекта с помощью иммунореабилитации.
Проведенный сравнительный по клинико-иммунологическим характеристикам анализ двух групп, рандомизированных по приему Мирамистина в острый (ринит, аденоидит, фарингит) период заболевания, показал следующее.
Рис. 4. Динамика частоты ОРИ и степени гипертрофии лимфоидного глоточного кольца после проведенного лечения в группах, получавших и неполучавших Мирамистин.
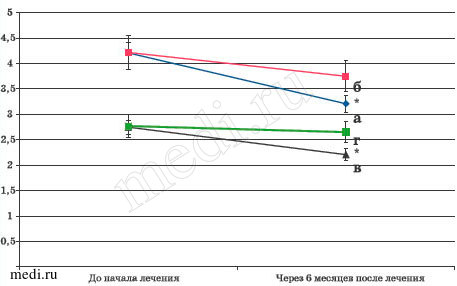
а - частота респираторных инфекций, число/год, (Мирамистин+); б - частота респираторных инфекций, число/год, (Мирамистин-); в - степень гипертрофии лимфоидного глоточного кольца, число/год, (Мирамистин+); г - степень гипертрофии лимфоидного глоточного кольца, число/год, (Мирамистин-).
Через 6 месяцев (рис. 4) после начала лечения (10 дней базисной терапии и 6 месяцев мукозальной вакцинации) в группе детей, получавших Мирамистин в острый период заболевания, число ОРИ достоверно снизилось (анализ за 6 месяцев, экстраполирование на 1 год) с Ме=4,35 (LQ=3,91; UQ=4,71) до Ме=3,33 случаев/год (LQ=3,06; UQ=3,49) (р<0,05). В то же время в группе детей, получавших в острый период заболевания только базисную терапию, не включавшую Мирамистин, через 6 месяцев число ОРИ также уменьшилось, но достоверных различии с исходным уровнем не получено (р>0,05). Похожая ситуация наблюдалась при анализе изменения степени гипертрофии миндалин лимфоидного глоточного кольца (рис. 4). Степень гипертрофии миндалин лимфоидного глоточного кольца достоверно снизилась в группе детей, получавших Мирамистин в острый период заболевания - с Ме=2,81 степени (LQ=2,51; UQ=2,97) до Ме=2Д2 степени (LQ=2,04; UQ=2,43) (р<0,05). В группе сравнения средняя степень гипертрофии миндалин лимфоидного глоточного кольца также уменьшилась, но достоверных различий с исходным уровнем не получено (р>0,05).
Выраженные изменения после проведенного 6-месячного лечения касались некоторых системных и локальных иммунных показателей (рис. 5). В крови у пациентов, получавших в острый период Мирамистин, достоверно снизились концентрации АСГ (с Ме=72,84 (LQ=62,41; UQ=83,51) до Ме=52,09 МЕ/мл (LQ=44,26; UQ=58,35) (р<0,05) и АСЛО (с Ме=48,29 (LQ=39,31; UQ=56,38) до Ме=27,29 МЕ/мл (LQ=21,15; UQ=32,21) (р<0,05) - основных антител, определяющих развитие ревматической патологии. Причем, как видно из рис. 5, заметное снижение антител произошло за 6 месяцев лечения, но не в период реконвалесценции ОРИ. В группе сравнения для этих иммунопатологических реакций достоверных различий с исходным уровнем не получено (р>0,05).
Рис. 5. Динамика синтеза локального TNFα (НФС) и антител к антигенам БГСА в крови после проведенного лечения в группах, получавших и неполучавших Мирамистин.
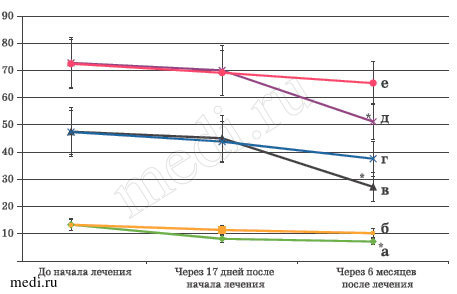
а - TNFα, пг/мл, (НФС), (Мирамистин+); б - TNFα, пг/мл, (НФС), (Мирамистин-); в - АСЛО, МЕ/мл, (кровь), (Мирамистин+); г - АСЛО, МЕ/мл, (кровь), (Мирамистин-); д - АСГ, МЕ/мл, (кровь), (Мирамистин+); е - АСГ, МЕ/мл, (кровь), (Мирамистин-).
В НФС у детей основной группы через 6 месяцев после лечения отмечено достоверно значимое снижение TNFα по отношению к исходному уровню (с Ме=13,55 (LQ=11,21; UQ=16,32) до Ме=7,19 пг/мл (LQ=5,21; UQ=8,17) (р<0,05). В группе сравнения этот показатель достоверно не изменился (р>0,05).
Особенности экспрессии условно-патогенных и патогенных представителей назофарингеального биотопа изменился после проведения противовоспалительной терапии с участием Мирамистина и иммунореабилитации (рис. 6).
Рис. 6. Динамика условно-патогенной и патогенной микрофлоры в глоточном биотопе после проведенного лечения в группах, получавших и неполучавших Мирамистин.
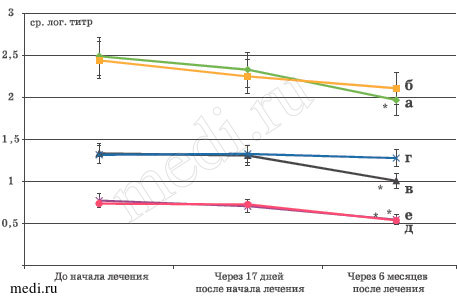
а - Str. pyogenes, с.л.т., кровь, (Мирамистин+); б -Str.pyogenes, с.л.т., кровь, (Мирамистин-); в - Str.pneumoniae, с.л.т., кровь, (Мирамистин+); г -Str. pneumoniae, с.л.т., кровь, (Мирамистин-); д - P. aeruginosa, с.л.т., кровь, (Мирамистин+); е - P. aeruginosa, с.л.т., кровь, (Мирамистин-).
Из рис. 6 видно, что достоверно значимое снижение (по отношению к первичному исследованию) колонизации слизистых оболочек носа и глотки через 6 месяцев после начала лечения было показано для трех микроорганизмов и только в группе получавших Мирамистин. Выявили снижение среднего логарифмического титра КОЕ/тампон следующих микроорганизмов: Streptococcus pyogenes - с Ме=2,51 (LQ=2,13; UQ=2,78) до Ме=1,97 с.л.т. (LQ=1,65; UQ=2,28) (р<0,05); Str. pneumoniae - с Ме=1,33 (LQ=1,19; UQ=1,48) до Ме=0,98 с.л.т. (LQ=0,71; UQ=1,19) (р<0,05); P. aeruginosa - с Ме=0,74 (LQ=0,61; UQ=0,89) до Ме=0,51 с.л.т. (LQ=0,46; UQ=0,59) (р<0,05).
Известно, что отсутствие антигена является важным фактором для формирования эффективного вакцинального иммунного ответа, в т.ч. и для мукозальных вакцин [15]. С этих позиций факт снижение колонизации слизистых оболочек носа и глотки Streptococcus pyogenes и другими микроорганизмами с патогенными свойствами у детей, получавших Мирамистин в острый период заболевания, указывает на первичную эффективную санацию слизистых оболочек носа и глотки от этих микроорганизмов. Именно локальное применение Мирамистина в острый период респираторного заболевания (ринит, аденоидит, фарингит) у детей раннего и дошкольного возраста с гипертрофией миндалин лимфоидного глоточного кольца эффективно санирует слизистую оболочку носа и глотки от Streptococcus pyogenes, Str. pneumoniae и P. aeruginosa, создавая предпосылки для дальнейшей иммунореабилитации и снижения этиологической значимости этих микроорганизмов в развитии аутоиммунных и аллергических заболеваний.
Заключение
Таким образом, проведенное исследование показало, что в группе детей с рецидивирующими ОРИ, с гипертрофией миндалин лимфоидного глоточного кольца и с сенсибилизацией к Streptococcus pyogenes риск формирования аутоиммунной и аллергической патологии повышен, что подтверждается высокой частотой как наследственной отягощенности по аллергическим заболеваниям, так и дебютом этой патологии на первом году жизни. Иммуноаллергологические профили этих детей дополнительно указывают на наличие системных аллергических и атопических иммунных реакций на стрептококки и синегнойную палочку, а также локального воспаления в носоглотке. В то же время топическое применение Мирамистина, как препарата с антибактериальной (включая противогрибковый эффект), противовирусной активностью и способного активировать подавленный врожденный иммунитет, в лечении острого заболевания JIOP-органов (ринита, аденоидита, фарингита) у этих детей с последующей их иммунореабилитацией приводит к эффективному снижению колонизационной активности на слизистых оболочках носа и глотки патогенных стрептококков (Streptococcus pyogenes, Str. pneumoniae) и синегнойной палочки. Кроме того, после курса базисной терапии с включением Мирамистина и иммунореабилитации у этих детей в отличии от группы сравнения снижается уровень иммунопатологических реакций на антигены БГСА и воспалительного процесса (связанного с TNFα) на слизистых оболочках носа и глотки. С этих позиций топическое введение Мирамистина на слизистые оболочки носа и глотки в острый период заболевания у детей из группы риска по формированию БГСА-ассоциированной патологии является важным этапом восстановительного лечения.
ЛИТЕРАТУРА
- Кутенкова НЖ. Роль атонической сенсибилизации к условно-патогенной микрофлоре в патогенезе рецидивирующих респираторных инфекций у детей раннего и дошкольного возраста: Автореф. дисс. ... канд. мед. наук. Кемерово, 2012.
- Dale JB, Niedermeyer ShE, Agbaosi T, Hysmith ND, Penfound ThA, Hohn CIM, Pullen M, Bright MI, Murrell DS, Shenep LE, Courtney HS. Protective Immunogenicity of Group A Streptococcal M-Related Proteins. Clinical and Vaccine Immunology. 2015; 22 (3): 344-355. doi: 10.1128/CVI.00795-14
- Armstrong C. AHA Guidelines on Prevention of Rheumatic Fever and Diagnosis and Treatment of Acute Streptococcal Pharyngitis. Am. Fam. Physician. 2010; 81 (3): 346-359.
- Luca-Harari B, Darenberg J, Neal Sh, Siljander T, Strakova L, Tanna A, Creti R, Ehelund K, Koliou M, Tassios PT, van der Linden M, Straut M, Vuopio-Varkila J, Bouvet A, EfstratiouA, Schalen C, Henriques-Normark B.JasirA. Clinical and Microbiological Characteristics of Severe Streptococcus pyogenes Disease in Europe. Journal of Clinical Microbiology. 2009; 47(4): 1155-1165. doi: 10.1128/JCM.02155-08.
- DinklaK.Rohde M, J arisen WTM, Kaplan EL, Chhatwal GS, Talay SR. Rheumatic fever-associated Streptococcus pyogenes isolates aggregate collagen. J. Clin. Invest. 2003; 111 (12): 1905-1912. doi: 10.1172/JCI200317247.
- Mead PhB. Vaginal-rectal colonization with group A streptococci in late pregnancy. Infectious Diseases in Obstetrics and Gynecology. 2000; 8 (5-6): 217-219. doi: 10.1155/ S1064744900000302.
- Lamagni ThL, Neal Sh, Keshishian C, Alhaddad N, George R, Duckworth G, Vuopio-Varkila J, Efstratiou A. Severe Streptococcus pyogenes Infections, United Kingdom, 2003-2004. Emerging Infectious Diseases. 2008; 14 (2): 201-209. doi: 10.3201/eidl402.070888.
- Кривошеий. Ю.С., Нестерова И.Е., Рудько АЛ. Морфологическое изучение влияния поверхностноактивных веществ на кожу и слизистые. Морфогенез и регенерация. Киев: б/и, 1977: 98-100.
- Кривошеий Ю.С. Противомикробные свойства новых ПАВ и обоснование их медицинского применения: Автореф. дисс. ... докт. мед. наук. Киев, 1985: 35.
- Успехи медицинской микологии. Ю.В. Сергеев, ред. М.: Национальная Академия Микологии, 2004; 4 (9): 227-228.
- Самсыгина ГА. Противовоспалительная терапия острых респираторных инфекций у детей. Педиатрия. 2011; 90(1): 102-106.
- Фенспирид. Реестр лекарственных средств. PeJIeC. ру (21.04.2001). rlsnet.ru/mnn_index_id_1783. htm
- Инструкция по применению лекарственного препарата для медицинского применения РИБОМУНИЛ. МЗ РФ, П№ 011369/01, 19.02.2013//http://www.pierre-fabre-russia.ru/upload/medialibrary/20032014/Ribomunil-pills_18.02.2013.pdf
- Yagupsky Р, Landau D, Beck A, Dagan R. Carriage of Streptococcus pyogenes among infants and toddlers attending day-care facilities in closed communities in southern Israel. Eur. J. Clin. Microbiol Infect Dis. 1995; 14 (1): 54-58. doi: 10.1590/S0036-36342007000500002.
- Йегер JI. Клиническая иммунология и аллергология. М.: Медицина, 1994; 3.


