Детский церебральный паралич и эпилепсия
Статьи
Опубликовано в журнале:
« Вопросы практической педиатрии» Том 11, №4, 2016, с. 66-72
А.А.Холин, Н.Н.Заваденко, Е.С.Есипова
Российский национальный исследовательский медицинский университет им. Н.И.Пирогова, Москва, Российская Федерация
Частота встречаемости эпилепсии при ДЦП, по данным различных исследований, вставляет от 28 до 75%. У детей с ДЦП наблюдается широкий спектр эпилепсий - от крайне тяжелых форм, относящихся к эпилептическим энцефалопатиям, до прогностически благоприятных сочетаний с доброкачественными идиопатическими формами. Факторами риска развития эпилепсии при ДЦП являются: наличие неонатальных судорог; низкая оценка по шкале Апгар (<4 баллов); глубокая недоношенность (<31 нед гестации); неонатальная реанимация; отягощенный семейный анамнез по эпилепсии; ДЦП, обусловленный пренатальными факторами, особенно церебральными дисгенезиями; перенесенные внутриутробные инфекции (особенно герпетический энцефалит); гемиплегические и тетраплегические формы ДЦП; тяжелая степень умственной отсталости; наличие эпилептиформных разрядов на ЭЭГ. Рассматриваются особенности лечения эпилепсии при ДЦП, в том числе при наличии фармакорезистентности. Перспективы лекарственной терапии когнитивных нарушений связаны с применением ноотропных препаратов, стимулирующих механизмы нейропластичности и улучшающих состояние высших психических функций, но при этом не вызывающих нарастания эпилептиформной активности.
Ключевые слова: антиэпилептическая терапия, детский церебральный паралич, когнитивные нарушения, эпилепсия.
Cerebral palsy and epilepsy
A.A.Kholin, N.N.Zavadenko, E.S.Esipova
N.I.Pirogov Russian National Research Medical University, Moscow, Russian Federation
The incidence of epilepsy in CP, according to different authors, is 28 to 75%. Children with CP might have a wide range of epilepsies - from very severe forms referring to epileptic encephalopathy to prognostically favourable combinations with benign idiopathic forms. Risk factors of development of epilepsy in CP are: neonatal convulsions, low Apgar scores (<4 scores); deep prematurity (<31 wks of gestation); neonatal resuscitation; a family history of epilepsy; CP associated with prenatal factors, especially cerebral dysgenesis; intrauterine infections (especially herpes encephalitis); hemiplegic and tetraplegic forms of CP; severe mental retardation; epileptiform EEG discharges. The article discusses specificities of treating epilepsy in CP, including cases of drug resistance. Perspectives of drug therapy for cognitive disorders are related to the use of nootropic preparations that stimulate mechanisms of neuroplasticity and improve the higher mental functions but do not exacerbate epileptiform activity.
Keywords: anti-epileptic therapy, cerebral palsy, cognitive disorders, epilepsy.
Детский церебральный паралич (ДЦП) является сложным заболеванием центральной нервной системы (ЦНС), которое развивается в результате поражения, возникшего во внутриутробном, интранатальном и раннем постнатальном периодах, или вследствие аномалии головного мозга, при этом действие повреждающих факторов на незрелый мозг определяет разнообразие сочетаний двигательных и сенсорных расстройств, а также лежит в основе нарушений когнитивных функций, что необходимо учитывать при обосновании восстановительного лечения и социальной реабилитации больных [1].
Актуальной проблемой является развитие пароксизмальных расстройств у детей с ДЦП, особенно эпилепсии. Так, частота неонатальных судорог у детей с ДЦП превышает среднепопуляционную в 17 раз, фебрильных судорог -в 2,5 раза, а эпилепсии - более чем в 40 раз [2]. Наличие эпилепсии утяжеляет клиническую картину ДЦП, осложняет проведение реабилитационных мероприятий и влияет на прогноз двигательных, интеллектуальных функций, а также может представлять угрозу для жизни. Проблемой также является возможность аггравации эпилептических приступов и их появление de novo при применении интенсивных методов нейрореабилитации (электрофорез, иглорефлексотерапия, электроретиностимуляция и др.).
Эпилепсия при ДЦП встречается, по данным различных исследований, c вероятностью от 28 до 62 и даже 75% [4-6]. Наиболее реалистичными выглядят российские данные Е.Д.Белоусовой - 43,2% [2], что практически в точности подтверждается популяционными исследованиям в Швеции -44% [7]. Максимальная вероятность возникновения эпилепсии отмечается при гемиплегической (70,6%) и тетраплегической (66,1%) формах ДЦП [5].
Факторами риска развития эпилепсии при ДЦП являются [2, 8-11]: наличие неонатальных судорог; низкая оценка по шкале Апгар (<4 баллов); глубокая недоношенность (<31 нед гестации); неонатальная реанимация; отягощенный семейный анамнез по эпилепсии; ДЦП, обусловленный пренатальными факторами, особенно церебральными дисгенезиями; перенесенные внутриутробные инфекции (особенно герпетический энцефалит); гемиплегические и тетраплегические формы ДЦП; тяжелая степень умственной отсталости; наличие эпилептиформных разрядов на ЭЭГ (электроэнцефалограмме).
Особенности течения эпилепсии в сочетании с ДЦП [2, 5, 8-11]:
- в большинстве случаев (до 74,2%) эпилепсия у детей с ДЦП дебютирует на 1-м году жизни;
- часто ДЦП сочетается с тяжелыми эпилептическими энцефалопатиями младенческого и раннего детского возраста (синдромами Отахара, Веста, Марканда-Блюме-Отахара, Леннокса-Гасто и др.);
- в клинической картине преобладают сложные фокальные, вторично-генерализованные и так называемые «псевдогенерализованные» эпилептические приступы (атипичные абсансы, билатеральные тонические спазмы и миоклонические приступы фокального генеза);
- часто сочетаются эпилептические и неэпилептические пароксизмы, а также возможна их схожесть по кинематике, что вызывает сложности трактовки и дифференциальной диагностики. Примерами могут служить дистонические атаки по типу асимметричного шейного тонического рефлекса (АШТР) и тонические версивные эпилептические приступы;
- наличие эпилепсии усугубляет двигательные и когнитивные нарушения при ДЦП. При этом присоединение эпилептических приступов и эпилептиформных разрядов приводит к появлению когнитивной эпилептиформной дезинтеграции либо парциального когнитивного дефекта, а также возможному усилению моторного дефицита и потере определенных двигательных и речевых навыков. Эти явления нарушают такой стержневой критерий ДЦП, как отсутствие прогредиентности процесса;
- часто сочетаются ДЦП и доброкачественные эпилептиформные разряды детства (ДЭРД). У детей с перивентрикулярной лейкомаляцией и диффузными нарушениями миелинизации благоприятный прогноз для собственно эпилептических приступов сочетается с фармакорезистентностью эпилептиформных разрядов (типа ДЭРД) и дезинтегративных эпилептиформных процессов;
- у детей с ДЦП (за исключением случаев, обусловленных церебральными дисгенезиями) может отсутствовать корреляция между очагами эпилептиформной активности и зоной максимально выраженных структурных изменений при нейровизуализации;
- нередко возникает рефлекторная провокация приступов под воздействием аудиогенной и соматосенсорной стимуляции. Существует проблема дифференциальной диагностики стартл-рефлексов и стартл-эпилепсии у детей с ДЦП;
- более высокий риск рецидива эпилепсии у детей с ДЦП после отмены антиэпилептических препаратов (АЭП).
У детей с ДЦП наблюдается широкий спектр эпилепсий - от крайне тяжелых форм, относящихся к эпилептическим энцефалопатиям, до прогностически благоприятных сочетаний с доброкачественными идиопатическими формами.
Дети с тяжелым гипоксически-ишемическим поражением ЦНС и формированием ДЦП являются угрожаемыми по развитию тяжелых эпилептических энцефалопатий младенческого возраста. У больных синдромом Отахара нередко констатируется гемипарез или тетрапарез (клиника ДЦП); отмечаются разнообразные нарушения мышечного тонуса как с явлениями спастичности (чаще), так и гипотонии. У всех больных отмечается задержка психомоторного развития с первых месяцев жизни; с возрастом формируется тяжелая умственная отсталость. Безусловно, часть пациентов старшего детского возраста, которая наблюдается неврологами с диагнозом «ДЦП, симптоматическая фокальная эпилепсия, умственная отсталость» перенесли на определенном этапе развития (в первом полугодии жизни) синдром Отахара [12].
Нарушения двигательного развития у больных синдромом Веста различны и могут варьировать от умеренной задержки формирования установочных позотонических рефлексов до полного отсутствия развития двигательных навыков и установочных рефлексов с формированием ДЦП, либо лобной астазии-абазии. Наиболее тяжелые варианты синдрома двигательных нарушений у больных синдромом Веста включают тетраплегическую форму ДЦП и развитие атонически-астатического синдрома (форма Фёрстера) [13]. При синдроме Веста наличие тетрапареза отмечено у 24,6% детей, гемипареза - у 10,8%. При этом дети с инфантильными спазмами и гемипаретической формой ДЦП, как правило, имели на ЭЭГ асимметричную гипсаритмию по типу унилатеральной, а в структуре приступов преобладают асимметричные инфантильные спазмы с последующим присоединением типичных парциальных приступов и трансформацией в симптоматические фокальные формы эпилепсии с соответствующими ЭЭГ-паттернами в виде региональной эпилептиформной активности [14]. Пока еще недостаточно изучен вопрос, какие изменения на ЭЭГ предшествуют развитию гипсаритмии. Накапливаются клинические наблюдения, свидетельствующие о прогностически неблагоприятном появлении пятиточечных эпилептиформных комплексов (подобных ДЭРД) у детей первых месяцев жизни с гипоксически-ишемическим поражением ЦНС и лейкопатией. Данный паттерн (рис. 1) предшествовал появлению гипсаритмии, эпилептических спазмов и развитию эпилептической энцефалопатии (рис. 2). Появление комплексов типа ДЭРД в раннем младенческом возрасте нередко ассоциируется в последующем с тяжелыми когнитивными нарушениями у пациентов и может быть предиктором развития эпилептической энцефалопатии [15].
Рис. 1. ЭЭГ пациента Б-Х.А., мальчик, 4 мес. Диагноз: «Последствия тяжелого перинатального поражения ЦНС гипоксически-ишемического генеза. Задержка психомоторного и предречевого развития. Угроза по формированию ДЦП». Запись ЭЭГ во время бодрствования за 2 мес до дебюта у мальчика инфантильных спазмов. В правой центрально-теменной области отмечаются низкоамплитудные пятиточечные эпилептиформные комплексы, схожие по морфологии с «доброкачественными эпилептиформными разрядами детства» в центральных отделах.
Рис. 2. ЭЭГ того же пациента Б-Х.А., 8 мес. Диагноз в динамике через 4 мес: «Детский церебральный паралич. Спастический тетрапарез. Синдром инфантильных спазмов. Задержка психомоторного развития». А - запись ЭЭГ во время бодрствования с наличием модифицированной гипсаритмии с мультирегиональным компонентом (правая теменная, левая и правая лобные области). Б - запись ЭЭГ во время сна с наличием модифицированной гипсаритмии с персистированием «супрессивно-взрывного» паттерна и доминирующим региональным акцентом в правой теменной области. В - запись ЭЭГ во время серии флексорных аксиальных и аксоризомелических тонических спазмов со статусным течением. Отмечаются диффузные иктальные пробеги «lafa» с правополушарной теменной заинтересованностью, постприступное угнетение биоэлектрической активности, неполное восстановление картины модифицированной гипсаритмии, прерываемое следующим спазмом.
А
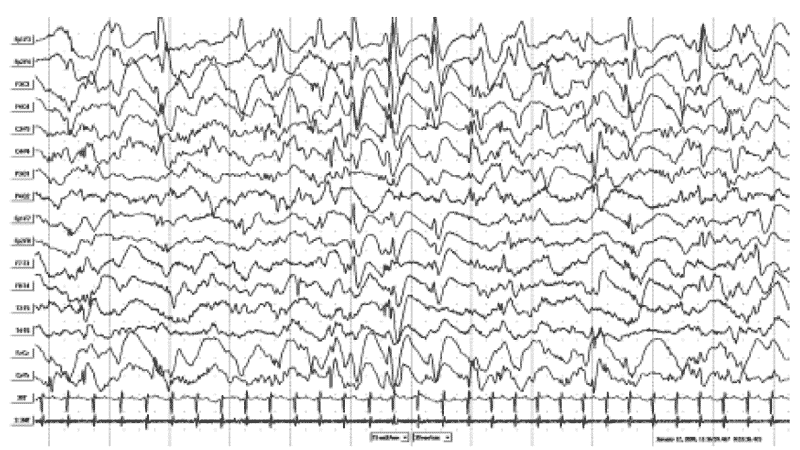
Б
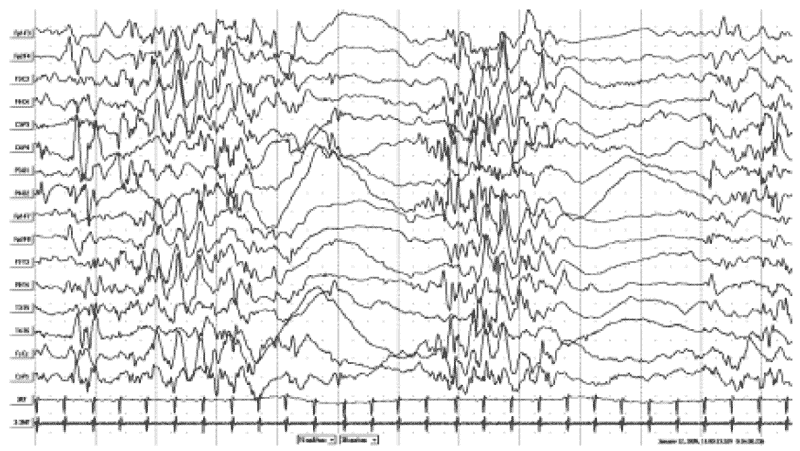
В
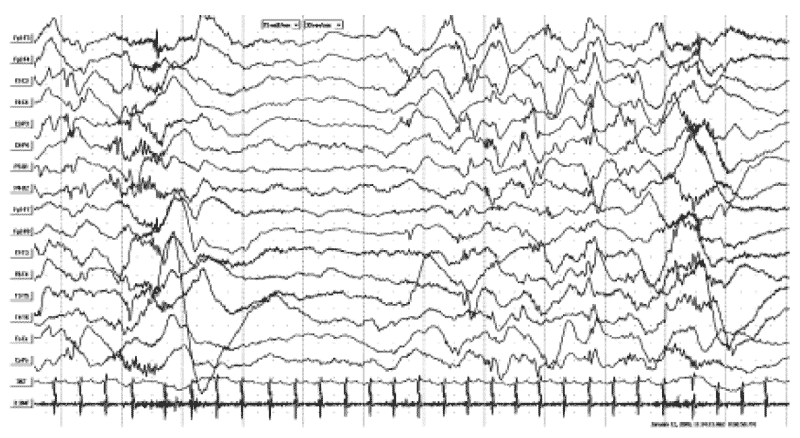
Примеры сочетания ДЦП, фокальной эпилепсии и наличия эпилептиформных разрядов типа ДЭРД нередки в клинической практике. В качестве примера приводим данные магнитно-резонансной томографии (МРТ) и ЭЭГ пациента Ш.И. (рис. 3, 4).
Рис. 3. Магнитно-резонансная томограмма больного Ш.И., 7 лет.
Диагноз: «Детский церебральный паралич, гемипаретическая форма (правосторонний гемипарез). Симптоматическая фокальная эпилепсия с правосторонними гемиконвульсивными, адверсивными, диалептическими и миоклонически-астатическими приступами. Порэнцефалическая киста теменно-височной области слева».
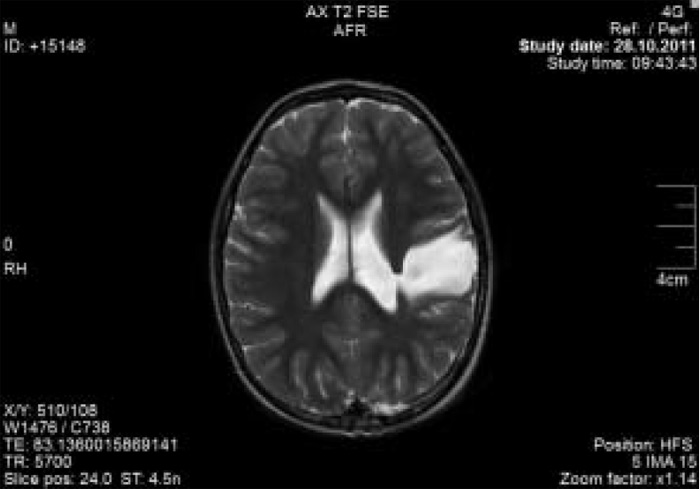
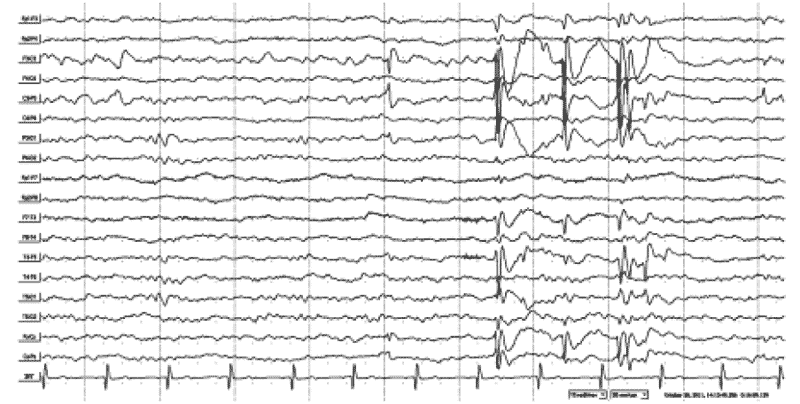
Рис. 4. ЭЭГ бодрствования больного Ш.И., 7 лет (тот же пациент). Региональная эпилептиформная активность в левой центральной и центрально-теменно-височной области в виде комплексов «острая-медленная» и «пик-волна». Региональные эпилептиформные разряды по своей морфологии нередко соответствуют ДЭРД, но также в виде высокоамплитудных медленных остро-медленноволновых разрядов и в сочетании с продолженным региональным замедлением.
За последние десятилетия в мировой научной и клинической практике накапливается опыт наблюдения пациентов с так называемой «двойной патологией» - наличием структурных нарушений в головном мозге и тяжелых двигательных нарушений в сочетании с эпилептическим идиопатическим компонентом (включая эпилептиформные разряды типа ДЭРД, благоприятный прогноз для эпилептических приступов и регресс эпилептиформных разрядов к достижению пубертата). К.Ю.Мухин и соавторы назвали данный особый эпилептический синдром с благоприятным течением эпилепсии, но с тяжелыми неврологическими нарушениями «фокальная эпилепсия детского возраста со структурными изменениями в мозге и доброкачественными эпилептиформными паттернами на ЭЭГ», сокращенно - ФЭДСИМ-ДЭПД [3].
Лечение эпилепсии у детей с ДЦП
Препаратами выбора в лечении эпилепсии у детей являются вальпроаты за счет широкого спектра действия, высокой эффективности и низкой вероятности аггравации. Вальпроаты применяются в дозировках 20-100 мг/кг/сут. Следует особо подчеркнуть, что высокая частота бульбарных расстройств у детей с ДЦП вызывает серьезные проблемы с применением таблетированных и капсульных форм АЭП. Данная проблема успешно решается применением таких форм вальпроатов, как депакин (хроносфера, сироп) и конвулекс (капли).
Помимо вальпроатов, в случаях приступов по типу атипичных абсансов, а также при ДЭРД-ассоциированных состояниях целесообразно применение сукцинимидов в суточных дозировках 20-35 мг/кг/сут.
У детей с ДЦП и эпилепсией, особенно при сочетании с когнитивными нарушениями, целесообразно применение леветирацетама, разрешенного в России у детей с 2-летнего возраста. Утвержденные терапевтические дозировки составляют 20-80 мг/кг/сут. Достоинством леветирацетама является сочетание антиэпилептического и ноотропного эффектов. Применение леветирацетама у детей первых двух лет жизни в более высоких дозировках требует коллегиального решения и информированного согласия.
В случаях применения препаратов карбамазепиновой группы, окскарбазепина, ламотриджина и топирамата у педиатрических пациентов до 7-летнего возраста следует учитывать риск аггравации феномена вторичной билатеральной синхронизации на ЭЭГ с клиническими проявлениями в виде аггравации миоклонических приступов, атипичных абсансов, а также вторично-генерализованных судорожных приступов. Данную группу препаратов следует комбинировать с АЭП широкого спектра и низкой аггравационной способности (вальпроатами), а также их применение требует тщательного динамического видео-ЭЭГ-контроля с целью раннего выявления признаков фармакоиндуцированной аггравации.
Учитывая высокий риск рецидивов эпилепсии и тяжесть структурных дефектов головного мозга у пациентов с ДЦП, продолжительность антиэпилептической терапии должна составлять не менее трех лет с момента достижения клинической ремиссии.
Стойкая ремиссия эпилептических приступов при ДЦП достигается более чем у половины пациентов (53,2 [5], 65 [2] и 75,3% [16]). Наиболее высокие показатели ремиссии эпилепсии при ДЦП гипоксически-ишемического генеза - 77,9% [6].
При наличии фармакорезистентной эпилепсии необходимо решать вопрос о возможности эпилептической хирургии, что будет целесообразно при церебральных дисгенезиях, особенно в случаях фокальных кортикальных дисплазий. Напротив, наличие структурного дефекта гипоксически-ишемического или постгеморрагического генеза и эпилептиформных разрядов типа ДЭРД контралатерально (в потенциально «здоровой» гемисфере как следствие сочетания ДЦП и идиопатического эпилептического компонента) является противопоказанием для эпилептической хирургии.
При фармакорезистентности и отсутствии возможности хирургической коррекции следует рассмотреть вопрос о целесообразности применения кетогенной диеты и имплантации вагостимулятора (VNS-терапии).
Перспективы лекарственной терапии когнитивных нарушений связаны с применением ноотропных препаратов, стимулирующих механизмы нейропластичности и улучшающих состояние высших психических функций [17]. При выборе лекарственной терапии в случаях сочетаний ДЦП с эпилепсией или субклинической эпилептиформной активностью на ЭЭГ следует отдавать предпочтение ноотропным препаратам, которые не вызывают нарастания эпилептиформной активности.
С.В.Балканская и соавт. [18] применили ноотропный препарат Пантогам (гопантеновая кислота) как дополнение к АЭП при лечении 21 пациента 6-8 лет с роландической эпилепсией, сопровождавшейся когнитивными нарушениями. С использованием тестовых компьютерных систем когнитивные параметры проанализированы до и после курса лечения гопантеновой кислотой на фоне базовой терапии АЭП. Продемонстрировано достоверно значимое положительное влияние препарата на показатели: кратковременной зрительной памяти, уровня внимания и точности образного мышления, распределения и переключения внимания, максимального темпа двигательных реакций, оперативности психических процессов.
В.И.Гузева и соавт. обследовали две группы детей 4-7 лет с разными формами эпилепсии и нарушений развития речи: основную (n = 40) и сравнения (n = 23) [19]. Пациенты принимали АЭП: вальпроаты (57 и 65%), топирамат (13 и 25%), карбамазепин (26 и 7%), окскарбазепин (4 и 3%). Пантогам (гопантеновая кислота) 10% сироп назначался в основной группе в дозе 20-30 мг/кг/сут курсом в течение 2 мес в дополнение к АЭП. При повторной ЭЭГ после этого курса у детей основной группы не выявлено изменения числа случаев с наличием эпилептиформной активности на ЭЭГ, но при этом уменьшилось число случаев с общими диффузными изменениями и задержкой созревания базового ритма с 47,5 до 40%, а у 7,5% ЭЭГ стала соответствовать возрастной норме. Различная степень эффективности Пантогама подтверждена у 77,5% детей с эпилепсией при нарушениях речи [19]. Одновременно в основной группе после лечения Пантогамом установлено существенное улучшение памяти (уменьшение числа ошибок, связанных с запоминанием слов), способности к обобщению и умения детей дифференцировать существенные и несущественные признаки предметов, а также кинетического праксиса [20]. У всех детей с эпилепсией отмечена хорошая переносимость препарата при отсутствии учащения приступов.
В качестве метаболической терапии детям с ДЦП, особенно в сочетании с эпилепсией, рекомендуется применение L-карнитина (препарат Элькар). L-карнитин улучшает белковый и жировой обмен, повышает устойчивость к физическим нагрузкам, угнетает образование кетокислот и анаэробный гликолиз, снижает выраженность лактат-ацидоза, способствует экономному расходованию гликогена и увеличению его запасов в печени и мышцах, оказывает анаболическое и липолитическое действие [21 ]. Пациентам с эпилепсией, принимающим вальпроаты и имеющим признаки карнитиновой недостаточности, следует периодически принимать курсы L-карнитина в дозах 20-100 мг/кг/сут.
Родителям пациентов с ДЦП с эпилепсией важно придерживаться ряда рекомендаций. Необходимо учитывать, что в настоящее время квалифицированный подбор АЭП, который осуществляет врач, позволяет в большинстве случаев постепенно достичь полного прекращения приступов у пациентов. В повседневной жизни важную роль играет организация здорового режима, спокойная домашняя обстановка. Особых ограничений в питании пациентам не требуется. Полезны занятия гимнастикой, физкультурой, но без элементов соревнования. Детям и особенно подросткам следует избегать позднего отхода ко сну и непривычно раннего пробуждения. Это особенно существенно при приступах, возникающих рано утром, в период пробуждения. Следует уменьшить время просмотра телепередач и компьютерных игр, но ни в коем случае не запрещать их (они должны быть полностью исключены лишь при фотосенситивной эпилепсии - форме эпилепсии, при которой приступы вызываются ритмичными световыми мельканиями). Физиотерапия с применением методик электро- и магнитотерапии противопоказана из-за риска аггравации эпилептических приступов и эпилептиформных разрядов на ЭЭГ.
Школьные занятия и задания должны выполняться в полном объеме. Необоснованные ограничения могут негативно сказаться на развитии ребенка как личности и способствовать формированию у него «комплекса неполноценности». Важно, чтобы ребенок не чувствовал себя изолированным от общества.
СПИСОК ЛИТЕРАТУРЫ
- Немкова СА, Намазова-Баранова ЛС, Маслова ОИ, Заваденко НН, Холин АА, Каркашадзе ГА, и др. Детский церебральный паралич: диагностика и коррекция когнитивных нарушений. М., Союз педиатров России, 2012, 56 с.
- Белоусова ЕД. Факторы риска, тактика лечения и прогноз судорожного синдрома и эпилепсии у детей с детским церебральным параличом. Автореф. дисс. ... докт. мед. наук. М., 2004, 48 с.
- Мухин КЮ, Миронов МБ, Боровиков КС, Петрухин АС. Фокальная эпилепсия детского возраста со структурными изменениями в мозге и доброкачественными эпилептиформными паттернами на ЭЭГ (ФЭДСИМ-ДЭПД) (предварительные результаты). Русский журнал детской неврологии. 2010;5(1):3-18.
- Bax M, Tydeman C, Flodmark 0. dinical and MRI Correlates of Cerebral Palsy. The European Cerebral Palsy Study. JAMA. 2006:296(13):1602-8.
- Bruck I, Antoniuk SA, Spessatto A, Bem RS, Hausberger R, Pacheco CG. Epilepsy in children with cerebral palsy. Arq Neuropsiquiatr. 2001;59(1):35-9.
- Rolon-Lacarriere OG, Hernandez-Cruz H, Tableros-Alcantara CM, Perez-Moreno JC. Control of epilepsy in children and adolescents suffering from cerebral palsy, with respect to their etiology and cerebral lesion background. Rev Neurol. 2006;15;43(9):526-30.
- Himmelmann K, Uvebrant P. Function and neuroimaging in cerebral palsy: a population-based study. Dev Med Child Neurol. 2011;53(6):516-21.
- Arpino C, Curatolo P, Stazi MA, Pellegri A, Vlahov D. Differing risk factors for cerebral palsy in the presens of mental retardation and epilepsy. J Child Neurol. 1999;14(3):151-5.
- Garfinkle J, Shevell MI. Cerebral palsy, developmental delay, and epilepsy after neonatal seizures. Pediatr Neurol. 2011;44(2):88-96.
- Mert GG, Incecik F, Altunbasak S, Herguner 0, Mert MK, Kiris N, et al. Factors affecting epilepsy development and epilepsy prognosis in cerebral palsy. Pediatr Neurol. 2011;45(2):89-94.
- Zelnik N, Konopnicki M, Bennett-Back 0, Castel-Deutsch T, Tirosh E. Risk factors for epilepsy in children with cerebral palsy. Eur J Paediatr Neurol. 2010;14(1):67-72.
- Ohtahara S, Ohtsuka Y, Oka E. Epileptic encephalopathies in early infancy. Indian J Pediatr. 1997 Sep-0ct;64(5):603-12.
- Dulac 0, Tuxhorn I. Infantile spasms and West syndrome. In: Epileptic syndromes in infancy, childhood and adolescence. 3 edition. Eds. J.Roger, M.Bureau, Ch.Dravet, P.Genton, C.A.Tassinari, P. Wolf - London: John Libbey, 2002, pp. 47-63.
- Холин АА. Возрастная фармакоиндуцированная эволюция младенческих и ранних детских форм эпилепсии. Автореф. дисс. ... канд. мед. наук. М., 2005, 29 с.
- Холин АА. Эпилептический статус в младенческом и раннем детском возрасте. Автореф. дисс. ... докт. мед.наук. М., 2010, 54 с.
- Zafeiriou DJ, Kontopoulos EE, Tsikoulas I. Characteristics and prognosis of epilepsy in children with cerebral palsy. J Child Neurol. 1999;14:289-94.
- Заваденко НН, Немкова СА. Нарушения развития и когнитивные дисфункции у детей с заболеваниями нервной системы. Научно-практическое руководство. М.: МК, 2016, 360 с.
- Балканская СВ, Студеникин ВМ, Кузенкова ЛМ, Маслова ОИ. Ноотропные препараты в коррекции когнитивных функций у детей с эпилепсией. Вопросы современной педиатрии. 2007;6(2):44-8.
- Гузева ВИ, Гузева ВВ, Гузева ОВ, Охрим ИВ, Згода ВН. Исследование терапевтического влияния гопантеновой кислоты (пантогама) у детей с эпилепсией и речевыми нарушениями. Педиатрия. Журнал имени Г.Н. Сперанского. 2015;94(3):148-55.
- Гузева ВИ, Гузева ВВ, Гузева ОВ, Охрим ИВ, Згода ВН. Диагностика и коррекция когнитивных нарушений у детей дошкольного возраста с эпилепсией. Журнал неврологии и психиатрии им. С.С.Корсакова. 2015;115(10):51-5.
References
- Nemkova SA, Namazova-Baranova LS, Maslova 0I, Zavadenko NN, Kholin AA, Karkashadze GA, et al. Detskii tserebral'nyi paralich: diagnostika i korrektsiya kognitivnykh narushenii. Moscow, Soyuz pediatrov Rossii, 2012, 56 p.
- Belousova ED. Faktory riska, taktika lecheniya i prognoz sudorozhnogo sindroma i epilepsii u detei s detskim tserebral'nym paralichom. Dissertation. Moscow, 2004, 48 p. (In Russian).
- Mukhin KYu, Mironov MB, Borovikov KS, Petrukhin AS. Focal epilepsy of childhood with structural brain changes and benign epileptiform discharges in EEG, FECSBC-BEDC (preliminary results). Russian Journal of Child Neurology. 2010;5(1):3-18. (In Russian).
- Bax M, Tydeman C, Flodmark 0. dinical and MRI Correlates of Cerebral Palsy. The European Cerebral Palsy Study. JAMA. 2006:296(13):1602-8.
- Bruck I, Antoniuk SA, Spessatto A, Bem RS, Hausberger R, Pacheco CG. Epilepsy in children with cerebral palsy. Arq Neuropsiquiatr. 2001;59(1):35-9.
- Rolon-Lacarriere 0G, Hernandez-Cruz H, Tableros-Alcantara CM, Perez-Moreno JC. Control of epilepsy in children and adolescents suffering from cerebral palsy, with respect to their etiology and cerebral lesion background. Rev Neurol. 2006;15;43(9):526-30.
- Himmelmann K, Uvebrant P. Function and neuroimaging in cerebral palsy: a population-based study. Dev Med Child Neurol. 2011;53(6):516-21.
- Arpino C, Curatolo P, Stazi MA, Pellegri A, Vlahov D. Differing risk factors for cerebral palsy in the presens of mental retardation and epilepsy. J Child Neurol. 1999;14(3):151-5.
- Garfinkle J, Shevell MI. Cerebral palsy, developmental delay, and epilepsy after neonatal seizures. Pediatr Neurol. 2011;44(2):88-96.
- Mert GG, Incecik F, Altunbasak S, Herguner 0, Mert MK, Kiris N, et al. Factors affecting epilepsy development and epilepsy prognosis in cerebral palsy. Pediatr Neurol. 2011;45(2):89-94.
- Zelnik N, Konopnicki M, Bennett-Back 0, Castel-Deutsch T, Tirosh E. Risk factors for epilepsy in children with cerebral palsy. Eur J Paediatr Neurol. 2010;14(1):67-72.
- 0htahara S, 0htsuka Y, 0ka E. Epileptic encephalopathies in early infancy. Indian J Pediatr. 1997 Sep-0ct;64(5):603-12.
- Dulac 0, Tuxhorn I. Infantile spasms and West syndrome. In: Epileptic syndromes in infancy, childhood and adolescence. 3 edition. Eds. J.Roger, M.Bureau, Ch.Dravet, P.Genton, C.A.Tassinari, P. Wolf - London: John Libbey, 2002, pp. 47-63.
- Kholin AA. Vozrastnaya farmakoindutsirovannaya evolyutsiya mladencheskikh i rannikh detskikh form epilepsii. Dissertation. Moscow, 2005, 29 p. (In Russian).
- Kholin AA. Epilepticheskii status v mladencheskom i rannem detskom vozraste. Dissertation. Moscow, 2010, 54 p. (In Russian).
- Zafeiriou DJ, Kontopoulos EE, Tsikoulas I. Characteristics and prognosis of epilepsy in children with cerebral palsy. J Child Neurol. 1999;14:289-94.
- Zavadenko NN, Nemkova SA. Narusheniya razvitiya i kognitivnye disfunktsii u detei s zabolevaniyami nervnoi sistemy. Moscow, 2016, 360 p.
- Balkanskaya SV, Studenikin VM, Kuzenkova LM, Maslova 0I, Tomilova AYu. Nootrope medications for cognitive disorders correction in children with epilepsy. Current pediatrics. 2007;6(2):92-6. (In Russian).
- Guzeva VI, Guzeva VV, Guzeva 0V, 0khrim IV, Zgoda VN. Surveillance of the therapeutic influence of Hopantenic acid (Pantogam) in children with epilepsy and speech disorders. Pediatria. Journal named after G.N.SPERANSKY. 2015; 94(3):148-55. (In Russian).
- Guzeva VI, Guzeva VV, Guzeva 0V, 0khrim IV, Zgoda VN. Diagnosis and correction of cognitive impairment in preschool age children with epilepsy. Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova. 2015;115(10):51-5. (In Russian).
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 pikfarma.ru
pikfarma.ru