Состояние детей, рожденных от многоплодной беременности, протекающей на фоне резус-изоиммунизации
СтатьиЛ.И. Ильенко1, д-р мед. наук, профессор, А.Г. Коноплянников1, д-р мед. наук, профессор, А.П. Кирющенков2, С.Р. Актулаева1
1 ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, г. Москва
2 ГБУЗ «Городская клиническая больница им. С.С. Юдина Департамента здравоохранения города Москвы»
Ключевые слова: многоплодная беременность, резус-изоиммунизация, гемолитическая болезнь, неонатальная заболеваемость
Keywords: multiple pregnancy, Rh-alloimmunization, hemolytic disease, neonatal morbidity
Резюме. Гемолитическая болезнь плода и новорожденного (ГБПиН) - распространенное заболевание, вызванное несовместимостью матери и плода по резус-фактору (изоиммунизация), являющееся одной из причин неонатальной заболеваемости и смертности.
Цель. Оценить состояние детей, рожденных от матерей с многоплодной беременностью и резус-изоиммунизацией.
Материалы и методы. Обследовано 124 новорожденных из двоен (118) и троен (6): 36 детей родились без признаков ГБ (I группа); 48 - с легким течением (II группа); 13 - со среднетяжелым течением (III группа); 27 - с тяжелыми формами заболевания (IV). 100 (80,6%) детей было из ДХДА двойни, 18 (14,5%) - из МХДА двойни, 6 (4,8%) - тройни.
Результаты. Отмечена высокая частота недоношенности при многоплодии (67,7%), составляющая 61,1%, 54,2%, 69,2% и 100% в I, II, III и IV группах соответственно. Асфиксия выявлена у 4,8% детей и только после экстренного кесарева сечения либо после родов через естественные родовые пути. Внутрижелудочковые кровоизлияния (ВЖК) II-IV степени, обусловленные недоношенностью и асфиксией, диагностированы у 0%, 8,3%, 23,1%, 25,9% детей I, II, III и IV групп соответственно; гипоксически-ишемические поражения ЦНС у 8,3%, 6,3%, 30,8%, 40,7%; ателектазы легких у 13,9%, 14,5%, 15,4% и 37% (р < 0,05). Заменные переливания крови выполнены только в III и IV группах - у 38,5% и 70,4% соответственно (р < 0,05). Врожденные пороки развития выявлялись у 6%, 16,7% и 16,7% детей из ДХДА и МХДА двоен и троен, соответственно (р > 0,05). Погиб один (0,8%) новорожденный IV группы из МХДА двойни.
Заключение. На перинатальные исходы многоплодной беременности с резус-иммунизацией влияет не только тяжесть ГБПиН, но и метод родоразрешения, недоношенность, а также хориальность.
Summary. Hemolytic disease of the fetus and newborn (HDFN) is a common disease caused by maternal and fetal Rh factor incompatibility (alloimmunization). It is one of the causes of neonatal morbidity and death. Purpose. Assess the condition of newborns from Rh-alloimmunised multiple pregnancy. Materials and methods. 124 newborns from twins (118) and triplets (6) were examined: 36 children were born without signs of HD (group I); 48 - with a mild forms (group II); 13 - with a moderate forms (group III); 27 - with severe forms (group IV). 100 (80.6%) newborns were DCDA twins, 18 (14.5%) -MCDA twins, 6 (4.8%) - triplets. Results. There was a high incidence of prematurity in multiple pregnancy (67.7%), which is 61.1%, 54.2%, 69.2% and 100% in groups I, II, III and IV, respectively. Asphyxia was detected in 4.8% of children, only after an emergency caesarean section and vaginal delivery. Intraventricular hemorrhages (IVH) II-IV degree due to prematurity and fetal asphyxia were diagnosed in 0%, 8.3%, 23.1% and 25.9 % (groups I, II, III and IV, respectively); ischemic-hypoxic encephalopathy - in 8.3%, 6.3%, 30.8% and 40.7%; pulmonary atelectasis - in 13.9%, 14.5%, 15.4% and 37% (р < 0.05). Exchange transfusions were performed only in groups III and IV - 38.5% and 70,4%, respectively (p < 0.05). Congenital malformations were detected in 6%, 16.7% and 16.7% DCDA and MCDA twins and triplets, respectively (p > 0.05). One newborn (0.8%) from MCDA twins died (group IV). Conclusion. The perinatal outcomes of multiple pregnancies with Rh-immu-nization are affected not only by the severity of HDFN, also by the method of delivery, prematurity and chorionicity.
Для цитирования: Состояние детей, рожденных от многоплодной беременности, протекающей на фоне резус-изоиммунизации / Л.И. Ильенко [и др.] // Практика педиатра. 2025. № 1. С. 23-30.
For citation: The condition of children born from multiple pregnancies occurring against the background of Rh-alloimmunization / L.I. Ilyenko [et al.] // Pediatrician's Practice. 2025;(1): 23-30. (In Russ.)
Гемолитическая болезнь плода и новорожденного (ГБПиН), обусловленная резус-изоиммунизацией, несмотря на широкое внедрение иммунопрофилактики, является распространенным заболеванием и возможной причиной неонатальной смертности [1-5].
Резус-изоиммунизация отмечается у 0,1% беременных с многоплодием, что в три раза реже, чем при одноплодной беременности [6, 7]. Однако работ, посвященных оценке состояния детей, рожденных от матерей с многоплодной беременностью и резус-изоиммунизацией, в современной литературе практически нет, что послужило основанием для нашего исследования.
МАТЕРИАЛЫ И МЕТОДЫ
Проведено сплошное исследование, включающее 124 новорожденных от матерей с многоплодием и резус-изоиммунизацией, обследованных за период с 2006 по 2020 г. на базе ГБУЗ «Центр планирования семьи и репродукции (ЦПСиР) Департамента здравоохранения города Москвы» (ныне - «ГКБ имени С.С. Юдина»).
Критерии включения в исследование: дети, зачатые самопроизвольно или посредством экстракорпорального оплодотворения (ЭКО), от многоплодной беременности двойней или тройней с дихориальным (ДХ) и монохориальным (МХ) типами плацентации, протекающей на фоне резус-изоиммунизации.
Критерии исключения: АВО-сенсибилизация; водянка плода неиммунного генеза; селективный перенос эмбрионов с резус-отрицательным генотипом в программе ВРТ.
У 9 из 124 (7,3%) детей матери были первородящими, у 26 (21%) - первобеременными. Из дихориальной диамниотической (ДХДА) двойни было 100 (80,6%) детей; из монохориальной диамниотической (МХДА) двойни - 18 (14,5%), в том числе с фетофетальным трансфузионным синдромом (ФФТС) - 2; из дихориальной триамниотической (ДХТА) тройни - 6 (4,8%). Самопроизвольно зачаты 99 из 124 (79,8%) новорожденных; посредством ЭКО - 25 (20,5%), при этом 16 из 25 (64%) детей родились с признаками ГБ, в том числе 5 (20%) - с тяжелыми формами заболевания.
В зависимости от наличия и тяжести ГБН все новорожденные разделены на четыре группы: в I группу вошли 36 из 124 (29%) детей без признаков заболевания (уровень гемоглобина в пуповинной крови 180-200 г/л): 20 - с резус-положительной принадлежностью крови, 16 - с резус-отрицательной; во II - 48 (38,7%) детей с легким течением желтушной формы ГБ (уровень гемоглобина 140-179 г/л); в III группу включены 13 (10,5%) новорожденных со среднетяжелым течением желтушной формы (уровень гемоглобина 100-139 г/л); в IV - 27 (21,8%) детей с тяжелыми формами заболевания (уровень гемоглобина <100 г/л), в том числе 3 - с отечной формой ГБ (ОФГБ).
У матерей во время беременности для диагностики ГБП и анемии плода применяли доплерографию с оценкой максимальной скорости кровотока (МСК) в средней мозговой (СМА) артерии плода по методике G. Mari и соавт. [8], учитывающей отклонения значений МСК СМА плода от медианы (multiples of the median, МоМ). Внутриутробное переливание крови (ВПК) в сроки 28 и 32 нед гестации однократно выполнено трем плодам у 2 (3,2%) беременных при значениях значения МСК СМА плода >1,5 МоМ.
Сроки родоразрешения новорожденных I группы составили 35,5 ± 2,3 нед гестации, II - 35,7 ± 2,0 нед, III - 33,8 ± 2,9 нед, IV - 32,4 ± 1,9 нед. Через естественные родовые пути родились 50 из 124 (40,3%) новорожденных [37 из 50/74% - из I-II групп], путем планового кесарева сечения (КС) - 14 (11,3%) [13 из 14/92,8% - из I-II групп], экстренного кесарева сечения (ЭКС) - 60 (48,4%) [33 из 60/55% - из III-IV групп].
Параметры физического развития новорожденных определялись согласно нормативам (НФР), разработанным для детей от многоплодной беременности.
Для статистической обработки данных применяли пакет программ IBM SPSS Statistics 23. Для определения нормальности распределения использовали обобщенный тест Д’Агостино - Пирсона. Данные с нормальным распределением представляли как среднее значение ± стандартное отклонение, для их сравнения использовали t-test. Качественные данные представляли как абсолютное значение (n) и %, для их сравнения использовали точный тест Фишера. Результаты считали статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ
Доношенными родились 40 (32,3%) детей. Недоношенными были 84 (67,7%) ребенка: 22 из 36 (61,1%) -из I группы (без признаков ГБ), 26 из 48 (54,2%) - II (легкое течение), 9 из 13 (69,2%) - III (среднетяжелое). Частота недоношенности в IV группе (тяжелые формы ГБ) составила 100%, что было статистически больше, чем в I-III группах (р < 0,05).
В удовлетворительном состоянии родилось 118 детей (95,2%); в состоянии умеренной асфиксии -5 (4%) детей I, II и IV групп из ДХДА (3) и МХДА (2) двоен, зачатых самопроизвольно и рожденных в сроки 29-30 нед гестации путем экстренного кесарева сечения (ЭКС). Тяжелая асфиксия диагностирована у 1 (0,8%) ребенка из спонтанной ДХДА двойни со среднетяжелым течением желтушной формы ГБ (III группа), рожденного через естественные родовые пути в срок 29 нед гестации в связи с развитием у матери спонтанной родовой деятельности. Следовательно, частота асфиксии зависела не только от тяжести ГБ, но и от метода родоразрешения, так как была выше у пациенток, родоразрешенных досрочно через естественные родовые пути, чем посредством экстренного КС.
Таблица 1. Параметры физического развития новорожденных (M ± SD)
|
Параметры физ. развития |
Срок гестации на момент родоразрешения |
|||
|
29-316нед |
32-336 нед |
34-366 нед |
37-38 нед |
|
|
масса, г |
1668,5 ± 384,2 |
1822,9 ± 198,6* |
2398,4 ± 402,4* |
2613,5 ± 304,8* |
|
рост, см |
40,7 ± 4,9 |
40,9 ± 2,4 |
44,3 ± 4,6* |
47,3 ± 1,5* |
|
МРП |
40,6 ± 5,7 |
44,6 ± 5,3* |
54,6 ± 6,5* |
55,1 ± 5,2* |
* Значения статистически значимо отличаются от таковых в сроки 29-316 нед (р < 0,05).
Таблица 2. Средняя суммарная масса близнецов и разница в их массе (M ± SD)
|
Срок (нед) |
Средняя суммарная масса новорожденных, г |
Разница в массе, г/% |
|
|
29-316 |
2813,8 ± 305,6 |
243,3 ± 156,5 |
7,3 ± 4,5% |
|
32-336 |
3795,8 ± 376,5* |
265,4 ± 176,1* |
9,2 ± 7,1%* |
|
34-366 |
4789,5 ± 478,3* |
278,2 ± 195,5* |
10,4 ± 8,3%* |
|
37-38 |
5235,4 ± 512,3* |
268,3 ± 213,5* |
9,5 ± 7,2%* |
* Значения статистически значимо отличаются от таковых в сроки 29-316 нед (р < 0,05).
Дыхательные расстройства (ДР) различной степени тяжести при рождении выявлены практически у половины детей (61 из 124/49,2%): в I группе -у 27,8% (10 из 36), во II - у 35,4% (17 из 48); частота ДР в III (9 из 13/69,2%) и IV (25 из 27/92,6%) группах была статистически значимо выше, чем в I группе (р < 0,05), что, на наш взгляд, обусловлено высокой частотой недоношенности при тяжелых формах ГБН, поскольку недоношенность была фактором риска возникновения дыхательных расстройств (OR 4.12; 95% ДИ:1.23-8.56, p = 0,001). У 52 из 61 (85,2%) новорожденных с дыхательными расстройствами выполнялась респираторная поддержка: у 30 - искусственная вентиляции легких (ИВЛ), у 22 -вспомогательная вентиляция с постоянным положительным давлением (CPAP).
Признаки морфофункциональной незрелости (МФН) выявлены у 14 из 40 (35%) доношенных детей I-III групп.
Параметры физического развития новорожденных представлены в табл. 1 и 2. Маловесными к сроку гестации родились 33 (26,6%) ребенка.
Также нами отмечено, что масса, рост и массо-ростовой показатель (МРП) в аналогичные сроки гестации у новорожденных из ДХДА двоен были больше, чем у детей из МХДА двоен и троен, однако различия были статистически незначимые (р > 0,05). Не влиял на параметры физического развития новорожденных и метод наступления многоплодной беременности (спонтанная или посредством ВРТ) (р > 0,05).
Дополнительно установлено, что параметры физического развития детей I и II групп были статистически значимо больше (р < 0,05), чем таковые у новорожденных III и IV групп, из-за больших сроков родоразрешения и более низкой частоты недоношенности в I и II группах (35,5 ± 2,3 и 35,7 ± 2,0 недель гестации; 61,1% и 54,2%, соответственно), по сравнению с III и IV группами (33,8 ± 2,9 и 32,4 ± 1,9 нед; 69,2% и 100%). Следовательно, дети с тяжелыми формами ГБН чаще были недоношенными и, как следствие, имели меньшие параметры физического развития, чем дети без ГБ или легким течением заболевания (табл. 3).
Таблица 3. Параметры физического развития новорожденных различных групп (M ± SD)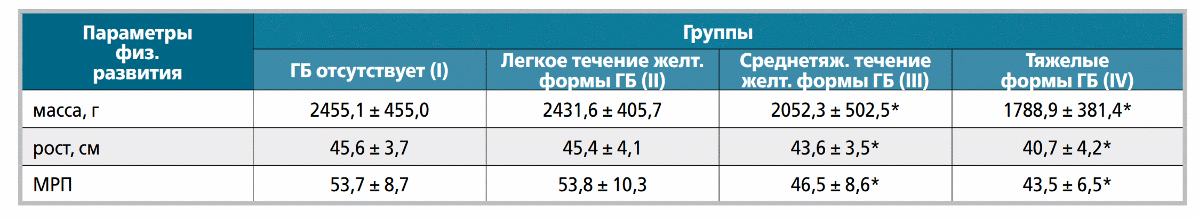
* Значения статистически значимо отличаются от таковых в I и II группах (р < 0,05).
При проведении исследования особое внимание уделялось последствиям перенесенной перинатальной гипоксии-ишемии, в частности внутрижелудочковым кровоизлияниям (ВЖК) II-IV степени, диагностированным у 14 (11,3%) детей. ВЖК чаще выявлялись при тяжелых формах ГБН, чем при легком течении желтушной формы заболевания: 25,9% и 8,3% (р = 0,04). Также обращало внимание, что большинство детей с ВЖК (9 из 14; 64,3%) родились преждевременно в сроки 29-31 нед гестации.
На возникновение гипоксического поражения ЦНС без ВЖК оказывала влияние тяжесть ГБН, так как заболевание реже выявлялось в I (8,3%) и II группах (6,3%), чем в III (30,8%) и IV (40,7%) группах (р < 0,05) (табл. 4).
Таблица 4. Заболеваемость у 124 новорожденных (n/%)
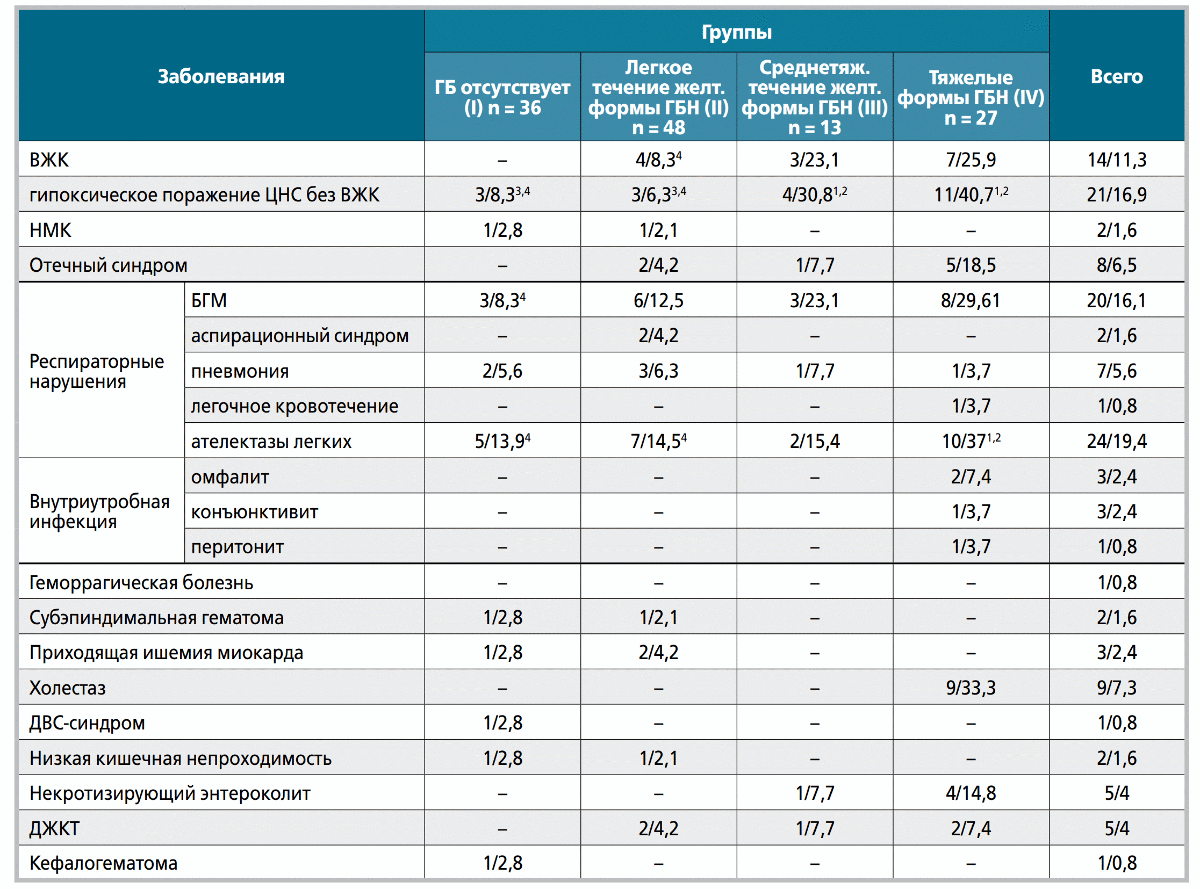
n - значения статистически значимо отличаются от показателей в n группе (р < 0,05).
Также нами установлено, что тяжесть гемолитической болезни влияла на частоту развития таких заболеваний, как ателектазы легких, болезнь гиалиновых мембран (БГМ) и некротизирующий энтероколит (НЭК), поскольку они чаще возникали у детей с тяжелыми формами ГБ, по сравнению с новорожденными из I и II групп (р < 0,05), что мы связываем с высокой частотой недоношенности пациентов IV группы. При построении логистической регрессии подтверждено, что фактором развития БГМ и НЭК была недоношенность (OR 4.35; 95% ДИ:1.56-9.58, p = 0,001). Холестаз диагностирован только в IV группе - у трети детей (33,3%).
Врожденные пороки развития [ВПР] (дефект межпредсердной перегородки, дефект межжелудочковой перегородки, агенезия почки, гидронефроз почки и пр.) обнаружены у 10 (8,1%) детей; статистически значимых различий между группами не выявлено. Частота ВРТ у детей из ДХДА двоен (6 из 100/6%) была ниже, чем у новорожденных из МХДА двоен (3 из 18/16,7%) и троен (1 из 6/16,7%); однако различия оказались статистически незначимы (р > 0,05).
Результаты клинического и биохимического анализов крови новорожденных различных групп представлены в табл. 5.
Таблица 5. Показатели клинического и биохимического анализов крови у детей с ГБ при рождении (n = 124)
|
Лабораторные показатели |
Группы |
|||
|
I (n = 36) |
II (n = 48) |
III (n = 13) |
IV (n = 27) |
|
|
Hb, г/л |
181,2 ± 24,1 |
173,6 ± 23,2* |
150,5 ± 26,8* |
97,1 ± 24,7* |
|
Ht, % |
52,2 ± 6,6 |
49,7 ± 6,5 |
41,6 ± 9,0* |
27,6 ± 5,1* |
|
Эритроциты, х1012/л |
4,9 ± 0,6 |
4,7 ± 0,6 |
3,8 ± 0,7* |
2,3 ± 0,9* |
|
Лейкоциты, х109 |
16,1 ± 3,3 |
14,9 ± 3,2 |
14,2 ± 3,9* |
13,1 ± 3,0* |
|
Тромбоциты, тыс. ед/мкл |
262,0 ± 36,9 |
264,9 ± 43,8 |
240,8 ± 13,2* |
224,6 ± 46,7* |
|
Билирубин общ., ммоль/л |
22,9 ± 6,3 |
31,1 ± 4,2* |
44,9 ± 6,9* |
73,4 ± 12,9* |
|
Билирубин прям., ммоль/л |
2,9 ± 0,1 |
3,1 ± 0,1 |
9,6 ± 1,4* |
17,2 ± 1,4* |
|
Белок, г/л |
46,5 ± 4,4 |
47,9 ± 3,5 |
39,6 ± 3,1* |
33,0 ± 3,6* |
|
АЛТ, ед/л |
8,1 ± 1,6 |
8,3 ± 1,3 |
14,2 ± 1,3* |
15,8 ± 1,9* |
|
АСТ, ед/л |
40,6 ± 4,0 |
42,5 ± 33,0 |
45,0 ± 10,2 |
61,3 ± 6,9* |
|
ПТИ, % |
67,0 ± 8,5 |
66,3 ± 5,3 |
60,3 ± 9,8 |
58,0 ± 8,2 |
|
pH |
6,8 ± 0,07 |
7,3 ± 0,07 |
7,3 ± 0,09 |
7,3 ± 0,08 |
|
BE, ммоль/л |
-3,9 ± 1,9 |
-4,5 ± 3,2 |
-5,2 ± 3,1 |
-5,2 ± 3,1 |
|
лактат, ммоль/л |
2,3 ± 0,3 |
2,7 ± 1,0 |
3,1 ± 0,7 |
3,2 ± 0,8 |
* Значения статистически значимо отличаются от таковых в I группе (р < 0,05).
Установлено, что у детей со среднетяжелым течением желтушной формы ГБ (III группа) и тяжелыми формами заболевания (IV группа), по сравнению с новорожденными I группы (отсутствует ГБ), были ниже уровни гемоглобина и гематокрита, количество эритроцитов, лейкоцитов и тромбоцитов, содержание белка, протромбиновый индекс (ПТИ); также были выше уровни общего билирубина, прямого билирубина, аланинаминотрансферазы (АЛТ) и значения дефицита буферных оснований ВЕ (р < 0,05).
При рождении у детей из МХДА двоен с тяжелыми формами ГБ (IV группа) по сравнению с новорожденными из ДХДА двоен и троен IV группы, были ниже (р < 0,05) уровни гемоглобина (63,7 ± 2,5; 98,7 ± 28,8 и 108,6 ± 26,2 г/л соответственно) и гематокрита (18,8 ± 3,1; 28,2 ± 7,6 и 30,3 ± 5,2%), количество эритроцитов (1,4 ± 0,1; 2,4 ± 0,3 и 2,8 ± 0,3 х1012/л) и тромбоцитов (167,0 ± 17,2; 224,8 ± 26,2 и 303,0 ± 24,7 тыс. ед/мкл), ПТИ (45,5 ± 3,7; 68,0 ± 2,7 и 72,0 ± 5,4%); также был выше уровень общего билирубина (79,4 ± 7,6; 68,5 ± 6,5 и 67,7 ± 5,3) и значения дефицита буферных оснований (-7,3 ± 4,1; -4,7 ± 3,1 и -5,3 ± 1,6 ммоль/л), что свидетельствовало о негативном влиянии МХ типа плацентации на тяжесть ГБ у новорожденных.
ЗПК в количестве от 1 до 6 выполнено каждому пятому ребенку (24 из 124/19,4%) на 0-3 сутки жизни: всем троим детям с ОФГБ, 16 из 24 (66,7%) -с тяжелым течением желтушной формы заболевания, 5 из 13 (38,5%) - со среднетяжелым течением ГБН. Одно ЗПК выполнено 16 (12,9%) детям: 5 (38,5%) - из III группы (среднетяжелое течение), 11 (40,7%) - из IV группы (тяжелые формы ГБ) (рис. 1).
Более одного ЗПК проводилось только в IV группе: 2 ЗПК - у 3 (11,1%) детей, 3 ЗПК - у 1 (3,7%), 4 ЗПК -у 2 (7,4%), 5 ЗПК - у 1 (3,7%), 6 ЗПК - у 1 (3,7%) ребенка.
Стоит подчеркнуть, что если у большинства детей с тяжелыми формами ГБ, не получавших внутриутробное лечение (17 из 25/68%), проводилось от 1 до 6 ЗПК (у 8 - многократные), то у новорожденных, перенесших внутриутробную гемотрансфузию, ЗПК либо не требовалось (2 из 3/75%), либо выполнено однократно (у 1 ребенка).
Помимо тяжести ГБН, факторами риска проведения ЗПК были: значения максимальной скорости кровотока в средней мозговой артерии плода >1,1 МоМ (OR 3.17; 95% ДИ:1.93-5.24, p = 0,002), МХ тип плацентации (OR 2.17; 95% ДИ:1.12-7.72, p = 0,002), беременность тройней (OR 4.63; 95% ДИ:1.06-24.49, p = 0,002).
Простая гемотрансфузия на 1-5 сутки жизни проведена у 27 из 124 (21,8%) новорожденных, переливание плазмы - у 26 (20,9%); чаще в IV группе, чем во II и III группах (р < 0,05) (рис. 1).

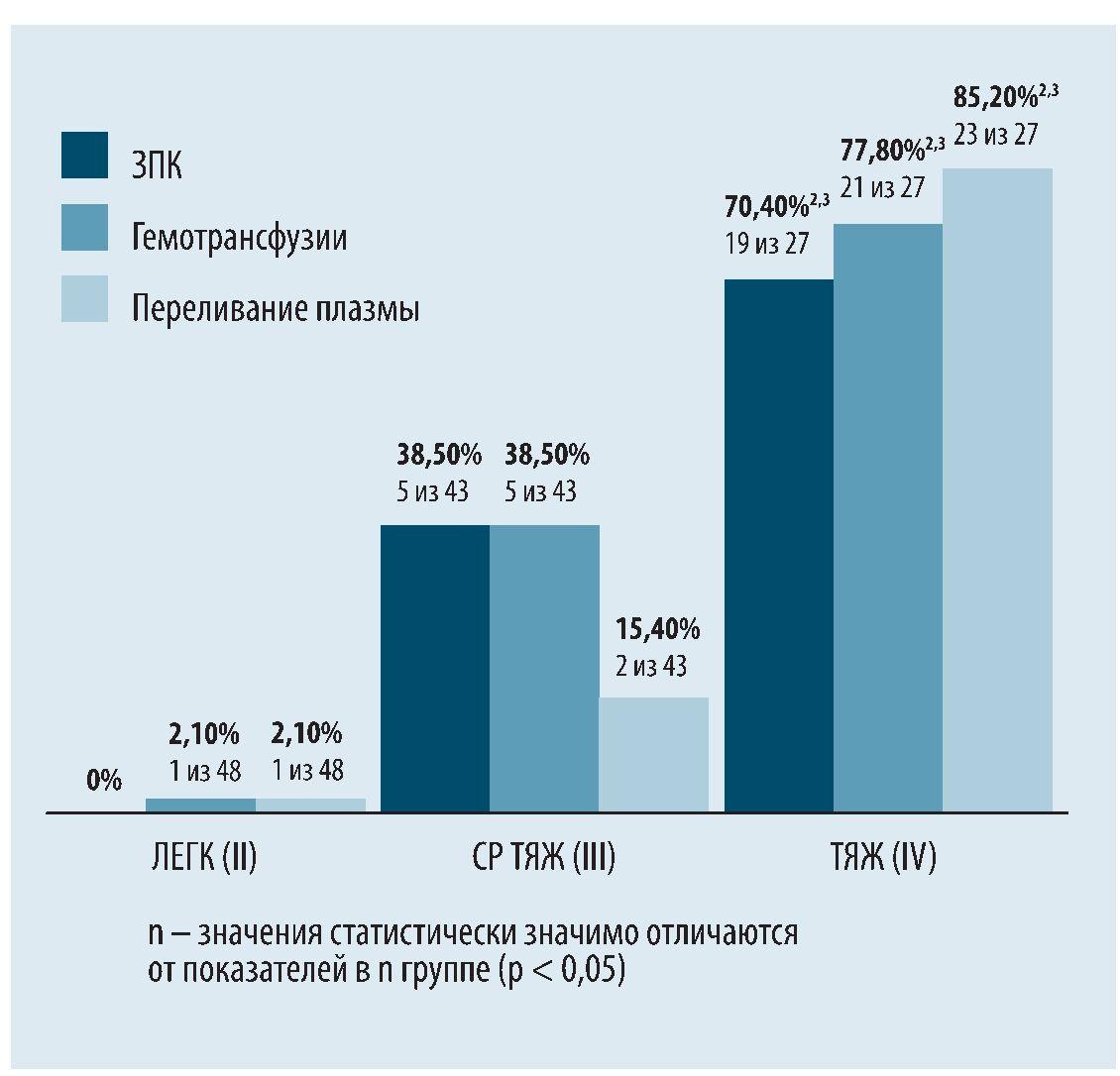
Рис. 1. Частота ЗПК, гемотрансфузий и переливания плазмы у новорожденных с ГБ
В результате проведенного лечения у детей IV группы (тяжелые формы ГБ) концентрации гемоглобина и гематокрита повысились с 97,1 ± 24,7 г/л и 27,6 ± 5,1% (при рождении) до 163,8 ± 27,4 г/л и 46,6 ± 9,4% (на 6-й день жизни) соответственно (р < 0,05), тем не менее оставаясь на более низком уровне, чем в I группе (190,0 ± 10,7 г/л и 55,1 ± 4,6% соответственно).
Также у новорожденных IV группы благодаря лечению на 6-й день жизни отмечена нормализация уровня общего билирубина (168,6 ± 56,8 ммоль/л против 171,1 ± 31,7 ммоль/л - в I группе; р > 0,05). В то же время концентрация прямого билирубина у детей III и IV групп (43,6 ± 23,7 и 49,2 ± 24,5 ммоль/л соответственно), несмотря на лечение, оставалась статистически значимо выше (р < 0,05), чем в I группе в этот же период (17,6 ± 11,6 ммоль/л). У детей без ГБ (I группа) на 6-й день жизни были ниже значения дефицита буферных оснований, чем у новорожденных с ГБ II, III и IV групп: 2,52 ± 2,5; -0,28 ± 6,5; -0,36 ± 2,4 ммоль/л и -0,48 ± 3,5 ммоль/л соответственно (р < 0,05).
На 8-е сутки жизни погиб один новорожденный (0,8%) из МХДА двойни, родившийся в срок 29 нед гестации с ОФГБ, гипоксически-ишемическим поражением ЦНС, кровоизлиянием в мозжечок, гипертрофической кардиомиопатией.
Длительность пребывания 123 новорожденных в стационаре варьировала от 2 до 21 дня. Выписано домой 38,2% (47 из 123) детей. Редко выписывались дети, гестационный возраст при рождении которых составлял 34 нед (14,3%); с увеличением срока гестации росла частота выписки детей домой, составляя в 35 нед 50%, в 36 нед - 60%, в 37 нед - 67,9%, в 38 нед - 83,3%. Домой выписывались дети только из I, II и III групп (52,8%, 47,9% и 38,5% соответственно). На второй этап переведены 76 из 123 (61,8%) детей, нуждающихся в продолжении лечения.
Обсуждение. Известно, что недоношенными рождаются 47-72,3% детей от многоплодной беременности как при резус-изоиммунизации, так и без таковой [9-12]. В нашем исследовании также подтверждена высокая частота недоношенности среди детей от многоплодной беременности (67,7%) и установлена зависимость этого показателя от наличия и тяжести ГБ: при отсутствии заболевания (I группа), легком (II группа) и среднетяжелом течении (III группа) желтушной формы недоношенными рождались реже, чем при тяжелых формах ГБ (IV группа) [61,1%; 54,2%; 69,2% и 100% соответственно; р < 0,05], из-за высокой частоты наступления преждевременных родов в IV группе.
Недоношенность была фактором риска возникновения дыхательных расстройств (OR 4.12; 95% ДИ:1.23-8.56, p = 0,001), выявленных практически у половины детей (49,2%), рожденных от многоплодной беременности. На частоту дыхательных расстройств также влияли наличие и тяжесть ГБ, так как они реже выявлялись при отсутствии заболевания и легком течении желтушной формы ГБ (27,8% и 35,4% соответственно), чем при тяжелых формах ГБ (92,6%; р < 0,05).
Впервые нами изучено состояние новорожденных от многоплодной беременности не только при различных степенях тяжести ГБ, но и в зависимости от метода наступления беременности, родоразрешения, а также типа плацентации. Установлено, что асфиксия чаще диагностирована у детей, рожденных досрочно через естественные родовые пути, а также посредством экстренного КС. Следовательно, для улучшения перинатальных исходов при многоплодной беременности, протекающей на фоне резус-изо-иммунизации, в сочетании с недоношенностью при выборе метода родоразрешения предпочтение следует отдавать плановому КС.
Нами установлено, что на параметры физического развития детей от многоплодной беременности влияли только наличие и степень тяжести ГБ, поскольку из-за низкой частоты недоношенности у детей без признаков ГБ или с легким течением болезни эти показатели были больше, чем у новорожденных со среднетяжелым течением и тяжелыми формами ГБ (р < 0,05). Метод наступления беременности (самопроизвольная или посредством ВРТ) не влиял на параметры физического развития новорожденных (р > 0,05), что противоречило данным H. Zhao и со-авт., выявивших более низкую массу тела у детей из двоен с ГБ, зачатых с помощью ЭКО, по сравнению с самопроизвольно зачатыми близнецами (1801,3 ± 531,9 и 2213,6 ± 538,9 г; р = 0,007) [9].
Анализ состояния детей по группам показал, что вследствие недоношенности у детей с тяжелыми формами ГБ (IV группа) и среднетяжелым течением желтушной формы заболевания (III группа) чаще (р < 0,05), чем у новорожденных с легким течением (II) или без признаков ГБ (I), диагностировано гипоксическое поражение ЦНС без ВЖК (40,7%; 30,8%; 6,3% и 8,3%). ВЖК II-IV степени чаще выявлялись в IV группе, чем в I: 25,9% и 8,3% (р = 0,04). Ателектазы легких реже диагностированы в I и II группах, чем в IV: 13,9%, 14,5% и 37% соответственно (р < 0,05). БГМ реже определялась в I группе, чем в IV: 8,3% и 29,6% (р < 0,05).
Холестаз развился у 33,3% новорожденных с тяжелыми формами ГБ, некротизирующий энтероколит (НЭК) - у 7,7% и 14,8% детей III и IV групп с хронической внутриутробной гипоксией, рожденных в сроки 29-33 нед гестации. Высокую частоту НЭК (7,3%) у детей из двоен с ГБ отметили и H. Zhao и со-авт. [9]. Фактором развития БГМ и НЭК была недоношенность (OR 4.35; 95% ДИ:1.56-9.58, p = 0,001).
Проведенный нами анализ лабораторных показателей крови у детей от многоплодной беременности выявил не только зависимость от наличия и степени тяжести ГБ, но и влияние на изученные параметры типа хориальности (р < 0,05). Связь МХ типа плацентации с неблагоприятными перинатальными исходами у беременных без резус-изоиммунизации описана в литературе [13-19]. В нашем исследовании МХ тип (даже без специфических осложнений) усугублял тяжесть состояния новорожденных с тяжелыми формами ГБ, так как у детей IV группы из МХДА двоен без ФФТС, по сравнению с детьми из ДХДА двоен, были ниже уровни гемоглобина и гематокрита, количество эритроцитов и тромбоцитов; также был выше уровень общего билирубина и значения дефицита буферных оснований.
Единого мнения о количестве ЗПК, необходимых детям с ГБ из двоен, среди авторов нет [9, 10, 20, 21]. В нашем исследовании ЗПК выполнено в количестве от 1 до 6 на 0-3 сутки жизни у 19,4% детей. Стоит подчеркнуть, что при ОФГБ и тяжелом течении желтушной формы заболевания из-за преждевременного родоразрешения частота проведения ЗПК была выше, чем при среднетяжелом течении ГБН (100%; 66,7% и 38,5% соответственно; р < 0,05).
Важно подчеркнуть, что внутриутробное лечение позволило снизить количество ЗПК у новорожденных с тяжелыми формами ГБ с 1-6 до 0-1. Однако особенностью нашего исследования является малая выборка пациентов, которым выполнены внутриутробные гемотрансфузии (n = 3).
Помимо тяжести ГБН, факторами риска проведения ЗПК были: значения максимальной скорости кровотока в средней мозговой артерии плода >1,1 МоМ (OR 3.17; 95% ДИ:1.93-5.24, p = 0,002), МХ тип плацентации (OR 2.17; 95% ДИ:1.12-7.72, p = 0,002), беременность тройней (OR 4.63; 95% ДИ:1.06-24.49, p = 0,002).
Учитывая тот факт, что 64% детей, зачатых посредством ЭКО, страдали гемолитической болезнью, в том числе 20% - тяжелыми формами заболевания, пациенткам с резус-изоиммунизацией, особенно при наличии отягощенного акушерского анамнеза, в программах ЭКО следует рекомендовать проведение пре-имплантационной генетической диагностики и перенос резус-отрицательного эмбриона в полость матки.
Частота постнатальной гибели составила 0,8%. Погиб новорожденный с ОФГБ из МХДА двойни, родившийся в срок 29 нед гестации, по причине ги-поксически-ишемического поражения ЦНС, кровоизлияния в мозжечок, гипертрофической кардиомиопатии, что подтверждает влияние тяжести ГБН и МХ типа плацентации на перинатальные исходы многоплодной беременности, протекающей на фоне резус-изоиммунизации.
ЗАКЛЮЧЕНИЕ
Таким образом, среди детей с ГБ, рожденных от многоплодной беременности, отмечается высокая частота недоношенности (67,7%), составляющая 100% у новорожденных с тяжелыми формами ГБ.
Для улучшения перинатальных исходов у беременных с тяжелыми формами ГБП и многоплодием, характеризующимся высокой частотой преждевременных родов, при выборе метода родоразрешения предпочтение следует отдавать плановому КС.
МХ тип плацентации ассоциируется с неблагоприятными перинатальными исходам резус-конфликтной многоплодной беременности, так как усугубляет тяжесть состояния новорожденных с тяжелыми формами ГБ, является фактором риска проведения ЗПК и постнатальной гибели.
Помимо тяжести ГБН и МХ типа плацентации, факторами риска проведения ЗПК являются значения максимальной скорости кровотока в средней мозговой артерии плода >1,1 МоМ и беременность тройней.
Внутриутробное переливание крови снижает число ЗПК у новорожденных с ГБ от многоплодной беременности даже при небольшой выборке пациентов. Целесообразно проведение дальнейших исследований для оценки эффективности и безопасности ВПК при многоплодии.
Литература
1. Макогон А.В. Ранние внутриутробные внутрисосудистые трансфузии крови в лечении анемии плода // Российский вестник акушера-гинеколога. 2022. Т. 22, № 5. С. 49-55.
2. Савельева Г.М., Коноплянников А.Г., Караганова Е.Я. и др. Наш опыт многократных внутриутробных переливаний крови плоду с тяжелой формой гемолитической болезни при резус-конфликте // Акушерство и гинекология. 2022. № 2. С. 65-71.
3. Гинзбург Б.Г. Группы крови системы AB0, Rh-фактор и привычное невынашивание беременности // Российский вестник акушера-гинеколога. 2022. Т. 22, № 2. С. 103-107.
4. Prevalence and determinants of RH alloimmunization in Rh-negative women in teaching hospitals of Addis Ababa, Ethiopia: a hospital-based cross-sectional study / M.B. Maruta [et al.] // Frontiers in Global Women’s Health. 2023. Vol. 4. P. 1167736.
5. Клинические рекомендации Минздрава РФ «Резус-изоиммунизация. Гемолитическая болезнь плода» [Электронный ресурс]. 2020. С. 23. URL: disuria.ru/_ ld/9/993_kr20R55R56mz.pdf?ysclid=m53nj9fh7e72657900 (дата обращения: 25.12.2024).
6. Rahimi-Levene N., Chezar J., Yahalom V. Red blood cell alloimmunization prevalence and hemolytic disease of the fetus and newborn in Israel: A retrospective study // Transfusion. 2020. Т. 60, № 11. С. 2684-2690.
7. Fetal and Neonatal Middle Cerebral Artery Hemodynamic Changes and Significance under Ultrasound Detection in Hypertensive Disorder Complicating Pregnancy Patients with Different Severities / P. Zhou [et al.] // Computational and Mathematical Methods in Medicine. 2022. Vol. 2022. P. 1-14.
8. Noninvasive Diagnosis by Doppler Ultrasonography of Fetal Anemia Due to Maternal Red-Cell Alloimmunization / G. Mari [et al.] // New England Journal of Medicine. 2000. Vol. 342, No. 1. P. 9-14.
9. Retrospective analysis of 55 twin neonates with haemolytic disease of the newborn // H. Zhao [et al.] / Immunologic Research. 2017. Vol. 65, No 3. P. 699-705.
10. Discordant intrauterine transfusion in dichorionic twin pregnancy with Rh isoimmunization / J. Wu [et al.] // Transfusion and Apheresis Science. 2017. Vol. 56, No. 6. P. 883-885.
11. Калашников С.А., Сичинава Л.Г. Течение и исходы многоплодной беременности, наступившей при использовании вспомогательных репродуктивных технологий // Акушерство и гинекологи. 2020. № 10. С. 71-77.
12. Avnon T., Ovental A., Many A. Twin versus singleton pregnancy in women > 45 years of age: comparison of maternal and neonatal outcomes // Journal of Maternal-Fetal and Neonatal Medicine. 2021. Vol. 34, No. 2. С. 201-206.
13. Перинатальные исходы беременности двойней, осложненной гибелью одного из плодов, при разных типах плацентации / К.В. Костюков, А.Т. Никитина, А.Е. Черепанова, К.А. Гладкова // Акушерство и гинекология. 2023. № 7. С. 40-46.
14. Развитие острой фето-фетальной трансфузии при родоразрешении монохориальных диамниотических двоен / А.В. Михайлов [и др.] // Вопросы гинекологии, акушерства и перинатологии. 2024. Т. 23, № 1. С. 39-46.
15. Зеркальный синдром при осложненном течении беременности монохориальной двойней / М.А. Курцер [и др.] // Акушерство и гинекология. 2023. № 1. С. 123-128.
16. Перинатальные исходы индуцированной беременности после переноса одного и двух эмбрионов / С.А. Калашников, Л.Г. Сичинава, А.Г. Коноплянников, Е.И. Папышева // Российский вестник акушера-гинеколога. 2023. Т. 23, № 1. С. 64-69.
17. Outcomes of Monoamniotic Twin Pregnancies from the First Trimester Onward / С. Van Audenhove [et al.] // Fetal Diagnosis end Therapy. 2022. Vol. 49, No. 7-8. P. 361-367.
18. Twin-to-Twin Transfusion Syndrome in monochorionic, monoamniotic twin pregnancy with common umbilical cord insertion / F.P. Szkodziak [et al.] // Ginekologia Polska. 2022. Vol. 93, No. 2. P. 177-178.
19. Neonatal outcomes between discordant monochorionic and dichorionic twins / Y.H. Park [et al.] // Journal of Maternal-Fetal and Neonatal Medicine 2021. Vol. 34, No. 13. P. 20802088.
20. Gedik Ozkose Z., Oglak S.C. The combined effect of anti-D and non-D Rh antibodies in maternal alloimmunization // Journal of Turkish Society of Obstetric and Gynecology. 2021. Vol. 18, No. 3. P. 181-189.
21. Thomsen W.C., Afify Z.A. Late Hyporegenerative Anemia Following Successful Management of Rh-D Alloimmunization: Still an Underappreciated Entity // Clinical Pediatrics. (Phila). 2021. Vol. 60, No. 9-10. P. 399-402.
Информация о финансировании. Финансирование данной работы не проводилось.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Участие авторов:
Концепция и дизайн исследования - Л.И. Ильенко, А.Г. Коноплянников
Сбор и обработка материала - А.П. Кирющенков, С.Р. Актулаева
Статистическая обработка - А.П. Кирющенков
Написание текста — А.П. Кирющенков Редактирование - Л.И. Ильенко, А.Г. Коноплянников

