Актуальные проблемы медикаментозной терапии коронавирусной инфекции COVID-19 у детей
СтатьиИ.М. Османов1, д-р мед. наук, профессор, Л.Н. Мазанкова1,2, д-р мед. наук, профессор, С.Н. Борзакова1,2,3, канд. мед. наук, Э.Р. Самитова1,2, канд. мед. наук, А.К. Миронова1,2, канд. мед. наук, А.В. Винокуров3, канд. мед. наук, С.О. Котенко1
1 ГБУЗ «Детская городская клиническая больница им. З.А. Башляевой Департамента здравоохранения г. Москвы»
2 ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования Минздрава России», г. Москва
3 ГБУ «Научно-исследовательский институт организации здравоохранения и медицинского менеджмента Департамента здравоохранения г. Москвы»
Резюме. В статье представлен обзор публикаций по применению ряда этиотропных и патогенетических лекарственных средств для терапии легкой и среднетяжелой форм новой коронавирусной инфекции COVID-19 у детей, в том числе анализ опубликованных данных по поиску новых препаратов, предотвращающих развитие тяжелых и критических форм инфекционного процесса, для внедрения в клиническую практику.
Ключевые слова: COVID-19, дети, ремседивир, нирматрелвир, ритонавир, паксловид, интерферонотерапия, интерферон-а2Ь, витамин D, 2-дезокси-D-глюкоза, плитидепсин, «МИР 19®», уридин, аминодигидрофталазиндион натрия, «Галавит»
Summary. The article presents an overview of publications on the use of a number of etiotropic and pathogenetic drugs for the treatment of mild and moderate forms of the new COVID-19 coronavirus infection in children, including an analysis of published data on the search for new drugs that prevent the development of severe and critical forms of the infectious process for implementation into clinical practice.
Keywords: COVID-19, children, remsedivir. nirmatrelvir, ritonavir, paxlovid, interferon therapy, interferon-a2b, vitamin D, 2-deoxy-D-glucose, plitidepsin, «Mir 19®», uridine, aminodihydrophthalazinedione sodium, «Galavit»
Введение
Несмотря на значительные усилия по поиску эффективных, безопасных и доступных лекарственных средств для лечения новой коронавирусной инфекции у детей, предпринимаемые с начала эпидемии, данная проблема остается актуальной [1-4] по ряду объективных причин: проведение клинических исследований у детей подчиняется определенным правилам, клиническое течение коронавирусной инфекции имеет свои особенности, происходит формирование новых штаммов вируса, резистентных к разработанным ранее лекарственным препаратам.
Клинические испытания новых лекарственных средств против SARS-CoV-2 у детей начинаются после успешного подтверждения их эффективности и безопасности у взрослых пациентов. Кроме того, заболевание COVID-19 у детей протекает преимущественно в бессимптомной и легкой форме [2, 5-7], что обуславливает необходимость осторожного, консервативного подхода к применению противовирусных, патогенетических и иммунотропных препаратов у пациентов данной возрастной группы [1, 2, 8, 9]. Использование вышеперечисленных лекарственных средств ограничено случаями тяжелого течения коронавирусной инфекции, а также группой детей, у которых имеются факторы риска такого течения [2, 5, 9-11], что затрудняет организацию и увеличивает сроки проведения клинических исследований. Все это существенно замедляет формирование доказательной базы эффективности и безопасности лекарственных препаратов для лечения новой инфекции SARS-CoV-2 у детей.
Количество химических соединений, которые рассматриваются как кандидаты для лечения COVID-19, на сегодняшний день превышает 300 наименований и продолжает ежегодно увеличиваться [12, 13]. Однако полный цикл доклинических и клинических испытаний фармакологического препарата с возможностью использования его у детей продолжается достаточно длительное время. С целью скорейшего получения результата мировым медицинским сообществом широко используется стратегия по оценке возможности применения разработанных ранее противовирусных, патогенетических, иммуномодулирующих препаратов, использовавшихся у детей для борьбы с другими близкими по патогенезу к SARS-CoV-2 инфекционными заболеваниями.
В статье представлен обзор публикаций по применению ряда этиотропных и патогенетических лекарственных средств в терапии легких и среднетяжелых форм новой коронавирусной инфекции у детей и о перспективных препаратах для использования в педиатрии, показавших высокую эффективность и безопасность у взрослых пациентов.
Материалы и методы
Проанализированы доступные отечественные и зарубежные публикации, посвященные лечению COVID-19 у детей. С целью оценки частоты и эффективности применения лекарственных препаратов у детей с новой коронавирусной инфекцией использованы данные наиболее крупных международных систематических обзоров [14, 15], включающих оценку 5794 и 3350 публикаций. Для систематического анализа были отобраны 97 и 129 исследований, содержащих сведения о методах лечения 8243 детей до 14 лет и 10 251 детей 0 до 17 лет включительно с различными формами новой коронавирусной инфекции в период с декабря 2019 по июнь 2021 г. Госпитализированы были 57,4% заболевших [15].
Для определения наиболее перспективных препаратов опирались на данные обновляемых клинических рекомендаций и систематического обзора лекарственных средств для лечения COVID-19, по версии ВОЗ [9, 16-18].
На момент подготовки публикации данные ресурсы включали сведения 463 клинических испытаний с участием 166 581 пациента.
Для получения данных о разрабатываемых препаратах - кандидатах для применения в качестве лекарств против COVID-19 - использовали специализированный информационный интернет-ресурс: COVID-19 Candidates - GEN - Genetic Engineering and Biotechnology News (genengnews.com) [18].
Результаты
Данные о применении лекарственных средств для лечения коронавирусной инфекции у детей, приведенные в систематических обзорах [14, 15], демонстрируют, что 79% больных не принимали препаратов (при бессимптомном течении) или получали только поддерживающую симптоматическую терапию.
Лишь 21% всех пациентов, включенных в обзор [14], получали связанную с COVID-19 терапию. Как правило, это были дети со среднетяжелыми и тяжелыми формами течения заболевания (moderate and severe), в том числе с мультисистемным воспалительным синдромом (MIS-C) (табл. 1). У 15,3% детей применялись противовирусные препараты, из которых наиболее часто использовался ремдесивир (у 6,2% включенных в обзор детей, без сообщений о серьезных побочных эффектах). Фавипиравир, осельтамивир, ритонавир/лопинавир, рибавирин и умифенавир получали 1,5; 1,4; 0,5; 0,3 и 0,2% пациентов соответственно.
Таблица 1.
Частота применения лекарственных препаратов у детей с коронавирусной инфекцией COVID-19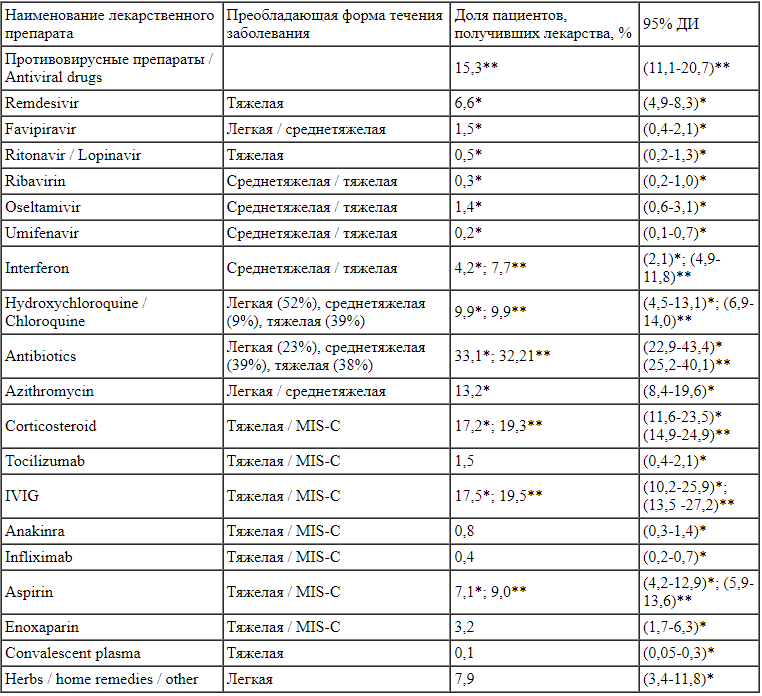
Примечание: ДИ - доверительный интервал.
Источники данных:
* COVID-19 treatment in children: A systematic review and meta-analysis / P.K. Panda [et al.] // Journal of Family Medicine and Primary Care. 2021. Vol. 10, № 9. Р. 3292-3302 [14].
** Clinical characteristics, treatment and outcomes of paediatric COVID-19: A systematic review and meta-analysis / O. Irfan [et al.] // Archives of Disease in Childhood. 2021. Vol. 106. Р. 440-448 [15].
У госпитализированных детей [15] наиболее часто использовались противомикробные препараты (32,2%), внутривенный иммуноглобулин (IVIG) (19,5%) и кортикостероиды (19,3%). Другие схемы лечения включали аспирин, инотропные препараты, ингаляционный интерферона (IFN-а), противомалярийные препараты.
В 91% случаев тяжелого течения коронавирусной инфекции [14] дети получали противовоспалительные препараты, среди которых преобладали кортикостероиды (17%) и аспирин (9%). Внутривенный иммунный глобулин (IVIG) применялся в 17,5%, интерферон - в 4,2% [14] и 7,7% [15], тоцилизумаб -в 1,5% и анакинра - в 0,8% случаев.
При мультисистемном воспалительном синдроме у детей наиболее часто использовался IVIG (81%), за которым следовали аспирин (67%), кортикостероиды (64%), инотропные препараты (62%) и антикоагулянты (56%, в основном низкомолекулярный гепарин) [14].
Оценка эффективности и безопасности примененных противовирусных препаратов у детей затруднена. В большинстве публикаций отсутствуют результаты завершенных клинических испытаний в этом направлении. Данные обсервационных исследований также ограничены [1, 9]. По сравнению со взрослыми, у детей COVID-19 протекает в более легких формах, смертность низкая и потребность в госпитализации минимальна. Все это обуславливает необходимость включения в исследование большего количества наблюдений для подтверждения клинических эффектов исследуемого препарата.
Опубликованные руководящие документы по лечению коронавируса у детей в основном были экстраполированы из рекомендаций для взрослых и для детей с другими вирусными инфекциями, а также учитывали мнения экспертов [1, 4, 19, 20]. Из ряда противовирусных препаратов, представленных в таблице 1, значительная часть не подтвердила эффективность и/или безопасность в рандомизированных контролируемых исследованиях у взрослых. Так, современные международные и национальные согласительные документы не рекомендуют применение хлорохина, гидроксихлорохина и азитромицина, лопинавира и ритонавира, рибавирина, фавипиравира, осельтамивира и умифенавира для лечения коронавирусной инфекции при любой клинической форме у взрослых и детей [1, 2, 4, 9].
К противовирусным препаратам, подтвердившим свою эффективность при нетяжелой и среднетяжелой формах COVID-19, относят комбинацию нирматрелвира и ритоняавира, молнупиравира и ремдесивира. Последний может применяться и при тяжелой форме заболевания. Молнупиравир не рекомендован пациентам до 18 лет из-за отсутствия данных о возможном отрицательном действии в отдаленном периоде [21].
Ремдесивир и комбинация нирматрелвира и ритонавира, согласно зарубежным и отечественным рекомендациям, могут применяться в начальной стадии заболевания только для определенных возрастных подгрупп детей с высоким риском тяжелого течения коронавирусной инфекции [1, 9] по решению врачебной комиссии [5, 11].
Ремдесивир ингибитор РНК-зависимой РНК-полимеразы является противовирусным агентом широкого спектра действия, первоначально синтезированным и разработанным исследовательским институтом инфекционных заболеваний Армии США совместно с компанией Gilead Sciences в 2015 году для лечения инфекции, вызванной вирусом Эбола [22]. Препарат изучался для применения в педиатрии при данном заболевании [23]. Ремдесивир обладает активностью in vitro против различных коронавирусов, включая SARS-CoV-2. Его активный метаболит в качестве аналога аденозина выступает за включение в формирующиеся РНК-цепи с помощью РНК-зависимой РНК-полимеразы вируса SARS-CoV-2, что приводит к задержке обрыва цепи во время репликации вирусной РНК. Имеет благоприятный профиль безопасности для взрослых и детей [5]. Первоначальные клинические исследования препарата демонстрировали скромные результаты [24]. Основные сведения о его клинической эффективности при COVID-19 базируются на данных большого рандомизированного контролируемого исследования у взрослых: при приеме препарата достоверно сокращалось время до выздоровления по сравнению с плацебо, но не было показано статистически значимой разницы в смертности к 29-му дню [25].
У детей с высоким риском тяжелого течения коронавирусной инфекции ремдесивир может рассматриваться как дополнение к поддерживающей терапии в начальной стадии заболевания, при развитии потребности в кислородотерапии, хотя убедительные данные об эффективности и безопасности его использования отсутствуют [26, 27]. Имеются сведения о его эффектах при применении в небольших группах детей с тяжелыми формами коронавирус-ной инфекции [28, 29]. Однако необходима дальнейшая оценка результатов клинических исследований у детей.
Последние отечественные рекомендации позволяют использовать ремдесивир у госпитализированных пациентов старше 12 лет со средней и тяжелой формами болезни без цитокинового шторма. У детей до 12 лет - по решению врачебной комиссии и при получении информированного согласия родителей или законных представителей [5, 11].
Ремдесивир - препарат для внутривенного введения, курс применения которого варьирует от 5 до 10 дней, что ограничивает его использование в амбулаторных условиях. Фармакокинетические исследования у детей продолжаются, но результаты пока недоступны. Рекомендованная схема применения приведена в таблице 2.
Список лекарственных средств, строго противопоказанных для совместного приема с препаратами нирматрелвир + ритонавир, приводится в клиническом протоколе [11].
Таблица 2.
Схемы применения противовирусной терапии при легкой и среднетяжелой формах COVID-19 у детей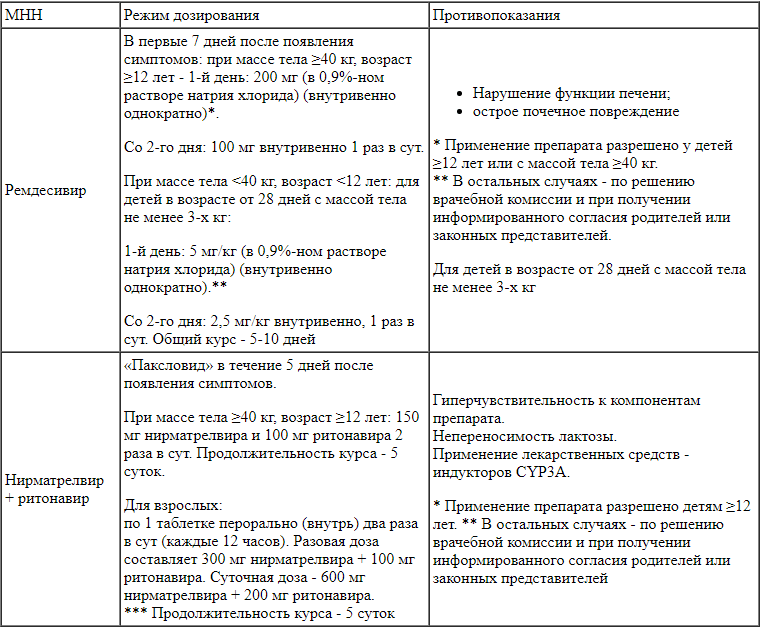
* Разрешено Европейским медицинским агентством и FDA.
** Разрешено применение в Российской Федерации.
*** Дозировка для взрослых пациентов.
Нирматрелвир (также PF-07321332) - новый противовирусный препарат, пероральный ингибитор протеазы 3CLpro, разработанный компанией Pfizer [30]. Предназначен для блокирования активности основного протеазного фермента, который необходим коронавирусу для репликации. В клинической практике применяется с ритонавиром, который служит для замедления метаболизма PF-07321332 цитохромами и поддержания более высоких концентраций основного препарата в кровотоке [31].
О начале разработки и доклинических испытаниях препарата компания объявила в марте 2020 г. В ноябре 2021 года Pfizer информировала о положительных результатах исследования II/III фазы, в том числе о сокращении госпитализаций или смертельных исходов на 89% при назначении PAXLOVID™ (таблетки нирматрелвира [PF-07321332] и таблетки ритонавира) в течение трех дней после появления симптомов ковида и на 85%, если лечение начинать в течение первых пяти дней [30, 32]. Дальнейшие клинические исследования проходили в том числе и на территории Российской Федерации [33]. В декабре 2021 г. были завершены II/III фазы клинических испытаний препарата в качестве средства от COVID-19 (NCT04960202). Всего в двух рандомизированных контролируемых исследованиях (EPIC-SR и HR) приняли участие 3100 пациентов с нетяжелыми формами заболевания в амбулаторных условиях. Ни в одном из включенных исследований не участвовали дети или беременные [34]. Тогда же получено одобрение Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (Food and Drug Administration, FDA) и Европейского комитета по лекарственным средствам (Committee for Medicinal Products for Human Use, CHMP) для экстренного использования PAXLOVID™ при лечении COVID-19 легкой и средней степени у взрослых и детей (12 лет и старше, с массой тела не менее 40 кг). А в 2022 г. начато производство дженерической версии препарата 35 компаниями. В Российской Федерации заявили о регистрации, производстве генерических копий («Скайвира», «Миробивир» и «Нирматрелвир ПСК») и проведении клинических испытаний три фармакологических производителя [35].
В начале марта 2022 года Pfizer начала клинические испытания «Паксловида» у детей. Исследование EPIC-PEDS (NCT05261139) II/III фазы (нерандомизированное, открытое, многоцентровое, международное) направлено на проверку препарата в лечении симптоматической коронавирусной инфекции COVID-19 у негоспитализированных детей (от младенцев до 17-летних) (n = 140), находящихся в группе риска прогрессирования заболевания до тяжелой формы [36]. В клиническом исследовании NCT05438602 II фазы (рандомизированное, двойное слепое, многоцентровое) тестировался «Паксловид» среди иммунокомпрометированных (с ослабленной иммунной системой) пациентов в возрасте 12 лет и старше. Нирматрелвир с ритонавиром назначался курсом в 5, 10 или 15 дней [37].
В России комбинация нирматрелвир + ритонавир в августе 2022 года вошла в обновленные схемы лечения COVID-19, разработанные Министерством здравоохранения Российской Федерации [5], а в октябре - в протоколы лечения детей с COVID-19 Департамента здравоохранения г. Москвы [11]. Препарат рекомендован к применению не вакцинированным против SARS-CoV-2 или переболевшим COVID-19 в течение последних шести месяцев детям старше 12 лет с лабораторно подтвержденной коронавирусной инфекцией COVID-19, а также иммунокомпрометированным детям из группы риска тяжелого течения COVID-19. У детей до 12 лет - по решению врачебной комиссии и при получении информированного согласия родителей или законных представителей (см. табл. 2).
Моноклональные вируснейтрализующие антитела
Обнадеживающие перспективы противовирусной терапии COVID-19 у детей открылись с появлением на фармацевтическом рынке искусственных (рекомбинантных) моноклональных вируснейтрализующих антител (МВНА). МВНА класса IgG1, которые нейтрализуют вирусы путем связывания с неперекрывающимися эпитопами рецепторсвязывающего домена S-белка SARS-CoV-2 и характеризуются отсутствием феномена антителозависимого усиления действия инфекции. Блокировка взаимодействия S-белка SARS-CoV-2 с ангиотензинпревращающим ферментом 2 (АПФ2) приводит к подавлению инфицирования клеток хозяина и останавливает репликацию вируса. В настоящее время за рубежом используются однокомпонентные (сотровимаб, регданвимаб), а также комбинированные (бамланивимаб + этесевимаб; касиривимаб + имдевимаб) препараты, показавшие высокую эффективность в период клинических испытаний.
Однако серьезной проблемой применения МВНА является снижение чувствительности к разработанным препаратам новых вирусных штаммов, возникших в результате эволюции (например, замена L452R или E484K в шиповидном белке, который является мишенью блокирующих антител). Все это требует избирательного применения МВНА с учетом чувствительности доминирующего штамма коронавируса [38].
Все препараты из этой группы не зарегистрированы в Российской Федерации, в связи с чем их назначение возможно при наличии лекарственного средства в субъекте РФ и положительного решения врачебной комиссии о применении, а также разрешения на временное обращение [5, 11, 39]. Использование препаратов на основе МВНА рекомендуется в стационарах, а также в условиях дневного стационара в срок не позднее 7-10-го дня от начала болезни для детей с высоким риском развития тяжелой инфекции, вызванной COVID-19 [5, 11]. Лекарства вводятся внутривенно под наблюдением медицинского персонала. Все это требует определенных организационных мер при оказании медицинской помощи. Кроме того, достаточно высокая стоимость препаратов МВНА сужает возможности их широкого применения.
Поиск эффективных и доступных лекарственных средств для борьбы с коронавирусной инфекцией у детей ведется в направлении применения патогенетической и иммуномодулирующей терапии для активизации иммунной системы ребенка и мобилизации неспецифических защитных механизмов.
Одним из таких направлений стало применение интерферонотерапии COVID-19 у детей. Патогенетическим обоснованием применения этой группы препаратов являются сведения о ключевой роли среди факторов врожденного противовирусного иммунитета системы интерферонов (ИФН), которая реализует свои эффекты через альфа- и гамма-интерфероновые рецепторы. Контакт с вирусом приводит к немедленному выбросу и дальнейшей продукции ИФН I типа, активации и увеличению количества естественных киллеров (NK-клеток), которые уничтожают зараженные вирусом клетки, синтезу цитокинов, инициирующих последующее включение в активную работу механизмов адаптивного иммунитета [1-3]. Достаточная и своевременная выработка интерферонов является решающим фактором, предотвращающим дальнейшее развитие инфекционного процесса [40-42].
В исследованиях in vitro была подтверждена высокая чувствительность SARS-CoV-2 к интерферонам. При обработке культуры pHAE интерферонами I или III типа за 24 часа до заражения количество вирусной РНК снижалось в три раза по сравнению с необработанными зараженными культурами, а репликация вируса уменьшалась на 90% [43]. Аналогичные данные о снижении продукции вируса в культуре клеток в 1000-10 000 раз под воздействием интерферонов приводят другие авторы [44].
Однако данные об эффективности клинического применения интерферонов при инфекции COVID-19 не столь убедительны и находятся в стадии накопления и анализа. В ряде зарубежных клинических рекомендаций применение интерферонов для борьбы с новой коронавирусной инфекцией считается необоснованным [1].
С другой стороны, о положительном опыте применения препаратов интерферона у детей сообщается в большом количестве исследований [45-47]. В публикациях на начало 2021 г. о роли интерферонов в иммунопатогенезе COVID-19 и клинической эффективности лекарственных препаратов на основе рекомбинантного интерферона-а2Ь в лечении детей отечественные авторы приводят аргументы о целесообразности включения препаратов интерферона в схемы терапии COVID-19 у детей как в виде монотерапии, так и в комбинациях с другими противовирусными средствами [48]. Сообщается о положительных результатах применения рекомбинантного интерферона-а2Ь в лекарственной форме «ректальные суппозитории» у детей с легкой (острая респираторная вирусная инфекция) и среднетяжелой формами (нетяжелая пневмония, пневмония с дыхательной недостаточностью) заболевания в составе сочетанной терапии: с антиоксидантами [49, 50], противовирусными препаратами и их комбинациями [51-53]. Учитывая накопленный положительный опыт, рекомбинантный интерферон альфа-2Ь включен в последние отечественные рекомендации в качестве обязательных назначений при легкой и среднетяжелой формах COVID-19 у детей [5, 10, 11].
Другой точкой приложения в борьбе с коронавирусной инфекцией может стать модуляция антиоксидантного ответа клеток человеческого организма, который оказался решающей детерминантой прогрессирования ряда вирусных заболеваний. Вызванный вирусом SARS-CoV-2 окислительный стресс играет значительную роль в жизненном цикле вируса, а также в патогенезе развития заболевания [54-56], что открывает широкое поле для апробации уже известных антиоксидантных препаратов и поиска новых активных веществ. Среди известных и клинически апробированных препаратов применялись: витамин С, глутатион, тиамин, биотин и токоферол; омега-3 и омега-6 полиненасыщенные жирные кислоты, N-ацетилцистеин. Однако убедительных данных об эффективности данных лекарственных средств в доступных публикациях не найдено.
Исключение составляет опыт применения витамина D [57]. Установлено, что дефицит/недостаточность витамина D повышает вероятность заражения и тяжелого течения COVID-19 [58]. Пациенты с дефицитом витамина D (<20 нг/мл) в 14 раз чаще имели тяжелое течение заболевания или находились в критическом состоянии, чем лица с содержанием 25(OH)D ≥40 нг/мл (ОШ 14, 95% ДИ 4-51, p < 0,001) [59]. Мета-анализ показал, что вероятность развития тяжелых стадий COVID-19 в 5 раза выше у пациентов с дефицитом витамина D [60]. В европейских странах, у жителей которых уровень витамина 25(OH)D в среднем был меньше или равен 50 нмоль/л, летальность при COVID-19 была выше, чем в государствах, у населения которых содержание 25(OH)D было больше 50 нмоль/л (ОР 2,155, 95% ДИ 1,068-4,347, p = 0,032) [61]. Сообщается о протоколе профилактики и лечения инфекции с помощью «витаминного коктейля», имеющего в своем составе витамин С, метионин, цинк, кверцетин, витамин D, применение которого дало положительные клинические результаты [62]. Все эти данные послужили основанием для включения витамина D в протоколы лечения детей с COVID-19 Департамента здравоохранения г. Москвы [11].
Отдельный интерес представляет применение аминодигидрофталазиндиона натрия (5-амино-2,3-дигидро-1,4-фталазиндион натрия, алюминол, drug MP 1032) для предотвращения тяжелого течения коронавирусной инфекции и профилактики «цитокинового шторма». Это лекарственное средство обладает комбинированным антиоксидантным, иммуномодулирующим и противовоспалительным механизмами действия.
Иммуномодулирующие свойства препарата были обнаружены отечественными исследователями в начале 1980-х годов. В 1997 г. он был зарегистрирован под названием «Галавит» и разрешен к клиническому применению [63]. Препарат активно изучался российскими учеными в начале 2000-х годов [64-66]. В результате были подтверждены его иммуномодулирующие и обнаружены антиоксидантные и противовоспалительные свойства.
Антиоксидантная активность «Галавита» проявляется как за счет прямого подавления некоторых гиперреактивных соединений (гипохлорит ион, перекисный радикал), модуляции активности антиоксидантных ферментов, в частности, через редокс-чувствительный транскрипционный фактор (Nrf2), защищающий клетки и ткани от токсинов, окислительного стресса и канцерогенов [67], а также за счет снижения выработки гиперактивированными макрофагами активных форм кислорода, что в итоге способствует защите тканей и органов от разрушительного воздействия радикалов, снижению уровня оксидантного стресса и выраженности интоксикации организма [68-70].
Иммуномодулирующий механизм действия препарата связан со способностью регулировать функционально-метаболическую активность фагоцитарных клеток (моноцитов/макрофагов, нейтрофилов), которые играют ключевую роль в патогенезе воспалительной реакции. Кроме того, «Галавит» нормализует антителообразование, повышает функциональную активность антител, опосредованно стимулирует выработку эндогенных интерферонов (ИФН-а, ИФН-у) клетками-продуцентами. Усиливая фагоцитарную, бактерицидную и цитотоксическую активность клеток иммунной системы при ее исходном дефиците, препарат повышает неспецифическую резистентность организма к инфекционным заболеваниям различной этиологии, способствует более быстрой элиминации возбудителя из организма, сокращает частоту, выраженность и длительность инфекций [63, 68].
Противовоспалительное действие препарата обусловлено обратимым ингибированием на 6-8 часов избыточного синтеза гиперактивированными макрофагами/моноцитами фактора некроза опухолей-а (ФНО-а), ИЛ-1, ИЛ-6 и других провоспалительных цитокинов, уровень которых определяет степень воспалительных реакций, их цикличность [66, 71, 72].
С 2007 года в Российской Федерации «Галавит» разрешен и активно используется у детей с 6 лет для лечения частых рецидивирующих заболеваний дыхательных путей и лор-органов (частые ОРВИ, бронхит, пневмония, хронический тонзиллит, отит и аденоидит), воспалительных заболеваний слизистой полости рта и горла, болезней пародонта, инфекционных кишечных заболеваний, сопровождающихся интоксикацией и/или диареей, лечения и профилактики урогенитальных инфекций бактериальной и вирусной этиологии. Стоит отметить, что в Узбекистане с 2017 года суппозитории «Галавит» 50 мг разрешены к применению у детей с года (регистрационное удостоверение № 02902/04/17 от 21.04.2017). В Азербайджане с 2022 года таблетки подъязычные «Галавит» 25 мг показаны для неспецифической профилактики новой коронавирусной инфекции.
За длительный период клинического применения препарата выполнено более 100 исследований, в которых участвовали более 3700 пациентов, в том числе детей. Сообщается о его успешном применении у детей с частыми ОРВИ, заболеваниями лор-органов, синдромом лимфоаденопатии, гриппом, хроническими инфекциями и нейродегенеративными заболеваниями [72-74]. При этом не было зарегистрировано серьезных осложнений и побочных эффектов.
По состоянию на октябрь 2022 года в Российской Федерации зарегистрировано три продукта с действующим веществом аминодигидрофталазиндиона натрия: оригинальный препарат «Галавит» (ООО «СЭЛВИМ»), «Тамерит» (ООО «АБИДА-ФАРМА») и «Тамерон» (АНО «Институт инженерной физики»). «Галавит» представлен в виде подъязычных таблеток 25 мг, ректальных суппозиториев 50 и 100 мг, порошка для приготовления раствора для внутримышечного введения 50 и 100 мг. «Тамерит» и «Тамерон» выпускаются в виде лиофилизата при приготовлении раствора для внутримышечного введения 100 мг [75].
По данным реестра разрешений на проведение клинических исследований лекарственных средств (rosminzdrav.ru), наиболее близкими к завершению клинических испытаний (IV фаза) находятся лекарственные формы на основе препарата «Галавит»: таблетки подъязычные 25 мг (для детей с 12 лет) и суппозитории ректальные 100 и 50 мг (для детей с 6 лет) [76, 77].
С развитием пандемии коронавирусной инфекции возрос интерес к возможности применения его для профилактики и лечения различных форм заболевания. В период начала подъема заболеваемости, до разработки вакцин этот препарат использовался как эмпирическое средство профилактики и предотвращения развития среднетяжелых и тяжелых форм COVID-19 у медицинских работников красной зоны. Был получен положительный клинический результат, а накопленный опыт трансформировался в масштабные наблюдательные исследования [78, 79]. В результате было показано достоверное снижение частоты развития средних и тяжелых форм заболевания COVID-19 (16,6 против 28,5%, р < 0,05) в группе медицинских работников, профилактически принимавших таблетированные формы аминодигидрофталазиндиона натрия («Галавита») в дозировке 25 мг 2 раза в сутки (что соответствовало суточной дозе 50 мг) в течение четырех недель. Профилактический эффект препарата «Галавит» получил подтверждение в логистической регрессии, показавшей статистическую значимость влияния на риск развития COVID-19 факта приема препарата.
Сообщается об успешном применении аминодигидрофталазиндиона натрия в составе комплексной терапии коронавирусной пневмонии. Добавление к стандартной схеме лечения иммуномодулирующих препаратов способствовало купированию клинических проявлений, увеличению SpO2, уменьшению объема поражения легочной паренхимы [80, 81]. Выполненный в 2020 г. анализ опубликованных материалов позволил сделать вывод о возможности применения аминодигидрофталазиндион натрия в лечении COVID-19 в рамках клинических исследований (NCT04932941) [82]. Последующая оценка данных публикаций позволила обосновать целесообразность назначения препарата «Галавит» пациентам в активную фазу инфекционного процесса и на реабилитационном этапе после перенесенного COVID-19 [83].
Препарат включен в Клинический протокол лечения детей с новой коронавирусной инфекцией (COVID-19), находящихся на стационарном лечении в медицинских организациях государственной системы здравоохранения города Москвы [11].
Анализ раздела интернет-ресурса Genetic Engineering & Biotechnology News (GEN), аккумулирующего сведения о химических субстанциях, перспективных для использования в качестве лекарственных средств для борьбы с коронавирусной инфекцией, свидетельствует о проведении масштабных исследований и постоянно возрастающем числе изучаемых субстанций, превышавшем на момент подготовки публикации 300 единиц [12]. Проработка такого количества информации выходит за рамки возможностей данного обзора, поэтому авторы выделили лишь некоторые сообщения, посвященные близким к завершению испытаниям, а также разработкам отечественных исследователей.
Результаты ряда исследований, проведенных в развивающихся странах, были опубликованы в 2021 году. В них сообщается об эффективности применения ивермектина и доксициклина у небольшого числа детей [84-86], однако этих данных недостаточно, чтобы рекомендовать препараты к широкому использованию.
Недавно одобренный в Индии препарат «2-дезокси-D-глюкоза» (DCGI), произведенный Организацией оборонных исследований и разработок (DRDO), может использоваться у пациентов в возрасте 4 лет и старше, но требует проведения дополнительных испытаний. [87]
На этапе клинических исследований находится ингаляционный препарат EXO-CD4 [88], который представляет собой экзосомы, несущие белок CD24, обладающий противовоспалительным действием. Препарат экзосом получают из генно-модифицированных клеток линии T-REx™-293 с высоким уровнем экспрессии CD24. EXO-CD4 предназначен для ликвидации негативных последствий «цитокинового шторма». По предварительным данным, препарат безопасен, а его применение в ограниченной группе взрослых пациентов с COVID-19 позволило добиться их быстрого выздоровления.
В доклинических исследованиях in vitro плитидепсин (аплидин), разрабатывавшийся в качестве противоракового лекарственного средства, оказался в 27,5 раза более эффективным средством против коронавируса SARS-CoV-2, чем ремдесивир. Плитидепсин взаимодействует с фактором трансляции eEF1A и подавляет процесс репликации вируса [89]. По предварительным результатам клинического исследования II фазы, применение «Плитидепсина» приводило к сокращению срока госпитализации больных COVID-19: в течение 15 дней были выписаны 81% пациентов, получавших «Плитидепсин», по сравнению с 47% пациентами на базовой терапии [90].
Примером перспективных отечественных разработок может служить созданный в ФГБУ «ГНЦ Институт иммунологии» ФМБА России комплексный препарат «МИР 19®», который действует на основе РНК-интерференции. В состав препарата входит миРНК siR-7-EM, обладающая противовирусным действием, и дендримерный пептид KK46, способствующий поглощению действующего вещества клетками при топическом применении [91, 92]. Как показали исследования, препарат способен блокировать SARS-CoV-2 in vitro и in vivo [93]. В настоящее время проводятся клинические испытания препарата «МИР 19®», по предварительным результатам которых показаны его безопасность и хорошая переносимость.
Определенный интерес представляет сообщение ученых из лаборатории митохондриального транспорта ИТЭБ РАН, которые показали, что пиримидиновый препарат «Уридин» оказывает выраженное протекторное действие против гипоксического повреждения ткани лёгкого и сердца, а также способен предотвращать так называемый «цитокиновый шторм» зараженного вирусом организма. Разработчики считают, что сочетание «Уридина» с антиоксидантом - водным раствором дигидрокверцетина «Таксифолин аква» - с высокой эффективностью нейтрализует активные формы кислорода. Сочетание этих препаратов должно предупреждать развитие осложнений при COVID-19 и способствовать ускоренному восстановлению организма после инфекции [94].
В обзоре публикаций продемонстрирована возможность использования препаратов группы сукцинатов в условиях гипоксии при COVID-19. Обосновано применение препарата «Реамберин» при гипоксических состояниях, вызванных коронавирусной пневмонией [95].
Обширный фронт научных исследований позволяет с оптимизмом смотреть на решение проблемы медикаментозной терапии коронавирусной инфекции у детей.
Рассматривая перспективы этой проблемы, необходимо учитывать, что важнейшая роль в предотвращении заболеваемости, обусловленной вирусом COVID-19, развития тяжелого течения болезни у пациентов из группы риска принадлежит иммунопрофилактике. Успешное внедрение вакцинации от SARS-CoV-2 у детей и подростков может оказать существенное влияние на распространенность и клинические формы коронавирусной инфекции, что в свою очередь скажется на выборе и практике применения лекарственных средств у пациентов данной возрастной категории.
Для повышения обоснованности и эффективности медикаментозной терапии необходима консолидация сведений о результатах применения лекарственных средств, направленных на лечение коронавирусной инфекции у детей, и формирование доказательной базы их эффективности. Важной задачей является информирование медицинских работников практического звена о состоянии данной проблемы для обеспечения обоснованной и результативной помощи детям с различными формами коронавирусной инфекции.
Заключение
Разработка безопасных и доступных лекарственных средств для лечения новой коронавирусной инфекции у детей остается актуальной проблемой, пока далекой от достижения оптимальных результатов. Её решение требует дальнейшего проведения в данной возрастной группе клинических исследований эффективности и безопасности наиболее перспективных лекарственных средств с учетом изменений чувствительности новых штаммов вируса, а также возрастающих возможностей иммунопрофилактики.
Необходима консолидация научных знаний по данному вопросу и соответствующее информирование медицинского сообщества, оказывающего практическую помощь детям с различными формами коронавирусной инфекции.
Литература
1. COVID-19 Treatment Guidelines Panel. Coronavirus Disease 2019 (COVID-19) Treatment Guidelines. National Institutes of Health.
2. Clinical management of COVID-19: living guideline, 15 September 2022. Geneva: World Health Organization; 2022.
3. Immune-Modulating Drug MP1032 with SARS-CoV-2 Antiviral Activity In Vitro: A potential Multi-Target Approach for Prevention and Early Intervention Treatment of COVID-19 / S. Schumann [et al.] // International Journal of Molecular Sciences. 2020. Vol. 21. Р. 8803. DOI:10.3390/ ijms21228803.
4. Multicenter initial guidance on use of antivirals for children with coronavirus disease 2019/severe acute respiratory syndrome coronavirus 2 / K. Chiotos [et al.] // Journal of the Pediatric Infectious Diseases Society. 2020. Vol. 9(6). Р. 701-715.
5. Временные методические рекомендации. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 16 (18.08.2022)
6. COVID-19 Infection in Children and Infants: Current Status on Therapies and Vaccines / G. Malcangi [et al.] // Children (Basel). 2022. Feb 12. Vol. 9, № 2. Р 249. DOI: 10.3390/children9020249. PMID: 35204969; PMCID: PMC8870718.
7. Ya-Hong H.U., Kai-Hu Y.A.O. Clinical characteristics and epidemiological significance of coronavirus disease 2019 in children and adolescents // Chinese Journal of Contemporary Pediatrics Europe. 2022. Aug 15. Vol. 24, № 8. Р. 846-852. DOI: 10.7499/j.issn.1008-8830.2205026.
8. Treatment of Children with COVID-19: Position Paper of the Italian Society of Pediatric Infectious Disease / E. Venturini [et al.] // Italian Journal of Pediatrics. 2020. Vol. 46. Р. 139. DOI: 10.1186/ s13052-020-00900-w.
9. Therapeutics and COVID-19: living guideline, 16 September 2022. Geneva : World Health Organization, 2022.
10. Особенности клинических проявлений и лечения заболевания, вызванного новой коронавирусной инфекцией (COVID-19) у детей : Методические рекомендации Минздрава России. (Версия 2 от 03.07.2020).
11. Об утверждении Клинического протокола лечения детей с новой коронавирусной инфекцией (COVID-19), находящихся на стационарном лечении в медицинских организациях государственной системы здравоохранения города Москвы : приказ департамента здравоохранения г. Москвы от 12.10.2022 № 960. М., 2022.
12. Genetic Engineering & Biotechnology News (GEN) COVID-19 Drug & Vaccine Candidate Tracker.
13. Strategies for Targeting SARS CoV-2: Small Molecule Inhibitors - The Current Status / N. M. Beeraka [et al.] // Frontiers in Immunology. 2020. Sep. 18. Vol. 11. Р 552925. DOI: 10.3389/ fimmu.2020.552925.
14. COVID-19 treatment in children: A systematic review and meta-analysis / P. K. Panda [et al.] // Journal of Family Medicine and Primary Care. 2021 Sep. Vol. 10, № 9. Р. 3292-3302.
15. Clinical characteristics, treatment and outcomes of paediatric COVID-19: A systematic review and meta-analysis /O. Irfan [et al.] // Archives of Disease in Childhood. 2021 Vol. 106. Р 440-448.
16. Living guidance for clinical management of COVID-19. Geneva: World Health Organization, 2021
17. Drug treatments for covid-19: living systematic review and network meta-analysis / R. Siemieniuk [et al.] // BMJ. 2020. Vol. 370. Р 2980. DOI: 10.1136/bmj.m2980.
18. COVID-19 Candidates - GEN - Genetic Engineering and Biotechnology News (genengnews.com).
19. Multidisciplinary guidance regarding the use of immunomodulatory therapies for acute coronavirus disease 2019 in pediatric patients / D.E. Dulek [et al.] // Journal of the Pediatric Infectious Diseases Society. 2020. Vol. 9, № 6. Р. 716-737.
20. Updated guidance on use and prioritization of monoclonal antibody therapy for treatment of COVID-19 in adolescents / J. Wolf [et al.] // Journal of the Pediatric Infectious Diseases Society. 2022. Vol. 11, № 5. Р. 177-185.
21. FDA Presentations for the November 30, 2021 Meeting of the Antimicrobial Drugs Advisory Committee.
22. Antiviral Compound Provides Full Protection from Ebola Virus in Nonhuman Primates.
23. Prevention CfDCa. SARS-CoV-2 Variant Classifications and Definitions. 2021.
24. Remdesivir for 5 or 10 days in patients with severe COVID-19 / J.D. Goldman [et al.] // New England Journal of Medicine. 2020. Vol. 83, № 19. Р. 1827-1837.
25. Remdesivir for the treatment of Covid-19 - Final report / J. H. Beigel [et al.] // New England Journal of Medicine. 2020. Vol. 383, № 19. Р 1813-1826.
26. Multicenter interim guidance on use of antivirals for children with coronavirus disease 2019/severe acute respiratory syndrome coronavirus 2 / K. Chiotos [et al.] // Journal of the Pediatric Infectious Diseases Society. 2021. Vol. 10, № 1. Р. 34-48.
27. Early Remdesivir to Prevent Progression to Severe Covid-19 in Outpatients / R.L. Gottlieb [et al.] // New England Journal of Medicine. 2022. Vol. 386, № 4. Р 305-315.
28. Compassionate use of remdesivir in children with COVID-19 / A. Mendez-Echevarria [et al.] // European Journal of Pediatrics. 2021 Vol. 180. Р 1317-1322.
29. Compassionate Use of Remdesivir in Children With Severe COVID-19 / D.L. Goldman [et al.] // Pediatrics. 2021. May. Vol. 147, № 5. Р 2020047803. DOI: 10.1542/peds.2020-047803.
30. Candidate: PAXLOVID™ (nirmatrelvir; PF-07321332).
31. What is Australia’s potential new COVID treatment?
32. EPIC-HR: Study of Oral PF-07321332/Ritonavir Compared With Placebo in Nonhospitalized High Risk Adults With COVID-19.
33. Оценка безопасности и эффективности двух схем перорального введения препарата pf-07321332/ритонавир в профилактике симптомов инфекции SARS-CoV-2 у взрослых, контактировавших в домашних условиях с лицом с симптоматическими проявлениями инфекции COVID-19
34. EPIC-HR Investigators. Oral Nirmatrelvir for High-Risk, Nonhospitalized Adults with Covid-19 / J. Hammond [et al.] // New England Journal of Medicine. 2022. Apr 14. Vol. 386, № 15. Р 1397-1408. DOI: 10.1056/NEJMoa2118542.
35. «Паксловид» для лечения ковида. Все подробности.
36. EPIC-Peds: A Study to Learn About the Study Medicine Called PF-07321332 (Nirmatrelvir)/Ritonavir in Patients Under 18 Years of Age With COVID-19 That Are Not Hospitalized But Are at Risk for Severe Disease.
37. A Study to Learn About the Study Medicines (Called Nirmatrelvir/Ritonavir) in People 12 Years Old or Older With COVID-19 Who Are Immunocompromised.
38. P revention CfDCa. SARS-CoV-2 Variant Classifications and Definitions. 2021.
39. Об особенностях обращения лекарственных препаратов для медицинского применения, которые предназначены для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайной ситуации и для организации оказания медицинской помощи лицам, пострадавшим в результате чрезвычайных ситуаций, предупреждения чрезвычайных ситуаций, профилактики и лечения заболеваний, представляющих опасность для окружающих, заболеваний и поражений, полученных в результате воздействия неблагоприятных химических, биологических, радиационных факторов : постановление Правительства Российской Федерации от 3 апреля 2020 г. № 441. М., 2020.
40. Детские инфекции : Справочник практического врача / под ред. проф. Л.Н. Мазанковой. 3-е изд., перераб. и доп. М. : МЕДпресс-информ, 2021. 328 с.
41. Инфекционные болезни : национальное руководство / под ред. Н.Д. Ющука, Ю.Я. Венгерова. 3-е изд., перераб. и доп. М. : ГЭОТАР-Медиа, 2021.
42. Clinical virology manual. 5th ed. / ed. by M.J. Loeffelholz, R.L. Hodinka, S.A. Young, B.A. Pinsky. ASM Press, 2016. DOI: 10.1128/9781555819156.
43. Type I and Type III IFN Restrict SARS-CoV-2 Infection of Human Airway Epithelial Cultures / А. Vanderheiden [et al.] // BioRxiv. 2020.05.19.105437. DOI: 10.1101/2020.05.19.105437.
44. SARS-CoV-2 is sensitive to type I interferon pretreatment / K.G. Lokugamage [et al.] // BioRxiv preprint. 2020. DOI: 10.1101/2020.03.07.982264
45. Ведение детей с заболеванием, вызванным новой коронавирусной инфекцией (SARS-CoV-2) / Ю.С. Александрович [и др.] // Педиатрическая фармакология. 2020. Т. 17, № 2. С. 103-118. DOI: 10.15690/pf.v17i2.2096.
46. Лечение детей, инфицированных COVID-19, в непрофильном стационаре / Д.О. Иванов [и др.] // Педиатр. 2020. Т. 11, № 2. С. 5-14. DOI: 10.17816/PED1125-14.
47. Гасилина Е.С. Рациональная этиопатогенетическая интерферонотерапия у детей с инфекцией COVID-19 // Эффективная фармакотерапия. 2021. Т. 17. С.14-22.
48. Мазанкова Л. Н., Горбунов С. Г., Самитова Э. Р. Значение интерферонотерапии при COVID-19 у детей // Детские инфекции. 2021. Т. 20, № 1. С. 34-38. DOI: 10.22627/20728107-2021-20-1-34-38.
49. Современные возможности интерферонов в лечении детей с COVID-19 / А.И. Сафина [и др.] // Медицинский совет. 2021. № 1. С. 59-65.
50. Оптимизация противовирусной терапии новой корона-вирусной инфекции COVID-19 у детей / Г.П. Мартынова [et al.] // Педиатрия. Журнал им. Г.Н. Сперанского. 2021. Т. 100, № 3. С. 208-218.
51. Эффективность комплексной терапии препаратами рекомбинантного интерферона альфа 2b (ВИФЕРОН®) в лечении новой коронавирусной инфекции COVID-19 у детей / М.А. Строганова [и др.] // Инфекционные болезни в современном мире: эволюция, текущие и будущие угрозы : тезисы докладов научно-практической конференции. М., 2021. С. 153.
52. Хлынина Ю.О., Арова А.А., Невинский А.Б. Оценка эффективности рекомбинантного интерферона a-2b для лечения и профилактики новой коронавирусной инфекции у детей // Сборник трудов XIII Ежегодного Всероссийского конгресса по инфекционным болезням имени академика В.И. Покровского; IV Всероссийской научно-практической конференции; VI Всероссийского симпозиума. М., 2021.161 с.
53. COVID-19 у детей в мегаполисе: клинико-эпидемиологические и терапевтические аспекты / Р.А. Иванова [и др.] // Практическая медицина. 2020. Т. 18. С. 119-127.
54. COVID 19 и окислительный стресс / Б.В. Черняк [и др.] // Биохимия. 2020. Т. 85, вып. 12. С. 1816-1828.
55. Даренская М.А., Колесникова Л.И., Колесников С.И. COVID-19: окислительный стресс и актуальность антиоксидантной терапии // Вестник РАМН. 2020. Т. 75, № 4. С. 318-325. DOI: 10.15690/vramn1360.
56. Mironova G.D., Belosludtseva N.V, Ananyan M.A. Prospects for the use of regulators of oxidative stress in the comprehensive treatment of the novel coronavirus disease 2019 (covid-19) and its complications // European Review for Medical and Pharmacological Sciences. 2020. Vol. 24, № 16. P. 8585-8591.
57. Современные аспекты применения витамина D в клинической практике // Русский медицинский журнал. Мать и дитя. 2022. Т. 5, № 3. С. 244-252. DOI: 10.32364/26188430-2022-5-3-244-252.
58. Prognostic and Therapeutic Role of Vitamin D in COVID-19: Systematic Review and meta-analysis / H.A. Dissanayake [et al.] // Journal of Clinical Endocrinology and Metabolism. 2022. Vol. 107, № 5. P 1484-1502. DOI: 10.1210/clinem/dgab892.
59. Pre-infection 25-hydroxyvitamin D3 levels and association with severity of COVID-19 illness / A.A. Dror [et al.] // PLoS One. 2022. Vol. 17, № 2. e0263069. DOI: 10.1371/journal. pone.0263069.
60. The role of vitamin D in the age of COVID-19: A systematic review and meta-analysis / R. Ghasemia, [et al.] // International Journal of Clinical Practice. 2021. Vol. 75, № 11. e14675. DOI: 10.1111/ijcp.14675.
61. Mean Vitamin D levels in 19 European Countries & COVID-19 Mortality over 10 months / A. Ahmad, C. Heumann, R. Ali, T. Oliver // MedRxiv. 2021. Vol. 03, № 11. Р 21253361. DOI: 10.1101/2021.03.11.21253361.
62. EVMS Critical Care COVID-19 Management Protocol 0514-2020 evms.edu/covidcare.
63. Боковикова Т.Н., Багирова В.Л., Черникова Е.П. Новый препарат «Галавит»: методы анализа и стандартизации // Фарматека. 1999. № 2. С. 53-55.
64. Nelyubov M. V. Cytokins in the pathogenesis of astrakhan spotted fever and North Asian scrub typhus: problems of immunocorrection // Bulletin of Experimental Biology and Medicine. 2002. Vol. 134, № 2. Р 165-167.
65. Гришина Т.Н., Кузьмина Е.Г., Захарова Н.С. Иммуномодулирующие свойства препарата «Галавит» (клиническое использование и механизмы действия) // «Галавит» : Сборник статей. М., 2002. С. 6-15.
66. Латышева Т.В., Щербакова О.В. Клинические аспекты использования отечественного иммуномодулятора «Галавита» // Фарматека. 2004. № 7. С. 51-54.
67. Choongho Lee. Therapeutic Modulation of Virus-Induced Oxidative Stress via the Nrf2-Dependent Antioxidative Pathway // Hindawi Oxidative Medicine and Cellular Longevity. 2018. Oct 31. Article ID 6208067. DOI: 10.1155/2018/6208067
68. Добрица В.П., Ботерашаили Н.М., Добрица Е.В. Современные иммуномодуляторы для клинического применения : Руководство для врачей. СПб. : Политехника, 2001. С. 164-165.
69. Retrovirus-induced oxidative stress with neuroimmunodegeneration is suppressed by antioxidant treatment with a refined monosodium a-luminol (Galavit) / Y Jiang [et al.] // Journal of Virology. 2006. Vol. 80. Р. 4557-4569. DOI: 10.1128/ JVI.80.9.4557-4569.2006.
70. Опыт применения препарата «Галавит» у гинекологических больных с гнойными воспалительными заболеваниями органов малого таза / С.Н. Буянова [и др.] // Медицинский альманах. 2012. № 5. С. 78-81.
71. Латышева Т.В., Сетдикова Н.Х., Манько К.С. Вторичные иммунодефициты. Возможности использования отечественного иммуномодулятора «Галавит» // Цитокины и воспаление. 2005. Т. 4, № 3. С. 95-99.
72. Румянцев А.Г., Щербина А.Ю. Эффективность препарата «Галавит» у часто и длительно болеющих детей старше 6 лет // Российский вестник перинатологии и педиатрии. 2008. Т. 53, № 6. С. 100-101.
73. Попов Н.Н., Савво А.Н., Колиушко Е.Г. Эффективность применения иммуномодуляторов «Галавит» и «Рибомунил» в лечении детей с частыми заболеваниями лор-органов, сопровождающимися синдромом лимфоаденопатии // Экспериментальная и клиническая медицина. 2010, Т. 4, № 49. С. 107-112.
74. Селькова Е.П. Отчет о результатах контролируемого эпидемиологического наблюдения эффективности препарата «Галавит» в профилактике острых респираторных вирусных инфекций (ОРВИ) и гриппа у детей организованных коллективов. М. : МНИИЭМ им. Г.Н. Габричевского Роспотребнадзора, 2012.
75. Государственный реестр лекарственных средств. Зарегистрированные лекарственные препараты с МНН «Аминодигидрофталазиндион натрия».
76. Реестр разрешений на проведение клинических исследований лекарственных средств (rosminzdrav.ru) препарат аминодигидрофталазиндион натрия.
77. Инструкция по медицинскому применению лекарственного препарата Галавит®.
78. Профилактика средних и тяжелых форм COVID-19 аминодигидрофталазиндионом натрия («Галавит»®) у медицинского персонала «красной зоны» / С.В. Колесов [и др.] // Иммунология. 2020. Т. 41, № 6. С. 527-539.
79. Профилактика коронавирусной инфекции COVID-19 аминодигидрофталазиндионом натрия (Галавит®) у медицинских работников «красной зоны»: результаты многоцентрового наблюдательного исследования / С.В. Колесов [и др.] // Инфекционные болезни: новости, мнения, обучение. 2022. Т. 11, № 1.
80. Опыт применения иммуномодуляторов для профилактики коронавирусной инфекции (COVID-19) у медицинского персонала и осложнений пневмонии у больных COVID-19 / A. А. Свистунов [и др.] // Терапия. 2020. № 7. С. 156-164.
81. Применение иммуномодулирующего препарата аминодигидрофталазиндиона натрия для предотвращения прогрессирования пневмонии при COVID-19 / А.А. Свистунов [и др.] // Терапевтический архив. 2020. Т. 92, № 11. С. 65-70.
82. Возможность применения препарата, содержащего аминодигидрофталазиндион натрия, у пациентов с COVID-19, в том числе для терапии «цитокинового шторма» / B. М. Цветов [и др.] // Качественная клиническая практика. 2020. № 4S. С. 4-7. DOI: 10.37489/2588-0519-2020-S4-4-7/
83. Аминодигидрофталазиндион натрия в профилактике, лечении и реабилитации пациентов с заболеваниями органов дыхания / Д.И. Трухан [и др.] // Consilium Medicum. 2021. Т. 23, № 3. С. 296-303. DOI: 10.26442/20751753.2021.3.200839.
84. Safety and efficacy of ivermectin and doxycycline monotherapy and in combination in the treatment of COVID-19: A scoping review / S. Bhowmick [et al.] // Drug Safety 2021. Vol. 44. Р. 635-644.
85. Doxycycline treatment of high-risk COVID-19-positive patients with comorbid pulmonary disease / P.A. Yates [et al.] // Therapeutic Advances in Respiratory Disease. 2020. Vol. 14. Р 1753466620951053.
86. The FDA-approved drug ivermectin inhibits the replication of SARS-CoV-2 in vitro / L. Caly [et al.] // Antiviral Research. 2020. Vol. 178. Р 104787.
87. How new DRDO Drug 2-DG works on human cells and fights Covid-19. 2021. Last accessed on 2021 Jun 20
88. Evaluation of the Safety of CD24-Exosomes in Patients With COVID-19 Infection.
89. Plitidepsin has potent preclinical efficacy against SARS-CoV-2 by targeting the host protein eЕF1А / K.M. White [et al.] // Science. 2021. Science, 2021. Vol 371, Issue 6532. Р. 926931.
90. Concept Study to Evaluate the Safety Profi le of Plitidepsin in Patients With COVID-19 (APLICOV-PC). ClinicalTrials.gov Identifi er: NCT04382066.
91. Хаитов М.Р., Шиловский И.П., Кофиади И.А. и др. Средство для ингибирования репликации вируса SARS-CoV-2, опосредованного РНК-интерференцией. Патент № 2733361 от 15.09.2020. Заявка № 2020123316 от 14.07.2020.
92. Комбинированное лекарственное средство, обладающее противовирусным эффектом в отношении нового коронавируса SARS-CoV-M.R Хаитов [и др. //] Патент № 2746362 от 12.04.2021. Заявка № 2021106335 от 11.03.2021.
93. Silencing of SARS-CoV-2 with modifi ed siRNA-peptide dendrimer formulation / M. Khaitov [et al.] // Allergy. 2021. Apr 10.
94. Mironova G.D., Belosludtseva N.V., Ananyan M.A. Рrospects for the use of regulators of oxidative stress in the comprehensive treatment of the novel coronavirus disease 2019 (covid-19) and its complications // European Review for Medical and Pharmacological Sciences. 2020. Vol. 24, № 16. С. 8585-8591.
95. О возможности использования препаратов группы сукцинатов в условиях гипоксии при COVID-19 / Ю.П. Орлов [и др.] // Общая реаниматология. 2021. Т. 17, № 3. С. 78-98. DOI: 10.15360/1813-9779-2021-3-78-98.

