Тактика комбинированной иммунобиологической терапии новой коронавирусной инфекции (COVID-19) у ребенка с иммунодефицитным состоянием
СтатьиЛ.Н. Мазанкова1, д-р мед. наук, профессор, главный внештатный специалист по инфекционным болезням у детей ДЗМ, Э.Р. Самитова1,2, канд. мед. наук, И.М. Османов1,2, д-р мед. наук, профессор, главный внештатный детский специалист-нефролог ДЗМ, В.Г. Акимкин3, д-р мед. наук, профессор, академик РАН, Н.А. Драчева1, Е.П. Каурова2, Н.В. Лобань2, М.А. Анцупова2
1 ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, г. Москва
2 ГБУЗ «Детская городская клиническая больница им. З.А. Башляевой Департамента здравоохранения г. Москвы»
3 ФБУН «Центральный научно-исследовательский институт эпидемиологии» Роспотребнадзора
Резюме. В статье на клиническом примере продемонстрирована эффективность иммунобиологической терапии COVID-19 у ребенка с диффузной В-клеточной лимфомой. Для иммунобиологический терапии использована комбинация ингибитора рецептора интерлейкина 6 (ИЛ-6), иммуноглобулина человека против COVID-19, рекомбинантных вируснейтрализующих моноклональных антител класса IgG1 к SARS-CoV-2. Несмотря на двукратное введение иммуноглобулина, у больного сохранялась клиническая картина COVID-19 - длительное вирусовыделение (до 40 дней). Элиминация вируса произошла на 3-й день после введения рекомбинантных вируснейтрализующих моноклональных антител класса IgG1 к SARS-CoV-2.
Ключевые слова: COVID-19, SARS-CoV-2, вируснейтрализующие моноклональные антитела класса IgG1 к SARS-CoV-2, тоцилизумаб, иммуноглобулин человека против COVID-19, иммунодефицитное состояние, дети
Summary. The article presents a clinical observation of the course of COVID-19 in a child with diffuse B-cell lymphoma using a combination of immunobiological therapy (type 6 interleukin inhibitor, human immunoglobulin against COVID-19, recombinant virus-neutralizing monoclonal antibodies of the IgG1 class to SARS-CoV-2). Despite the double injection of COVID-globulin, the patient retained the clinical picture of coronavirus infection COVID-19, and also noted a long-term viral shedding (up to 40 days), with the elimination of the virus on the 3rd day after the introduction of recombinant virus-neutralizing monoclonal antibodies of the IgG1 class to SARS-CoV-2.
Keywords: COVID-19, SARS-CoV-2, SARS-CoV-2 neutralizing monoclonal IgG1 antibodies, tocilizumab, human immunoglobulin against COVID-19, immunodeficiency, children
Введение
Новая коронавирусная инфекция (COVID-19) может протекать в тяжелой форме, длительно, с формированием носительства SARS-CoV-2 в группах риска, в том числе у пациентов с иммунодефицитными состояниями. Именно поэтому актуальной для мирового здравоохранения остается разработка новых стратегий лечения данного заболевания [1].
У детей с иммунодефицитными состояниями в современной врачебной практике широко применяется иммунобиологическая терапия - эффективный метод лечения инфекционных заболеваний [2]. Данные доказательной медицины и предыдущий опыт лечения других вирусных инфекций, таких как грипп, SARS, MERS и лихорадка Эбола, указывают на снижение летальности пациентов от этих инфекций при использовании свежезамороженной плазмы и внутривенного иммуноглобулина [2-4]. Отечественный опыт ведения взрослых и детей с COVID-19 детально описан в действующих временных методических рекомендациях «Профилактика, диагностика и лечение новой коронавирусной инфекцией (COVID-19)» (15-я версия от 22.02.2022) [5].
Несмотря на сообщения о преобладании бессимптомных и легких форм COVID-19 у детей, около 1% случаев приходится на тяжелые и крайне тяжелые формы этой инфекции, возникающие преимущественно у больных с коморбидной патологией из групп риска [6, 7].
В Москве разработан «Клинический протокол лечения детей с новой коронавирусной инфекцией (COVID-19)», в котором подробно изложены алгоритмы оказания медицинской помощи детям с данным заболеванием [8]. В этом протоколе регламентировано проведение иммунобиологической терапии ингибиторами рецепторов интерлейкина-6 (ИЛ-6). Это препарат тоцилизумаб - рекомбинантное гуманизированное моноклональное антитело к человеческому рецептору ИЛ-6 из подкласса иммуноглобулинов IgG1, которое уменьшает воспаление, блокируя рецепторы к провоспалительному цитокину ИЛ-6. Показанием к его применению является тяжелое течение COVID-19: пневмония с прогрессирующей дыхательной недостаточностью (ДН) (КТ 2-4), мультисистемный воспалительный синдром, рефрактерный к глюкокортикостероидам в сочетании с внутривенными иммуноглобулинами (в течение 48 ч), цитокиновый шторм/гемофагоцитарный синдром.
В «Клиническом протоколе лечения детей с новой коронавирусной инфекцией (COVID-19)» рекомендовано применение высокоочищенного препарата иммуноглобулина человека против COVID-19 как способ пассивной иммунизации детей из групп риска тяжелого течения инфекции. Показанием к применению (в составе комплексной терапии) является инфекция, вызванная SARS-CoV-2 [8].
Инновационным подходом к терапии COVID-19 считается использование рекомбинантных антител человека класса IgG1 к SARS-CoV-2 [9]. В Москве с октября 2021 г. стало широко доступно использование в педиатрической практике однокомпонентного препарата (сотровимаб) и комбинации препаратов (бамланивимаб и этесевимаб) у пациентов из групп риска в рамках профилактики тяжелого течения COVID-19 [8].
Несмотря на накопленный двухлетний клинический опыт в борьбе с пандемией COVID-19, многие вопросы лечения и профилактики этой инфекции требуют обсуждения. Особый интерес представляют иммунологические изменения в организме ребенка при инфицировании вирусом SARS-CoV-2, которые нуждаются в дальнейшем изучении.
С целью демонстрации особенностей течения COVID-19 и тактики ведения детей из группы риска -с онкологическими заболеваниями, которые сопровождаются иммунодефицитными состояниями и иммуносупрессивной терапией основного заболевания, -приводим нижеследующее клиническое наблюдение.
Клиническое наблюдение
Ребенок П., 17 лет, находился на стационарном лечении в Детской городской клинической больнице им. З.А. Башляевой с 07.12.2021 по 20.01.2022 (44 койко дня). Больной был переведен из Национального медицинского исследовательского центра онкологии им. Н.Н. Блохина с направляющим диагнозом: «U07.1 Коронавирусная инфекция COVID-19, двусторонняя пневмония, средней степени тяжести, ДН I-II степени. Пансинусит? Диффузная В-клеточная лимфома с поражением желудка, лимфоузлов брюшной полости, состояние после химиотерапии (6 курсов). Носитель центрального венозного катетера».
При поступлении пациент предъявлял жалобы на слабость, кашель, затрудненное дыхание, повышение температуры тела до 40,2°С, озноб.
Анамнез жизни: ребенок от первой беременности, протекавшей с токсикозом в I триместре, первых своевременных самостоятельных родов. Масса тела при рождении - 3350 г, рост - 52 см. Период новорожденно-сти без особенностей. В физическом и нервно-психическом развитии не отставал. Наблюдается у гематолога, онколога по поводу основного заболевания - диффузной В-клеточной лимфомы с поражением желудка, лимфоузлов брюшной полости (состояние после 6 курсов химиотерапии); имеется фебрильная нейтропения. Наследственность не отягощена. Аллергическая реакция в виде кожной сыпи на препарат «Бисептол». Ребенок вакцинирован только в родильном доме (против гепатита В и туберкулеза), далее не прививался из-за отказа родителей от вакцинации. Перенесенные заболевания (со слов матери): острые респираторно-вирусные инфекции, ветряная оспа, острые кишечные инфекции неустановленной этиологии, острый отит, внебольничная пневмония. Травм не было.
В анамнезе лапароскопическая биопсия желудка, аутологичная трансплантация стволовых клеток 24.11.2021. За пределы России не выезжал, контакта с инфекционными больными не было.
Из анамнеза заболевания: со слов матери, первые признаки онкологического заболевания (боли в спине, слабость, быстрая утомляемость) появились у ребенка в декабре 2020 г. Ребенок многократно обследован по месту жительства (в г. Ульяновске). В июне 2021 г. установлен клинический диагноз «диффузная В-клеточная лимфома». Для дальнейшего обследования и лечения 10.06.2021 ребенок переведен из Ульяновска в Москву, в Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина.
С 29.11.2021 у больного отмечалось покашливание. Выполнена 01.12.2021 мультиспиральная компьютерная томография (МСКТ) легких, признаков пневмонии не обнаружено. С 03.12.2021 кашель усилился, температура тела повысилась до 39,0-40,2°С, дыхание стало затрудненным. Проведена симптоматическая терапия (антипиретиками, местными антисептиками), но на ее фоне клинические проявления острого респираторного заболевания сохранялись, в связи с чем 07.12.2021 была выполнена повторная МСКТ легких, при которой выявлена полисегментарная двусторонняя пневмония (КТ-2). В ходе МСКТ лицевого скелета 07.12.2021 констатировано снижение пневматизации придаточных пазух носа (картина пансинусита). При исследовании назофарингеального мазка методом полимеразной цепной реакции (ПЦР) на COVID-19 07.12.21 у ребенка и у матери получен положительный результат, в связи с чем ребенок в сопровождении родителя поступил в инфекционное отделение № 1 Детской городской клинической больницы им. З.А. Башляевой.
Состояние при поступлении тяжелое из-за синдрома интоксикации (ребенок вялый, капризный, аппетит снижен, пьет мало), гипертермии (температура тела 38,9°С), ДН I степени. Сознание ясное. Астенического телосложения. Масса тела 42 кг, рост 171 см, индекс массы тела 14,3 кг/м2. Кожные покровы и видимые слизистые оболочки бледные, высыпаний нет, алопеция после химиотерапии. Диффузная гиперемия слизистой оболочки ротоглотки. Носовое дыхание затруднено, отделяемое слизистое. Кашель малопродуктивный, навязчивого характера, голос звонкий. Дыхание поверхностное, регулярное. Аускультативно в легких выслушивается жесткое дыхание с ослаблением в нижних отделах с двух сторон, мелкопузырчатые и проводные хрипы в нижних отделах легких на высоте вдоха и выдоха. Смешанная одышка, частота дыхательных движений 26 в минуту, SpQ2 96%. Тоны сердца приглушены, ритмичные, тахикардия (частота сердечных сокращений 108 в минуту), сердечные шумы отсутствуют. Артериальное давление 96/65 мм рт. ст. Печень выступает на 2 см из-под правого края реберной дуги, нижний край ровный, безболезненный. Периферические отеки и цианоз отсутствуют. Центральный венозный катетер функционирует, без признаков воспаления.
При исследовании назофарингеального мазка методом ПЦР 07.12.2021 обнаружена РНК SARS-CoV-2. Секвенирование генома SARS-CoV-2 показало, что у пациента вариант «дельта» SARS-CoV-2 (штамм B. 1.617.2). Результат иммуноферментного анализа (ИФА) крови на наличие антител к SARS-CoV-2 от 08.12.2021: IgM - 0,31 (N 0-2), IgG - 1,34 (N 0-10), единица измерения ОСЕ.
Результат общего анализа крови (ОАК) при поступлении (08.12.2021): анемия средней степени тяжести -уровень гемоглобина 87 г/л (норма 120-140 г/л), выраженная лейкопения - число лейкоцитов 0,6 х 109/л (норма 4-9 х 109/л) с палочкоядерным сдвигом до 14%, лимфопения - количество лимфоцитов 9% (норма 19-37%), значительная тромбоцитопения - число тромбоцитов 17-20 х 109 /л (норма 180-380 х 109 /л), гематокрит 23,8% (норма 36,0-47,0%).
Результат биохимического анализа крови (БАК) от 08.12.2021: нет значительных изменений уровня мочевины (2,7 ммоль/л) и креатинина (59 мкмоль/л), снижено содержание общего белка до 49,2 г/л (норма 63-77 г/л), глобулина до 14,7 г/л (норма 21-37 г/л), повышено соотношение альбумин/глобулины до 2,35 (норма 1,0-1,9) и уровень острофазных маркеров воспаления - ферритина до 937 нг/мл (норма 10150 нг/мл) и С-реактивного белка (СРБ) до 108,4 мг/л (норма0-5мг/л).Уровень прокальцитонина в норме -0,17 нг/мл (норма до 0,5 нг/мл).
Коагулограмма от 08.12.2021: повышен уровень фибриногена до 4,63 г/л (норма 1,8-3,5 г/л) и D-димера до 1353 нг/мл (норма 0-500 нг/мл) (см. таблицу).
Динамика лабораторных показателей в период госпитализации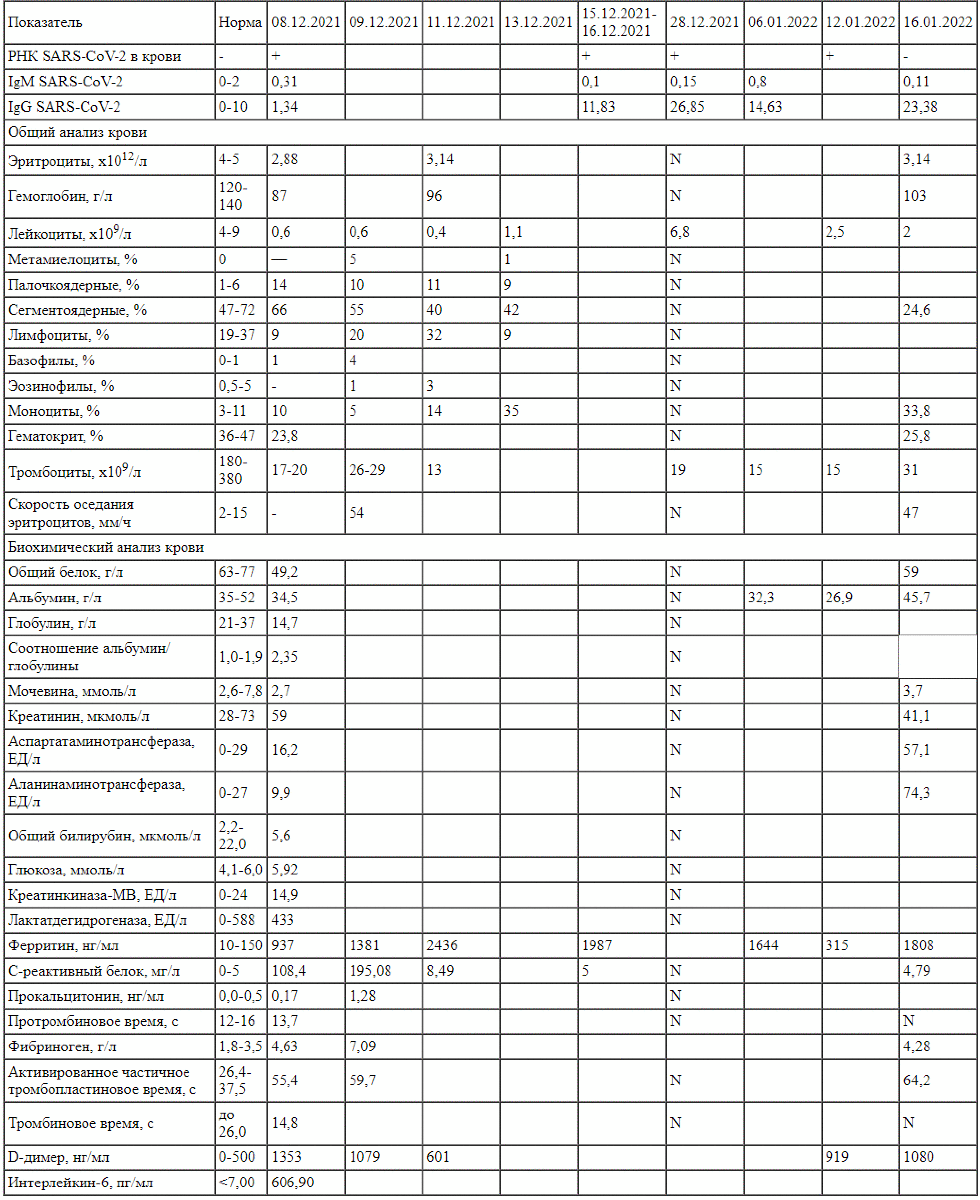 Результат общего анализа мочи (ОАМ) при поступлении (08.12.2021): удельный вес снижен до 1005 г/л (норма 1012-1022 г/л), протеинурия (0,25 г/л).
Результат общего анализа мочи (ОАМ) при поступлении (08.12.2021): удельный вес снижен до 1005 г/л (норма 1012-1022 г/л), протеинурия (0,25 г/л).
Ребенок проконсультирован оториноларингологом 08.12.2021, диагностирован острый пансинусит и двусторонний туботит.
С учетом жалоб (на слабость, кашель, затрудненное дыхание, повышение температуры тела до 40,2°С, озноб) и анамнеза заболевания (острое начало заболевания, положительные результаты ПЦР-диагностики COVID-19, изменения в легких, характерные для вирусной пневмонии, по результатам МСКТ (КТ-2)), данных клинико-лабораторного и инструментального обследований (выраженный синдром интоксикации, повышение температуры тела до 40,2°С, катаральный синдром в виде разлитой гиперемии зева, явлений ринита, малопродуктивный кашель, аускультативные изменения в легких (ослабление дыхания, мелкопузырчатые хрипы)), данных ОАК (лейкопения, тромбоцитопения с палочкоядерным нейтрофилезом, повышение уровня маркеров гуморального воспаления (СРБ, ферритина)), изменений в коагулограмме (высокий уровень D-димера, фибриногена), был поставлен клинический диагноз.
Основной диагноз: Коронавирусная инфекция, вызванная вирусом COVID-19 (U07.1), вирус идентифицирован, двусторонняя полисегментарная пневмония, ДН I-II степени, тяжелая форма. Осложнения основного заболевания: ДН I-II степени (J96.0). Вторичная тромбоцитопения (D69.5). Тяжелая белково-энергетическая недостаточность (E43). Острый пансинусит (J01.4). Двусторонний туботит у ребенка с диффузной В-крупноклеточной лимфомой с поражением желудка, лимфоузлов брюшной полости. Иммуноподвариант из постфолликулярных клеток. III стадия, 2-я группа риска. Состояние после 6 курсов полихимиотерапии по протоколу B-NHL-BFM-95. Аферез периферических стволовых клеток крови от 27.10.2021. Аутотрансплантация гемопоэтических стволовых клеток от 24.11.2021.
При повторном исследовании назофарингеального мазка методом ПЦР 08.12.2021 обнаружена РНК SARS-CoV-2.
Назначена комбинированная антибактериальная терапия (мерапенем из расчета 120 мг/кг/сут внутривенно, ванкомицин из расчета 40 мг/кг/сут внутривенно, азтреонам из расчета 90 мг/кг/сут внутривенно, метронидазол из расчета 22,5 мг/кг/сут внутривенно), противовирусная терапия (ацикловир в дозе 750 мг/м2/сут внутривенно), антифунгицидные препараты (каспо-фунгин 1,5 мг/кг/сут внутривенно), системные глюкокортикостероиды (дексаметазон из расчета 10 МЕ/м2 внутривенно), гранолоцитарный колониестимулирующий фактор (ГКСФ) - до достижения уровня лейкоцитов периферической крови 5,5 х 109/л (ликастин в дозе 480 мг/сут подкожно), дезинтоксикационная терапия глюкозо-солевыми растворами, симптоматическое и патогенетическое лечение: ингибиторы протонной помпы (омепразол), муколитики (бромгексин), антиагреганты (гепарин в дозе 100 МЕ/кг/сут внутривенно), гепатопротекторы (урсофальк), сорбенты (смекта), антипиретики (литическая смесь, парацетамол, нурофен), местные антисептики (колларгол, мирамистин), деконгестанты (називин). Ежедневный контроль веса; в связи с выраженной тромбоцитопенией показано внутривенное введение облученного тромбоконцентрата (40 мл на 10 кг массы тела). По результатам дообследования 08.12.2021: уровень N-концевого полипептида натрийуретического гормона (В-типа) повышен до 468,80 пг/мл (норма <125 пг/мл), тропонина I - повышен до 21,4 нг/л (норма <15,6 нг/л). Уровень ИЛ-6 (иммунологическое исследование от 08.12.2021) значительно превышен (в 86 раз) - 606,90 пг/мл (норма <7,00 пг/мл) (см. таблицу).
Проведена телемедицинская консультация (08.12.2021) с участием ведущих профильных детских специалистов Департамента здравоохранения г. Москвы и Минздрава России: онколога, гематолога, трансплантолога, пульмонолога, инфекциониста, по итогам которой с учетом тяжести и уровня маркеров «цитокинового шторма» ребенку назначен ингибитор ИЛ-6 тоцилизумаб («Актемра») из расчета 8 мг/кг внутривенно через инфузомат, однократно, при коррекции лейкопении ГКСФ и тромбоцитопении тромбоконцентратом (40 мл на 10 кг массы тела, 200 мл).
На 2-е сутки (09.12.2021) с момента проведения иммунобиологической терапии у ребенка с иммунодефицитным состоянием состояние по-прежнему расценено как тяжелое, повышения температуры тела не было, данные о состоянии органов и систем оставались прежними. После трансфузии тромбоконцентрата в контрольном ОАК сохранялась тромбоцитопения (26-29 х 109/л), лейкопения (0,6 х 109/л), высокая скорость оседания эритроцитов (54 мм/ч), нейтрофилез (10 %) со сдвигом до метамиелоцитов (5,0%). В контрольных анализах: повышен уровень фибриногена до 7,09 г/л (норма 1,80-3,50 г/л), D-димера до 1079,0 нг/мл (норма 0,0-500,0 нг/мл), ферритина до 1381 нг/мл (норма 10-150 нг/мл), возрос уровень прокальцитонина до 1,28 нг/мл (норма <0,5 нг/мл) и СРБ до 195,08 мг/л (норма <5,00 мг/мл) (см. таблицу). При ультразвуковом исследовании (УЗИ) органов брюшной полости выявлены признаки спленомегалии, диффузных изменений поджелудочной железы, лимфаденопатия.
Учитывая высокий риск развития генерализованной бактериальной инфекции у ребенка с иммунодефицитным состоянием на фоне онкогематологической патологии и тяжелым течением COVID-19 после проведения биологической терапии тоцилизумабом и низкий уровень специфических иммуноглобулинов против SARS-CoV-2 (IgM - 0,31, IgG - 1,34) телемедицинский консилиум, в который вошли специалисты Департамента здравоохранения г. Москвы и Минздрава России, 09.12.2021 принял решение о внутривенном введении иммуноглобулина человека против COVID-19 из расчета 1 мл/кг/сут с иммунозаместительной целью.
С 10.12.2021 по 11.12.2021 у ребенка отмечались эпизоды повышения температуры тела до фебрильных значений преимущественно в ночное время, сохранялись симптомы интоксикации (слабость, вялость), ДН I-II степени, катаральный синдром без тенденции к регрессу. В ОАК от 11.12.2021 - нарастание лейкопении (0,4 х 109/л) с относительным палочкоядерным нейтрофилезом и моноцитозом (палочкоядерные - 11%, сегментоядерные - 40%, лимфоциты 32%, эозинофилы - 3%, моноциты - 14%) сохраняется анемия (гемоглобин 96 г/л, эритроциты - 3,14 х 1012/л), критически выраженная тромбоцитопения - 13 х 109/л. (см. таблицу).
Ребенку проведена повторная трансфузия тромбо-концентрата. Достигнута стабилизация состояния к 13.12.2021, в ОАК количество лейкоцитов увеличилось до 1,1 х 109/л на фоне введения ГКСФ, число тромбоцитов - до 42 х 109/л. Состояние ребенка незначительно улучшилось, лихорадка была купирована, катаральные проявления и интоксикационный синдром оставались без значительной динамики. По лабораторным данным на 6-й день с момента проведения терапии тоцилизумабом и 5-й день с момента введения иммуноглобулина человека против COVID-19 (14.12.2021) наблюдалось снижение уровня острофазных маркеров воспаления: СРБ до 8,49 мг/л, D-димера до 601 нг/мл, однако уровень ферритина сохранялся повышенным (2436 нг/мл). При исследовании назофарингеального мазка методом ПЦР (15.12.2021) получен положительный результат (выявлена РНК SARS-CoV-2).
Несмотря на достигнутый клинический эффект от комбинированной иммунобиологической терапии ингибитором ИЛ-6 и иммуноглобулином против COVID-19, нормализацию температуры тела, незначительное улучшение общего состояния, на фоне тенденции к нормализации показателей ОАК и маркеров гуморального воспаления в контрольном ОАК от 15.12.2021 снова зафиксировано критическое снижение содержания тромбоцитов до 7-12 х 109/л (см. таблицу).
Проведена третья трансфузия тромбоконцентрата, после которой отмечено кратковременное повышение содержания тромбоцитов периферической крови, однако 17.12.2021 возникла потребность в очередной, четвертой трансфузии тромбоконцентрата в связи с падением уровня тромбоцитов до 16 х 109/л.
На 10-е сутки после введения тоцилизумаба и 9-е сутки после введения иммуноглобулина против COVID-19 (18.12.2021) общее состояние ребенка, активность, аппетит улучшились, катаральные явления, симптомы ДН, аускультативные изменения в легких регрессировали, показатели коагулограммы и уровень маркеров воспаления пришли в норму (СРБ <5 мг/л, ферритин 1987 нг/мл) (см. таблицу). Продолжен курс антибактериальной, противогрибковой и противовирусной терапии (суммарно 10 дней). Тем не менее сохранялось активное вирусовыделение (обнаружена РНК SARS-CoV-2 в назофарингеальном мазке от 19.12.2021 (на 12-й день лечения), по данным ИФА крови (16.12.2021) концентрация антител к вирусу SARS-CoV-2 оставалась низкой (IgM - 0,1, IgG - 11,83). По результатам МСКТ по-прежнему выявлялись изменения в легких по типу «матового стекла» (КТ-2, вовлечение до 30% паренхимы легких), характерные для вирусного поражения, отмечались линейные уплотнения (формирование фиброзных изменений (?)).
В связи с отсутствием гуморального иммунного ответа на инфекцию (низким уровнем антител классов IgM, IgG к SARS-CoV-2) к концу 2-й недели заболевания, несмотря на проведение пассивной иммунизации иммуноглобулином человека против COVID-19 с иммунозаместительной целью, консилиум рекомендовал повторное внутривенное введение иммуноглобулина из расчета 1 мл/кг/сут и пятую трансфузию тромбоконцентрата в связи очередным падением уровня тромбоцитов (до 16 х 109/л).
После этого 22.12.2021 у ребенка возникла макрогематурия (моча цвета «мясных помоев», эритроцитурия (до 150-160 в после зрения)), протеинурия (0,25 г/л). Отмечалось увеличение массы тела и развитие периферических отеков по типу пастозности, в связи с чем к лечению добавлен петлевой диуретик (фуросемид). По результатам заочной консультации онколога рекомендовано продолжить антибактериальную и противогрибковую терапию (завершить курс азтреонама), продолжить введение ГКСФ, провести повторную трансфузию тромбоконцентрата при снижении уровня тромбоцитов до 20 х 109/л и менее.
При УЗИ органов брюшной полости и почек 23.12.2021 выявлены диффузные изменения стенок чашечно-лоханочной системы обеих почек, микрокальцинат правого надпочечника, умеренное увеличение правой доли печени, диффузные изменения поджелудочной железы, небольшое количество взвеси в мочевом пузыре. В ОАМ - макрогематурия со снижением в динамике. В ОАК - уменьшение количества тромбоцитов до 20 х 109/л, лейкопения (2,2 х 109/л), анемия (79 г/л). В БАК - снижение уровня альбумина до 22,8 г/л при нормальных значениях креатинина и мочевины, маркеров гуморального воспаления.
Проведена шестая трансфузия тромбоконцентрата и первая трансфузия эритроцитарной массы, внутривенное введение альбумина с заместительной целью.
С 24.12.2021 по 27.12.2021 (на 17-20-й день лечения) состояние ребенка стабильное, ближе к тяжелому, отечный синдром купирован, лихорадки не было, сохранялась умеренная интоксикация (слабость, плохой аппетит), снижение массы тела до 43,5 кг (кахексия), умеренная гиперемия зева. На фоне уменьшения количества тромбоцитов до 19 х 109/л зафиксирован эпизод носового кровотечения.
Проведена седьмая трансфузия тромбоконцентрата. Методом ИФА определен уровень антител к вирусу SARS-CoV-2 в крови (28.12.2021): IgM - 0,15, IgG - 26,85. При исследовании назофарингеального мазка методом ПЦР (29.12.2021) обнаружена РНК SARS-CoV-2.
С 29.01.2021 по 02.01.2022 состояние ребенка стабильное, с минимальной выраженностью симптомов интоксикации, купированием катаральных проявлений. Показатели БАК, ОАМ, коагулограмма 02.01.2022 в пределах референсных значений, в ОАК - нормализация числа лейкоцитов до 6,8 х 109/л, уменьшение количества тромбоцитов до 19 х 109/л, в связи с чем проведена восьмая трансфузия тромбоконцентрата, от введения ГКСФ решено воздержаться.
При исследовании назофарингеального мазка методом ПЦР 04.01.2022 обнаружена РНК SARS-CoV-2. При МСКТ 04.01.2022 визуализирована картина течения двустороннего полисегментарного интерстициального процесса с положительной динамикой за счет уменьшения интенсивности изменений. Степень тяжести на момент исследования КТ-2.
С 05.01.2022 у ребенка отмечается снижение диуреза, появление периферических отеков в ночное время. По результатам лабораторных исследований крови (06.01.2022): тромбоцитопения (15 х 109/л), анемия легкой степени, гипоальбуминемия (32,3 г/л), повышенный уровень ферритина (1644 нг/мл). Методом ИФА крови выявлено снижение в динамике уровня антител к вирусу SARS-CoV-2 (IgM - 0,8, IgG - 14,63). При УЗИ визуализированы признаки диффузных изменений стенок чашечно-лоханочной системы обеих почек. Курс получаемой антибактериальной терапии завершен, назначен диуретик (фуросемид), девятая трансфузия тромбоконцентрата, ципрофлоксацин перорально по 500 мг 2 раза в сутки офф-лейбл.
С 07.01.2022 по 11.01.2022 сохраняются незначительные отеки по типу пастозности голеней, стоп, передней брюшной стенки. На 36-е сутки лечения (12.01.2022) в контрольном назофарингеальном мазке методом ПЦР выявлена РНК SARS-CoV-2. В ОАК -лейкопения (2,5 х 109/л, тромбоцитопения 15 х 109/л); проведена десятая трансфузия тромбоконцентрата. Уровень D-димера 919 нг/мл, ферритина 315 нг/мл, азотовыделительная функция почек сохранена, гипоальбуминемия -26,9 г/л, гипогликемия (см. таблицу). Электрокардиограмма и эхокардиограмма (12.01.2022) - без патологии.
В связи с длительно сохраняющимся вирусовыделением (37 дней), вирусным поражением легких по данным МСКТ, отсутствием формирования иммунного ответа на коронавирусную инфекцию у ребенка с иммунодефицитным состоянием из группы риска по тяжелому течению COVID-19 13.01.2022 телемедицинский консилиум, состоящий из специалистов Департамента здравоохранения г. Москвы и Минздрава России, с целью элиминации SARS-CoV-2 принял решение об однократном внутривенном введении препарата рекомбинантных моноклональных антител класса IgG1 к SARS-CoV-2 (сотровимаб) в дозе 500 мг офф-лейбл.
С 16.01.2022 (на 3-и сутки после введения моноклональных антител) РНК SARS-CoV-2 методом ПЦР в назофарингеальном мазке не обнаружена, методом ИФА крови 17.01.2022 выявлено снижение уровня антител к SARS-CoV-2 класса IgM (0,11) и повышение уровня антител класса IgG (23,38). По данным контрольного ОАК сохранялась лейкопения (3,3 х 109/л), анемия средней тяжести, тромбоцитопения (31 х 109/л). По результатам БАК от 18.01.2022 уровень альбумина нормализовался. Сохранялась умеренная гипопротеинемия. Показатели коагулограммы пришли в норму, уровень ферритина оставался повышенным до 1808 нг/мл, что связано с лимфопролиферативным заболеванием ребенка.
Обсуждение
Детям, входящим в группу риска тяжелого течения COVID-19 в связи с иммунодефицитным состоянием, можно назначать ингибитор ИЛ-6 в дозе ниже рекомендованной (по массе тела), как было показано в клиническом примере (в данном случае - 8 мг/кг (при массе >30 кг доза 12 мг/кг; при >30 кг доза 8 мг/кг), из-за риска развития генерализованного бактериального процесса.
Иммуноглобулин против COVID-19 был применен у ребенка на 2-й день после введения тоцилизумаба (ингибитора ИЛ-6), который обладает способностью снижать иммунный ответ организма человека на инфекционные агенты, так как ИЛ-6 является одним из важнейших медиаторов острой фазы воспаления, стимулирует пролиферацию и дифференцировку B-клеток, T-клеток и лейкоцитопоэз, а избыточная продукция ИЛ-6 вызывает повреждение тканей вследствие аутоиммунной реакции, например повреждение суставов при ревматоидном артрите, активирует остеокласты, повреждающие костную ткань. В связи с этим было принято решение о повторном введении иммуноглобулина против COVID-19 из-за несостоятельности гуморального и клеточного иммунитета у ребенка с В-клеточной лимфомой.
Вируснейтрализующие моноклональные антитела были применены вне протокола (срок болезни превышал 10 дней с момента первых клинических симптомов COVID-19) по решению врачебной комиссии для элиминации вируса из организма ребенка с В-клеточной лимфомой с длительным вирусовыделением в назофарингеальном мазке (срок заболевания 37 дней) у ребенка с иммунодефицитным состоянием. Продемонстрирована эффективность данной тактики: SARS-CoV-2 в контрольных мазках не определялся с 3-го дня применения.
Выше было упомянуто, что с конца 2021 года стали доступны для использования в педиатрической практике г. Москвы рекомбинантные моноклональные антитела класса IgG1 к SARS-CoV-2 в рамках профилактики (до 7-10-го дня заболевания) у пациентов из групп риска тяжелого течения COVID-19, но у этой же группы детей с длительным вирусовыделением можно использовать моноклональные антитела класса IgG1 к SARS-CoV-2 с элиминационной целью, как было продемонстрировано на клиническом примере.
Заключение
Данный клинический пример демонстрирует особенности комбинированной иммунобиологической терапии COVID-19 у ребенка с иммунодефицитным состоянием на фоне острой В-клеточной лимфомы, с несостоятельностью иммунного ответа против вируса SARS-CoV-2 (вариант «дельта» штамм B.1.617.2): несмотря на подавление «цитокинового шторма», двукратное введение иммуноглобулина человека против COVID-19 с иммунозаместительной целью, не произошло полного выздоровления пациента, так как сохранялся положительный результат теста на COVID-19. Обращает на себя внимание длительное вирусовыделение (около 40 дней) у больного с иммунодефицитным состоянием за счет онкологического заболевания.
Элиминация SARS-CoV-2 наступила спустя 3 дня после введения рекомбинантных моноклональных антител класса IgG1 к SARS-CoV-2, что подтверждает эффективность данного препарата. Он может быть использован не только для профилактики тяжелого течения COVID-19 (до 7-10-го дня заболевания), но и после 10-го дня от начала заболевания у лиц с иммунодефицитными состояниями для быстрой элиминации вируса из организма, т. е. при длительном вирусовыделении у детей из групп риска тяжелого течения COVID-19. Накопленный нами опыт свидетельствует о том, что эти дети требуют индивидуального подхода к лечению COVID-19, и элиминация SARS-CoV-2 в этих случаях помогает своевременно начать специализированное лечение основного заболевания в профильном лечебном учреждении.
Литература
1. Jahanshahlu L., Rezaei N. Monoclonal antibody as a potential anti-COVID-19 // Biomedicine & Pharmacotherapy. 2020. Vol. 129.
2. Immunotherapy for infectious diseases in haematological immunocompromise / M.T. Cutino-Moguel, C. Eades, K. Rezvani, D. Armstrong-James // British Journal of Haematology. 2017. Vol. 177, No. 3. P 348-356.
3. COVID-19, SARS and MERS: are they closely related? / N. Petros-illo [et al.] // Clinical Microbiology and Infection. 2020. Vol. 26, No. 6. P. 729-734.
4. Walker L.M., Burton D.R. Passive immunotherapy of viral infections: ’super-antibodies’ enter the fray // Nature Reviews Immunology. 2018. Vol. 18, No. 5. P. 297.
5. Временные методические рекомендации «Профилактика, диагностика и лечение новой коронавирусной инфекцией (COVID-19)». Версия 15 от 22.02.2022.
6. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study / F. Zhou [et al.] // Lancet. 2020. Vol. 395. P. 1054-1062.
7. Tocilizumab for the treatment of severe COVID-19 pneumonia with hyperinflammatory syndrome and acute respiratory failure: a single center study of 100 patients in Brescia, Italy / P. Toniati [et al.] // Autoimmunity Reviews. 2020. Vol. 19, No. 7.
8. Клинический протокол лечения детей с новой коронавирусной инфекцией (COVID-19) / под ред. А.И. Хрипуна. М., 2021.
9. Смирнов В.С., Тотолян А.А. Некоторые возможности иммунотерапии при коронавирусной инфекции // Инфекция и иммунитет. 2020. Т. 10, № 3. C. 446-458.

