Возможности профилактики инфекции мочевой системы у детей с использованием различных вариантов противорецидивной терапии
СтатьиО.В. Шатохина, ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России
Резюме. В статье дан обзор современных тенденций и результатов исследований по проблеме противорецидивной терапии инфекции мочевой системы (ИМС) у детей с использованием как антибактериальных уро-септических препаратов, так и фитотерапевтических средств. Проанализированы доказательные исследования в направлении традиционных методов терапии рецидивов ИМС во взрослой и детской популяции. Сделан акцент на эффективности препарата Канефрон® Н в виде моно- и комплексной терапии при острой ИМС, в периоде восстановления, в противорецидивных и межрецидивных лечебных мероприятиях.
Ключевые слова: инфекция мочевой системы, острый цистит, пиелонефрит, противорецидивная терапия, уросептическая терапия, антибиотики, фитопрепарат, Канефрон® Н
Summary. The article provides an overview of current trends and research results on the problem of anti-relapse therapy of urinary system infection (USI) in children with the use of both antibacterial uroseptic drugs and phytotherapeutic agents. The evidence-based studies in the direction of traditional methods of treatment of recurrent USI in the adult and child population are analyzed. Emphasis is placed on the effectiveness of the drug Canephron® N in the form of mono-and complex therapy for acute USI, in the recovery period, in anti-relapse and inter-relapse therapeutic measures.
Keywords: urinary system infection, acute cystitis, pyelonephritis, anti-relapse therapy, uroseptic therapy, antibiotics, herbal medicine, Canephron® N
Инфекция мочевой системы (ИМС) является одной из наиболее частых причин обращения к врачу как детей, так и взрослых. Около 150 млн человек в среднем в год имеют подтвержденную ИМС [1], протекающую с ярко выраженными симптомами (дизурия, цисталгия, лихорадка, пиурия). Первый пик заболеваемости приходится на первый год жизни (примерно у 0,7% девочек и у 2,7% мальчиков) [2, 3], второй - в возрасте от 2 до 4 лет (примерно у 7,8% девочек и у 1,7% мальчиков), что соответствует возрасту приучения к туалету [4-6]. К 16 годам 11,3% девочек и 3,6% мальчиков имеют в анамнезе ИМС [4, 7, 8]. Рецидивы ИМС особенно часто встречаются у девочек [9]. Более половины девочек при этом будут иметь рецидивирующее течение инфекции [7, 10].
Наиболее часто возбудителем является кишечная микрофлора. На Escherichia coli приходится от 80 до 90% случаев ИМС у детей [5, 11, 12]. Другие микроорганизмы включают Enterobacter aerogenes, Klebsiella pneumoniae, Proteus mirabilis, Citrobacter, Pseudomonas aeruginosa, Enterococcus spp. и Serratia spp. [3, 7, 10, 11, 12].
Рецидивы ИМС часто являются результатом несоблюдения режима лечения, неадекватной антимикробной терапии, бактериальной резистентности, нарушения уродинамики в нижних отделах мочевого тракта (особенно пузырно-мочеточникового рефлюкса) или иммунодефицитных состояний [13, 14]. Рецидивирующая ИМС обычно не приводит к рубцеванию почки у детей без структурной почечной аномалии [15]. Таким образом, профилактика антибиотиками/уросептиками редко бывает оправданна, если принять во внимание побочные эффекты и возникновение резистентности к противомикробным препаратам, связанное с их частым употреблением при ИМС [16-18]. Систематический обзор 7 рандомизированных контролируемых исследований 2017 г. с участием 1427 детей с симптоматической или фебрильной ИМС (пиелонефритом) не показал значимого влияния антибиотикопрофилактики на образование рубцов в почках (отношение шансов (ОШ) 0,83; 95% доверительный интервал (95% ДИ) 0,55-1,26), как и субанализ, ограниченный детьми с пузырно-мочеточниковым рефлюксом (ОШ 0,79; 95% ДИ 0,51-1,24) [19]. Профилактическое использование антибиотиков/уросептиков при рецидивах ИМС расценивается неоднозначно, так как несколько масштабных исследований этой проблемы у детей показали статистически благоприятный эффект профилактической фармакотерапии [5]. К настоящему времени как оптимальная рассматривается непрерывная антимикробная профилактика у детей с частыми пиелонефритами (фебрильной ИМС) независимо от наличия нарушения уродинамики [17, 20]. В некоторых случаях прибегают к непрерывной антимикробной профилактической терапии у детей с пузырно-мочеточниковым рефлюксом IV или V степени или другой аномалией с грубым нарушением уродинамики [21].
С профилактической целью наиболее часто у детей применяются низкие дозы нитрофурантоина, фу-рагина, триметоприма сульфаметоксазола, фосфомицина, цефалексина, цефтриаксона, амоксициллина клавуланата [22, 23]. Антимикробные препараты следует назначать в зависимости от результатов посева мочи на микрофлору и чувствительность к антибиотикам. Однако из-за чрезмерного и неправильного назначения наиболее часто употребляемых в практике антибактериальных препаратов появление устойчивых к ним уропатогенов становится все более распространенным явлением, что приводит к неэффективности основных вариантов антибиотикотерапии [24]. Устойчивость к антибиотикам была движущей силой инициатив по разработке новых классов антибактериальных препаратов, и срочно требуется внедрение альтернативных методов лечения и профилактики ИМС.
Развитие устойчивых к антибиотикам бактерий все чаще приводит к неэффективности антибактериальной терапии, и плохо поддающаяся терапии ИМС становится все более распространенной [25]. Кроме того, относительно высокая частота рецидивов ИМС затрудняет эффективное лечение этих инфекций [26].
B. Foxman и M. Buxton предполагают, что эмпирические методы лечения ИМС следует пересмотреть по следующим причинам [27]:
Таким образом, преимущества эмпирической антибактериальной терапии могут не перевешивать риски [31, 32]. Новые и инновационные стратегии предотвращения рецидивов ИМП и альтернативные методы лечения считаются высокоприоритетными [27].
Запуск и разработка Стратегии традиционной медицины ВОЗ на 2014-2023 гг. направлены на поддержку и реализацию исследований и программ по повышению роли народной (традиционной) медицины в сохранении здоровья населения [33]. Стратегия направлена на разработку новых направлений в здравоохранении (включая использование дополнительных и традиционных лекарственных средств) в качестве высокого приоритета. Пересмотр традиционных лекарств является наиболее привлекательным вариантом для разработки новых методов лечения инфекций, поскольку лекарства растительного происхождения использовались для этого сотни лет.
Из наиболее популярных и исследованных лекарственных средств хорошо зарекомендовали себя препараты на основе клюквы, которые препятствуют адгезии бактерий к уроэпителию [34]. Продукты из клюквы все чаще используются для профилактики ИМС, особенно у взрослых пациентов [34, 35]. Традиционные средства на основе клюквы включают клюквенный сок, клюквенные капсулы, желатинизированные продукты и свежую цельную клюкву [16]. Метаанализ 7 рандомизированных контролируемых исследований 2017 г., проведенных с участием 1498 женщин в возрасте ≥18 лет с ИМП в анамнезе, показал, что клюква снижает риск ИМС на 26% (ОШ 0,74; 95% ДИ 0,55-0,98) [36]. Использование продуктов из клюквы для профилактики рецидивирующей ИМС у детей исследовано менее полно. Более того, длительное регулярное употребление продуктов из клюквы может иметь противопоказания, особенно для маленьких детей [16].
Пробиотики использовались для профилактики ИМС у детей и взрослых [37-39]. Метаанализ Cochrane (2017 г.) на основании 6 рандомизированных и квазирандомизированных контролируемых исследований с участием 352 детей и взрослых с ИМС не выявил значительного снижения риска рецидива ИМС у пациентов, получавших пробиотики, по сравнению с теми, кто получал плацебо (отношение рисков 0,82; 95% ДИ 0,60-1,12) с широкими доверительными интервалами [39]. Авторы отметили, что положительные эффекты нельзя исключать, поскольку данных было немного и они были получены в результате небольших исследований с плохой методологической отчетностью.
В настоящее время в ряде случаев считается целесообразным использование традиционных растительных средств не только для профилактики рецидивов, но и для изолированного лечения не осложненных нарушением уродинамики эпизодов ИМС. Согласно действующему руководству Европейской ассоциации урологов (EAU) [40], а также междисциплинарному руководству Германии по диагностике и терапии инфекций мочевых путей (ИМП) у взрослых, антибиотики по-прежнему считаются препаратами 1-й линии при ИМП, но симптоматическое лечение без антибиотиков рекомендовано рассматривать в случаях острого неосложненного цистита с легкими или умеренными симптомами [41]. Применение растительных препаратов также является подходящим подходом к лечению ИМП без применения антибиотиков [42, 43].
Одним из таких препаратов, одобренных в 31 стране для кратковременного и длительного лечения различных урологических заболеваний, является Канефрон® Н, который содержит траву золототысячника (Centaurium erythraea), корни любистока (Levisticum officinale) и листья розмарина (Rosmarinus officinalis) [44]. Препарат обладает так называемыми «многоцелевыми» свойствами, включая спазмолитическое [45], диуретическое [46], антиоксидантное [47], антиадгезивное [48], противовоспалительное и обезболивающее действие [49].
Эффективность Канефрона Н была продемонстрирована в ряде клинических исследований [44, 50-52]. В 2018 г. F.M. Wagenlehner и соавт. провели рандомизированное двойное слепое двумя плацебо-контролируемое исследование III фазы, которое продемонстрировало, что лечение женщин с острой ИМП с помощью Канефрона Н не уступает по эффективности лечению антибиотиком фосфомицина трометамолом и предотвращает дополнительный прием антибиотиков [52].
В одном из последних исследований M. Holler и соавт. были проанализированы данные реальной клинической практики (real world data) в Германии за 2016-2019 гг. С целью оценки эффективности препаратов растительного происхождения из электронной базы данных были отобраны сведения о 160 912 пациентках с острым циститом, которые принимали Канефрон® Н либо антибиотики. Оказалось, что растительный препарат был сопоставим по эффективности с противомикробными средствами и был даже более эффективным в снижении числа рецидивов ИМП. Таким образом, были подтверждены клинические данные предыдущих интервенционных исследований [55].
Это, по сути, первое исследование такого масштаба в Германии, доказывающее эффективность монотерапии Канефроном Н в качестве симптоматического лечения ИМП. Данные подтверждают важную роль препарата в снижении частоты использования антибиотиков и резистентности к ним.
Представленные результаты не вызывают удивления, поскольку Канефрон® Н является хорошо изученным и одобренным лекарственным средством. Достоверной разницы в частоте развития рецидивов ИМП между фитопрепаратом и антибактериальной терапией в течение 1-30 дней исследования не было. При продолжении наблюдения в период с 31-го по 365-й день частота дополнительных назначений антибиотиков была значительно ниже после терапии Канефроном Н, чем после антибактериальной терапии.
О профилактическом эффекте данного растительного препарата, применяемого либо в составе комбинированной терапии, либо в качестве монотерапии у пациентов, страдающих ИМП, сообщалось в нескольких клинических исследованиях [54-58].
Канефрон® Н не только эффективен для лечения ИМС, но и хорошо переносится [59]. В отличие от антибиотиков, этот растительный лекарственный препарат не влияет на микробиоту кишечника так сильно, как фосфомицин или нитрофурантоин [60]. Это особенно важно, поскольку исследования микробиома мочи показали, что бессимптомная бактериурия, по-видимому, оказывает защитное действие против уропатогенов [61], и препарат может рассматриваться как «основной препарат выбора» в случае рецидивирующих инфекций [62].
В последние годы было исследовано несколько вариантов лечения ИМП без применения антибиотиков, в том числе с использованием нестероидных противовоспалительных препаратов у взрослых [63-65] и растительных препаратов, таких как Angocin (содержит траву настурции и корень хрена) [42] и Канефрон® Н. По сравнению с нестероидными противовоспалительными препаратами Канефрон® Н не только оказывает обезболивающий и противовоспалительный эффект, но и действует более разнообразно, облегчая симптомы, благодаря нескольким компонентам лекарственной смеси (1:1:1): траве золототысячника, корню любистока и листьям розмарина. Благодаря спазмолитическому [45], противовоспалительному и антиноцицептивному [49] эффектам фитопрепарат уменьшает выраженность симптомов, связанных с уретритом и циститом (таких, как боль, спазм и частое мочеиспускание). Кроме того, антиадгезивный эффект препарата [48] способствует устранению бактерий из мочевыводящих путей.
В педиатрической практике использование Канефрона Н при ИМС уже несколько десятилетий позволяет достичь максимальных результатов при проведении уросептических и противорецидивных мероприятий, что подтверждено результатами большого количества исследований.
Комбинированная терапия антибактериальным препаратом в сочетании с Канефроном у детей при остром цистите детально описана в работе Д.Д. Иванова и С.В. Кушниренко [66]. Моноцентровое открытое проспективное рандомизированное контролируемое исследование в параллельных группах проведено с участием 60 девочек в возрасте от 3 до 12 лет, находившихся на стационарном и амбулаторном лечении. В исследовании было показано, что добавление растительного препарата к антибактериальной терапии ускоряет регресс симптомов острого цистита у 93,3% детей в сравнении с монотерапией антибиотиками (70%) (см. рисунок), а также использование препарата Канефрон® Н у детей с острым циститом на протяжении 3 мес. достоверно снижает частоту рецидивов заболевания и увеличивает долю пациентов с сохраненной ремиссией до 96,7% (табл. 1).
Эффективность 3-месячного профилактического лечения инфекции нижних мочевых путей с применением Канефрона Н и без него по критерию «сохранение ремиссии» (по результатам моноцентрового открытого проспективного рандомизированного контролируемого исследования в параллельных группах [66])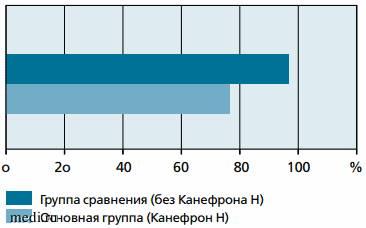
Таблица 1.
Число рецидивов цистита к концу 3-месячного периода наблюдения (по результатам моноцентрового открытого проспективного рандомизированного контролируемого исследования в параллельных группах [66]) * Достоверность различий по сравнению с группой сравнения, рХ2 < 0,05.
* Достоверность различий по сравнению с группой сравнения, рХ2 < 0,05.
Еще одно исследование эффективности использования Канефрона Н с противорецидивной целью при остром и хроническом пиелонефрите было проведено А.В. Еремеевой в 2020 г. Выборка составила 167 пациентов в возрасте от 2 до 12 лет, разделенных на группы по нозологическому принципу [67]. Пациенты с острым пиелонефритом в качестве профилактики получали Канефрон® Н в течение месяца, группа контроля не получала никакого лечения, а дети с хроническим пиелонефритом были распределены в зависимости от противорецидивной терапии по 3 группам:
В группах пациентов с острым пиелонефритом при последовательной терапии антибиотиками, а затем Канефроном Н в течении 1 мес. рецидивы заболевания отсутствовали в первые 6 мес. (100%) после окончания антибактериальной терапии, а также наблюдалась тенденция к увеличению периода ремиссии по сравнению с группой, в которой растительный препарат при остром пиелонефрите не применялся. Среди пациентов с хроническим пиелонефритом наименее эффективной оказалась схема монотерапии фуразидином: в группе, где она применялась, противорецидивный эффект статистически значимо (р < 0,05) уступал таковому в группах, в которых после антибиотикотерапии назначался Канефрон® Н. Среди этих пациентов оптимальные результаты по увеличению периода ремиссии получены при проведении комбинированной терапии фуразидином и Канефроном Н.
Возможность назначения растительного препарата в виде монотерапии при неосложненной инфекции нижних мочевых путей у детей рассматривалась М. Эрманом. С этой целью в амбулаторных условиях Канефроном Н было пролечено 15 пациентов 2-7 лет, был отмечен хороший эффект терапии - санация мочи к 8-му дню лечения и отсутствие рецидивов ИМС у 14 из 15 пациентов [68]. В случае осложненной ИМС и назначения антибиотиков автор рекомендует назначение Канефрона Н в виде вспомогательной терапии, а в период стихания воспаления -в виде монотерапии, что способствует сокращению сроков санации мочи и увеличению длительности межрецидивных промежутков.
Высокая эффективность и безопасность [66-71] использования Канефрона Н в детской нефрологической практике позволяет назначать терапию этим препаратом в условиях амбулаторного [69] и санаторно-курортного лечения [70]. В проспективном многоцентровом исследовании В.В. Длин и соавт. проанализировали результаты моно- и комбинированной терапии ИМС, а также противорецидивной терапии Канефроном Н у детей (п = 632) в условиях амбулаторий 20 крупных городов России. Основной вывод исследования заключается в том, что лечение данным фитопрепаратом детей в возрасте 1-17 лет безопасно и хорошо переносится, как в режиме монотерапии, так и в комплексе с антибиотиками. Это позволяет рекомендовать его широкое использование для лечения и профилактики заболеваний мочевыделительной системы [69]. Высокий комплаенс обеспечивается возможностью выбора формы выпуска препарата у разных возрастных групп - твердой (таблетки) и жидкой (капли). Назначение Канефрона Н в этом исследовании было проанализировано не только при ИМС (цистит, пиелонефрит), но при кристаллурии (дисметаболической нефропатии), мочекаменной болезни и нефритах. Применение фитопрепарата при уролитиазе и дисметаболической нефропатии достоверно снижало кристаллобразование и агрегационные свойства мочи. Подобные выводы сделаны Г. Летифовым (2017) при использовании Канефрона Н в комплексной терапии ИМС и дисметаболических нефропатий у детей [71]. Применение Канефрона Н у детей с высокой активностью микробно-воспалительного процесса в мочевыделительной системе приводит к исчезновению клинической симптоматики и нормализации лабораторных показателей активности патологического процесса в более короткие сроки, а также к достоверному повышению антикристаллообразующих свойств мочи, уменьшению патологической кристаллизации, что, в свою очередь, снижает риск рецидива ИМС.
В рандомизированном исследовании Н.Н. Каладзе, Е.И. Слободян у пациентов в возрасте от 6 до 17 лет (n = 40) с рецидивирующим течением ИМС вне обострения при санаторно-курортном лечении были показаны возможности пролонгированного применения Канефрона Н с целью восстановления функции почек. Общая длительность приема препарата составила 9 нед., по окончании терапии было отмечено достоверное снижение уровня провоспалительных цитокинов в сыворотке крови (табл. 2), а также ликвидирован дисбаланс между про- и противовоспалительными цитокинами [70]. Показатели здоровья и биохимические данные 40 детей основной группы сравнивались с показателями 15 здоровых детей. Результаты исследования не вызывают сомнений в возможности использования фитопрепарата при санаторно-курортном лечении детей с ИМС с ренопротективной целью.
Таблица 2.
Динамика параметров цитокинового профиля сыворотки крови у детей, больных хроническим пиелонефритом (М ± m) (по результатам рандомизированного исследования [70])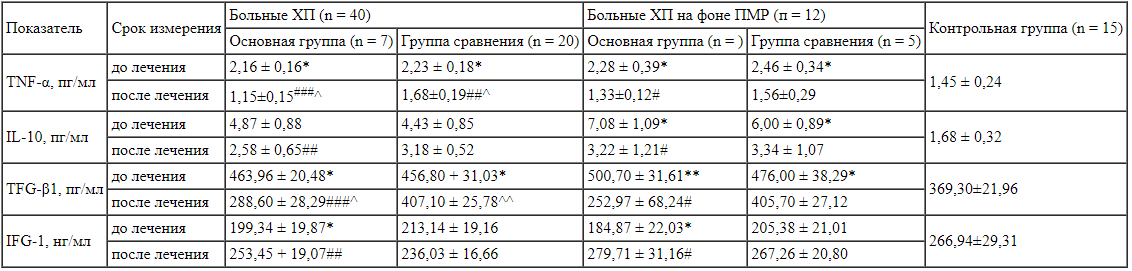 Примечание: *р < 0,05 - уровень значимости при сравнении исходного значения с контрольной группой; ** р < 0,01; #р < 0,05 - уровень значимости при сравнении значений до и после лечения; ##р < 0,01; ###р < 0,001; ^р < 0,05 - уровень значимости при сравнении 1-й и 2-й групп после лечения; ^^р < 0,01.
Примечание: *р < 0,05 - уровень значимости при сравнении исходного значения с контрольной группой; ** р < 0,01; #р < 0,05 - уровень значимости при сравнении значений до и после лечения; ##р < 0,01; ###р < 0,001; ^р < 0,05 - уровень значимости при сравнении 1-й и 2-й групп после лечения; ^^р < 0,01.
Несмотря на развитие фармакологии в направлении антибактериальной терапии, сложность в создании антибиотиков и быстрое развитие резистентности в сочетании с ограничениями по применению и безопасности в лечении детей, побочными эффектами, связанными с системным воздействием антибиотиков и их переносимостью, ставят перед педиатрами и терапевтами необходимость поиска альтернативных путей. Традиционные методы терапии, к которым все чаще обращается современная медицина, позволяют расширить терапевтические возможности, повысить безопасность и комплаентность лечения ИМС у детей, а исследования по этой проблеме у взрослых пациентов - подсказать наиболее перспективные пути развития.
Все представленные выше исследования показывают, что варианты лечения без антибиотиков приемлемы и требуют проведения отдельных клинических строго регламентированных исследований в педиатрии.
Литература
1. Urinary tract infections: Epidemiology, mechanisms of infection and treatment options / A.L. Flores-Mireles, J.N. Walker, M. Caparon, S.J. Hultgren II Nature Reviews Microbiology. 2015. Vol. 13. P 269-284.
2. Chang S.L., Shortliffe L.D. Pediatric urinary tract infections II Pediatric Clinics of North America. 2006. Vol. 53, No. 3. P 379-400.
3. Simoes e Silva A.C., Oliveira E.A. Update on the approach ofurinary tract infection in childhood II Jornal de Pediatria. (Rio J.).
2015. Vol. 91, No. 6, Suppl. 1. P S2-S10.
4. Expert panel on pediatric imaging: ACR appropriateness criteria, urinary tract infection-child I B.K. Karmazyn [et al.] II Journal of the American College of Radiology. 2017. Vol. 14, No. 5S. P S362-S371.
5. Korbel L., Howell M., Spencer J.D. The clinical diagnosis and management of urinary tract infections in children and adolescents II Paediatrics and International Child Health. 2017. Vol. 37, No. 4. P. 273-279.
6. Clark C.J., Kennedy W.A., II, Shortliffe L.D. Urinary tract infection in children: When to worry II Urologic Clinics of North America. 2010. Vol. 37, No. 2. P. 229-241.
7. Stephens G.M., Akers S., Nguyen H., Woxland H. Evaluation and management of urinary tract infections in the school-aged child II Primary Care. 2015. Vol. 42, No. 1. P. 33-41.
8. Larcombe J. Urinary tract infection in children II American Family Physician. 2010. Vol. 82, No. 10. P. 1252-1256.
9. Larcombe J. Urinary tract infection in children: recurrent infections II BMJ Clinical evidence. 2015. Vol. 2015. P. 0306.
10. Schlager T. A. Urinary tract infections in infants and children II Microbiology Spectrum. 2016. Vol. 4, No. 5.
11. Acute pyelonephritis in children I W. Morello, C. La Scola, I. Alberici, G. Montini II Pediatric Nephrology. 2016. Vol. 31, No. 8. P 1253-1265.
12. Urinary tract infections in infants and children: Diagnosis and management I J.L. Robinson, J.C. Finlay, M.E. Lang, R. Bortolussi // Paediatrics & Child Health. 2014. Vol. 19, No. 6. P 315-325.
13. Streptococcus pneumoniae urinary tract infection in pedeatrics I R. Pougnet, J. Sapin, L. De Parscau, L. Pougnet II Annales de Biologie Clinique (Paris). 2017. Vol. 75, No. 3. P. 348-350.
14. Early Antibiotic treatment for pediatric febrile urinary tract infection and renal scarring I N. Shaikh [et al.] II JAMA Pediatrics.
2016. Vol. 170, No. 9. P 848-854.
15. Canadian Paediatric Society, Community Paediatrics Committee, Infectious Diseases and Immunization Committee. Prophylactic antibiotics for children with recurrent urinary tract infections I J.L. Robinson, J.C. Finlay, M.E. Lang, R. Bortolussi II Paediatrics & Child Health. 2015. Vol. 20, No. 1. P 45-51.
16. Evaluation and management of recurrent urinary tract infections in children: State of the art I M. Awais [et al.] II Expert Review of Anti-infective Therapy. 2015. Vol. 13, No. 2. P 209-231.
17. Robinson J.L., Le Saux N. Management of urinary tract infections in children in an era of increasing antimicrobial resistance II Expert Review of Anti-infective Therapy. 2016. Vol. 14, No. 9. P 809-816.
18. RIVUR Trial Investigators. Antimicrobial prophylaxis for children with vesicoureteral reflux // The New England Journal of Medicine. 2014. Vol. 370, No. 25. P 2367-2376.
19. Antibiotic prophylaxis for urinary tract infection-related renal scarring: a systematic review / I.K. Hewitt [et al.] // Pediatrics.
2017. Vol. 139, No. 5.
20. Urinary tract infection in children / A.K.C. Leung, A.H.C. Wong, A.A.M. Leung, K.L. Hon // Recent Patents on Inflammation & Allergy Drug Discovery. 2019. Vol. 13, No. 1. P 2-18.
21. Профилактическое назначение антибиотиков детям с рецидивирующими инфекциями мочевыводящих путей /
J.L. Robinson, J.C. Finlay, M.E. Lang, R. Bortolussi ; Канадское педиатрическое общество, Общественный педиатрический комитет, Комитет по инфекционным заболеваниям и иммунизации // Педиатр. Здоровье ребенка. 2015. Т. 20, № 1. С. 45-51.
22. Sedberry-Ross S., Pohl H.G. Urinary tract infections in children // Current Urology Reports. 2008. Vol. 9, No. 2. P. 165-171.
23. Baumer J.H., Jones R.W. Urinary tract infection in children, National Institute for Health and Clinical Excellence // Archives of Disease in Childhood: Education and Practice Edition. 2007. Vol. 92, No. 6. P 189-192.
24. Developing new antimicrobial therapies: are synergistic combinations of plant extracts/compounds with conventional antibiotics the solution? / M.J. Cheesman, A. Ilanko, B. Blonk, I.E. Cock // Pharmacognosy Reviews. 2017. Vol. 11, No. 22. P. 57-72.
25. Medina M., Castillo-Pino E. An introduction to the epidemiology and burden of urinary tract infections // Therapeutic Advances in Urology. 2019. Vol. 11.
26. Risk factors for second urinary tract infection among college women / B. Foxman [et al.] // American Journal of Epidemiology. 2000. Vol. 151, No. 12. P. 1194-1205.
27. Foxman B., Buxton M. Alternative approaches to conventional treatment of acute uncomplicated urinary tract infection in women // Current Infectious Disease Reports. 2013. Vol. 15, No. 2. P 124-129.
28. Extended-spectrum β-lactamase-producing Gram-negative pathogens in community-acquired urinary tract infections: an increasing challenge for antimicrobial therapy / S. Meier [et al.] // Infection. 2011. Vol. 39, No. 4. P. 333-340.
29. Increasing prevalence of ESBL production among Irish clinical Enterobacteriaceae from 2004 to 2008: an observational study / J. Fennell [et al.] // BMC Infectious Diseases. 2012. Vol. 12, No. 116.
30. The pervasive effects of an antibiotic on the human gut microbiota, as revealed by deep 16S rRNA sequencing / L. Dethlefsen, S. Huse, M.L. Sogin, D.A. Relman // PLoS Biology. 2008. Vol. 6.
31. Trautner B.W, Gupta K.K. The advantages of second best: comment on “Lactobacilli vs antibiotics to prevent urinary tract infections” // Archives of Internal Medicine. 2012. Vol. 172. P 712-714.
32. Baerheim A. Empirical treatment of uncomplicated cystitis // Scandinavian Journal of Primary Health Care. 2012. Vol. 30, No. 1. P 1-2.
33. World Health Organization. WHO Traditional Medicine Strategy: 2014-2023. Geneva: World Health Organization, 2013.
34. Goldman R.D. Cranberry juice for urinary tract infection in children // Canadian Family Physician. 2012. Vol. 58, No. 4. P 398-401.
35. Highly standardized cranberry extract supplementation (Anthocran®) as prophylaxis in young healthy subjects with recurrent urinary tract infections / A. Ledda [et al.] // European Review for Medical and Pharmacological Sciences. 2017. Vol. 21, No. 2. P. 389-393.
36. Cranberry reduces the risk of urinary tract infection recurrence in otherwise healthy women: A systematic review and meta-analysis / Z. Fu, D. Liska, D. Talan, M. Chung // Journal of Nutrition. 2017. Vol. 147, No. 12. P 2282-2288.
37. The diagnosis, evaluation and treatment of acute and recurrent pediatric urinary tract infections / B. Becknell, M. Schober, L. Korbel, J.D. Spencer // Expert Review of Anti-infective Therapy. 2015. Vol. 13, No. 1. P. 81-90.
38. Lee S.J., Cha J., Lee J.W. Probiotics prophylaxis in pyelonephritis infants with normal urinary tracts // World Journal of Pediatrics. 2016. Vol. 12, No. 4. P 425-429.
39. Schwenger E.M., Tejani A.M., Loewen P.S. Probiotics for preventing urinary tract infections in adults and children // Cochrane Database of Systematic Reviews. 2015. No. 12. CD008772.
40. European Association of Urology Guidelines on Urological Infections / G. Bonkat [et al.]. EAU Guidelines Office; Arnhem, 2020.
41. The 2017 Update of the German Clinical Guideline on Epidemiology, Diagnostics, Therapy, Prevention, and Management of Uncomplicated Urinary Tract Infections in Adult Patients. Part II: Therapy and Prevention / J. Kranz [et al.] // Urologia Internationalis. 2018. Vol. 100. P. 271-278.
42. Results of a randomized, prospective, double-dummy, double-blind trial to compare efficacy and safety of a herbal combination containing Tropaeoli majoris herba and Armoraciae rusticanae radix with co-trimoxazole in patients with acute and uncomplicated cystitis / R. Stange [et al.] // Research and Reports in Urology. 2017. Vol. 9. P. 43-50.
43. Prevention and treatment of uncomplicated lower urinary tract infections in the era of increasing antimicrobial resistance -non-antibiotic approaches: a systemic review / S. Wawrysiuk,
K. Naber, T. Rechberger, P. Miotla // Archives of Gynecology and Obstetrics. 2019. Vol. 300. P 821-828.
44. Naber K.G. Efficacy and safety of the phytotherapeutic drug Canephron® N in prevention and treatment of urogenital and gestational disease: Review of clinical experience in Eastern Europe and Central Asia // Research and Reports in Urology. 2013. Vol. 5. P 39-46.
45. Brenneis C., Kunstle G., Haunschild J. Spasmolytic activity of Canephron N on the contractility of rat and human isolated urinary bladder; Proceedings of the 13th Congress of the International Society for Ethnopharmacology; Graz, Austria. 2-6 September 2012.
46. Experimental diuretic effects of Rosmarinus officinalis and Centaurium erythraea / M. Haloui, L. Louedec, J.-B. Michel,
B. Lyoussi II Journal of Ethnopharmacology. 2000. Vol. 71. P 465-472.
47. Canephron® N alleviates pain in experimental cystitis and inhibits reactive oxygen/nitrogen species as well as microsomal prostaglandin E2 synthase-1 I B. Nausch [et al.] II Der Urol. 2015. Vol. 54. P 28.
48. Kunstle G., Brenneis C., Haunschild J. 671 Efficacy of Canephron® N against bacterial adhesion, inflammation and bladder hyperactivity II European Urology Supplements. 2013. Vol. 12. P e671.
49. The standardized herbal combination BNO 2103 contained in Canephron® N alleviates inflammatory pain in experimental cystitis and prostatitis I B. Nausch [et al.] II Phytomedicine. 2019. Vol. 60. P 152987.
50. Davidov M.I., Bunova N.E. Comparative assessment of Canephron® N and ciprofloxacin as monotherapy of acute uncom-plicated cystitis in women II Urologiia. 2018. Vol. 4. P 24-32.
51. Davidov M.I., Voitko D.A., Bunova N.E. Treatment of acute uncomplicated cystitis in women with antibiotic allergy or intolerance II Urologiia. 2019. Vol. 5. P. 64-71.
52. Non-antibiotic herbal therapy (BNO 1045) versus antibiotic therapy (fosfomycin trometamol) for the treatment of acute lower uncomplicated urinary tract infections in women: a double-blind, parallel-group, randomized, multicentre, non-inferiority phase III trial I F.M. Wagenlehner [et al.] II Urologia Internationalis. 2018. Vol. 101. P. 327-336.
53. Treatment of urinary tract infections with Canephron® in Germany: a retrospective database analysis I M. Holler [et al.] II Antibiotics (Basel). 2021. Vol. 10, No. 6. P. 685.
54. Sabadash M., Shulyak A. Canephron® N in the treatment of recurrent cystitis in women of child-bearing age: a randomised controlled study II Clinical Phytoscience. 2017. Vol. 3. P. 9.
55. Evaluation of experience with a combination phytotherapeutic drug in pregnant women (a multicenter retrospective observational study) I V.N. Serov [et al.] II Obstetrics & Gynecology. 2013. Vol. 9. P 105-112.
56. A 12-month comparative study of Canephron® N administration in the treatment of pa-tients with the urinary tract infection I I.O. Dudar [et al.] II Zdorovie Muzhchiny 2010. Vol. 3. P 85-90.
57. Ordzhonikidze N.V., Yemelyanova A.I., Petrova S.B. Complication prevention and treatment in pregnants and puerperants with urinary tract diseases II Obstetrics & Gynecology. 2009. Vol. 6. P. 41-45.
58. Perepanova T.S., Khazan P.L. Phytopreparation Canephron® N in the treatment and prophylaxis of urinary tract infections II Vrachebnoye Soslovie. 2005. Vol. 5. P. 44-46.
59. An open label, non-controlled, multicentre, interventional trial to investigate the safety and efficacy of Canephron® N in the management of uncomplicated urinary tract infections (uUTIs) I D. Ivanov [et al.] II Clinical Phytoscience. 2015. Vol. 1. P. 7.
60. How the microbiome is influenced by the therapy of urological diseases: Standard versus alternative approaches I K.G. Naber [et al.] II Clinical Phytoscience. 2017. Vol. 3. P. 8.
61. Is preoperative assessment and treatment of asymptomatic bacteriuria necessary for reducing the risk of postoperative symptomatic urinary tract infections after urologic surgical procedures? I T. Cai [et al.] II Urology. 2017. Vol. 99. P. 100-105.
62. Wullt B., Svanborg C. Deliberate Establishment of asymptomatic bacteriuria—a novel strategy to prevent recurrent UTI II Pathogens. 2016. Vol. 5. P. 52.
63. Ibuprofen versus fosfomycin for uncomplicated urinary tract infection in women: randomised controlled trial I I. Gagyor [et al.] II BMJ. 2015. Vol. 351. P h6544.
64. Recurrent urinary tract infections and complications after symptomatic versus antibiotic treatment: follow-up of a randomised controlled trial I J. Bleidorn [et al.] II German Medical Science. 2016. Vol. 14.
65. Symptomatic treatment of uncomplicated lower urinary tract infections in the ambulatory setting: randomised, double blind trial I A. Kronenberg [et al.] II BMJ. 2017. Vol. 359. P. j4784.
66. Иванова Д.Д., Кушниренко С.В. Оценка лечебного и профилактического потенциала препарата Канефрон Н при острых циститах у детей: результаты клинического исследования II Почки. 2013. № 3(5). С. 9-13.
67. Еремеева А.В. Оценка клинической эффективности различных схем противорецидивной терапии у детей с пиелонефритом II Педиатрия. Consilium Medicum. 2020. № 2.
С. 62-66.
68. Эрман М.В. Фитотерапия в лечении инфекции мочевой системы у детей II Эффективная фармакотерапия. 2014. № 16. С. 18-22.
69. A non-interventional, prospective, multicenter study for evaluation of the use of the herbal medicinal product Canephron® N in the pediatric outpatient population in Russia I V Dlin [et al.] II Clinical Phytoscience. 2018. Vol. 4. P. 31.
70. Каладзе Н.Н., Слободян Е.И., Патогенетически ориентированный метод оптимизации восстановительного лечения детей, больных хроническим пиелонефритом II Современная педиатрия. 2012. № 2(42). С. 1-6.
71. Летифов Г.М. Место Канефрона Н в комплексной терапии инфекции мочевой системы и дисметаболических нефропатий у детей II Практика педиатра. 2017. Март-апрель. С. 36-40.

