Вспомогательная иммунотерапия у пациентов с иммунодефицитом и часто болеющих детей
СтатьиОпубликовано в журнале:
«СПРАВОЧНИК ПОЛИКЛИНИЧЕСКОГО ВРАЧА»; № 9; 2010; стр. 7-14.
М.Ю.Елисеева3, В.Н.Царев1, К.Н.Масихи5, Л.В.Осидак4, И.Ф.Баринский2, Т.В.Царева1, ОАМынбаев1
1Московский государственный медико-стоматологический университет;
2НИИ вирусологии им. Д.И.Ивановского РАМН;
3Институт репродуктивных технологий AltraVita, Москва;
4НИИ гриппа РАМН, Санкт-Петербург;
5Институт Роберта Коха, Берлин, Германия
Актуальность проблемы
Антибактериальные препараты существенно снизили заболеваемость и смертность от инфекционных заболеваний и тем самым сохранили и продолжают спасать жизнь и здоровье миллионов людей. Однако применение антибиотиков и других антибактериальных препаратов при вирусных инфекциях бесполезно, а порой опасно и вредно. Беспорядочный и бесконтрольный прием антибиотиков наряду с осложнениями, побочными и токсическими эффектами, способствует формированию антибиотико-устойчивых штаммов возбудителей инфекций.
Профилактика и лечение заболеваний дыхательных путей, включая острые респираторные вирусные инфекции (ОРВИ) и сезонный грипп, у контингента «проблемных» пациентов с иммунодефицитом, особенно часто болеющих детей (ЧБД), является актуальной проблемой современного здравоохранения. Это обусловлено наличием противопоказаний к вакцинации у таких лиц, отсутствием адекватных лечебных противовирусных средств и изменчивостью вирусов. В большинстве случаев этиологическими факторами заболеваний дыхательных путей являются вирусные инфекции и миксинфекция. Так, по данным литературы, более 200 разных представителей, включая 4 семейства РНК-содержащих вирусов (ортомиксо-, парамиксо-, короно- и пикорновирусы) и 2 семейства ДНК-содержащих вирусов (адено- и герпесвирусы), могут вызывать острые заболевания дыхательных путей (Е.И.Давидовская, 2006).
При этом спектр противовирусных средств для эффективного лечения заболеваний дыхательных путей ограничен, особенно осложненных форм ОРВИ и гриппа, которые сопровождаются тяжелыми последствиями для контингента пациентов с иммунодефицитом. Более того, на фоне ОРВИ и сезонного гриппа часто развиваются воспалительные заболевания верхних дыхательных путей с формированием вторичного иммунодефицита, поэтому отмечается повышенный интерес практических врачей к иммуномодулирующим средствам. Многочисленные публикации по данной проблеме свидетельствуют о широком применении разных иммуномодуляторов при ОРВИ, гриппе и заболеваниях верхних дыхательных путей как у взрослых, так и у детей, что представлено в Кохрановском обзоре (Del-Rio-Navarro и соавт., 2006) и других публикациях.
Другой аспект проблемы иммунотерапии связан с агрессивной маркетинговой технологией фармацевтических компаний. На лекарственном рынке стран СНГ циркулируют многочисленные препараты, рекомендуемые для повышения иммунитета, порой сомнительного происхождения и с отсутствием клинически доказанных результатов их эффективности. Это затрудняет практическим врачам выбор оптимального иммуностимулятора для лечения и профилактики вирусных инфекций у пациентов с нарушениями в иммунной системе.
Известно, что пурины играют важную роль в поддержании гомеостаза в организме. С одной стороны, нарушение метаболизма пуринов, в частности дефицит фермента аденозина диаминазы, сопровождается патологией лимфоцитов, продуцирующих антитела, что приводит к тяжелому наследственному аутосомально-рессесивному иммунодефициту. С другой стороны, избыток мочевой кислоты у новорожденных приводит к тяжелым психоневрологическим нарушениям (аутизму), а у взрослых - к подагре и ревматоидному артриту. Инозин (Инозин F, Рибоксин) - лекарственный дериват пуринов, обладая противовоспалительным, анаболическим, метаболическим, антигипоксическим и антиаритмическим свойствами, принимает участие в регуляции многих физиологических процессов в организме. Инозин Пронабекс (ИП) - синтетический аналог инозина, получен путем соединения инозина с вспомогательной молекулой, которая повышает его доступность для лимфоцитов и таким образом усиливает его иммуностимулирующие свойства. За более чем 38-летний период применения лекарственных аналогов ИП не зарегистрированы случаи серьезных побочных эффектов. Так, по данным Newport Pharmaceuticals Ltd, между 1971 и 2005 г. около 1,25 млрд таблеток было назначено 20 млн пациентам в среднем по 3 г в день в течение 10 дней. При этом менее 1500 случаев побочных эффектов было зарегистрировано. Основными побочными эффектами при приеме ИП являются транзиторное повышение концентрации мочевой кислоты (МК) в сыворотке и в моче, а другие симптомы, такие как нарушение функции печени (повышение концентрации АЛТ/ АСТ), зуд, сыпь, тошнота, дискомфорт в желудочно-кишечном тракте (ЖКТ), недомогание, головокружение, головные боли и артралгия, регистрировались реже. Существуют многочисленные данные клинических исследований, свидетельствующие об эффективности ИП как иммуностимулирующего и противовирусного агента у «проблемных» или «трудных» пациентов с иммунодефицитом. Это, по-видимому, связано с отсутствием у ИП выраженного плейотропного эффекта, характерного для цитокинов (интерферонов), что обусловливает непредсказуемость фармакологического поведения цитокинов. Более того, применение экзогенных цитокинов лимитировано у контингента «проблемных» пациентов, особенно ЧБД, со сниженным иммунитетом в связи с отсутствием соответствующих эффекторных клеток или наличием патогномоничных факторов заболевания, препятствующих активации лимфоцитов. Короткий период полураспада экзогенных цитокинов и необходимость применения таких цитокинов в высоких дозах для достижения терапевтического эффекта стимулирует исследователей к поиску наиболее приемлемого и адекватного иммунопотенциатора, принимающего участие в регуляции иммунных процессов в организме, но не обладающего побочными эффектами цитокинов. К таким иммуностимуляторам можно отнести ИП, предшественником которого являются природные пурины. Представлен систематический обзор и метаанализ литературы касательно применения ИП у контингента пациентов с нарушениями в иммунной системе и ЧБД.
Методы исследования
Информационный поиск источников, опубликованных с 1980 по 2010 г., был проведен в электронных англо- и русскоязычных базах данных. Кроме того, некоторые данные мы получили от авторов ранее опубликованных работ и с сайта производителя препарата.
Таблица 1.
Суточная доза, способы и цель назначения ИП у контингента пациентов с вторичным иммунодефицитом и добровольцев
| Источники | Цель | Контингент больных и добровольцев | Возраст | Режим назначения | |
| Суточная доза | Сроки | ||||
| Абелевич и соавт., 2008 3-7 лет | Лечение аллергических заболеваний на фоне ОРВИ | Дети от 3 до 7 лет с повышенной заболеваемостью ОРВИ, сочетанием вирусных и бактериальных инфекций, тяжелыми затяжными бактериальными инфекциями на фоне нарушения иммунного статуса и сочетанных форм аллергических заболеваний кожи и дыхательных путей | 3-7 лет | 0,5 г | 15 дней |
| Буцель, 2007 | Лечение ангины на фоне ОРВИ | Дети в возрасте 5-16 лет и взрослые 20-35 лет с ангиной на фоне ОРВИ | 5-16 лет | 50 мг/кг | В течение 5-7 дней |
| 20-35 лет | 3-4 г | ||||
| Крыжановский, 2006 | Лечение ОРВИ | Контингенту пациентов с нарушениями в иммунной системе ИП был применен после противогриппозной вакцинации на фоне базисной терапии, в качестве вспомогательной терапии - больным ОРВИ | Не указан | 50 мг/кг | Ежедневно или 3 раза в неделю в течение 8-9 нед. |
| Профилактика ОРВИ | Часто и длительно болеющим пациентам ИП назначали в профилактическом режиме | 3 г | В течение 5-7 дней | ||
| Осидак и соавт., 2008 | Лечение ОРВИ и профилактика повторных эпизодов | Дети в возрасте от 1 года до 18 лет, включая контингент ЧБД, получавшие ИП с целью лечения и последующей профилактики повторных эпизодов ОРВИ | Дети (от 1 года до 18 лет) | 50 мг/кг | от 5-10 дней |
| Парамонова, Волкова, 2006 | Профилактика ОРВИ | Дети в возрасте 4-10 лет. Часть из них имели контакт с больными ОРВИ | 4-10 лет | 50 мг/кг | 3 раза в неделю в течение 4 нед |
| Профилактика ОРВИ* | 100 мг/кг | В течение 5 дней | |||
| Newport Pharm Ltd | Лечение хронической РВИ | Взрослые с хроническими инфекционными заболеваниями респираторной и мочевыделительной систем | 80,0±6,9 года | 4 г | В течение 3 мес |
| Профилактика и лечение хронической РВИ | Дети с хроническими респираторными инфекционными заболеваниями на фоне ослабленной иммунной системы | Дети | 50-100 мг/кг | В течение 7-15 дней | |
| Golebiowska-Wawrzyniak и соавт., 2005 | Профилактика РВИ | Дети в возрасте 3-15 лет с РВИ на фоне клеточного иммунодефицита | 3-15 лет | 50 мг/кг | В течение 10 дней 3 курса ежемесячно |
| Litzman и соавт., 1999 | Профилактика ОРВИ | Дети в возрасте 4-8 лет с респираторными рецидивирующими вирусными инфекциями находились под наблюдением родителей, которые регистрировали по протоколу симптомов и признаков ОРВИ | 4-8 лет | 50 мг/кг | Ежедневно в течение 6 нед, затем дважды в неделю в течение следующих 6 нед |
| Longley и соавт., 1973 | Профилактика гриппа | Здоровые взрослые добровольцы, мужчины и женщины | Не указан Взрослые | 2,5 г | В течение 10 дней |
| Pachuta и соавт, 1974 | Профилактика риновирусной инфекции | Здоровые взрослые добровольцы, мужчины-заключенные | 21-48 лет | 6 г | В течение 10 дней |
При определении критериев отбора мы исходили из того, что применялись аналоги ИП (Изопринозин и Гроприносин) при заболеваниях дыхательных путей (ОРВИ и грипп) у контингента пациентов с нарушениями в иммунной системе. При этом режим приема препарата не учитывался. В данный обзор были включены доступные источники, в которых оценивалась эффективность вспомогательной иммунотерапии с применением аналогов ИП в профилактике и лечении респираторных инфекционных заболеваний, включая ОРВИ и сезонный грипп, у контингента пациентов с нарушениями в иммунной системе, особенно ЧБД, а также испытание ИП у добровольцев.
С тем чтобы определить пригодность результатов, выбранных нами источников для метаанализа, изучали дизайн исследования и качество изложения результатов исследования в этих работах (табл. 1). Исходя из качества изложения результатов исследования, для метаанализа были использованы результаты 6 источников (Парамонова, Волкова, 2006; Осидак и соавт, 2008; Longley и соавт., 1973; Pachuta и соавт., 1974; Litzman и соавт., 1999; Golebiowska-Wawrzyniak и соавт., 2005). Вначале были обобщены данные лечебно-профилактического режима применения ИП (Изопринозина) у детей (Парамонова, Волкова, 2006; Осидак и соавт., 2008), затем у взрослых добровольцев, инфицированных вирусом гриппа и риновируса (Longley и соавт., 1973; Pachuta и соавт., 1974).
Результаты исследования
Метаанализ результатов лечебно-профилактического применения ИП при респираторных инфекциях
Метаанализ эффективности применения ИП в лечебно-профилактическом режиме по частоте и характеру эпизодов ОРВИ по сравнению с показателями контрольной группы и/или до приема ИП был проведен по результатам 5 работ. Обобщенные результаты этих источников свидетельствуют, что частота и продолжительность эпизодов ОРВИ значительно сокращаются у детей после профилактического приема ИП по сравнению с аналогичными показателями контроля, а также показателями до приема ИП (Изопринозина) (Парамонова, Волкова, 2006; Осидак и соавт., 2008; Golebiowska-Wawrzyniak и соавт., 2005; Newport Pharm Ltd) и только результаты одной работы не подтвердили лечебно-профилактическую эффективность ИП при рецидивирующих респираторных инфекциях (Litzman и соавт., 1999).
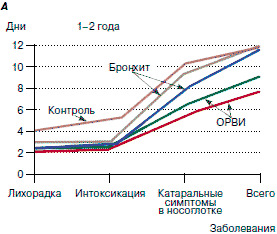
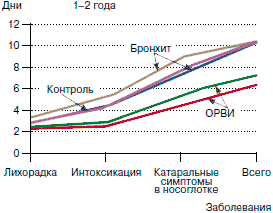
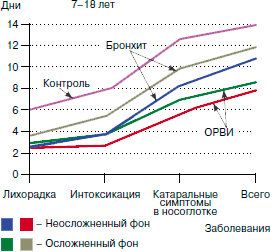
Согласно данным Осидак и соавт. (2008 г.) применение ИП (Изопринозина) у детей, включая лиц с неблагополучным преморбидным фоном, способствовало сокращению продолжительности практически всех симптомов заболевания, в том числе температурной реакции, интоксикации и катаральных явлений в носоглотке (рис. 1, А). При этом продолжительность эпизодов ОРВИ не превышала 6-8 дней у 64-70% детей, принимавших ИП (Изопринозин), что существенно превосходит аналогичный показатель у детей контрольной группы (4-25%).
Рис. 1. Лечебно-профилактическая эффективность ИП у детей: А - согласно данным Осидак и соавт. (2008 г.).
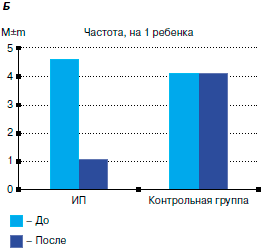
В аналогичной по принципу работе с меньшим количеством детей Парамонова и Волкова (2006 г.) также показали профилактическую эффективность ИП в отношении снижения частоты и продолжительности эпизодов ОРВИ (см. рис. 1, Б). После применения ИП число детей, перенесших первичные и повторные эпизоды ОРВИ, уменьшилось в 3,5 раза по сравнению с аналогичным показателем контрольной группы.
Рис. 1. Лечебно-профилактическая эффективность ИП у детей: Б - Парамоновой, Волковой (2006 г.).
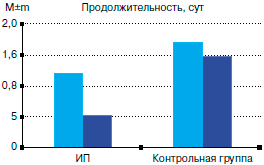
Парамонова и Волкова (2006 г.) считают, что подтверждением лечебно-профилактической эффективности ИП является сравнительно легкое течение ОРВИ, снижение в 3-4 раза частоты развития таких осложнений, как острый бронхит, пневмония и отит. Проводив сравнительные клинические и углубленные иммунологические исследования у детей с рецидивирующими респираторными инфекциями, получившими лечение ИП, Golebiowska-Wawrzyniak и соавт. (2005 г.) подтверждают выводы российских ученых, такие как сокращение частоты эпизодов рецидивов респираторных инфекций на 81,2%, или в 5,31 раза, по сравнению с показателями до применения ИП. При этом степень тяжести ОРВИ снизилась на 60,3%, или в 2,52 раза, продолжительность эпизодов ОРВИ сократилась на 88,2%, или в 8,44 раза, и общий индекс клинических симптомов снизился на 72,5%, или в 3,64 раза, по сравнению с аналогичными показателями до применения ИП. В результате применения ИП Golebiowska-Wawrzyniak и соавт. (2005 г.) уменьшили применение антибиотиков у детей на 93,5%, или в 15,3 раза, а также других неантибактериальных препаратов на 78,3%, или в 4,51 раза. Однако в плацебо-контролируемой работе, выполненной с целью профилактики острой рецидивирующей респираторной инфекции у детей 4-8 лет, Litzman и соавт. (1999 г.) не обнаружили существенного различия между ИП и плацебо-контролем. Эффективность ИП оценивалась в плане частоты и продолжительности эпизодов, по тяжести симптомов ОРВИ (по продолжительности кашля и повышения температуры тела), а также по развитию фарингитов, ринитов и других осложнений. Тем не менее, Litzman и соавт. (1999 г.) отмечают повышение числа CD3+, CD4+ и CD8+-клеток, а также Т-лимфоцитов в крови в период лечения с ИП.
Представляют также интерес результаты лечения хронических инфекционных заболеваний респираторного и мочеполового трактов у больных с ослабленной иммунной системой (Newport Pharm Ltd). При этом у 100 больных преклонного возраста ИП назначали по 4 г/сут в течение 3 мес, а 850 детям ИП назначали по 50-100 мг/кг в течение 7-15 дней. Оценка эффективности лечения проводилась по клиническому улучшению общего состояния больных, снижению симптомов заболевания (кашель, насморк, головные и мышечные боли), по частоте проявления желудочно-кишечных расстройств, по степени редукции продолжительности проявления клинических симптомов и снижению частоты рецидивов заболевания, а также содержания иммуноглобулинов (Ig): IgG, IgA и IgM.
Анализ клинических данных свидетельствует о существенном снижении продолжительности проявления симптомов в среднем от 5,44 сут у больных, получивших плацебо, до 2,58 сут после приема ИП. Частота рецидивов заболевания после приема ИП составила 23,0%, а после плацебо - 40,0%. При этом применение ИП способствовало существенному повышению концентрации Ig - IgG, IgA и IgM у детей с ослабленной иммунной системой.
Обобщенный анализ результатов применения ИП у взрослых добровольцев, искусственно инфицированных вирусом гриппа и риновирусом
Результаты последующих двух источников представляют особый интерес (табл. 2), поскольку Longley и соавт. (1973 г.) и Pachuta и соавт. (1974 г.) проводили испытание на небольшом контингенте добровольцев (30 и 37 индивидов соответственно), причем контингентом исследования Pachuta и соавт. (1974 г.) являлись заключенные одного пола. После рандомизации добровольцы получали либо ИП, либо плацебо. Далее Longley и соавт. (1973 г.) инфицировали добровольцев вирусом гриппа A(H3N2)/HongKong, а Pachuta и соавт. (1974 г.) - риновирусом типа 32 или 44.
Согласно данным табл. 2, обобщенный анализ результатов свидетельствует, что некоторый положительный клинический лечебно-профилактический эффект ИП был отмечен у добровольцев после инокуляции риновирусной инфекции (p=0,13 и 0,15). Это может быть связано с тем, что популяция в данной работе являлась совершенно однородной - мужчины-заключенные. По нашему мнению, для получения клинических результатов для полноценной статистической обработки количество добровольцев было недостаточным в обеих работах. Тем не менее, тяжесть лихорадки (температурная реакция) и проявления гриппозного состояния у добровольцев, получивших плацебо-профилактику гриппа, оказалась немного выше по сравнению с аналогичными показателями ИП, но различие не было существенным. При этом динамика выделения вируса и количество изолятов оказались существенно низкими после ИП по сравнению с плацебо, несмотря на небольшое расхождение цифровых показателей (0<0,05).
Таблица 2.
Эффективность применения ИП для профилактики искусственно индуцированной инфекции гриппа и риновируса у взрослых добровольцев
| Источник | Частота и продолжительность проявления гриппа и риновируса, m±SEM и 95% ДИ нижний - верхний | ||||||
| Частота | Продолжительность, сут | ||||||
| ИП | Плацебо | Р | ИП | Плацебо | Р | ||
| Longley и соавт., 1973 | см. рис. 4, 5* | =0,1 | см. рис. 4, 5* | >0,05 | |||
| Pachuta и соавт., 1974 | m±SEM | 0,37±0,11 | 0,61±0,12 | =0,15 | 0,63±0,23 | 1,17±0,26 | =0,13 |
| 95% ДИ | 0,13-0,61 | 0,36-0,86 | 0,14-1,12 | 0,62-1,71 | |||
Следует отметить, что применение ИП способствовало 24-кратному повышению средне-геометрической величины образования сывороточных вируснейтрализующих антител, что может предохранить этих индивидов от рецидивов или повторного инфицирования гриппом более надежно.
Анализ результатов Pachuta и соавт. (1974 г.) свидетельствует, что применение ИП привело к снижению как частоты (0=0,15), так и тяжести (p=0,13) проявления риновирусной инфекции, обусловленной штаммами типа 32 и 44 (рис. 2, А). При этом аналогичные тенденции прослеживаются и в динамике по отдельным данным по каждому типу риновируса 32 и 44 (см. рис. 2, Б).
Рис. 2. Частота и тяжесть проявления риновирусной инфекции в зависимости от использования ИП и плацебо: А - суммированные и Б - индивидуальные показатели, согласно данным Pachuta и соавт. (1974 г.).
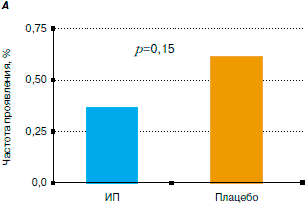
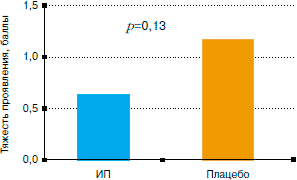
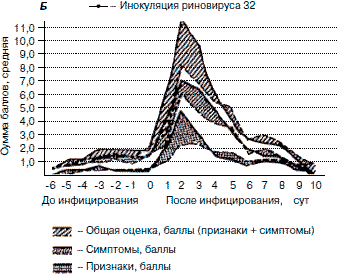
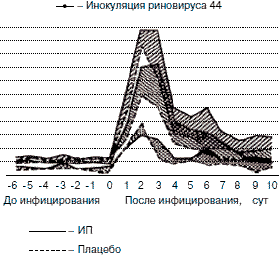
Динамика образования нейтрализующих антител после инокуляции возбудителей риновирусной инфекции в зависимости от использования ИП и плацебо также свидетельствует о некотором повышении титра антител у добровольцев, получивших ИП, по сравнению с аналогичным показателем плацебо-контроля.
Обобщенный анализ клинико-лабораторных данных, полученных у здоровых добровольцев, свидетельствует, что прием ИП индивидами, инфицированными вирусом гриппа, способствовал существенному снижению выделения вируса, количества его изолятов, а также значительному росту титра вируснейтрализующих антител в сыворотке крови по сравнению с аналогичными показателями плацебо-контроля. При этом после ИП отмечаются также снижение температурной реакции (0=0,1) и редукция суммарных баллов общей заболеваемости по сравнению с аналогичными показателями плацебо-контроля (0=0,1), но они не имели существенного различия (0>0,05). Это дало Longley и соавт. (1973 г.) обоснование для опровержения гипотезы о наличии противогриппозного свойства ИП в отношении использованного им штамма вируса A(H3N2)/Hong Kong, несмотря на существенную редукцию выделения вируса.
О наличии положительных эффектов ИП при риновирусной инфекции, индуцированной типами 32 и 44, свидетельствует анализ результатов, полученных у добровольцев, инфицированных риновирусом. Так, аналогично результатам предыдущей работы Pachuta и соавт. (1974 г.) также обнаружили значительное снижение выделения вируса, количества его изолятов, а также существенный рост титра вируснейтрализующих антител в сыворотке крови по сравнению с аналогичными показателями плацебо-контроля. При этом частота и тяжесть проявления риновирусной инфекции были также менее выраженными после применения ИП по сравнению с аналогичными показателями плацебо-контроля. Однако отсутствие существенного различия в показателях не позволило Pachuta и соавт. (1974 г.) подтвердить гипотезу, хотя они заключили, что ИП может снизить проявления риновирусной инфекции.
Обобщенный анализ побочных эффектов применения ИП
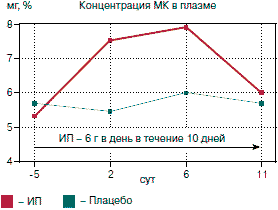
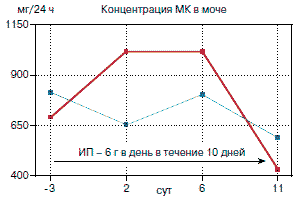
Анализ свидетельствует, что в 2 работах побочные эффекты отсутствовали (Парамонова, Волкова, 2006; Абелевич и соавт., 2008), а в 4 источниках информация про нежелательные реакции вообще отсутствует (Крыжановский, 2006; Буцель, 2007; Golebiowska-Wawrzyniak и соавт., 2005; Newport Pharm Ltd). В других 4 исследованиях авторы детально указали спектр и характер осложнений, связанных с приемом ИП (Осидак и соавт, 2008; Longley и соавт., 1973; Pachuta и соавт., 1974; Litzman и соавт., 1999). При этом, согласно данным Осидак и соавт. (2008 г.) развитие нежелательных явлений, таких как тошнота, боль в эпигастрии, сухость кожи, аллергическая реакция, сонливость и повышение концентрации трансаминаз печени (АЛТ), в ответ на применение ИП было нечастым и не сопровождалось отменой препарата. Litzman и соавт. (1999 г.) отмечает позитивный противонуклеарный титр, равный 1:40, при отсутствии клинических симптомов и других лабораторных изменений, включая изменение концентрации МК, печеночных проб, считающихся побочными эффектами ИП. Longley и соавт. (1973 г.) обнаружили повышения концентрации МК на 6-й день терапии с ИП, которая возросла с 5,7 до 7,9. Затем при повторном исследовании на 10-й день терапии отмечено снижение концентрации МК до базального уровня (рис. 3).
Рис. 3. Динамика содержания МК в плазме и в моче у добровольцев на фоне приема ИП в суточной дозе по 6 г в течение 10 дней.
Обсуждение
Механизм противовирусной активности ИП недостаточно ясен, но существуют множественные трактовки. Так, например, ИП, активируя функцию депрессивных лимфоцитов, подавляет синтез вирусной РНК, что сопровождается ингибированием роста вируса. Считается, что ИП, с одной стороны, стимулируя дифференцировку Т-лимфоцитов в цитотоксические Т-клетки и Т-хелперы, а также повышая продукцию лимфокинов, способствует выработке интерлейкинов (ИЛ) ИЛ-1, ИЛ-2 и интерферона-g и функциональную активность NK-клеток. ИП также потенцирует морфофункциональную состоятельность нейтрофилов и моноцитов, усиливая хемотаксис макрофагов и фагоцитоз, и таким образом нормализует клеточный иммунитет. С другой стороны, стимулируя дифференцировку В-лимфоцитов в плазматические клетки и повышая продукцию антител, нормализует гуморальный иммунитет. При этом происходит повышение концентрации IgG, IgA и IgM, а также поверхностных маркеров комплемента и вируснейтрализующих антител, что было продемонстрировано в проанализированных нами источниках. Согласно данным литературы вспомогательная иммунотерапия с применением ИП приводит к морфофункциональному восстановлению и активации клеточного звена иммунной системы. Так, например, результаты применения ИП для лечения хронических инфекционных заболеваний респираторного тракта, представленные компанией Newport Pharm Ltd, демонстрируют повышение концентрации IgG, IgA и IgM под воздействием ИП у детей с ослабленной иммунной системой.
Аналогичные результаты, свидетельствующие об улучшении показателей иммунограммы у детей с нарушениями в иммунной системе, продемонстрировали Абелевич и соавт. (2008 г.), которые изучали показатели клеточного и гуморального иммунитета до лечения с ИП, затем спустя 2 нед и 2 мес после лечения. При этом на раннем этапе отмечена активация В-клеточного звена иммунитета с увеличением IgA и IgM, а также возрастание концентрации CD8+-лимфоцитов и HLA-DR+-клеток, а на позднем этапе - переключение синтеза Ig с IgM на IgG, нормализация и/или повышения концентрации HLA-DR+-клеток и снижение количества CD3+-клеток. Такие же изменения в иммунологическом статусе у детей с рецидивирующими респираторными инфекциями, получившие лечение ИП, согласно данным Golebiowska-Wawrzyniak и соавт. (2005 г.) привели к повышению эффективности лечения детей с неблагоприятным преморбидным фоном и рецидивирующими респираторными инфекциями.
В ряде работ показана лечебно-профилактическая эффективность ИП при сочетанных заболеваниях респираторного тракта. Так, в наблюдениях Крыжановского (2006 г.) ИП был использован у 12 индивидов (часто и длительно болеющих) в качестве профилактики ОРВИ по 50 мг в день в течение 8-9 нед и у 14 больных с хронической болезнью легких для лечения ОРВИ по 3 г в день в течение 5-7 дней.
Из выводов автора следуют, что применение ИП в профилактическом режиме способствует снижению частоты развития и тяжести течения ОРВИ, продлевает период ремиссии. В лечебном режиме ИП «значительно сокращает длительность таких клинических проявлений, как боль в горле, насморк, кашель, способствует быстрому снижению температуры, ликвидации симптомов интоксикации, ускоряет обратное развитие воспалительных процессов, предотвращает осложнения». В опыте использования ИП Буцель (2007 г.) назначал ИП в суточной дозе детям по 50 мг/кг и взрослым по 3-4 г в течение 5-7 дней, что способствовало значительному уменьшению интенсивности головных болей, «сглаженному» проявлению ринофарингита и сокращению лихорадочного периода. В дальнейшем лечебно-профилактическая эффективность ИП (Изопринозин) была продемонстрирована путем изучения частоты эпизодов сезонного гриппа и ОРВИ в широкомасштабном многоцентровом постмаркетинговом исследовании с участием 121 врача в 13 городах Российской Федерации (Осидак и соавт., 2008), а также в открытой контролируемой работе с меньшим количеством детей (Парамонова, Волкова, 2006). Однако Litzman и соавт. (1999 г.), проводив плацебо-контролируемое исследование у детей 4-8 лет, с целью профилактики острой рецидивирующей респираторной инфекции, не обнаружили существенного различия между ИП и плацебо-контролем. Тем не менее, Litzman и соавт. (1999 г.) отмечают повышение числа CD3+, CD4+ и СD8+-клеток, а также Т-лимфоцитов в крови после лечения с ИП. Следует отметить, что клинические результаты Litzman и соавт. (1999 г.) получены на основе дневников родителей, которые регистрировали симптомы и клинические признаки ОРВИ. При этом некоторые критерии включения являются спорными. Так, например, новым эпизодом ОРВИ считали появление не менее 2 симптомов или признаков - кашель, ринит, боль в горле, в ухе, повышение температуры тела до 38,0°С и более продолжительностью не менее 4 дней при регистрации 4-дневного бессимптомного периода после перенесенного ранее эпизода ОРВИ.
Интерпретируя указанные данные, считаем, что клинические результаты профилактической эффективности ИП, продемонстрированные клиницистами (Крыжановский, 2006; Парамонова, Волкова, 2006; Осидак и соавт, 2008; Go ebiowska-Wawrzyniak и соавт., 2005), по-видимому, являются следствием повышения концентрации вируснейтрализующих антител под воздействием ИП на иммунную систему. При этом следует также отметить, что применение ИП у добровольцев, инфицированных вирусом гриппа и риновирусом, способствовало существенному снижению выделения вируса и повышению концентрации вируснейтрализующих антител (Longley и соавт. 1973; Pachuta и соавт., 1974). Это сопровождалось снижением тяжести и продолжительности симптомов манифестации искусственно инициированного инфекционного процесса по сравнению с аналогичными показателями плацебо-контроля (0=0,1).
Представляя обобщенный анализ результатов обследования и лечения 3843 индивидов из 10 источников, выполненных с целью оценки лечебно-профилактической эффективности ИП при ОРВИ (гриппе и риновирусе), считаем, что, несмотря на разнообразие методологических подходов, дизайна работ и контингента больных, с точки зрения доказательной медицины систематический подход с элементами метаанализа в целом свидетельствует о наличии позитивного лечебно-профилактического эффекта вспомогательной иммунотерапии ИП при ОРВИ, особенно у контингента ЧБД. Следует обратить внимание на то, что наряду с позитивными эффектами при приеме ИП происходит повышение концентрации МК в организме. При этом уровень содержания МК в плазме и моче зависит от дозы препарата и длительности его приема. Концентрация МК снижается сразу после прекращения приема ИП. На наш взгляд, такой побочный эффект ИП можно избежать путем чередования высокой дозы с низкой дозой двумя способами. Принцип 1-й схемы заключается в назначении ИП в нечетные дни по 3-4 г в день, а в четные - по 1-2 г в день. При этом продолжительность лечения выбирает врач в зависимости от индивидуальной особенности иммунной системы больного. Принцип 2-й схемы заключается в назначении ИП по 3-4 г в день в течение 5 дней и после 2-дневного перерыва по 1-2 г в день в течение следующих 5 дней. Мы имеем опыт лечения контингента больных с генитальными кондиломами, оролабиальным и генитальным герпесом, а также рецидивирующей угревой болезнью (акне вульгарис) по 2-й схеме. При этом курс лечения состоит в приеме ИП по 3-4 г в день в 2 приема с промежутком 2-3 ч в утренние время сутки в течение 5 дней. Затем после 2-дневного перерыва пациентки принимали ИП по 1-2 г в день по аналогичной схеме. Доза корректировалась индивидуально в зависимости от показаний и массы тела пациенток. Результаты вполне обнадеживающие и заключаются в исчезновении генитальных кондилом и акне вульгарис, а при рецидивирующем герпесе - в ускорении сроков заживления герпетической язвы без применения противогерпетических таблеток, только обработкой кремом Зовиракс на фоне приема ИП. Более того, отмечается удлинение периода ремиссии герпетической инфекции. Причем после приема ИП по указанному режиму приступы рецидивов оролабиального герпеса проходили без образования язв после применения крема Зовиракс и данный лечебный эффект сохранялся в течение 6 мес, пациентки находились под наблюдением.
Известно, что состоятельность иммунной системы определяет риск инфицирования, степень манифестации и исход инфекционных процессов. Соответственно, свойство ИП восстанавливать морфофункциональную потенцию иммунной системы, по-видимому, является ключом его противовирусного механизма действия при вирусных инфекциях, особенно у контингента проблемных пациентов и ЧБД с ослабленной иммунной защитой, о чем свидетельствуют результаты работ, проанализированных в настоящем обзоре.
Заключение
Представлен обобщенный анализ данных из 10 источников литературы, посвященный оценке эффективности вспомогательной иммунотерапии. ИП назначали 2534 пациентам (детям и взрослым) с нарушениями в иммунной системе и рецидивирующими ОРВИ, а также здоровым добровольцам. Эффективность лечебно-профилактической иммунотерапии оценивали, сравнивая с показателями плацебо у 74 и традиционных методов лечения у 275 больных. Результаты данного метаанализа свидетельствуют о значительном снижении частоты новых эпизодов ОРВИ у индивидов после лечебно-профилактического курса с ИП, особенно у контингента с иммунодефицитом и ЧБД, с отягощенным преморбидным фоном. Прослеживается тенденция сокращения длительности и тяжести ОРВИ на фоне лечения с ИП. В проанализированных нами источниках существуют также негативные факторы, снижающие достоверность представленных в них результатов, заключающиеся в разнообразии дизайна и бедности методологических подходов. Из этого следует необходимость проведения рандомизированных плацебо-контролируемых исследований для подтверждения эффективности вспомогательной иммунотерапии с ИП контингента пациентов с иммунодефицитом и рецидивирующими ОРВИ.


