Терапевтическая безопасность препарата Мальтофер
СтатьиПредыдущий раздел | Оглавление | Следующий раздел
4.2. Терапевтическая безопасность препарата Мальтофер®
4.2.1. Перенасыщение железом
Geisser и Muеller (1987) продемонстрировали отсутствие токсичности ГПК, основываясь на том, что активный транспорт железа осуществляется по принципу конкурентного обмена лигандами, уровень которых определяет скорость абсорбции железа. Данный процесс, предположительно происходит вместо пассивной диффузии. Это означает, что в случае насыщения железом, оно не поступает в организм из соединений ГПК. Риск интоксикации свободными ионами железа, проникающими в кровяное русло после насыщения железом транспортной системы, может быть исключен.
Напротив, простые соли железа всасываются даже при нормальном содержании железа или его избытке. Это всасывание путем пассивной диффузии может вызвать интоксикацию железом. Мембранный транспорт ограничивается лишь поверхностью мембраны и градиентом концентрации железа.
Ежегодно в Соединенных Штатах железосодержащие таблетки вызывают примерно 4.000 случайных отравлений. Значительная часть этих отравлений происходит у детей, а показатель смертности, указываемый в бюллетенях, приближается к 85 % (Litovitz с соавторами, 1992).
95% железосодержащих таблеток, продаваемых в США, содержат простые соли железа.
Рисунок 4-14
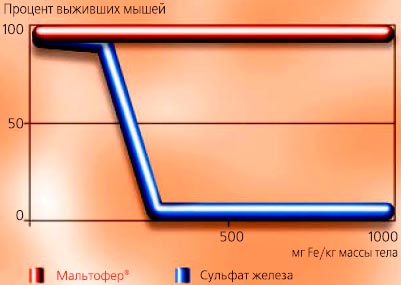
Количество выживших мышей в зависимости от дозы введенного железа. (Jacobs с соавторами, 1979).
В 1995 году Медицинский Бюллетень Федерального Департамента по Препаратам (FDA) утверждал, что количество маленьких детей, случайно проглотивших железосодержащие таблетки, возросло более чем в два раза по сравнению с 1986 годом. С 1986 года, в центры по контролю отравлений было сообщено о более чем 110.000 подобных случаев у детей в возрасте до 6 лет. Большая часть этих детей была госпитализирована, и, по меньшей мере, 33 ребенка погибло. Погибшие дети приняли от 5 до 98 железосодержащих таблеток (FDA, 1995).
4.2.2. Оксидативный стресс
Самая последняя публикация о безопасности ГПК рассматривает влияние на организм оксидативного стресса, инициируемого введением препаратов железа:
Железо должно находится в окисленном трехвалентном состоянии Fe (III) для того, чтобы быть включенным в состав ферритина и трансферрина. Большинство простых солей железа содержат его в двухвалентной форме, и, таким образом, им необходимо быть окисленными прежде, чем железо сможет всосаться и использоваться в организме. Эти окислительные процессы вызывают высвобождение свободных электронов, которые в свою очередь приводят к образованию свободных радикалов. Последние, помимо прочих повреждающих эффектов, активируют перекисное окисление липидов.
Наиболее значимый токсический побочный эффект простых солей железа не наблюдался после применения ГПК, так как ГПК доставляет трехвалентное железо непосредственно к ферритину и трансферрину посредством конкурентного лигандного обмена.
Tuomainen с соавторами (1999)
В условиях двойного слепого исследования в течение 4-х месяцев изучали влияние простых солей железа, ГПК и плацебо на восприимчивость липопротеинов плазмы к окислению у 48 доноров крови, имевших уменьшенные запасы железа в организме.
Рисунок 4-15
Окислительные процессы вызывают высвобождение свободных электронов, которые в свою очередь приводят к образованию свободных радикалов. Последние, помимо прочих повреждающих эффектов, активируют перекисное окисление липидов.
И сульфат железа, и ГПК вызвали значительное увеличение (p<0,05) среднего уровня гемоглобина и ферритина эритроцитов по сравнению с плацебо (см. Рис. 4-5).
Основной находкой исследования стал факт значительного увеличения восприимчивости липопротеинов очень низкой плотности (ЛОНП) и низкой плотности (ЛНП) к вызванному медью окислению в группе больных, принимавших сульфат железа. Максимальная скорость окисления была увеличена на 8,3% на фоне лечения сульфатом железа, в группе плацебо она осталась практически неизменной, а у больных, получавших ГПК, снизилась на 5,7%. Таким образом, скорость окисления под действием сульфата железа была увеличена на 8,8% по сравнению с плацебо и на 12,8% по сравнению с ГПК.
Тенденция к окислению под действием меди и гемин-перекиси водорода была одинаковой (см. Рис. 4-16 и 4-17).
Рисунок 4-16
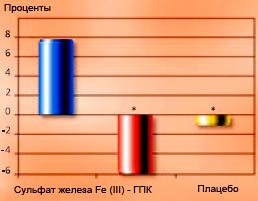
Изменения восприимчивости ЛОНП и ЛНП к окислению. (n=15 в группе); Изменение восприимчивости к окислению: изменение максимальной скорости окисления (наклонная линия) (mabs/мин): окисление, активированное медью. ГПК уменьшил восприимчивость к окислению (уменьшил максимальную скорость окисления), т.е. он действовал как антиоксидант.
*: Сульфат железа по сравнению с ГПК и плацебо: р<0,05.
Рисунок 4-17
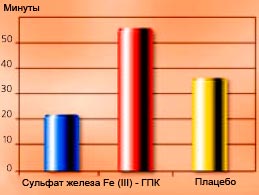
Временной интервал до окисления. (n=15 в группе); Изменение восприимчивости к окислению: временной интервал до окисления (мин.): окисление, активированное соединением гемин + Н2О2. Время окисления (период между введением вещества и началом процесса) было больше в группе больных, получавших ГПК, чем в группе больных, принимавших сульфат железа. Это означает, что концентрация свободных радикалов, которые действуют как катализаторы, была значительно меньше на фоне лечения ГПК.
Авторы делают заключение о том, что полученные данные очень важны в отношении лечения железодефицитной анемии. Эти результаты указывают на то, что быстрое восполнение запасов железа с помощью сульфата железа, по крайней мере, в комбинации с аскорбинатом, может оказывать нежелательное влияние на здоровье. По мнению авторов, при необходимости восполнения запасов железа, предпочтительнее использовать неионизированный ГПК, а не сульфат железа.
Другие возможные повреждения, вызываемые радикалами Fe2+/•OH-:
Результаты исследования, проведенного Sas с соавторами (1984), указывают на один из вышеуказанных эффектов.
В этом исследовании, 3 группы по 20 пациентов в каждой, получали лечение или ГПК или сульфатом железа или фумаратом железа в комбинации с витаминами. В течение 12-недельного периода исследования увеличение количества эритроцитов, а также уровня гемоглобина и гематокрита было одинаковым на фоне лечения всеми тремя препаратами.
Единственным существенным различием между ГПК и препаратом двухвалентного железа было увеличение уровня печеночных трансаминаз и дегидрогеназы у больных, получавших сульфат железа (II) (см. Рис. 4-18).
Рисунок 4-18
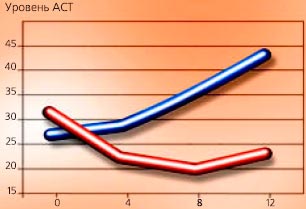
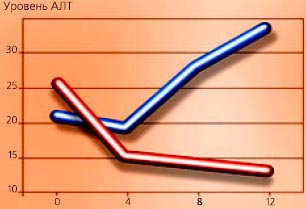
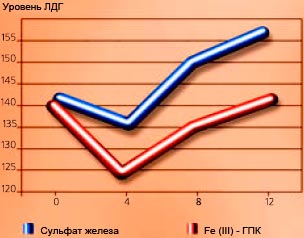
Увеличение уровня трансаминаз (АСТ и АЛТ) и лактатдегидрогеназы (ЛДГ) в печени после приема ГПК и препарата Fe (II). Уровень трансаминаз (АСТ и АЛТ) и лактатдегидрогеназы (ЛДГ), определенный на 0, 4, 8 и 12 неделях терапии полимальтозным комплексом гидроокиси железа (III) (ГПК) и сульфатом железа (II), (Sas с соавторами, 1984).
Авторы обсуждают полученные результаты, акцентируя внимание на опасности истощения транспортной способности сыворотки крови с последующим гемосидерозом ретикулоэндотелиальной системы (РЭС), и возможным токсическим действием на печень солей двухвалентного железа.
С одной стороны, благодаря оптимальной стабильности комплекса ГПК, железо эффективно захватывается транспортным белком, с другой стороны, в организме отсутствует свободная диффузия ионов железа.
4.2.3. Окрашивание зубов
Окрашивание зубов является общей проблемой лечения препаратами простых солей железа.
В лабораторных исследованиях изучалась реакция пластика и фарфора на сироп и капли ГПК. После 24-х часового воздействия, окрашивания не наблюдалось (Geisser, 1995).
С этими результатами согласуются и данные клинических исследований, которые выявили до 30% случаев появления темных пятен на зубах у детей, получающих сульфат железа, в то время как ГПК не оказывал подобных побочных эффектов (Schmidt, 1985).
4.3. Терапевтическая переносимость препарата Мальтофер®
Клинический опыт показывает, что пероральные препараты железа, особенно простые соли железа, вызывают неприятные побочные эффекты, включающие тошноту, боли в животе, диарею и запор. Индивидуальная чувствительность к терапии железом варьирует, и препараты железа не обязательно одинаково хорошо переносятся. Стандартные железосодержащие препараты, такие как сульфат железа, рекомендуется принимать перед едой во избежание снижения всасывания, которое обычно происходит, если эти препараты принимаются вместе с пищей (см. Рис. 4-21). Вероятно, что тяжесть вышеуказанных побочных эффектов, зависит от количества свободных ионов железа, выделившихся в желудочно-кишечном тракте.
Поскольку прием этих препаратов натощак приводит к еще более частым побочным эффектам (которые считаются основным препятствием восполнения железа), большинство врачей рекомендует принимать препараты вместе с пищей, а это сопровождается значительным уменьшением всасывания.
Данные по безопасности, полученные во время клинических исследований препарата Мальтофера® , свидетельствуют о низкой частоте побочных эффектов, что обеспечивает регулярный прием препарата Мальтофер® по сравнению с препаратами простых солей железа, в особенности у беременных женщин, младенцев и детей. Только в редких случаях наблюдаются симптомы раздражения желудочно-кишечного тракта, такие как чувство переполнения желудка, давления в области эпигастрия, тошнота, запор или диарея.
Опубликованы результаты клинического наблюдения 89 женщин с низким уровнем гемоглобина и гематокрита, получающих ГПК. У них оценивались эффективность, безопасность и переносимость препарата (Schams H., 1976). Лечебная доза составляла 2 таблетки в день в течение от 1 до 6 недель. Результаты показали значительное увеличение уровня гемоглобина и гематокрита даже после короткого курса лечения, хотя некоторые больные получили одновременную терапию тетрациклином.
Кроме того, было отмечено, что ГПК хорошо переносится. 97,6% больных оценили переносимость лекарства как хорошую или очень хорошую (см. Рис. 4-19).
Рисунок 4-19
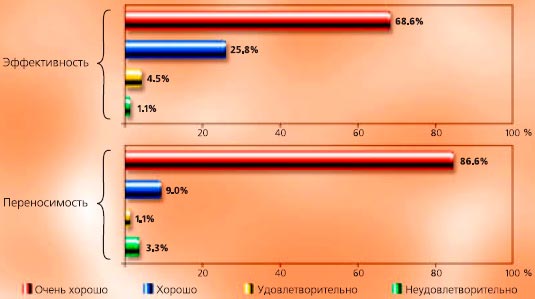
Эффективность и переносимость лечения ГПК. Клиническое наблюдение 89 женщин, получающих лечение ГПК. Лечебная доза составляла 2 таблетки в день. Результаты показали увеличение уровня гемоглобина и гематокрита. Переносимость лекарства оценили как хорошую или очень хорошую 97,6% больных (Schams Н., 1976).
Эти наблюдения согласуются с экспериментальными данными о частоте клеточных повреждений, геморрагических инфарктов и геморрагических эрозий, наблюдаемых у кроликов после введения ГПК в форме капель, сиропа и жевательных таблеток, и препаратов сульфата железа в виде стандартных таблеток или таблеток с непрерывным высвобождением (Schaub с соавторами, 1984).
Фотографии желудка экспериментальных животных на аутопсии (см. Рис. 4-20) запечатлели очевидное превосходство переносимости ГПК со стороны желудочно-кишечного тракта.
Рисунок 4-20
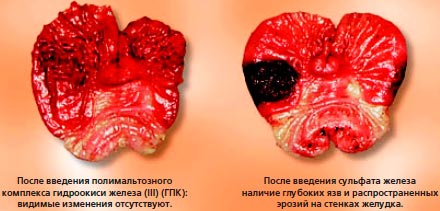
Желудок животных после введения Fe (III) - ГПК и сульфата железа (II).
4.4. Взаимодействие
Во время фармакокинетических и клинических испытаний, проводившихся с применением препарата Мальтофер® , не было обнаружено взаимодействий ГПК с компонентами пищи. Составляющие пищи и лекарства не оказывают влияния на биодоступность железа (Geisser, 1990).
Благодаря этому, ГПК может приниматься вместе с пищей и лекарствами в отличие от простых солей железа, которые рекомендуется принимать, как минимум за час до еды. Следует учитывать, что введение солей железа до еды заметно увеличивает частоту и степень повреждения желудка и изъязвлений двенадцатиперстной кишки, а также выраженность других побочных реакций. Поэтому, простые соли железа рекомендуют принимать вместе с пищей, а это значительно снижает всасывание железа.
Рис. 4-21 четко показывает, что всасывание железа из ГПК даже увеличивается, если препарат принимается вместе с пищей.
Рисунок 4-21

Влияние пищи на всасываемость различных препаратов железа. Хорошо известное взаимодействие с компонентами пищи простых солей железа уменьшает их всасывание. Побочные эффекты таких комплексов железа, как ГПК, не взаимодействующих с пищей, можно уменьшить до показателей плацебо (Kaltwasser и Werner, 1993).
4.5. Выводы
Клинические исследования, проведенные с применением препарата Мальтофер® по лечению недостаточности железа, показали терапевтическую эквивалентность ГПК и солей железа. Однако, препарат Мальтофер® вызывает значительно меньше побочных эффектов со стороны желудочно-кишечного тракта, чем соли железа.
Принимая во внимание хорошую переносимость, низкую токсичность и высокую степень утилизации неионизированного, макромолекулярного, водорастворимого железа из ГПК у больных анемией, можно считать его оптимальным препаратом для лечения различных железодефицитных состояний.
Было также доказано, что препарат Мальтофер® Фол может успешно предотвращать и лечить анемию во время беременности, и в том числе, во втором триместре беременности, когда потребность в железе самая высокая. Хорошая переносимость и отсутствие серьезных побочных эффектов, подтвержденные клиническими испытаниями, являются существенными факторами, обеспечивающими регулярный и длительный прием препарата.
Чрезвычайно важно восполнять запасы железа у младенцев и детей. Однако, плохая переносимость препаратов железа с одной стороны, и, возможно, недостаточная осведомленность о необходимости лечения с другой стороны, являются главными препятствиями для проведения заместительной терапии железом в этих возрастных группах. Исследования, проведенные с препаратом Мальтофер® (капли и сироп) у детей раннего возраста показывают, что данное лечение обеспечивает значительное улучшение гематологических показателей, т.е. повышение уровня гемоглобина, гематокрита, сывороточного железа и ферритина, и не сопровождается побочными эффектами, наблюдающимися у обычных препаратов солей железа.
Таблица 4-1.
ПРЕИМУЩЕСТВА ПРЕПАРАТА МАЛЬТОФЕР®
Мальтофер® отвечает всем требованиям идеального препарата железа для приема внутрь:
Приводят к регулярному и длительному приему препарата больными.
Предыдущий раздел | Оглавление | Следующий раздел
Комментарии
ПРАКТИКА ПЕДИАТРА
