Мониторинг расстройств сознания и современные методы их коррекции в отделении реанимации и интенсивной терапии
Статьи Опубликовано в журнале:
« АтмoсферА. Нервные болезни » №1, 2004г. Наталья Георгиевна Беневольская - невролог-реаниматолог городской клинической больницы № 15 им. О.М. Филатова г. Москвы.
Софья Алексеевна Румянцева -профессор кафедры неврологии и нейрохирургии ФУВ РГМУ.
Оценка функционального состояния организма в условиях отделения реанимации и интенсивной терапии является непременным условием адекватности терапии, но в большинстве отделений мониторинг ограничивается параметрами артериального давления, частоты сердечных сокращений, записью ЭКГ, и крайне редко используются количественные методы оценки неврологического статуса, включая методы оценки уровня депрессии сознания и функциональной активности головного мозга. В то же время именно адекватность функционирования центральной нервной системы, клинически проявляющаяся различными уровнями бодрствования, является результирующей реакции организма на любое патологическое или лечебное воздействие, позволяет объективизировать глубину воздействия критического состояния на системный и церебральный гомеостаз и качество терапии.
Длительная депрессия сознания у больных, перенесших критическое состояние любого генеза, является плохим прогностическим признаком. Она свидетельствует о выраженности расстройств интегративной деятельности мозга, обычно сопровождающихся утратой трофико-регуляторных влияний на соматическую сферу и являющихся маркером максимально тяжелого течения фоновой соматической патологии, в том числе синдрома полиорганной недостаточности (СПОН). Вопрос о соотношении процессов торможения и возбуждения в центральной нервной системе при терминальных состояниях, как и вообще в нейрореаниматологии, является одним из наиболее сложных и важных. У любого врача-реаниматолога возникает желание достичь быстрой активации корковых функций и восстановления сознания.
Однако несвоевременное пробуждение и гиперактивность корковых процессов в условиях несбалансированного системного метаболизма могут быть опасными и приводить к истощению нейромедиаторных систем. Анализ ЭЭГ наряду с клиническим мониторингом состояния сознания помогает ответить на вопрос о времени начала активации функций мозга.
Исход лечения с полноценным восстановлением всех функций организма, особенно когнитивных функций, зависит от тяжести и длительности поражения, своевременности и качества проведения экстренной реанимации, но не в меньшей степени от адекватности интенсивной, в том числе нейропротективной, терапии в постреанимационном периоде. Эта терапия может оказать определяющее влияние на профилактику и уменьшение вторичных системных и церебральных расстройств после начала реперфузии и реоксигенации.
Широко используемые в клинической практике методы активации центральной нервной системы, прежде всего корковых, стволовых, а также надсегментарных вегетативных ее звеньев, являются часто недостаточно эффективными. Ряд нейропротекторов, хорошо зарекомендовавших себя в эксперименте, до настоящего времени не имеет четких подтверждений клинической эффективности. Особенно важны поиски методов рациональной терапии и нейропротекции у наиболее тяжелой категории больных с вторичными неврологическими осложнениями и длительной депрессией сознания.
В связи с этим особый интерес представляет препарат Глиатилин, обладающий центральными холино-миметическими и мембраностабилизирующими свойствами и активирующий синаптическую рецепцию. В ряде публикаций показана его эффективность в лечении неврологических заболеваний.
В ходе настоящего исследования проведен количественный анализ частоты расстройств сознания у больных с экстрацеребральной патологией в отделении реанимации и интенсивной терапии (ОРИТ) с нейрореанимационным блоком в многопрофильном стационаре, а также изучены особенности течения неврологических расстройств и динамика состояния сознания у больных с экстрацеребральной патологией в посткритический период при использовании Глиатилина.
В ОРИТ клиники неврологии РГМУ и городской клинической больницы № 15 им. О.М. Филатова г. Москвы проведено лечение 1272 больных, из них с заболеваниями головного мозга 540 (42,5%), с неврологическими осложнениями экстрацеребральных заболеваний - 732 (57,5%). Соматический статус больных оценивали по шкалам SAPS и SAPS 2. Динамику состояния сознания и неврологического статуса оценивали по шкале комы Глазго и оригинальной шкале расстройств сознания и неврологического дефицита А.И. Федина.
Таблица 1.
Структура заболеваний в ОРИТ
| Церебральная патология | Число больных (n = 540) | Экстрацеребральная патология | Число больных (n = 732) | ||
|---|---|---|---|---|---|
| n | % | n | % | ||
| Инфаркт мозга | 260 | 49,1 | Перитонит | 255 | 34,9 |
| Геморрагический инсульт | 93 | 17,2 | Панкреонекроз | 127 | 17,4 |
| Черепно-мозговая травма | 63 | 11,6 | Желудочно-кишечные заболевания без перитонита | 238 | 32,5 |
| Токсическая энцефалопатия | 26 | 4,6 | Сочетанная травма | 30 | 4,1 |
| Эпилептический статус | 62 | 11,3 | Полостные ранения | 45 | 6,1 |
| Нейроинфекции | 10 | 1,6 | Сепсис | 12 | 1,6 |
| Миастения | 26 | 4,6 | Акушерское кровотечение | 17 | 2,3 |
| Эклампсия | 8 | 1,1 | |||
Таблица 2.
Частота расстройств сознания у больных с экстрацеребральной патологией
| Форма расстройства сознания | Число больных (n = 660) | |
|---|---|---|
| n | % | |
| Сонливость | 52 | 7,9 |
| Оглушение | 61 | 9,2 |
| Сопор | 188 | 28,5 |
| Глубокий сопор | 202 | 30,6 |
| Психовегетативное состояние | 6 | 0,9 |
| Кома | 151 | 22,9 |
В табл. 1 представлены данные об основных нозологических формах в ОРИТ с нейроблоком. В первой группе преобладали больные с инфарктом мозга, во второй - с заболеваниями желудочно-кишечного тракта. В табл. 2 показаны данные о представленности расстройств сознания у пациентов ОРИТ с первичной соматической патологией в посткритическом периоде. Нарушение сознания выявлено у 660 больных (90,2%) с экстрацеребральной патологией, что свидетельствует о высокой частоте расстройств сознания в результате выраженных диффузных постгипоксических нарушений и системного эндотоксикоза.
На рис. 1 представлены данные сравнительного анализа общего количества больных ОРИТ в коматозном состоянии и летальности в ОРИТ при экстра- и интра-церебральной патологии, свидетельствующие о высоком уровне летальности больных с экстрацеребральной патологией при депрессиях сознания.
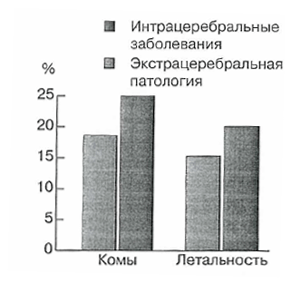
Рис. 1. Частота комы и летальность в ОРИТ.
Характерны также длительные сроки пребывания в ОРИТ больных с расстройствами сознания до уровня сопора и комы 1 (рис. 2). Наибольшая длительность пребывания в ОРИТ отмечена при психовегетативных состояниях.
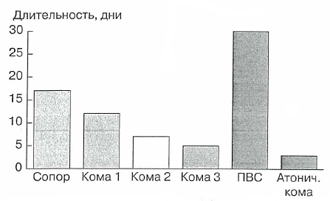
Рис. 2. Расстройства сознания и длительность пребывания больных в ОРИТ.
ПВС - психовегетативное состояние, атонич. кома- атоническая кома.
В ходе исследования у 70 больных ОРИТ с экстрацеребральной патологией, сопровождавшейся расстройствами сознания, проведен комплексный мониторинг неврологического и соматического статуса и клинико-инструментальный анализ эффективности холиномиметика Глиатилина, использованного в комплексной инфузионно-корригирующей терапии. У 18 больных этой группы причиной критического состояния стали: торакоабдоминальные колото-резаные и огнестрельные ранения, у 19 - тяжелые костно-травматические повреждения, у 7 - флегмоны и септические состояния, у 4 -перитонит, у 8 - панкреонекроз, у 10 — состояние после осложненного кесарева сечения, у 4 - тяжелая пневмония. 40 больным (57%) проводились искусственная вентиляция легких (ИВЛ) и стандартная инфузионно-корригирующая терапия. 30 больным (43%), отобранным методом случайной выборки, к стандартной терапии добавляли Глиати-лин в дозе 2000 мг в сутки внутривенно капельно в течение Юсут. Контрольная группа составила 40 больных. Фоновая тяжесть состояния в обеих группах составляла 10-12 баллов по SAPS и 35-37 баллов по SAPS 2.
Оценивались также: физиологический индекс тяжести, составлявший в обеих группах 39-42; уровень осложнений, равный в среднем 74-76%; предполагаемый уровень летальности по шкале POSSUM, составивший 52-56%; тяжесть полиорганной дисфункции по шкале MODS, составлявшая 6-8 баллов. Использование интегративных количественных шкал соматической дисфункции становится в настоящее время в ОРИТ главным методом объективизации тяжести состояния пациентов, так как позволяет изучать динамику течения заболевания и имеет прогностическое значение.
Анализ тяжести неврологических расстройств по количественной шкале расстройств сознания и очагового неврологического дефицита по шкале А.И. Федина позволил оценивать минимальную клиническую динамику по всем параметрам неврологического статуса.
Анализ функционального состояния мозга и объективизацию эффективности нейропротективной терапии проводили методом длительного прикроватного мониторирования ЭЭГ и КСАЭЭГ. При предварительных исследованиях у больных с фоновыми депрессиями сознания при экстрацеребральной патологии были выявлены тенденции опережающего снижения фоновой мощности спектра ЭЭГ при углублении тяжести соматического состояния у больных с экстрацеребральной патологией (рис. 3).
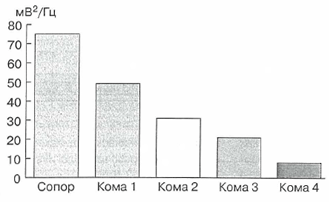
Рис. 3. Динамика суммарной мощности спектра ЭЭГ
при углублений расстройства сознания.
Клиническую эффективность проводимого лечения оценивали по скорости восстановления сознания, регрессу очаговых неврологических симптомов и когнитивных расстройств, длительности пребывания больных на ИВЛ в ОРИТ, степени регресса соматической дисфункции.
У больных в обеих группах фоновый уровень расстройств сознания составлял от 7 до 11 баллов по шкале комы Глазго и от 35 до 65 баллов по шкале А.И. Федина. Очаговые неврологические расстройства у пациентов были представлены синдромами энцефалопатии и энцефало-полинейропатии. Патология со стороны черепно-мозговых нервов выявлялась у 10% больных, нарушения двигательных функций - у 40%, мышечного тонуса - у 90%, вегетативной иннервации - у 80% больных СПОН.
При оценке по шкале А.И. Федина к началу терапии Глиатилином тяжесть очаговых неврологических расстройств составляла у больных обеих групп 76 ± ± 9 баллов. В группе пациентов, получавших Глиатилин, регресс очаговых неврологических симптомов происходил в среднем в течение 9 ± 4 сут, а при стандартной терапии - в течение 13 ±4 сут.
На момент перевода из ОРИТ в группе больных, получавших Глиатилин, тяжесть очаговых неврологических расстройств составляла по шкале А.И. Федина 12 ± 7 баллов, а при стандартной терапии - 20 ± 11 баллов (рис. 4). При этом у 70% пациентов с проведением стандартной терапии при переводе из ОРИТ отмечались явления энцефалопатии, проявлявшиеся прежде всего нарушением высших корковых функций, а именно: нарушения чтения и письма отмечены у 45% больных, нарушения плавности и беглости речи - у 80%; дезориентированность - у 50%. При терапии Глиатилином процент больных с нарушением высших корковых функций при переводе из ОРИТ составлял не более 30%.
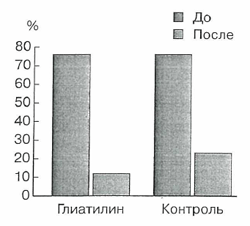
Рис. 4. Динамика регресса очаговых неврологических синдромов
при стандартной терапии и терапии Глиатилином.
У больных, получавших Глиатилин, восстановление сознания до уровня ясного по шкале комы Глазго (15 баллов) и до 5-10 баллов по шкале А.И. Федина происходило на 6 ± 3 сутки от момента начала введения Глиатилина, тогда как при стандартной терапии активация сознания наблюдалась на 10 ±4 сутки.
Средний койко-день пребывания в реанимации составил: при терапии Глиатилином 22 ± 4, при стандартной терапии 28 ± 2 сут; длительность пребывания на ИВЛ - 20 ± 4 при терапии Глиатилином и 26 ± 3 сут при стандартной терапии.
По данным мониторинга ЭЭГ при применении Глиатилина у больных отмечено нарастание суммарной мощности спектра в среднем с 43,5 ± 6,9 до 57,3 ±11,8 мкВ2за 10 дней терапии (в среднем по 1,4 мкВ2 в сутки), в то время как при проведении стандартной терапии средний прирост суммарной мощности спектра составлял не более 0,8 мкВ2 в сутки.
У 4 больных при мониторировании ЭЭГ отмечался стабильный на протяжении 4-5 сут наблюдения достоверно более высокий уровень суммарной мощности спектра по сравнению с остальными пациентами преимущественно за счет частот дельта- и тета-диапазонов, исходно составлявших до 78,5 ± 16,8% суммарной мощности спектра. Данная ЭЭГ-картина расценивалась как фоновый церебральный гиперметаболизм. У этих больных положительной клинико-электроэнцефалографической динамики при лечении Глиатилином не было.
Проведенные исследования позволяют сделать выводы о том, что у больных с экстрацеребральной патологией появление выраженных неврологических расстройств и длительные депрессии сознания являются предиктором прогрессирования тяжести соматической дисфункции. Включение в комплексное лечение центрального холиномиметика Глиатилина в дозе 2000 мг в сутки позволяет добиться уменьшения выраженности очаговых и диффузных неврологических расстройств, что способствует более ранней активизации больных, снижению длительности пребывания на ИВЛ и в ОРИТ.
Лечение Глиатилином, особенно в ОРИТ, следует проводить в условиях корреляционного соматоневрологического и ЭЭГ-мониторинга - для ранней оценки индивидуальной чувствительности к терапии и решения вопроса о целесообразности ее проведения.
