Влияние терапии диабетической нефропатии препаратом «Вессел Дуэ Ф» (сулодексид) на риск внутриглазных кровоизлияний у больных с пролиферативной диабетической ретинопатией
СтатьиОпубликовано в журнале:
Офтальмологические ведомости. Том II № 2 2009
Ф. Е. Шадричев
Санкт-Петербургский территориальный диабетологический центр Диабетическая нефропатия и ретинопатия — поздние осложнения сахарного диабета — являются основными причинами инвалидизации и смертности данной категории больных. Существует явная патогенетическая взаимосвязь диабетического поражения сетчатки и почек. Кроме этого, некоторые способы медикаментозного воздействия, направленные на нормализацию функции почек, могут влиять на течение диабетической ретинопатии. Работа посвящена изучению влияния стандартной терапии диабетической нефропатии препаратом «Вессел Дуэ Ф» (сулодексид) фирмы «Alfa Wasserman», на риск внутриглазных кровоизлияний (преретинальных и витреальных) у больных с пролиферативными изменениями сетчатки.
Ключевые слова: диабетическая нефропатия, пролиферативная диабетическая ретинопатия, сулодексид, лазеркоагуляция сетчатки, преретинальные кровоизлияния, витреальные кровоизлияния.
Диабетическая нефропатия — специфическое позднее осложнение сахарного диабета — является одной из основных причин инвалидизации и смертности больных диабетом. Половина случаев гемодиализа в США связана с диабетической нефропатией [11]. Терминальная почечная недостаточность является причиной смерти в 40 % случаев у больных сахарным диабетом 1 типа и в 5–10 % — у пациентов, страдающих сахарным диабетом 2 типа [10]. Такие значительные различия в уровнях летальности связаны в первую очередь с тем, что пациенты с сахарным диабетом 2 типа к моменту появления у них клинически значимой нефропатии имеют уже весь «набор» патологических состояний, связанных с инсулинорезистентностью, — дислипидемию, артериальную гипертензию и нарушение процессов фибринолиза (все те заболевания, которые входят в понятие «синдрома Х»).
Диабетическая нефропатия очень часто коррелирует с ретинопатией. Так, по данным WESDR1, пролиферативная диабетическая ретинопатия выявлялась в 5 раз чаще при сахарном диабете 1 типа и в 3 раза чаще при 2 типе диабета у больных с протеинурией, в отличие от пациентов без признаков диабетической нефропатии [19–22]. Тяжесть ретинопатии четко коррелирует и с тяжестью нефропатии. По данным Н. Б. Смирновой (1998), у пациентов с непролиферативной диабетической ретинопатией нефропатия выявлялась в 60 % случаев (у 9 % в стадии протеинурии), а у больных с пролиферативными изменениями сетчатки — в 91 % (у 64 % в стадии протеинурии) [6]. По данным М. В. Шестаковой (2003), на стадии начальных структурных изменений ткани почек ретинопатия выявляется в 5 % случаев, на стадии микроальбуминурии — в 20–50 %, а при наличии протеинурии — у 100 % больных [10]. N. V. Nielson c соавторами (1983) обнаружили, что 16,7 % больных с диабетической нефропатией были инвалидами по зрению, а среди пациентов без нефропатии только 6,6 % [26]. Очень многие авторы указывают на патогенетическую взаимосвязь диабетического поражения сетчатки и почек [1–5, 7, 8, 12, 13, 18, 23–25, 27–29]. Эта констатация неудивительна, принимая во внимание тот факт, что диабетическая нефропатия связана с нарушением метаболизма липидов, эндотелиальной дисфункцией, дисрегуляцией сосудистого тонуса, которая приводит к значительным гемодинамическим сдвигам, а также активацией тканевых факторов роста. Все эти патологические состояния принимают участие в процессе возникновения и прогрессирования и диабетической ретинопатии.
По мнению ряда исследователей, основной биохимической поломкой на уровне базальной мембраны клубочков при сахарном диабете является нарушение синтеза гепаран-сульфат гликозаминогликана, вследствие чего возникает утрата ее отрицательного заряда, что, в свою очередь, приводит к возникновению микроальбуминурии2 [14]. Гепаран-сульфат, кроме поддержания отрицательного заряда мембран, участвует в регуляции пролиферации мезангиальных3 клеток клубочков и гладкомышечных клеток сосудов, а также обладает антитромботическими и гиполипидемическими свойствами. Поэтому дефицит этого вещества, возникающий в условиях гипергликемии, является важным фактором возникновения и прогрессирования диабетических микроангиопатий. Восстановление же нормального содержания гепаран-сульфат гликозаминогликана может оказать протективное действие на микрососудистое русло.
В 1992 г. G. Gamboro с соавторами произвел первую попытку использовать гликозаминогликаны для лечения диабетической нефропатии у крыс с стрептозоциновым диабетом [16, 17]. Были получены положительные результаты — раннее назначение гликозаминогликанов предотвращало возникновение морфологических изменений в почечной ткани и появление микроальбуминурии. В последнее время для лечения диабетической нефропатии стали применять препарат «Вессел Дуэ Ф» (сулодексид) фирмы “Alfa Wasserman”, (Италия).4
Сулодексид представляет собой гликозаминогликан, получаемый из слизистых оболочек тонкого кишечника свиньи и на 80 % состоит из высокоподвижной гепариноподобной фракции (идуронилгликозаминогликан-сульфат), а на 20 % из дерматан-сульфата. Антитромботическое действие «Вессел Дуэ Ф» (сулодексид) связано с подавлением фактора Х, увеличением синтеза и секреции простациклина и снижением уровня фибриногена в плазме крови. Фибринолитический эффект возникает за счет повышения уровня тканевого активатора плазминогена (ТАП) в крови и снижения содержания в крови ингибитора ТАП. Препарат обладает и ангиопротективными свойствами, поскольку способен повышать отрицательный заряд эндотелиальных клеток и резистентность к повреждающему действию иммунных комплексов, липопротеидов низкой плотности и лейкоцитарных протеаз, а также уменьшать проницаемость базальной мембраны капилляров, продукцию экстра-целлюлярного матрикса. Кроме того, «Вессел Дуэ Ф» (сулодексид) подавляет пролиферацию клеток мезангия и гладкомышечных клеток сосудистой стенки.
Сулодексид обладает слабым антикоагуляционным действием, которое отмечается, в основном, при внутривенном введении больших доз препарата. Однако, поскольку диабетическая нефропатия часто коррелирует с пролиферативной диабетической ретинопатией, при которой вероятность возникновения преретинальных и витреальных геморрагий достаточно высока, необходимо было исследовать влияние терапии сулодексидом на риск массивных внутриглазных кровоизлияний.
Цель работы
Изучить влияние стандартной терапии диабетической нефропатии препаратом «Вессел Дуэ Ф» (сулодексид) фирмы “Alfa Wasserman” (Италия) на увеличение риска внутриглазных кровоизлияний (преретинальных и витреальных) у больных с пролиферативной диабетической ретинопатией, требующей лазерного лечения.
Методы обследования и лечения
В исследование включались пациенты с пролиферативной диабетической ретинопатией, которым планировались панретинальная лазеркоаугляция сетчатки и лечение препаратом «Вессел Дуэ Ф» по поводу диабетической нефропатии.
Терапия диабетической нефропатии препаратом «Вессел Дуэ Ф» (сулодексид) осуществлялась по схеме: 600 липопротеинлипазных единиц (ЛЕ) внутримышечно 1 раз в сутки в течение 10 дней, затем по 500 ЛЕ перорально 1 раз в сутки в течение 90 дней.
Офтальмологическое обследование в обязательном порядке включало биомикроскопию сетчатки при помощи асферических линз после медикаментозного расширения зрачка (раствор Мидриацила 1 % или его комбинации с раствором Ирифрина 10 %), а также фотографирование стандартных полей сетчатки.
Состояние сетчатки оценивалось по классификации Исследовательской группы по изучению раннего лечения диабетической ретинопатии — Early Treatment Diabetic Retinopathy Study (ETDRS) [15]. В исследование включались пациенты с пролиферативной диабетической ретинопатией 61 (неоваскуляризация сетчатки меньше половины площади диска зрительного нерва — ДЗН) и 65 уровня по ETDRS (неоваскуляризация сетчатки более половины площади ДЗН или неоваскуляризация ДЗН менее трети его площади). Критериями исключения из исследования были проведенная ранее лазерная коагуляция сетчатки, наличие витреальных (или преретинальных) геморрагий, оперативные вмешательства на исследуемом глазу в течение предыдущих 6 месяцев. В исследование не включались пациенты (глаза), у которых состояние оптических сред могло препятствовать выполнению адекватной панретинальной лазеркоагуляции сетчатки.
Панретинальная лазеркоагуляция сетчатки проводилась по стандартной методике (общее число коагулятов — 2000–3000, диаметр пятна — 500 мкм, количество сеансов — 3–4, интервал между сеансами — 2–4 недели) на установках “Visulas 532” и “Visulas 532s” фирмы “Zeiss”, Германия. Воздействие проводили на средней периферии сетчатки, оставляя свободной зону (при отсутствии в ней новообразованных сосудов) в 1 DP5 от носового края ДЗН, в 3 DP кверху и книзу и в 4 DP к височной стороне от анатомического центра макулы. Зоны плоской ретинальной неоваскуляризации обрабатывались сливными коагулятами, но несколько большей мощности. При наличии новообразованных сосудов на ДЗН коагуляты располагали практически вплотную к его краю [9].
После выполнения панретинальной лазеркоагуляции все пациенты наблюдались каждые три недели в течение 4 месяцев с обязательным осмотром глазного дна при помощи асферических линз. При появлении преретинальных или витреальных кровоизлияний производилось дополнительное фотографирование стандартных полей сетчатки.
Характеристика исследуемых групп
Общее число больных с пролиферативной диабетической ретинопатией (61–65 уровень по ETDRS), включенных в исследование, — 149 человек. Из них 86 пациентов (129 глаз), получавших «Вессел Дуэ Ф», входили в основную группу, а 63 (77 глаз) — в контрольную. На всех глазах (как в основной, так и в контрольной группе) была выполнена панретинальная лазеркоагуляция сетчатки.
Результаты
Не было получено достоверных различий по частоте внутриглазных кровоизлияний в основной и контрольной группе (соответственно 8,5 % и 10,4 %, р 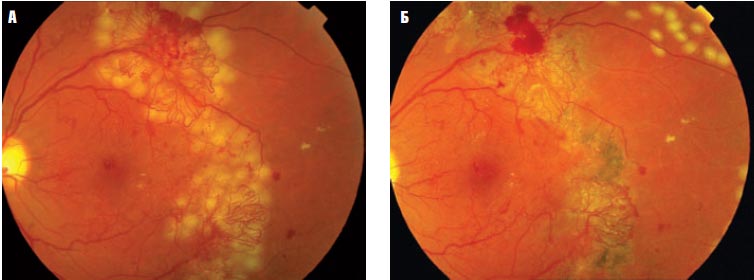
Рис. 1. Цветная фотография глазного дна
А — сразу после лазерного воздействия (прямая коагуляция новообразованных сосудов);
Б — через три недели после первого этапа лазерного воздействия (видно преретинальное кровоизлияние в области прямого воздействия на новообразованные сосуды)
Вывод
Применение «Вессел Дуэ Ф» в комплексном лечении диабетической нефропатии достоверно не увеличивает риск внутриглазных (преретинальных и витреальных) кровоизлияний у больных с пролиферативной диабетической ретинопатией при выполнении адекватной панретинальной лазеркоагуляции сетчатки. 1 Wisconsin Epidemiology Study of Diabetic Retinopathy – Висконсинское эпидемиологическое исследование диабетической ретинопатии. Список литературы
2 Данная теория получила название «гипотеза Steno» по названию госпиталя в Копенгагене (Дания), в котором работала группа исследователей, ее предложивших.
3 Мезангиальные клетки — это модифицированные гладкомышечные клетки сосудов, образующиеся из тех же клеток предшественников. Вместе с внеклеточным матриксом они образуют мезангий, который поддерживает структуру и функцию гломерулярного барьера. Мезангиальные клетки способны сокращаться и таким образом регулировать растяжимость гломерул в ответ на изменения давления. Эти клетки продуцируют компоненты мезангиального матрикса, который состоит из коллагена, ламинина, фибронектина и протеогликанов с цепями гепаран-сульфата и хондроитинсульфата. Мезангиальные клетки вырабатывают цитокины и факторы роста (фактор роста тробоцитов и инсулиноподобный фактор роста). Пролиферация мезангиальных клеток, наблюдающаяся при диабетической нефропатии, приводит к гиперпродукции матрикса, что, в свою очередь, вызывает гломерулосклероз.
4 Эффективность терапии диабетической нефропатии была подтверждена в многоцентровом двойном слепом плацебо-контролируемом исследовании DINAS — Diabetic Nephropathy Sulodexide Study, 1999.
5 1 DP (diametrum papillae) — один диаметр диска зрительного нерва (1500 микрон).
The effect of diabetic nephropathy therapy with “Vessel Due F” (sulodexide) on the risk of intraocular hemorrhages in patients with proliferative diabetic retinopathy
Shadrichev F. E. Summary. Diabetic nephropathy and diabetic retinopathy as diabetes mellitus late complications are the 29. main causes of disability and mortality in this category of patients. There is an evident pathogenic relationship between diabetic affection of the retina and kidneys. Moreover, some methods of therapy targeting renal function normalization, may influence diabetic retinopathy course. The study is dealing with investigation of effect of standard diabetic nephropathy treatment with “Vessel Due F” (sulodexide) [“Alfa Wasserman” production] on the risk of intraocular (pre-retinal and vitreal) hemorrhages in patients with proliferative retinopathy.
Key words: diabetic nephropathy, proliferative diabetic retinopathy, sulodexide, retinal photocoagulation, pre-retinal hemorrhages, vitreal hemorrhages.
Сведения об авторе:
Шадричев Федор Евгеньевич — к. м. н., заведующий, офтальмологическое отделение, Санкт-Петербургский территориальный диабетологический центр.
Shadrichev Fedor Evgenievich — candidate of medical science, head of the ophthalmology department, St.Petersburg territorial diabetology center.
