Эффективность рамиприла в профилактике сердечно-сосудистых и микрососудистых осложнений у больных сахарным диабетом: результаты исследований НОРЕ и MICRO-HOPE
Статьи Опубликовано в: "The Lancet" 2000г.; №355: С. 253–59 Группа исследователей HOPE (Heart Outcomes Prevention Evaluation)*Введение. Сахарный диабет - это мощный фактор риска развития сердечно-сосудистых заболеваний и поражения почек. Мы изучали эффективность ингибитора ангиотензинпревращающего фермента (АПФ) рамиприла в профилактике этих осложнений у больных сахарным диабетом.
Методы. В исследование HOPE (Heart Outcomes Prevention Evaluation) были включены 3577 больных сахарным диабетом в возрасте ≥55 лет, страдавших сердечно-сосудистыми заболеваниями или имевших еще, по крайней мере, один фактор риска. У этих пациентов отсутствовали протеинурия, сердечная недостаточность или снижение фракции выброса левого желудочка и не проводилась терапия ингибиторами АПФ. В соответствии с факториальным дизайном исследования больным назначали рамиприл 1 0 мг/сут или плацебо и витамин Ε или плацебо. Комбинированная конечная точка включала в себя инфаркт миокарда, инсульт и смерть от сердечнососудистых причин. В дополнительном исследовании основной конечной точкой служило развитие явной нефропатии.
Результаты. Исследование было завершено на 6 месяцев раньше намеченного срока (через 4,Б года) независимым комитетом по мониторированию безопасности, учитывая явное преимущество рамиприла перед плацебо. Лечение ингибитором АПФ привело к снижению риска комбинированной первичной конечной точки на 25% (95% доверительный интервал (95% ДИ) 12-36, p=0.0004), инфаркта миокарда на 22% (95% ДИ б-Зб), инсульта на 33% (95% ДИ 10-50), сердечно-сосудистой смерти на 37% (95% ДИ 21-Б1), смерти отлюбых причин на 24% (95% ДИ 8-37), реваскуляризации на 17% (95% ДИ 2-30) и нефропатии на 24% (95% ДИ 3-40, p=0.027). После внесения поправки на изменения систолического (2,4 мм рт. ст.) и диастолического (1,0 мм рт. ст.) АД достоверное снижение риска первичной конечной точки сохранялось на 25% (95% ДИ 12-36, p=0.0004).
Заключение. Рамиприл снижает риск развития сердечно-сосудистых осложнений и нефропатии у больных сахарным диабетом. Его эффективность в профилактике сердечно-сосудистых осложнений нельзя было объяснить только снижением АД. Препарат оказывает протективное действие на сосуды и почки у больных сахарным диабетом.
У больных сахарным диабетом наблюдается высокий риск развития сердечно-сосудистых заболеваний. В эпидемиологических исследованиях у мужчин с сахарным диабетом риск смерти от сердечно-сосудистых причин был в 2-3 раза выше, чем у пациентов без диабета, а у женщин - в 3-5 раз выше [1 -6]. Скорректированная по возрасту распространенность коронарной болезни сердца у белых взрослых больных сахарным диабетом составляет 45% против 25% у пациентов без диабета [7]. Доля сердечно-сосудистых заболеваний в структуре смертности больных сахарным диабетом достигает примерно 70% [8].
Наличие других факторов риска способствуют развитию сердечно-сосудистых заболеваний у больных сахарным диабетом. Абсолютный ежегодный риск фатальных и нефатальных сердечно-сосудистых осложнений у пациентов среднего и пожилого возраста, страдающих сахарным диабетом 2 типа, равен 4-5% [1,9-13]. Хотя в общей популяции распространенность заболеваний сердца снижается, у больных сахарным диабетом она изменилась в значительно меньшей степени, а у женщин, вероятно, даже повышается [13].
Экспериментальные, эпидемиологические и клинические исследования свидетельствуют о том, что ингибиторы ангиотензинпревращающего фермента (АПФ) могут задержать или предотвратить развитие сердечно-сосудистых осложнений. У больных сахарным диабетом их профилактический эффект был продемонстрирован после острого инфаркта миокарда [14], при наличии артериальной гипертонии [15-19] и низкой фракции выброса или сердечной недостаточности [20]. Ингибиторы АПФ снижают также риск развития нефропатии и других микрососудистых осложнений у больных сахарным диабетом 1 и 2 типа [17,21,22].
Хотя исследования показали, что ингибиторы АПФ задерживают или предупреждают развитие серьезных осложнений в некоторых подгруппах пациентов, их эффективность у широкого круга больных сахарным диабетом с высоким риском сердечно-сосудистых исходов не установлена. В исследовании HOPE изучался вопрос о том, приводит ли применение ингибитора АПФ рамиприла на фоне стандартной терапии к снижению риска сердечно-сосудистых осложнений у больных сахарным диабетом. В рамках исследования MICRO-HOPE изучалась также его эффективность в профилактике развития явной нефропатии. Ниже приводятся результаты этих двух исследований у больных сахарным диабетом [22].
Методы
Больные
Протокол исследований HOPE и MICRO-HOPE был описан ранее [23,24]. В исследование включали пациентов в возрасте ≥55 лет, страдавших и не страдавших сахарным диабетом. Критериями включения служили сердечно-сосудистые заболевания (коронарная болезнь сердца, инсульт или поражение периферических артерий) или сахарный диабет в сочетании с еще, по крайней мере, одним дополнительным сердечно-сосудистым фактором риска (общий холестерин более 5,2 ммоль/л, холестерин ЛВП менее 0,9 ммоль/л, артериальная гипертония, микроальбуминурия или курение). Основными критериями исключения были протеинурия или диабетическая нефропатия, другие тяжелые заболевания почек, гиперкалиемия, застойная сердечная недостаточность, низкая фракция выброса (менее 0,4), неконтролируемая гипертония, инфаркт миокарда или инсульт в течение предыдущих 4 недель, терапия витамином Ε или ингибиторами АПФ или гиперчувствительность к этим препаратам [23]. Исследование проводилось в 19 центрах Северной и Южной Америки и Европы. Протокол HOPE был утвержден этическими комитетами всех центров, а все больные дали письменное информированное согласие на участие в исследовании.
Во время вводного периода больные получали рамиприл в дозе 2,5 мг/сут в течение 7-10 дней, а затем плацебо - в течение 10-14 дней. Пациентов рандомизировали, если приверженность составляла, по крайней мере, 80%, отсутствовали побочные эффекты, сывороточная концентрация креатинина оставалась <200 мкмоль/л, а сывороточный уровень калия - <5,5 ммоль/л.
Дизайн исследования
Исследование имело факториальный дизайн (2x2), т.е. больных рандомизировали на группы рамиприла 10 мг и плацебо или витамина Ε 400 ME и плацебо. Пациенты посещали врача через 1 мес, а затем каждые 6 мес.
Комбинированная первичная конечная точка включала в себя инфаркт миокарда, инсульт или сердечнососудистую смерть. Вторичными конечными точками были смерть от любых причин, госпитализация по поводу застойной сердечной недостаточности или нестабильной стенокардии, реваскуляризация коронарных артерий или развитие явной нефропатии. Другими исходами служили любая сердечная недостаточность, прогрессирование стенокардии или развитие сахарного диабета у пациентов, не страдавших этим заболеванием. Одной из целей исследований HOPE и MICRO-HOPE было изучение эффективности рамиприла в профилактике развития этих исходов, а также микроальбуминурии и явной нефропатии у больных сахарным диабетом [22,25]. Все первичные и вторичные конечные точки регистрировались в отдельных формах и проверялись комитетом по конечным точкам слепым методом [33].
При каждом визите оценивали наличие сахарного диабета и изучали демографические и клинические характеристики на основании анамнеза и физического обследования. Сахарный диабет 2 типа диагностировали, если он развивался в возрасте старше 30 лет, а пациенты не принимали инсулин. Критериями диагностики артериальной гипертонии были прием антигипертензивных препаратов или систолическое или диастолическое АД более 160 и 90 мм рт. ст. соответственно. У больных сахарным диабетом определяли уровни гл и кирова нного гемоглобина (HbA1c) и сывороточного креатинина в лабораториях центров. Результаты анализа HbA1c выражали в процентах, превышавших верхнюю границу нормы. Регистрировали все случаи госпитализации по поводу гипогликемии.
В рамках исследования MICRO-HOPE измеряли экскрецию альбуминов с мочой исходно, через 1 год и в конце исследования (4,5 года) на основании отношения альбумин/креатинин в утренней порции мочи. Мочу хранили при -70°С. Коэффициент альбумин/креатинин измеряли в 4 лабораториях (Канада, Великобритания, Аргентина и Бразилия) [22]. Критерием микроальбуминурии в 1993 году было значение коэффициента ≥2 мг/ммоль/л у мужчин и женщин [33].
У больных с коэффициентом альбумин/креатинин >3б мг/ммоль после рандомизации анализировали белок или альбумины в суточной моче в лабораториях центров. Явную нефропатию диагностировали, если суточная альбуминурия составляла 300 мг или более, суточная протеинурия - 500 мг или более или коэффициент альбумин/креатинин - более 36 мг/ммоль при отсутствии результатов анализа суточной мочи (т.е. при наличии явной протеинурии). Результаты анализа суточной экскреции альбуминов или белка с мочой направляли в центральный офис, а все случаи явной нефропатии централизованно проверялись.
Статистический анализ
Дизайн исследования HOPE предполагал включение до 40 00 больных сахарным диабетом. Если частота осложнений у больных сахарным диабетом составляет 5% в год, то этот размер выборки позволял выявить снижение частоты инфаркта миокарда, инсульта и сердечно-сосудистой смерти на 18% в течение 5 лет со статистической силой 90% (двусторонняя ошибка альфа 0,05). Исследование было завершено на 6 месяцев раньше запланированного срока по рекомендации независимого комитета по мониторированию безопасности. Медиана наблюдения составила 4,5 года.
Мы приводим только результаты анализа, проводившегося в выборке intention to treat. Мы использовали метод регрессии Кокса со стратификацией больных с учетом рандомизации на группы витамина Ε и плацебо. Результаты приводятся в виде снижения относительного риска c 95% доверительным интервалом (95% ДИ). Для анализа выживаемости использовали кривые Каплана-Мейера, которые сравнивали с помощью метода log-rank. Динамику количественных переменных (H b A ι с, коэффициента альбумин/креатинин, АД, сывороточного креатинина) по сравнению с исходными значениями анализировали с помощью метода ANOVA с поправкой на исходные показатели. Коэффициенты альбумин/креатинин трансформировали, чтобы внести поправку на ненормальность распределения, а значения корректировали с учетом лабораторий, в которых производили изменения. С помощью метода регрессии Кокса оценивали зависимость частоты первичной конечной точки от типа сахарного диабета, противодиабетической терапии, наличия сердечно-сосудистых заболеваний в анамнезе, микрольбуминурии и артериальной гипертонии на момент рандомизации. С помощью того же метода оценивали влияние микроальбуминурии на риск развития явной нефропатии. Метод регрессии Кокса использовали также для оценки влияния рамиприла на частоту первичной конечной точки с поправкой на изменения АД во время исследования.
Результаты
Среди 9541 больного, включенного в исследование НОРЕ, 3654 (39,3%) страдали сахарным диабетом. Из анализа были исключены 77 больных, которые принимали участие в другом дополнительном исследовании, предполагавшем применение рамиприла в дозе 2,5 мг/сут или плацебо. Таким образом, анализировали результаты лечения у 3577 больных сахарным диабетом. Средний возраст составил 65,4 года. Среди них было 1322 (37%) женщин, а 1996 (56%) страдали артериальной гипертонией. Исходные характеристики больных групп рамиприла и плацебо были сходными (табл. 1).
Таблица 1. Исходные характеристики больных сахарным диабетом
| Рамиприл (n=1808) | Плацебо(n=1769) | |
|---|---|---|
| Демографические характеристики | ||
| Средний возраст, лет | 65,3 (6,4) | 696 (38%) |
| Женщины | 1112 (62%) | 65,6 (6,6%) |
| мужчины | 626 (35%) | 1143 (65%) |
| Клинические характеристики | ||
| Индекс массы тела, кг/м2 | 28,9(4,8) | 28,6(4,7) |
| Частота сердечных сокращений в минуту | 72,3 (11,4) | 72,5 (11,0) |
| Систолическое АД, мм рт. ст. | 141,7(19,6) | 142,3 (19,5) |
| Диастолическое АД, мм рт. ст. | 80(10,6) | 79,3 (10,7) |
| Лодыжечно-плечевой индекс | 0,97 (0,19) | 0,96 (0,18) |
| Отношение окружности талии и бедер | 0,93 (0,09) | 0,93 (0,08) |
| Окружность талии, см | 99,9 (12,7) | 99,6 (12,4) |
| Микроальбуминурия | 553 (31%) | 587 (33%) |
| Уровень НЬА1с, %* | 123 (30) | 124(32) |
| Сывороточный креатинин, мкмоль/л | 93,8 (22,3) | 94,0 (27,6) |
| Средняя длительность диабета, лет | 11,1 (10,2) | 11,8 (10,7) |
| Диабет 2 типа | 1774(98%) | 1722 (97%) |
| Артериальная гипертония | 1045 (58%) | 951 (54%) |
| Холестерин >5,2 ммоль/л | 1174(65%) | 1161 (66%) |
| Курение | 274(15%) | 270 (15%) |
| Коронарная болезнь сердца | 1046(58%) | 1093 (62%) |
| Перенесенный инсульт/эндартерэктомия | 124(7%) | 150(8%) |
| Поражение периферических сосудов | 311 (17%) | 361 (20%) |
| Без сердечно-сосудистых заболеваний | 604(33%) | 515 (29%) |
| Контроль гликемии | ||
| Только диета | 331 (18%) | 300 (17%) |
| Только инсулин | 432 (24%) | 482 (27%) |
| Только пероральные средства | 957 (53%) | 895 (51%) |
| Инсулин + пероральные средства | 88 (5%) | 92 (5%) |
| Другие препараты | ||
| Ацетилсалициловая кислота | 982 (54%) | 998 (56%) |
| Диуретики | 350 (19%) | 350 (20%) |
| Бета-блокаторы | 510 (28%) | 505 (29%) |
| Антагонисты кальция | 776 (43%) | 801 (45%) |
| Гиполипидемические средства | 409 (23%) | 390 (22%) |
Через 1 год прием рамиприла и плацебо продолжали 1486 (84%) и 1516 (88%) больных соответственно, а в конце исследования - 1045 (65%) и 992 (66%). Через 4 года 184 (1 2%) и 220 (1 5%) больных, рандомизированных в группы рамиприла и плацебо соответственно, принимали ингибиторы АПФ открытым методом. Немедицинские причины прекращения приема исследуемого препарата приведены в табл. 2. Единственным существенным побочным эффектом, послужившим причиной его отмены, был кашель, частота которого в группе рамиприла была на 5% выше, чем в группе плацебо. Частота госпитализаций по поводу гипогликемических реакций не отличалась между группами рамиприла и плацебо (2 и 2%), как и средние изменения сывороточной концентрации креатинина.
Таблица 2. Причины прекращения терапии
| Рамиприл (n=1808) | Плацебо(n=1769) | |
|---|---|---|
| Прием препарата прекращен в любой срок | 671 (37%) | 653 (37%) |
| Прием препарата прекращен к последнему визиту | 602 (33%) | 593 (34%) |
| Причины прекращения приема препарата* | ||
| Кашель | 133 (7%) | 37 (2%) |
| Гипотония/головокружение | 30 (2%) | 24(1%) |
| Ангионевротический отек | 5 (0,3%) | 1 (0,1%) |
| Гипертония | 60 (3%) | 100(6%) |
| Клинический исход | 138 (8%) | 171 (10%) |
| Другие | 511 (28%) | 503 (28%) |
| Применение ингибитора АПФ | ||
| Назначение открытым методом в любой срок* | 366(20%) | 431 (24%) |
| Причины назначения | ||
| Сердечная недостаточность | 116 (6%) | 133 (84) |
| Протеинурия | 57 (3%) | 54 (3%) |
| Гипертония | 123 (7%) | 173 (10%) |
| Другие | 181 (10%) | 191 (11%) |
Частота комбинированной первичной конечной точки, включавшей в себя инфаркт миокарда, инсульт или сердечно-сосудистую смерть, в группе рамиприла была значительно ниже, чем в группе плацебо (снижение относительного риска на 25% [95% ДИ 12–36], p=0,0004). Частота отдельных компонентов первичной конечной точки и других вторичных конечных точек при лечении рамиприлом также достоверно снизилась (табл. 3, рис. 1). Через 1 год лечение рамиприлом привело к снижению риска первичной конечной точки на 16% (от –14 до 39, p=0,26), а через 2 года – на 26% (6–41, p=0,011). В последующие годы этот эффект сохранялся.
Рис. 1. Кривые выживаемости Каплана-Мейера у больных сахарным диабетом.

Таблица 3. Клинические исходы в группах рамиприла и плацебо
| Рамиприл (n=1808) | Плацебо (n=1769) | Снижение относительного риска (95% ДИ) | Ρ | |
|---|---|---|---|---|
| Первичная конечная точка | ||||
| Комбинированная | 277 (15,3%) | 351 (19,8%) | 25% (12-36) | 0,0004 |
| Инфаркт миокарда | 185 (10,2%) | 229 (12,9%) | 22% (6-36) | 0,01 |
| Инсульт | 76 (4,2%) | 108(6,1%) | 33% (10-50) | 0,0074 |
| Сердечно-сосудистая смерть | 112 (6,2%) | 172 (9,7%) | 37% (21-51) | 0,0001 |
| Вторичные конечные точки | ||||
| Общая смертность | 196 (10,8%) | 248 (14,0%) | 24% (8-37) | 0,004 |
| Нестабильная стенокардия* | 213 (11,8%) | 207 (11,7%) | 0 (-21-17) | 0,99 |
| Сердечная недостаточность* | 81 (4,5%) | 79 (4,5%) | 1% (-34-28) | 0,93 |
| Реваскуляризация | 254(14,0%) | 291 (16,4%) | 17% (2-30) | 0,031 |
| Явная нефропатия+ | 117(6,5%) | 149 (8,4%) | 24% (3-40) | 0,027 |
| Другие исходы | ||||
| Любая сердечная недостаточность | 198 (11,0%) | 236 (13,3%) | 20% (4-34) | 0,019 |
| Транзиторная ишемическая атака | 80 (4,4%) | 104(5,9%) | 26% (1-45) | 0,04 |
| Прогрессирующая стенокардия | 363 (20,1%) | 397 (22,4%) | 13% (0-24) | 0,057 |
| Лазерная терапия ретинопатии | 170(9,4%) | 186 (10,5%) | 22% (-9-28) | 0,24 |
| Диализ | 10 (0,5%) | 8 (0,5%) | -20% (-205-53) | 0,70 |
| Явная нефропатия+, лазерная терапия ретинопатии или диализ | 273 (15,1%) | 312 (17,6%) | 16% (1-29) | 0,036 |
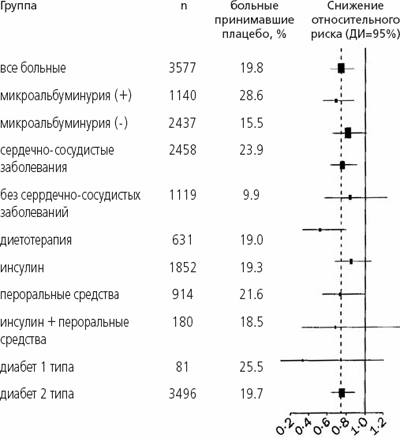
Благоприятный эффект рамиприла не зависел от наличия сердечно-сосудистых заболеваний в анамнезе (p=0,91), артериальной гипертонии (p=0,93), типа сахарного диабета (p=0,32) или сахароснижающей терапии (р=0,51). Результаты анализа эффективности рамиприла в различных подгруппах больных сахарным диабетом изображены на рис. 2.
Рис. 2. Эффективность рамиприла в профилактике первичной конечной точки в различных подгруппах.
Размер символа пропорционален числу больных. Пунктирная линия - общий риск
Через 1 год средние концентрации HbA1c увеличились на 1,5% (выше верхней границы нормы) в группе рамиприла и на 3,4% в группе плацебо (p=0,04). Через 2 года они снизились на 0,1 и 2,2% соответственно (p=0,016); при последующих визитах и в конце исследования динамика концентраций HbA1c была сопоставимой в двух группах (2,2 и 2,0% соответственно; p=0.8).
У больных группы рамиприла АД снизилось в несколько большей степени, чем у больных группы плацебо. К концу исследования систолическое АД снизилось на 1,92 мм рт. ст. при лечении рамиприлом и увеличилось на 0,55 мм рт. ст. в группе плацебо (p=0,0002); диастолическое АД снизилось на 3,30 и 2,30 мм рт. ст. соответственно (p=0,008; табл. 4). Эффект рамиприла на частоту первичной конечной точки сохранялся после внесения поправки на изменения АД (снижение относительного риска на 25%; ДИ 95% 12-Зб,р=0,0004).
Таблица 4. Изменения АД при лечении рамиприлом и плацебо
| АД, мм рт. ст. | Исходно | Через 1 мес | Через 2 года | Последний визит |
|---|---|---|---|---|
| Систолическое | ||||
| Рамиприл | 141,7 | -5,3 | -2,7 | -1,9 |
| Плацебо | 142,3 | -1,3* | 0,6* | 0,55** |
| Диастолическое | ||||
| Рамиприл | 80,0 | -2,6 | -2,6 | -3,3 |
| Плацебо | 79,3 | -0,3* | -1,05* | -2,3*** |
Коэффициент альбумин/креатинин исходно измеряли у 3498 (98%) больных, через 1 год - у 2914 (83%) из 3511, в конце исследования у 2671 (86%) из 310б. Во время исследования у 345 (10%) пациентов он повысился более 36 мг/ммоль, в связи с чем им предложили сдать суточную мочу для исключения явной нефропатии. Результаты были известны у 295 (85,5%) больных. Явную нефропатию выявили у 117 (7%) и 149 (8%) больных групп рамиприла и плацебо соответственно (снижение относительного риска на 24%; ДИ 95% 3-40, p=0,027). При использовании более жесткого определения явной нефропатии (включали только пациентов, у которых были известны результаты анализа суточной мочи) ее развитие зафиксировали у 100 (6%) больных группы рамиприла и 1 24 (7%) больных группы плацебо (снижение относительного риска на 22%; ДИ 95% от-2 до 40, p=0,07). При использовании еще более жестких критериев явной нефропатии (включали только пациентов, у которых были положительными результаты анализа суточной мочи и проводилась лазерная терапия по поводу ретинопатии) были получены сходные результаты (снижение относительного риска на 25%; ДИ 95% от -39 до 59, p=0,36).
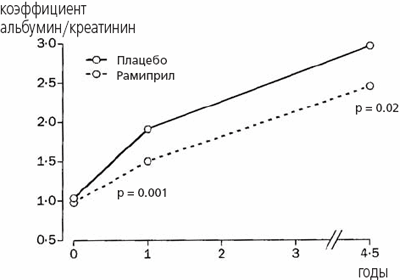
Явная нефропатия развилась у 225 (20%) и 41 (2%) больных, у которых исходно имелась и отсутствовала микроальбуминурия соответственно (относительный риск 14,0; ДИ 95% 10-19, p<0,0001). Лечение рамиприлом привело к снижению риска развития явной нефропатии у больных, у которых имелась или отсутствовала микроальбуминурия (взаимодействие p=0,51). Более того, терапия рамиприлом по сравнению с плацебо вызвала снижение коэффициента альбумин/креатинин через 1 год и в конце исследования (рис. 3). У больных, у которых исходно отсутствовала экскреция альбуминов с мочой, риск развития микроальбуминурии снизился недостоверно (на 9%; ДИ 95% от-4 до 20, p=0,17).
Рис. 3. Влияние рамиприла на альбуминурию.
Геометрическое среднее значение коэффициента альбумин/креатина у всех больных, у которых анализировали суточную мочу. С поправкой на лаборатории, в которых проводился анализ
Результаты анализа влияния рамиприла на частоту лазерной терапии по поводу диабетической ретинопатии или почечного диализа приведены в табл. 3. Терапия рамиприлом привела к снижению суммарной частоты микрососудистых исходов (явной нефропатии, диализа и лазерной терапии на 16%; ДИ 95% 1-29, p=0,036).
Обсуждение
Рамиприл значительно снизил риск развития сердечно-сосудистых осложнений (на 25-30%) у пациентов среднего и пожилого возраста с сахарным диабетом. Эффективность препарата не зависела от наличия сердечно-сосудистых заболеваний в анамнезе, артериальной гипертонии или микроальбуминурии, терапии инсулином или пероральными сахароснижающими средствами, типа сахарного диабета. Однако статистическая сила исследования была недостаточной для изучения эффектов в этих подгруппах больных. В конце исследования приверженность к лечению рамиприлом составила 65%, поэтому мы, вероятно, недооценили пользу терапии, которая могла бы оказаться выше при более высокой приверженности.
Рамиприл снизил также риск развития явной нефропатии, почечной недостаточности и применения лазерной терапии. Он не оказывал влияния на контроль гликемии.
Чтобы предупредить развитие инфаркта миокарда, инсульта, сердечно-сосудистой смерти, госпитализацию по поводу сердечной недостаточности, реваскуляризацию, явную нефропатию, лазерную терапию по поводу ретинопатии или назначение диализа у 1 пациента необходимо применять рамиприл в течение 4,5 лет у 15 пациентов высокого риска с сахарным диабетом.
Мы измеряли АД с помощью обычного метода, что является нормальным для клинической практики и крупных рандомизированных исследований. Мы не проводили мониторирование АД, что не позволяет исключить возможность ночной гипертонии в группе плацебо. Тем не менее, снижение риска развития сердечно-сосудистых осложнений было более значительным, чем можно было бы ожидать при достигнутой средней разнице АД между двумя группами. С помощью модели регрессии было показано, что эффективность рамиприла нельзя было объяснить только его антигипертензивным действием. В исследовании UKPDS [16] при разнице систолического и диастолического АД, равной 10 и 5 мм рт. ст. соответственно, риск инфаркта миокарда снизился на 21 %, а риск инсульта - на 44%. В исследовании SHEP [26] у больных сахарным диабетом снижение систолического и диастолического АД на 10 и 2 мм рт. ст. соответственно (на фоне терапии с использованием диуретика) сопровождалось уменьшением риска сердечно-сосудистых осложнений на 34%. В исследовании HOPE разница систолического и диастолического АД между группами составляла всего 2,2 и 1,4 мм рт. ст. соответственно, однако снижение риска развития инфаркта миокарда и инсульта было сопоставимым с таковым в UKPDS.
Эти соображения позволяют предположить, что благоприятные эффекты рамиприла в основном связаны с защитным действием ингибиторов АПФ на стенку артерий [27]. Ангиотензин II оказывает мощное прямое сосудосуживающее действие и усиливает рост гладкомышечных клеток, возможно, за счет индукции образования различных протоонкогенов и факторов роста. Он также способствует разрыву бляшки, вероятно, в результате стимуляции секреции эндотелина, ингибирования фибринолиза и усиления тромбообразования [27]. Брадикинин - это прямой вазодилататор, который усиливает высвобождение сосудорасширяющих веществ, таких как оксид азота и простациклин. Следовательно, эффекты ингибиторов АПФ могут опосредоваться снижением концентраций ангиотензина II и повышением уровней брадикинина.
Эффективность рамиприла в профилактике сердечно-сосудистых осложнений согласуется с результатами других исследований ингибиторов АПФ у больных сахарным диабетом, дизайн которых предполагал изучение их гипотензинового действия. Например, в исследовании Captopril Prevention Project [15] были рандомизированы 717 больных сахарным диабетом с тяжелой артериальной гипертонией. Через 6,1 года у больных, получавших каптоприл, частота инфаркта миокарда, инсульта или сердечно-сосудистой смерти снизилась на 14%; (95% ДИ 1 -26) по сравнению с таковой при лечении диуретиками и бета-блокаторами [15]. В исследовании UKPDS снижение АД при лечении каптоприлом или атенололом сопровождалось уменьшением риска развития сердечно-сосудистых и микрососудистых осложнений, однако каптоприл не имел преимуществ перед атенололом [17]. В этом исследовании были рандомизированы 758 больных, а частота неблагоприятных исходов составила 34%, поэтому оно позволяло выявить с высокой статистической силой (около 80%) только значительные различия между группами (например, снижение относительного риска на 30%). Однако разница эффектов двух активных препаратов должна быть меньше разницы эффектов активного препарата и плацебо и обычно составляет около 10%. Соответственно, подобная разница могла быть упущена. Результаты других исследований свидетельствуют о том, что по эффективности в профилактике сердечно-сосудистых осложнений ингибиторы АПФ имеют преимущества перед антагонистами кальция, хотя это не было первичной целью данных исследований [18,19,28].
Результаты анализа частоты микрососудистых осложнений оказались сходными с результатами предыдущих исследований, в которых ингибиторы АПФ снижали риск развития диабетической нефропатии [29,30] и почечной недостаточности [31 ] у больных сахарным диабетом 1 и 2 типа, а лизиноприл снижал риск развития диабетической ретинопатии у больных сахарным диабетом 1 типа [21]. Ограничение нашего исследования заключается в том, что коэффициент альбумин/креатинин измеряли в 4 лабораториях, а анализ суточной мочи проводили в многочисленных лабораториях. Тем не менее, мы вносили поправку на измерение коэффициента альбумин/креатинин, а результаты анализа суточной мочи подтверждались централизованно. Более того, благоприятный эффект рамиприла проявлялся несмотря, на повышенную вариабельность результатов измерения в разных лабораториях, что могло быть причиной недооценки его эффективности в профилактике явной нефропатии.
Мы также не подтверждали наличие явной нефропатии с помощью биопсии почек, что может иметь большое значение с учетом высокой частоты поражения почек другой этиологии у больных сахарным диабетом 2 типа [32,33]. Тем не менее, морфологические данные, полученные в нескольких исследованиях, свидетельствуют о том, что протеинурия является надежным маркером диабетической нефропатии у пациентов с сахарным диабетом 2 типа [34]. Более того, наши результаты не изменились при использовании более жесткого определения диабетической нефропатии (наличие суточной протеинурии в сочетании с ретинопатией, по поводу которой проводилась лазерная терапия). Кроме того, в эпидемиологических исследованиях выявлена высокая частота почечной недостаточности у больных сахарным диабетом 2 типа и нефропатией, которую диагностировали только на основании протеинурии [33]. Ограничением анализа частоты ретинопатии было то, что мы не проводили фотографирование сетчатки. Тем не менее, лазерная терапия по поводу диабетической ретинопатии является высокоспецифическим, хотя и нечувствительным маркером серьезной диабетической ретинопатии.
Дизайн исследования HOPE не предполагал изучение результатов антигипертензивного действия рамиприла, поэтому возможно только общее сравнение полученных данных с результатами других исследований. В исследовании HOPE рамиприл добавляли к терапии, которую пациенты получали ранее, а дозу его не титровали, чтобы добиться заранее выбранного снижения АД. Следовательно, подавление активности АПФ с помощью рамиприла в настоящем исследовании можно рассматривать как профилактическое вмешательство, обладающее различными механизмами действия, включая снижение АД. Применение рамиприла в сочетании с другими профилактическими мерами, такими как снижение АД, контроль гликемии, снижение уровней липидов, прекращение курения и лечение аспирином, должно способствовать дополнительному снижению риска развития сердечно-сосудистых и микрососудистых осложнений у больных сахарным диабетом.
Литература
1. Stamler J., Vaccaro О., Neanon J.D. Diabetes, ither risk factors and 1 2-yr cardio- vascular mortality for men screened in the Multiple Risk Factor Intervention Trial. Diabetes Care 1993;16:434-444.2. Kannel WB. McGee DL. Diabetes and cardiovascular disease: the Framingham study. JAMA 1 979;241:2035-38.
3. Fuller JH, Shipley MJ, Rose G, Jarrett RJ, Keen H. Mortality from coronary heart disease and stroke in relation to degree of glycaemia: the Whitehall study. BMJ 1983; 287: 867-70.
4. Barrett-Connor E, Cohn BA, Wingard DL, Edelstein SL Why is diabetes mellitus a stronger risk factor for fatal ischemic heart disease in women than in men? The Rancho Bernardo Study. JAMA 1991; 265:627-31.
5. Goldbourt U, Yaari S, Medalie JR. Factors predictive of long-tenn coronary heart disease mortality among 10059 male Israeli civil servants and municipal employees: a 23 year mortality follow-up in the Israeli Ischemic Heart Disease Study. Cardiology 1993; 82: 100-21.
6.MansonJE, ColdlitzGA, Stampfer MJ.etal. A prospective study of maturity-onset diabetes mellitus and risk of coronary heart disease and stroke in women. Arch Intern Med 1991; 151: 1141-47.
7. Wingard DL, Barrett-Connor E. Heart disease and diabetes. In: Harris Ml, Cowie CC, Stern MS, Boyko EJ, Reiber GE, Bennett PH, eds. Diabetes in America, 2nd edn. Washington: National Institutes of Health, 1995: 429-48.
8. Laakso M. Hyperglycemia and cardiovascular disease in type 2 diabetes. Diabetes 1999; 48: 937-42.
9. Morrish NJ, Stevens LK, Fuller JH, Keen H, Jarrett RJ. Incidence of macrovascular disease in diabetes mellitus: the London follow-up to the WHO multinational study of vascular disease in diabetics. Diabetologia 1991; 34: 584-89.
10. ETDRS Investigators. Aspirin effects on mortality and morbidity in patients widl diabetes mellitus: early treatment of diabetic retinopathy study report 14. JAMA 1992; 266: 1292-300.
11. Damsgaard EM, Froland A, Jorgensen OD, Mogensen CE. Eight to nine year mortality in known non-insulin dependent diabetes and controls. Kidney Int 1992;42: 731-35.
12. Neil A, Hawkins M, Potok M, Thorogood M, Cohen DA, Mann J. A prospective population-based study of microalbuminuria as a predictor of mortality in NIDDM. Diabetes Care 1993; 16: 996-1003.
13. Gu K, Cowie CC, Harris Ml. Diabetes and decline in heart disease mortality in US adults.JAMA 1999; 281: 1291-97.
14.Zuanetti G, Latini R, Maggioni AP, Franzosi M, Santoro L, Tognoni G. Effect of the ACE inhibitor lisinopril on mortality in diabetic patients with acute myocardial infarction: data from the GISSI-3 study. Circulation 1997; 96: 4239-45.
15. Hansson L, Lindholm LH, Niskanen L, et al. Effect of angiotensin-converting-enzyme inhibition compared with conventional therapy on cardiovascular morbidity and mortality in hypertension: the Captopril Prevention Project (CAPPP) randomized trial. Lancet 1999; 353: 611-16.
16. UK Prospective Diabetes Study (UKPDS) Group. Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38. BMJ 1998; 317: 703-13.
17. UK Prospective Diabetes Study (UKPDS) Group. Efficacy of atenolol and captopril in reducing risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 39. BM] 1998: 317: 713-20.
18. Tatti P. Pahor M, Byington RP, et al. Outcome results of the Fosinopril versus Amlodipine Cardiovascular Events Trial (FACET) in patients with hypertension and NIDDM. Diabetes Care 1998; 21: 597-603.
19. Estacio RO, Jeffers BW, Hiatt WR, Biggerstaff SL, Gifford N, Schrier RW. The effect of nisoldipine as compared with enalapril on cardiovascular outcomes in patients with non-insulin-dependent diabetes and hypertension. N Engl J Med 1998; 338:645-52.
20. Shindler DM, Kostis JB, Yusuf S, et al. Diabetes mellitus, a predictor of morbidity and mortality in the Studies of Left Ventricular Dysfunction (SOLVD) Trials and Registry. AmJCardwi 1996; 77: 1017-20.
21. Chaturvedi N, Sjolie AK, Stephenson JM, et al. Effect of lisinopril on progression of retinopathy in normotensive people with type 1 diabetes. EURODIAB Controlled Trial of lisinopril in Insulin Dependent Diabetes Mellitus. Lancet 1998; 351: 28-31.
22. Gerstein HC, Bosch J, Pogue J, et al. Rationale and design of a large study to evaluate the renal and cardiovascular effects of an ACE inhibitor and vitamin E in high-risk patients with diabetes: the MICRO-HOPE study. Diabetes Care 1996; 19: 1225-28.
23. HOPE Study Investigators. The HOPE (Heart Outcomes Prevention Evaluations) Study: the design of a large, simple randomized trial of an angiotensin converting enzyme inhibitor (ramipril) and vitamin E in patients at high risk of cardiovascular events. Can J Cardiol 11996; 12: 127-37.
24. The Heart Outcomes Prevention Evaluation Study Investigators. Effects of an angiotensin-converting-enzyme inhibitor, ramipril, on death from cardiovascular causes, myocardial infarction, and stroke in high-risk patients. N Engl J Med 2000 (in press).
25.Yusuf S, Lonn E. Anti-ischemic effects of ACE inhibitors: a review of current clinical evidence and ongoing clinical trials. Eur Heart J 1998; 19: J36-44.
26. Curb JD, Pressel SL, Cutler JA, et al. Effect of diuretic-based antihypertensive treatment on cardiovascular disease risk in older diabetic patients with isolated systolic hypertension: Systolic Hypertension in me Elderly Program Cooperative Research Group. JAMA 1996; 276: 1886-92.
27. Lonn EM, Yusuf S, Jha P, et al. Emerging role of angiotensin-converting enzyme inhibitors in cardiac and vascular protection. Circulation 1994; 90: 2056-69.
28. Hansson L, Lindholm LH, Ekbom T, et al. Randomized trial of old and new antihypertensive drugs in elderly patients: cardiovascular mortality and morbidity the Swedish Trial in Old Patients with Hypertension-2 study. Lancet 1999; 354: 1751-56.
29. Ravid M, Lang R, Rachmani R, Lishner M. Long-term renoprotective effect of angiotensin-converting enzyme inhibition in non-insulindependent diabetes mellitus: a 7 year follow-up study. Arch Inurn Med 1996; 156: 286-89.
30. Ravid M, Savin H, Jutrin I, Bental T, Katz B, Lishner M. Long-term stabilizing effect of angiotensin-converting enzyme inhibition on plasma creatinine and on proteinuria in normotensive type II diabetic patients. Ann Intern Med 1993; 118: 577-81.
31. Lewis EJ, Hunsicker LG, Bain RP, Rohde RD, Collaborative Study Group. The effect of angiotensin converting enzyme inhibition on diabetic nephropathy. N EnglJ Med 1993; 329: 1456-62.
32. Parving HH, Gall MA, Skott Petal. Prevalence and causes of albuminuria in non-insulin-dependent diabetic patients. Kidney Int 1992; 41: 758-62.
33. Ritz E, Orth SR. Nephropathy in patients with type 2 diabetes mellitus. N Engl J Med 1999; 341: 1127-33. 34. Olsen S, Mogensen CE. How often is NIDDM complicated with nondiabetic renal disease? An analysis of renal biopsies and me literature. Diabetologia 1996; 39: 1638-45.
