Перспективные подходы лекарственной терапии немелкоклеточного рака легкого
Статьи ОнкологияОпубликовано в сборнике Новое в терапии рака легкого (Москва, 2003) С. А. Тюляндин
Рак легкого и, в частности, его немелкоклеточный вариант, является основной причиной смерти от злокачественных новообразований. "Эпидемия" этого заболевания во многом обусловлена повсеместным распространением курения. У подавляющего большинства пациентов болезнь диагностируется в поздних стадиях, когда выполнение радикальной операции уже невозможно, а современные лучевая терапия и химиотерапия имеют лишь паллиативное значение. Использование программ ранней диагностики рака легкого, включающих выполнение ежегодной рентгенографии грудной клетки и цитологического исследования мокроты позволило увеличить пропорцию больных с ранними стадиями заболевания, что, однако, не улучшило отдаленные результаты лечения. Это еще раз подчеркивает, что клетки рака легкого диссеминируют уже на клинически
ранних стадиях заболевания. (I, II стадии). Все это делает актуальным поиски новых лекарственных средств для проведения эффективной системной терапии. Такие лекарственные средства могут быть созданы и уже создаются на основании углубленных знаний о биологии опухолевого роста, которые открывают новые мишени для противоопухолевой терапии.
Исследования последних лет свидетельствуют о наличии многочисленных изменений в геноме опухолевой клетки, которые определяют ее злокачественные свойств (бесконтрольная пролиферация, инвазия и метастазирование, редукция апоптоза, способность к стимуляции ангиогенеза, генетическая нестабильность, иммортализация и т. д.). Некоторые, часто встречающиеся нарушения в клетках НМРЛ, представлены в табл. 1 [1]
Таблица 1.
Генетические нарушения в клетках НМРЛ [1]
|
Ген |
Кодируемый белок и его функция |
Характер генетических нарушений |
Частота нарушений |
|
ERBB1 |
тирозинкиназный рецептор EGF |
гиперэкспрессия |
> 50% |
|
ERBB2 (HER2/neu) |
р185 - тирозинкиназный рецептор |
гиперэкспрессия амплификация |
25-30% |
|
Семейство генов RAS |
p21RAS - переносчик внутриклеточного сигнала |
мутации |
20-30% |
|
c-MYC |
c-myc - фактор транскрипции, регулирует клеточный цикл и активность теломеразы |
гиперэкспрессия амплификация |
50% |
|
PRAD1 |
циклин Д1 - в комплексе с циклин-зависимой киназой 4 стимулирует переход клетки из состояния GO в фазу G1 клеточного деления |
гиперэкспрессия амплификация |
47% 25% |
|
RB |
pRb - контролирует вход в S-фазу, регулируя активность фактора транскрипции E2F |
мутации отсутствие синтеза pRb |
3% 20-30% |
|
CDKN2 |
р16INK4 - ингибитор комплекса циклин Д1 и циклинзависимой киназы 4, предотвращает начало клеточной пролиферации |
мутации делеции |
10% 20% |
|
р53 |
р53 -фактор транскрипции; регулирует клеточный цикл и апоптоз, контролирует целостность генома |
мутации |
50% |
Таблица 2.
Частота гиперэкспрессии EGFR при различных гистологических вариантах рака легкого [З].
|
Гистологический вариант |
Число исследованных образцов |
Частота экспрессии EGFR |
|
Плоскоклеточный рак |
754 |
84% |
|
Аденокарцинома |
563 |
65% |
|
Крупноклеточный рак |
72 |
68% |
|
Мелкоклеточный рак |
19 |
0% |
Рецептор эпидермального фактора роста (EGFR).
Клетки НМРЛ содержат значительно большее число рецепторов EGF, чем нормальные клетки эпителия бронхов, особенно при плоскоклеточном варианте [2]. После связывания фактора роста (или лиганда) происходит димеризация рецептора и активация плазматической части рецептора, представленной тирозинкиназой Ц (см. рисунок 1). Лигандами для EGFR являются эпидермальный фактор роста (EGF) и трансформирующий фактор роста а. [З]. Сигналы, передаваемые при активации EGFR определяют пролиферативную активность клетки, способность к дифференцировке, инвазию и метастазирование, индукцию ангиогенеза и т. д. [3]. Существуют неопровержимые свидетельства о вовлеченности EGFR в опухолевую трансформацию эпителия бронхов [1]. Выключение EGFR в экспериментальных моделях приводит к торможению опухолевой пролиферации.
Рисунок 1. 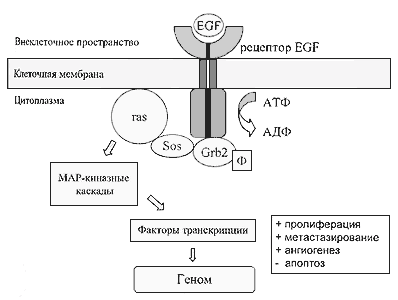
Другим, часто экспрессируемым рецептором на поверхности опухолевых клеток эпителия бронхов, особенно аденокарциномы, является рецептор ErbB-2 или HER2/neu [4]. ErbB-2 представляет собой рецептор семейства EGFR с тирозинкиназной активностью. Для этого рецептора не определен лиганд и считается, что он играет роль корецептора, в частности для EGFR, при формирования димерного комплекса и последующего аутофосфорилирования.
Таким образом, наличие экспрессии рецепторов семейства EGFR на поверхности опухолевых клеток НМРЛ, и участие в регуляции важнейших свойств опухолевой клетки делает их перспективными мишенями для разработки противоопухолевой терапии.
Моноклональные антитела специфично связываются с определенным рецептором и блокируют возможность передачи через него стимулирующего сигнала, что приводит к опухолевой регрессии. В настоящее время синтезированы моноклональные антитела к рецептору EGF (IMC-C225) и erbB2 (трастузумаб) и проводится их клиническое изучение у больных НМРЛ с экспрессией соответствующих рецепторов. Перспективность такого подхода была продемонстрирована у больных раком молочной железы при использовании трастузумаба и у больных плоскоклеточным раком головы и шеи при назначении С225 [5, 6]. В настоящее время проводятся изучение эффективности С225 у больных НМРЛ при проведении химиотерапии второй линии доцетакселом [7].
Изучается целесообразность использования трастузумаба в качестве добавления к стандартной химиотерапии у больных НМРЛ независимо от уровня экспрессии HER2/neu. Предварительный анализ проводящихся исследований дал основание говорить о безопасности добавления трастузумаба к стандартной химиотерапии и о возможном улучшении отдаленных результатов лечения [8]. При этом не отмечено взаимосвязи между уровнем экспрессии рецептора HER2/neu и эффективностью проводимой терапии. В качестве примера можно привести результаты II фазы изучения трастузумаба при его добавлении к еженедельному введению паклитаксела или доцетаксела в качестве первой линии химиотерапии [9]. Лечение получили 57 больных (HER2+ -13 больных и HER2- - 44). Эффективность и токсичность больных получавших паклитаксел и доцетаксел была одинаковой. Продолжительность жизни и 1-годичная выживаемость для больных с позитивным HER2 составила 14 месяцев и 51% соответственно, для HER2 негативных 19 месяцев и 62%. Обращает на себя внимание длительность жизни больных, которая при использовании еженедельного введения таксанов редко превышает 12 месяцев. Больные с позитивным HER2 имели неблагоприятные прогностические характеристики по сравнению с HER2 негативными пациентами, чем и объясняется разница в продолжительности жизни между двумя группами. Значение роли трастузумаба у больных НМРЛ должно быть определено при проведении рандомизированных исследований.
Не менее перспективным представляется нарушение функции цитоплазматической части рецептора, представленной тирозинкиназой. Синтезирован целый ряд химический соединений, способных ингибировать фосфорилирование тирозинкиназы, тем самым прерывая сигнал, передаваемый мембранной частью рецептора. ZD 1839 (Иресса) и OSI-774 (Эрлотиниб) из группы хинозолинов селективно ингибируют тирозинкиназу рецептора EGF и в настоящее время изучаются в клинике.
Для ZD 1839 (Иресса) была проведена первая фаза клинических испытаний, которая показала хорошую переносимость препарата при его пероральном приеме в течение 14 дней и активность его у больных НМРЛ. Из 16 больных НМРЛ, получавших лечение Ирессой, полная регрессия опухоли отмечена у 2 больных, частичная регрессия-у 2, еще у 2 больных регрессия менее 50% и стабилизация опухолевого процесса у 2 пациентов [10].
В 2002 году были доложены результаты сразу двух рандомизированных двойных слепых исследований (IDEAL 1 и 2) с ZD1839. В IDEAL-1 включались пациенты как минимум после одной линии химиотерапии [11], а в IDEAL-2 - после двух линий. При этом первая обязательно должна была включать препарат платины, а вторая -доцетаксел [12]. В обоих исследованиях пациенты рандомизировались на два дозовых режима: 250 мг или 500 мг ежедневно. Результаты представлены в таблице 3.
Таблица 3.
ZD1839 у ранее леченых больных НМРЛ: исследования IDEAL 1,2. [11,12].
|
|
IDEAL 1 |
IDEAL 2 |
||
|
250мг |
500мг |
250 мг |
500 мг |
|
|
Число пациентов |
105 |
105 |
102 |
114 |
|
IIIB стадия (%) |
80% |
80% |
15% |
8% |
|
Симптоматический эффект |
40.3% |
37% |
43% |
35% |
|
Объективный эффект |
18.4% |
19.0% |
12% |
9% |
|
Медиана выживаемости |
7.6 мес. |
7.9 мес. |
6.5 мес. |
5.9 мес. |
Эффективность была схожа при аденокарциноме и плоскоклеточном раке, однако была выше у женщин, чем у мужчин. Эффективность препарата была одинакова в качестве второй и третьей линий терапии. Очевидно, что ежедневная доза 250 мг является вполне адекватной, т. к. повышение ее до 500 мг лишь приводит к большей токсичности (сыпь, диарея 1/2 степени), не оказывая влияние на эффективность терапии.
Результаты клинических исследований подтвердили данные экспериментальных работ свидетельствовавших, что блокада EGFR может привести к регрессии опухоли. Эффект от приема Ирессы в виде улучшения общего состояния больного отмечается уже на второй неделе приема препарата. Эффективность, продемонстрированная ZD1839 при проведении второй-третьей линии терапии больных НМРЛ, позволяют рекомендовать его для применения в этом качестве взамен обычно рекомендуемого более токсичного доцетаксела.
Для OSI-774 (Эрлотиниб) проведена II фаза клинических испытаний у больных НМРЛ с наличием экспрессии EGFR и резистентных к цисплатину [13]. Частота объективного эффекта составила 11% и еще у 34% отмечалась стабилизация процесса при минимальной токсичности терапии. Эффект лечения не зависел от уровня экспрессии EGFR. Принимая во внимание неблагоприятный прогноз больных и отсутствие эффективных химиотерапевтических средств для их лечения, первые результаты применения OSI-774 следует признать перспективными.
Пути передачи внутриклеточного сигнала.
Сигнал от рецепторов EGF передается на молекулы-переносчики сигнала, среди которых важную роль играет белок K-Ras (p21RAS). При НМРЛ у 20-30% больных имеется точечная мутация гена K-RAS, в результате которой белок постоянно находится в активированном состоянии, имитируя и передавая стимулирующие к пролиферации сигналы [1]. Считается, что мутация гена RAS возникает вследствие воздействия нитрозоаминов табачного дыма. Все это послужило основанием считать белок К-Ras перспективной мишенью для прерывающих пролиферативного сигнала, идущего от рецепторов с тирозин-киназной активностью, включая EGFR. Известно, что белок K-Ras для выполнения своей функции должен приобрести соответствующую пространственную структуру и прикрепиться к внутренней поверхности клеточной мембраны. Для этого с помощью фермента фарнезилтрансферазы происходит присоединение 15 фарнезиловых групп на СООН-окончание белка. Без фарнелизации Ras не способен фосфорилироваться и передавать сигналы от рецептора к ядру клетки [14]. Были определены и синтезированы вещества, способные ингибировать активность фарнезилтрансферазы, что в эксперименте приводило к блокированию передачи внутриклеточного сигнала белком K-Ras и торможению опухолевого роста. В настоящее время эти препараты (L778, 123, SCH66336, R115777) проходят I-III фазу клинических испытаний, в том числе и у больных НМРЛ.
Перспективы применения ингибиторов фарнезилтрансферазы остаются неясными. Были представлены результаты двух рандомизированных исследований по применению R115777 при лечении больных диссеминированным колоректальным раком и распространенным раком поджелудочной железы [15, 16]. Больным колоректальным раком назначали постоянный прием R115777 в случае прогрессии после двух линий химиотерапии. Контрольная группа получала плацебо. Данные свидетельствуют, что прием R115777 не приводит к увеличению продолжительности жизни этой тяжелой группы пациентов. Больным распространенным раком поджелудочной железы проводили химиотерапию первой линии гемцитабином. На этом фоне одна половина больных получала R115777, а другая плацебо. Добавление R115777 не улучшило результаты химиотерапии гемцитабином. Вместе с тем, при проведении I фазы клинических испытаний препаратов R115777 и SCH66336 были продемонстрированы частичные регрессии при лечении больных НМРЛ.
Клеточный цикл.
Итогом передачи пролиферативного сигнала является вступление опухолевой клетки в процесс клеточного цикла, оканчивающегося делением и образованием двух дочерних клеток. Клеточный цикл - строго регулируемый процесс (см. рисунок 2). Он стимулируется на различных этапах комплексом циклинов и циклин-зависимых киназ [17]. Оказалось, что в клетках НМРЛ концентрация циклина Д1 (отвечающего за вхождение клетки в клеточный цикл) повышена в 5-100 раз по сравнению с нормальными клетками [18]. Это происходит за счет амплификации или гиперэкспрессии гена PRAD1, кодирующего циклин Д1, у 25% и 47% больных НМРЛ соответственно [19]. Повышенная продукция циклина Д1 способствует инициации клеточного деления.
Рисунок 2.
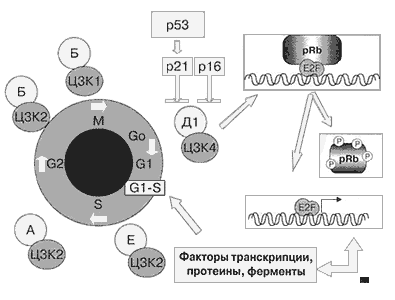
Важнейшим белком, который тормозит вхождение клетки в процесс деления, является белок ретинобластомы (Rb) - продукт гена-супрессора RB. Белок Rb связывает фактор транскрипции E2F. Комплекс циклина Д1 и циклинзависимой киназы 4 фосфорилируют белок Rb, в результате чего происходит разрыв связи с фактором транскрипции E2F. E2F, будучи активным, запускает транскрипцию различных генов и последующий синтез белков, ферментов и их ингибиторов, необходимых для перехода клетки из фазы G1 в фазу S [17]. Потеря одной копии и точечная мутация оставшейся копии гена-супрессора RB, кодирующего белок Rb, зафиксирована у 15-30% больных НМРЛ [20]. Белок р16INK4 подавляет активность комплекса циклина Д1 и циклин-зависимой киназы 4, предотвращая начало клеточной пролиферации. У 10-40% больных НМРЛ отмечаются делеция и точечная мутация оставшейся копии гена CDKN2, кодирующего p16INK4, а у 70% больных отсутствие экспрессии гена [1].
Ключевым регулятором клеточного цикла и процесса естественной гибели клетки (апоптоза) является белок р53. Ген р53 получил название "страж генома", благодаря своей центральной роли в поддержании стабильности генома многоклеточного организма и предотвращения удвоения поврежденной ДНК. р53 блокирует процесс деления клетки в случае повреждения ее ДНК временно для репарации или полностью, если эти повреждения невозможно устранить. В последнем случае р53 запускает механизм апоптоза [21]. Белок р53 является фактором транскрипции и регулирует активность большого количества генов, которые участвуют в торможении клеточного цикла, активации апоптоза и угнетении ангиогенеза. В частности, белок р53 является фактором транскрипции гена p21WAF, одного из важнейших ингибиторов циклин-зависимых киназ, и запускает производство белка р21 для остановки клеточного деления в случае повреждения ДНК.
р53 является центральным компонентом механизма, обеспечивающего удаление из организма патологически измененных клеток. Этот механизм полностью отсутствует у 50% больных НМРЛ в связи с делецией одной и мутацией другой копии гена р53 [22]. Таким образом, генетические изменения в клетках опухоли НМРЛ приводят к существенной потере контроля за ключевыми этапами клеточного цикла и, как следствие, за контролем пролиферации опухолевой клетки.
В эксперименте показано, что ингибирование циклин-зависимых киназ приводит к блокированию клеточного цикла. Определены субстанции, ингибирующие циклин-зависимые киназы, два представителя которых проходят клинические испытания [23]. Это флавопиридол, синтетический флавиноид, который в экспериментах продемонстрировал арест клеточного деления в момент перехода G1>S и G2>M. Показано, что в основе этого лежит ингибиция циклин-зависимой киназы 1, 2 и 4, вероятно, за счет потери киназами активных центров фосфорилирования. При проведении I фазы препарат вводился в виде постоянной внутривенной инфузии, и дозо-лимитирующей токсичностью была диарея, контролирующаяся приемом лоперамида. Кроме того, препарат вызывал миалгию, слабость, гриппо-подобный эффект. При суточной дозе 98 мг/м2 в крови достигается концентрация флавопиридола, которая в эксперименте была достаточной для ингибирования циклин-зависимых киназ. К сожалению, проведенная II фаза применения фловопиридола в виде 72-часовой инфузии оказалась неэффективной у больных НМРЛ [24]. В настоящее время проводится исследование, в котором инфузия фловопиридола предшествует введению паклитаксела. Другим препаратом из этой группы является UCN-01, изомер алкалоида стауоспорина, ингибирующий циклин-зависимые киназы 1 и 2. В клинике также испытывается в виде 72-часовой постоянной внутривенной инфузии. Дозо-лимитирующей токсичностью являются гипергликемия, тошнота и рвота, легочная недостаточность.
Считается, что мутации гена р53 играют ключевую роль в приобретении клеткой злокачественного фенотипа. Напрашивается простой подход-замена дефектного гена р53 на нормальный, что вновь даст возможность контролировать процесс клеточного деления опухолевой клетки. Нормальный ген р53 получен в достаточных количествах с помощью рекомбинантной технологии. Проблема заключается в том, как осуществить его адресную доставку к опухолевой клетке и включение в геном. Для этого используются вирусы, в частности аденовирус, в геном которого встроен нормальный ген р53. Аденовирус проникает и встраивается в геном опухолевой клетки, доставляя туда и нормальную копию гена р53.
В проведенном исследовании 9 больным немелкоклеточным раком легкого с наличием мутированного гена р53 производили интратуморальное введение аденовируса, содержащего нормальный ген р53 (Adp53). Показано, что перенос нормального гена в опухолевые клетки произошел у всех больных, что привело к заметному увеличению апоптоза. Противоопухолевый эффект был зафиксирован у 3 больных и еще у 3 отмечена стабилизация опухолевого роста [25]. Была предпринята попытка интратуморального введения Adp53 одновременно с системным введением цисплатина у 24 больных НМРЛ с нарушением функции р53 [26]. Противоопухолевый эффект отмечен у 2 больных, у 17 пациентов достигнута стабилизация процесса. Показана возможность применения Adp53 путем повторного бронхоальвеолярного орошения при бронхиолоальвеолярном раке легкого. У 2 больных из 9 зафиксирован противоопухолевый эффект [27]. Таким образом, заместительная генная терапия демонстрирует принципиальную возможность достижения клинического эффекта, что стимулирует продолжение исследований в этом направлении.
Опухолевая инвазия, ангиогенез и метастазирование.
Ангиогенез - формирование сети капилляров из эндотелиальных клеток, выстилающих мелкие венулы. Опухоль объемом 1 мм3 не может пролиферировать без формирования капилляра для доставки питательных веществ и кислорода. Клетки эндотелия имеют на своей поверхности рецептор к фактору роста эндотелия. Опухолевые клетки продуцируют в большом количестве фактор роста эндотелия (VEGF) и ферменты матричные металлопротеиназы. VEGF заставляет клетки эндотелия делиться и формировать капилляры в опухоли. Матричные металлопротеиназы разрушают внеклеточный матрикс, упрощая инвазию клеток эндотелия и образованных ими капилляров в опухолевую ткань. Инвазия сосудов в опухоль и способность опухолевых клеток растворять с помощью металлопротеиназ базальные мембраны обеспечивают им проникновение в кровоток с последующим метастазированием в другие органы и ткани [28, 29].
Ключевую роль в стимуляции опухолевого анигигенеза играет инактивация функции опухолевого супрессора р53 [17]. р53 контролирует экспрессию ингибиторов ангиогенеза, в частности активируя транскрипцию генов тромбоспондина 1 и 2, и подавляет транскрипцию гена VEGF. Гипоксия, которая непременно присутствует в опухолевой ткани без достаточного кровоснабжения, является фактором активации функции гена р53, что влечет за собой остановку клеточного деления, активацию тромбоспондинов и подавление продукции VEGF. Эти процессы должны предотвратить процесс ангиогенеза в опухоли и, в конечном итоге, привести к гибели опухолевых клеток. Поэтому инактивация функции р53 вследствие делеции и мутации при НМРЛ является важным этапом в приобретении опухолью способности стимулировать ангиогенез. Другим важнейшим фактором, способствующим стимуляции ангиогенеза и активности металлопротеиназ, является активация генов семейства RAS, которая часто отмечается при НМРЛ в результате мутации гена. Белок RAS стимулирует продукцию опухолевыми клетками VEGF и одновременно матриксных металлопротеиназ. Таким образом, изменение активности опухолевых супрессоров и онкогенов играет решающую роль в стимуляции ангиогенеза, опухолевой инвазии и метастазировании.
Подавление функции металлопротеиназ в эксперименте приводит не к гибели опухоли, а к ограничению или уменьшению ее размеров, подавлению ангиогенеза и метастазирования. Были синтезированы несколько препаратов, ингибирующих металлопротеиназы, которые находятся сейчас на этапе клинического изучения. К ним относятся маримастат, приномастат, Bay 12-9566, AG3340 и другие [29]. Учитывая, что ингибиторы металлопротеиназ не обладают прямым цитотоксическим эффектом, и при их применении можно ожидать лишь торможение опухолевого роста, в настоящее время проводятся рандомизированные исследования, в которых одним больным назначают химиотерапию, а другим - комбинацию химиотерапии и ингибиторов металлопротеиназ. В опухолях легкого, как мелкоклеточного так и немелкоклеточного характера, нередко наблюдается повышенная активность металлопротеиназ, что делает обоснованным изучение ингибиторов металлопротеназ при этой локализации опухоли [30]. В рандомизированном исследовании у больных мелкоклеточным раком легкого с полной или частичной регрессией после химиолучевой терапии назначение маримастата не улучшило результаты лечения по сравнению с плацебо [31]. Маримастат или плацебо назначали больным НМРЛ с отсутствием прогрессирования после проведенной химиотерапии первой линии, однако результаты этого исследования еще не опубликованы. Имеются результаты применения приномастата, который назначался больным IIIB-IV стадиями совместно с проводимой химиотерапией карбоплатином и паклитакселом. Результаты этого рандомизированного исследования показали, что приномастат не улучшил результаты химиотерапии по сравнению с плацебо [32]. Изучение другого ингибитора металлопротеиназ Bay 12-9566 при НМРЛ было остановлено компанией спонсором в связи с получением данных, что препарат ухудшил результаты лечения больных МРЛ в другом рандомизированном исследовании. Таким образом, несмотря на теоретические предпосылки эффективного применения ингибиторов металлопротеиназ в эксперименте, первый опыт клинического применения существующих ингибиторов этих ферментов разочаровывает. Возможно, что создание более селективных ингибиторов металлопротеиназ, назначение их больным только с повышенной активностью ферментов, сочетание с другими препаратами, влияющими на процесс инвазии, метастазирования и ангиогенеза, позволит найти место для этих лекарств при лечении больных НМРЛ.
В настоящее время в клинике изучается более 40 препаратов, ингибирующих различные звенья ангиогенеза. Это моноклональные антитела к рецепторам VEGF, физиологические ингибиторы ангиогенеза (ангиостатин, фрагмент плазминогена, и эндостатин, фрагмент коллагена 18-го типа), вещества, нарушающие процесс деления эндотелия (TNP-470) или их адгезию к элементам базальной мембраны (моноклональные антитела к интегрину avb3) и т. д.
Сообщены первые клинические данные применения моноклональных антител к рецептору VEGF (Mab VEGF) у больных НМРЛ [33]. В этом исследовании часть больных получала химиотерапию карбоплатином и паклитакселом (32 больных), в то время как во-второй группе одновременно с химиотерапией назначали Mab VEGF в дозе 7,5 мг/кг (32 больных) или 15 мг/кг (35 больных) в/в 3 раза в неделю до признаков прогрессирования. Назначение Mab VEGF в дозе 7,5 мг/кг не улучшило результаты химиотерапии. При назначении Mab VEGF в дозе 15 мг/кг отмечено увеличение числа объективных эффектов по сравнению с химиотерапией (с 25% до 34%) и увеличение продолжительности времени до прогрессирования (со 181 дня до 207 дней). Авторы сделали вывод, что добавление Mab VEGF к проводимой химиотерапии карбоплатином и паклитакселом приводит к увеличению числа объективных эффектов и удлинению времени до прогрессирования у больных НМРЛ.
Разработаны и находятся на этапе клинического применения молекулы, селективно ингибирующую тирозин киназу интрацеллюлярной части рецептора к VEGF. К ним относятся SU5416, первый опыт клинического применения которого у больных метастатическим колоректальным раком свидетельствует об клинической противоопухолевой активности препарата, и ZD6476 [34].
Заключение.
Наши возрастающие знания о молекулярно-генетических особенностях, имеющихся в клетках НМРЛ, открывают новые перспективные мишени для противоопухолевого воздействия. Уже сегодня первые препараты, созданные для поражения новых мишеней, пришли в клинику и демонстрирует значительную противоопухолевую активность. Их появление делает актуальным определение имеющихся в клетках опухоли молекулярно-генетических нарушений. Именно характер молекулярно-генетических нарушений, а не морфологический диагноз, будет определять выбор новых противоопухолевых препаратов или их комбинаций для индивидуальной терапии каждого больного.
Было показано, что новые противоопухолевые препараты обладают цистостатическим эффектом. Т. е. в отличие от классических противоопухолевых препаратов, которые убивают опухолевые клетки (цитотоксический эффект), новые препараты способны лишь тормозить или прекращать дальнейший рост опухоли (цитостатический эффект). В связи с этим, представляется перспективным их назначение совместно с современными противоопухолевыми препаратами не только при наличии диссеминированного процесса, но и с адъювантной целью. Экспериментальные и первые клинические данные свидетельствуют о синергизме их противоопухолевого эффекта.
Еще одним перспективным направлением применения новых цитостатиков является профилактика злокачественных опухолей и, в частности, НМРЛ. В настоящее время общепризнано, что канцерогенез - многоступенчатый процесс постепенного накопления мутаций и других генетических изменений, приводящих к нарушению регуляции клеточного цикла, апоптоза и дифференцировки. Уже сегодня стало возможным определять имеющиеся молекулярно-генетические повреждения в эпителии бронхов, ведущие к возникновению злокачественного процесса, на ранних стадиях, в том числе и на этапе предопухолевых изменений. Коррекция подобных изменений в предопухолевых очагах с помощью новых цитостатиков будет иметь своей целью предотвращение возникновения опухолевой клетки. Все это значительно увеличит возможности современной онкологии в борьбе с этим смертельным сегодня заболеванием.
Процесс передачи пролиферативного сигнала от рецептора эпидермального фактора роста (EGF) к АН К.
Эпидермальный фактор роста (EGF) соединяется с экстрацеллюлярными частями двух рецепторов (димером), в результате чего происходит активация плазматической части рецептора, представленной тирозинкиназой. Она аутофосфорилирируется и впоследствии фосфорилиоирует (присоединяет АТФ) молекулы-переносчики сигнала Grb2 и Sos. Те, в свою очередь, фосфорилируют белок Ras, прикрепленный к внутренней поверхности мембраны с помощью фарнезилового мостика. Активированный белок Ras передает сигнал через систему МАР-киназного каскада в ядро клетки к факторам транскрипции, которые инициируют транскрипцию отдельных генов с последующим производством соответствующих белков (трансляция), стимулирующих клеточную пролиферацию.
Регуляция перехода клетки через сверочную точку G1-S клеточного цикла деления.
Клеточный цикл деления стимулируется на различных этапах комплексом циклинов (Д1, Е, А, Б) и циклин-зависимых киназ (ЦЗК 1, 2, 4). Важнейшим этапом инициации клеточного цикла является прохождение клетки через сверочную точку из фазы G1 (пресинтетической) в фазу S (синтетическую, которая подготавливает процесс удвоения ДНК). Важнейшим белком, который тормозит вхождение клетки в процесс деления, является белок ретинобластомы (Rb). Белок Rb связывает фактор транскрипции E2F. Комплекс циклина Д1 и циклинзависимой киназы 4 фосфорилируют белок Rb, в результате чего происходит разрыв связи с фактором транскрипции E2F. E2F, будучи активным, запускает транскрипцию различных генов и последующий синтез белков, ферментов и их ингибиторов, необходимых для перехода клетки из фазы G1 в фазу S. Белки р16 и р21 подавляют активность комплекса циклина Д1 и ЦЗК4, предотвращая начало клеточной пролиферации. Белок р53 является фактором транскрипции гена р21 и запускает производство белка р21 для остановки клеточного деления в случае повреждения ДНК.
Список литературы к данной статье предоставляется по запросу.
Пожалуйста, представьтесь.
Новое в терапии рака легкого - Содержание
