Новый гидроксиэтилкрахмал: ГЭК 130/0,4, Волювен
СтатьиКонгресс по нефрологии
Baron J.-E
Профессор анестезиологии отделение анестезиологии и реанимации клиники Броссо, Париж, Франция
Объем крови - это критический фактор для поддержания стабильной гемодинамики и насыщения тканей кислородом. Объем жидкости в сосудах очень строго контролируется несколькими сложными механизмами, которые запускаются при разных условиях. В некоторых случаях, например, при остром кровотечении, сепсисе или при применении некоторых препаратов, организм должен выдержать абсолютное или относительное изменение объема крови, которое не может быть немедленно компенсировано регуляторными механизмами. В этих ситуациях основной целью плазмозамещающей терапии является временное увеличение объема крови, пока собственные системы организма не смогут устранить гиповолемию. За последние годы лечение гиповолемии сильно изменилось. Долгое время наиболее распространенным плазмозамещающим препаратом являлась свежезамороженная плазма (СЗП) или ее аналоги. В настоящее время показания к применению СЗП ограничены лечением некоторых нарушений свертывания крови. Побочным фактором этого изменения медицинской практики стало усиление использования человеческого альбумина. Из-за финансовых последствий этой стратегии несколько групп экспертов опубликовали рекомендации об оптимальных показаниях к применению различных плазмозамещающих препаратов.
Несмотря на эти рекомендации, тактика выбора оптимального препарата для лечения гиповолемии еще не определена. Помимо споров о выборе коллоида, продолжаются споры о преимуществах солевых растворов и коллоидов.
Физикохимические свойства гидроксиэтил крахмалов
Гидроксиэтилкрахмалы - это модифицированные природные полисахара. Природный крахмал в растворе нестабилен и быстро расщепляется а-амилазой. Гидроксилирование и этерификация проводятся для стабилизации раствора и замедления гидролиза1; при этом также значительно повышается гидрофильность молекул и их размер. Степень гидроксиэтилирования можно измерять по двум показателям: степень замещения и отношение положений замещения. Этот второй показатель учитывает случаи ди и тризамещения, которые происходят в некоторых молекулах глюкозы, и лучше отражает устойчивость крахмала к гидролизу а-амилазой. Молекула глюкозы подвергается гидроксиэтилированию преимущественно в С2 атоме, но также возможна модификация и в положениях СЗ и Сб. Гидроксиэтилирование по С2-положению дает набольшую устойчивость к а-амилазе. Отношение степени гидроксиэтилирования в 2 и 6 положениях (С2/С6) отражает тип гидроксиэтилирования. Важной характеристикой этих молекул также является молекулярный вес (MB). Хотя он не определяет фармакокинетики крахмала (которая зависит главным образом от степени и типа гидроксиэтилирования), но он является основным фактором, определяющим побочные эффекты препарата.
Первый гидроксиэтилкрахмал появился в продаже в Германии и США и имел высокий молекулярный вес (450 кДа).
Однако этот крахмал оказывал побочное действие на систему свертывания крови, в результаты чего он был изъят из продажи. К настоящему времени разработаны другие крахмалы с более низким молекулярным весом. Во Франции основными препаратами этой группы являются Elohes, Lomol, Heafusine и Haes-steril. Эти препараты имеют сходные, хотя и несколько различающиеся характеристики. Elohes представляет собой 6% раствор крахмала с MB 200 кДа и отношением положений замещения 0,62. Lomol представляет собой 10% крахмала с MB 250 кДа и отношением положений замещения 0,45. Haes-steril и Heafusine имеют близкие, хотя и не идентичные с Lomol характеристики, и выпускаются в 6% растворе.
Фармакокинетика гидроксиэтилкрахмалов
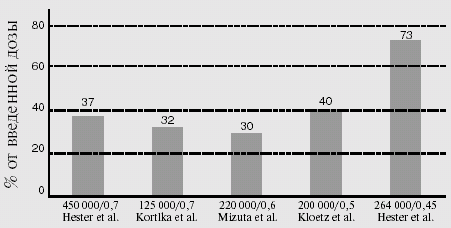
В отличие от декстранов, Фармакокинетика гидроксиэтилкрахмалов определяется в основном не MB, а степенью гидроксиэтилирования (рисунок 1).2,3 Основной путь выведения гидроксиэтилкрахмалов - с мочой. Определенная часть введенной дозы захватывается ретикулоэнд отел нал ьной системой, где гидроксиэтилкрахмал медленно расщепляется. Объем выведения гидроксиэтилкрахмала с мочой за 24 часа после введения зависит главным образом от степени гидроксиэтилирования. Для препарата Elohes время полувыведения молекул среднего размера составляет 7 часов, а крупных молекул - 5 дней. Для средних и крупных молекул препарата Lomol эти значения составляют соотв. 3 часа и 2 дня. В действительности обычные цифры плохо характеризуют фармакокинетику этих крайне неоднородных препаратов, поскольку они скорее отражают среднюю фармакокинетику всего препарата, а не его отдельных фракций. После инфузии гидрокси-этилкрахмала распределение его молекул по MB изменяется, во-первых, из-за более быстрого выведения более мелких молекул, а во-вторых, из-за частичного гидролиза крупных молекул с образованием более мелких молекул. Благодаря этому частичному гидролизу увеличение объема плазмы крови имеет тенденцию со временем усиливаться или стабилизироваться. Это явление наблюдается в основном в течение 2-4 часов после инфузии. Внутрисосудистый гидролиз некоторых гидроксиэтилкрах-малов а-амилазой ограничен из-за высокой степени их гидроксиэтилирования.4 Тканевое распределение этих крахмалов изучали в экспериментах на животных. Гидроксиэтилкрахмалы накапливаются и длительно удерживаются в ретикулоэндотелиальной системе, в том числе в селезенке, и постепенно расщепляются там с помощью мальтазы и комплекса сахараза-изомальтаза.
Рисунок 1.
Выведение с мочой различных гидроксиэтилкрахмалов, имеющих разный MB и степень гидроксиэтилирования. Молекулярный вес слабо влияет на выведение; основным фактором является степень гидроксиэтилирования.
Метаболизм гидроксиэтил-крахмалов изучался путем контроля уровня глюкозы в крови и моче, и никаких изменений не было обнаружено.5 Молекулярный вес молекул, выводимых с мочой у животных, низкий, но он значительно выше, чем вес молекул глюкозы. В условиях in vitro добавление гидроксиэтилкрахмала к плазме крови или раствору, содержащему а-амилазу, не приводило к какомулибо увеличению уровня глюкозы. Совместно эти данные свидетельствуют о том, что метаболизм гидроксиэтилкрахмалов происходит путем последовательного образования все более мелких фрагментов до фрагментов с MB примерно 40-50 кДа, которые достаточно малы, чтобы выводиться с мочой. Дальнейший метаболизм с образованием глюкозы или гидроксиэтилглюкозы не происходит. Основываясь на этих данных, можно заключить, что инфузия гидроксиэтилкрахмала не изменяет уровня глюкозы в крови. Однако у больных с неинсулинзависимым сахарным диабетом отмечены случаи гипергликемии и даже глюкозурии. Конечно, плазмозамещающие препараты применяются у больных в таких состояниях, в которых уже имеются другие факторы, нарушающие метаболизм глюкозы (напр., шок, оперативное вмешательство), и гидроксиэтил-крахмалы не обязательно являются причиной нарушения метаболизма глюкозы.
Учитывая количество гидроксиэтилкрахмалов на рынке и различие их физических и химических характеристик, сравнивать эти препараты очень трудно. Классификация по MB в условиях in vitro т.е. на высокомолекулярные (450 кДа), среднемолекулярные (200 кДа) и низкомолекулярные (70 кДа), не учитывает степени гидроксиэтилирования и соотношения С2/С6. Было бы более разумно сравнивать гидроксиэтилкрахмалы по их MB in vivo после частичного гидролиза исходного вещества.2 MB in vivo зависит от исходного MB, степени гидроксиэтилирования и соотношения С2/С6. Чем выше эти три показателя, тем выше MB in vivo. Этот подход позволил бы легко сравнивать разные препараты, поскольку для различения одного гидроксиэтилкрахмала от другого может использоваться один параметр.
Кроме того, MB in vivo является ключевым показателем для оценки коллоидного осмотического давления, фармакокинетики, накопления в плазме крови и тканях, а также побочного действия на свертывание крови и функции почек. Коллоидное осмотическое давление зависит от количества имеющихся молекул - показателя, который можно определить путем деления концентрации на средний MB in vivo. Если взять два гидроксиэтилкрахмала, один из которых имеет MB in vivo в 2 раза меньше, чем другой, то при одной и той же концентрации в растворе гидроксиэтилкрахмал с меньшим MB будет создавать вдвое большее коллоидное осмотическое давление. Другими словами, для достижения одинакового эффекта в случае раствора гидроксиэтилкрахмала с меньшим MB будет достаточно половинной концентрации.6 Кроме того, меньший MB означает, что вещество будет быстрее выводиться из организма и будет в меньших количествах накапливаться в плазме крови и ретикулоэндотелиальной системе. Побочные эффекты со стороны системы свертывания и, возможно, почек, тоже зависят от MB in vivo и концентрации препарата в плазме крови. Чем ниже MB in vivo, тем меньше крахмала накапливается в плазме крови при повторных введениях, и тем слабее нарушения свертывания крови.7,8 Нам представляется, что наилучшим гидроксиэтилкрахмалом является тот, который имеет MB in vivo, наименьший над порогом почечной фильтрации, составляющим 50-60 кДа. MB in vivo препарата Elohes составляет 140-150 кДа,4,7 что выше, чем у Haes-steril (110-120 кДа).7
Фармакологические свойства гидроксиэтил крахмалов
Для препарата Elohes начальное увеличение объема плазмы крови, превышающее объем введенного препарата, показано в нескольких исследованиях у послеоперационных больных и при нормоволемическом разбавлении крови.1,4,9 Эти исследования подтвердили, что эффективность этого раствора по показателю увеличения объема крови и улучшения функций сердечно-сосудистой системы равна или превышает эффективность человеческого альбумина.4,9 Длительность действия составляет около 24 часов. Degremon с соавт. обнаружили, что инфузия 500 мл Elohes увеличивает объем крови у послеоперационных больных на 693 мл. Этот эффект длится 24 часа, хотя концентрация Elohes постепенно снижалась и через 24 часа составляла 35% от максимальной. MB in vivo снижался в течение часа после инфузии и затем оставался постоянным в течение 24 часов. После инфузии Elohes концентрация альбумина сначала снижалась, а потом постепенно увеличивалась до 24 часов после инфузии. Эти данные свидетельствуют о том, что, хотя длительность действия препарата определенно зависит от его сохранения в кровотоке, долгий эффект Elohes объясняется действием и других механизмов (напр., внутрисосудистым гидролизом, уменьшающим MB in vivo, и, что более важно, мобилизацией межклеточного альбумина и адаптационных почечных механизмов). Сравнительные исследования, в которых бы измерялся внутри-сосудистый объем других гид-роксиэтилкрахмалов, отсутствуют. В результате можно проводить только непрямое сравнение. Для таких препаратов, как Lomol и Haes-steril, имеются данные об увеличении объема крови, превышающем объем введенного препарата.10 Длительность действия у них меньше, чем у Elohes, и составляет около 6 часов. Кobег с соавт.11 провели сравнение 6% и 10% раствора гидроксиэтилкрахмала 200/0,5 с 10% раствором декстрана 40 и 5,5%% раствором полижелатина. Это исследование показало увеличение объема крови после введения гидроксиэтилкрахмала в течение по крайней мере 6 часов, что больше, чем при введении желатина, который выводился через 3 часа.
Эффективность гидроксиэтилкрахмала 200 показана в разных клинических условиях: при нормоволемическом разбавлении крови, при замещении потери крови в ходе операций, при кардиологических операциях и сепсисе.12,14 В качестве аргумента против использования коллоидов в условиях реанимации часто выдвигалась концепция нарушения проницаемости капилляров. Причиной этого является то, что коллоиды не остаются внутри сосудов, а выходят в межклеточное пространство, увеличивают интерстициальное онкотическое давление и способствуют развитию отека. Однако при лечении 26 больных с сепсисом Rackow с соавт. обнаружили более низкую частоту отека легких среди больных, получавших гидроксиэтилкрахмал, по сравнению с больными, получавшими солевые растворы.15 Следует, однако, учитывать, что эти результаты были получены при использовании гетакрахмала, который имеет исключительно высокий MB in vivo. В экспериментальной модели ишемии и реперфузии Zikria показал снижение частоты развития инфаркта миокарда и тяжести отека при применении гидроксиэтилкрахмала.16 Это исследование было проведено с использованием особого крахмала - пента-крахмала, который имеет молекулы одного определенного MB. В различных работах подтверждена способность этого крахмала ослаблять отек в экспериментальных моделях ожога,17 ишемического/реперфузионного повреждения16,18,21 и сепсиса.22,23 Применение пентакрахмала у больных с сепсисом описано только в одной опубликованной работе, но в этой работе проводилось сравнение пентакрахмала с альбумином, и отек легких не изучался. Независимо от экспериментальных данных, нельзя сделать вывод о том, что пентакрахмал обладает подтвержденной способностью ослаблять отек в клинических условиях. Кроме того, этот препарат еще не выпущен в продажу. Интересно, однако, что экспериментальные исследования позволяют сделать предположение о том, что противоотечные свойства пентакрахмала обусловлены не создаваемым им коллоидным осмотическим давлением, а какими-то до сих пор не ясными свойствами этого вещества. Об этом свидетельствуют результаты других исследований имеющихся среднемолекулярных гидроксиэтилкрахмалов (не пентакрахмала). Например, в культуре эндотелиальных клеток Collins с соавт. продемонстрировали, что гидроксиэтилкрахмал по сравнению с альбумином может сильнее тормозить активацию эндотелиальных клеток и ослаблять неблагоприятное изменение проницаемости капилляров.24
Гидроксиэтилкрахмалы также могут подавлять адгезию лейкоцитов,13 что может играть важную роль в развития ишемического/ реперфузионного повреждения. Schmandt с соавт. установили, что гидроксиэтилкрахмал, применяемый для лечения геморрагического шока, не оказывает неблагоприятного влияния на функции клеточного иммунитета и на функции макрофагов.25 Eastlund с соавт. в этих же условиях обнаружили, что гидроксиэтилкрахмал не влияет на секрецию цитокинов, хемотаксис и миграцию моноцитов.26 Таким образом, ряд экспериментальных данных позволяет предположить, что Гидроксиэтилкрахмалы на самом деле должны оказывать благоприятное влияние на процессы воспаления при гиповолемическом шоке. Это предположение, по-видимому, косвенно подтверждается результатами клинического исследования, в котором гидроксиэтилкрахмал по сравнению с альбумином обеспечивал лучшее снабжение внутренних органов кислородом, регистрируемое по величине рН слизистой оболочки желудка больных сепсисом.14 В целом, имеющиеся данные свидетельствуют в пользу применения гидроксиэтилкрахмалов в условиях реанимации. Благоприятный эффект этих препаратов, по-видимому, больше связан с их влиянием на процесс воспаления, чем с создаваемым ими коллоидным осмотическим давлением. Однако при анализе соотношения риск/выгода применения гидроксикрахмалов следует также учитывать их побочные эффекты.
Побочные эффекты гидроксиэтил крахмалов
Влияние гидроксиэтилкрахмалов на свертывание крови изучалось многими авторами.3,27,29 Гидроксиэтилкрахмалы с высоким MB in vivo следует отличать от других типов гидроксиэтилкрахмал ов. При применении одного из таких препаратов - гетакрахмала - зарегистрированы многочисленные случаи аномального кровотечения.2
Продемонстрировано удлинение частичного протромбинового времени и снижение концентраций факторов VIII и Виллебранда.30,32 Эти данные и сообщения о развитии побочных эффектов являются основанием для прекращения применения этого препарата. Сообщения о побочных эффектах препарата Elohes не столь однозначны, поскольку однократное применение этого препарата даже в высоких дозах (33 мл/кг в течение 24 часов) не вызывает гематологических изменений.33 Однако многократное применение в течение 10 дней сопровождается четким нарушением лабораторных показателей, в том числе снижением концентраций факторов VIII и Виллебранда.2 Кроме того, в одном отчете контроля безопасности препарата приводится около дюжины случаев кровотечения, связанного с многократным применением препарата Elohes в течение нескольких дней, большинство из них произошли в нейрохирургической клинике. Большинство случаев кровотечения характеризовались нарушением гематологических показателей, в частности, снижением концентрации фактора Виллебранда.
После опубликования этого отчета в лицензию на продажу и в маркировку препарата было внесено указание на то, что применение препарата Elohes должно быть ограничено максимум 3 последовательными днями.
Treib с соавт. широко исследовали влияние различных гидроксиэтилкрахмалов на систему гемостаза и продемонстрировали влияние MB in vivo на тип и тяжесть нарушений свертывания. Нарушения свертывания наблюдаются после многократного применения гидроксиэтилкрахмалов в процессе 10-дневного курса разбавления крови препаратами, имеющими высокий MB in vivo по сравнению с исходным MB (in vitro), высокую степень гидроксиэтилирования или высокое соотношение С2/С6.2,7,34 Типичным препаратом этого типа является Elohes. Такие препараты накапливаются в организме с постепенным снижением их концентрации в плазме крови. Побочное влияние на показатели свертывания кров пропорционально концентрации препаратов в плазме крови. Сокращение тромбинового времени и снижение уровня фибриногена, вероятно, являются результатом ускорения полимеризации фибриногена. Уцлинение частичного протромбинового времени вызвано в основном уменьшением концентраций факторов свертывания VIII и Виллебранда. Наиболее вероятным механизмом развития этого эффекта является ускорение выведения комплекса фактор VIII/фактор Виллебранда после его связывания с молекулами гидроксиэтил-крахмалов. Снижение концентраций факторов свертывания
XI и XII наблюдается только при применении гидроксиэтилкрахмалов с очень высоким MB in vivo. Эти нарушения свертывания крови особенно выражены при многократном применении препарата Elohes в течение 10 дней и незначительны или отсутствуют при применении препаратов типа Haes-steril и Heafusine.2 В целом, имеющиеся данные свидетельствуют о том, что гидроксиэ-тилкрахмалы с низким MB in vivo (Haes-steril или Heafusine) оказывают незначительное действие или не влияют на гемостаз даже при многократном применении в течение 10 дней. Это не относится к препарату Elohes; такого применения этого препарата следует избегать.
Влияние гидроксиэтилкрахмалов на функции почек обсуждалось в недавно опубликованных статьях. Следует различать 2 ситуации: проведение хирургических операций и отдельно - пересадку почки. Синдром острой гиперонкотической почечной недостаточности был впервые описан при применении декстрана.39 Этот синдром развивается, когда коллоидное осмотическое давление поднимается до уровня, когда оно уравновешивает гидравлическое давление клубочковой фильтрации и, таким образом, подавляет формирование мочи. Такая ситуация наблюдается при достижении высокой концентрации коллоида в плазме крови, обычно после многократного введения препаратов. Анурия легче развивается в условиях снижения давления почечной перфузии, например, при шоке, ангиопатии или стенозе почечной артерии.36 Этот синдром описан при применении почти всех коллоидов: желатинов,37 декстранов,35 крахмалов,38 и концентрированного альбумина.39 В случае крахмалов развитие этого синдрома теоретически может облегчаться при многократном введении гидроксиэтилкрахмалов с высоким MB in vivo, что приводит к постепенному повышению их концентрации в плазме крови. Однако даже при введении в больших количествах в ходе операций на грудном и брюшном отделах аорты40 или в ходе ортопедических операций41 эти препараты, по-видимому, не повышают риска развития послеоперационной почечной недостаточности.
При трансплантации почки в биопсийных образцах пересаженной почки отмечалось повреждение типа осмотического нефроза, если донору проводилась терапия гидроксиэтил-крахмалом. В этом случае такое повреждение, по-видимому, происходит чаще, чем в случаях, когда донор не получал гидроксиэтилкрахмалов.42 Долгосрочное рандомизированное исследование, в котором сравнивался Elohes и желатин, показало худшее восстановление функций почки после трансплантации и более частую потребность в проведении гемодиализа среди больных, получавших гидроксиэтилкрах-мал.43 Механизм нарушения функций почки может быть связан с накоплением гидроксиэтилкрахмала в клетках канальцев. Однако гидроксиэтилкрахмал в участке осмотического нефроза не обнаружен, и такое же повреждение могут вызывать и многие другие препараты, особенно циклоспорин. Кроме того, в другом исследовании показано, что применение гидроксиэтилкрахмала, по-видимому, не влияет на частоту развития осмотического нефроза.44 Помимо этого, многоцентровое ретроспективное исследование не подтвердило какого-либо неблагоприятного действия гидроксиэтилкрахмалов на функцию трансплантата после пересадки почки.45
Иммунологическая инертность гидроксиэтилкрахмалов, по-видимому, очень высока.46 Частота аллергических реакций на них ниже, чем на декстраны и желатины. Тяжелые реакции наблюдаются очень редко.
Рисунок 2.
Кривая распределения молекулярного веса ГЭК 130/0,4 (Волювен) и ГЭК 200/0,5 (Haes-steril)
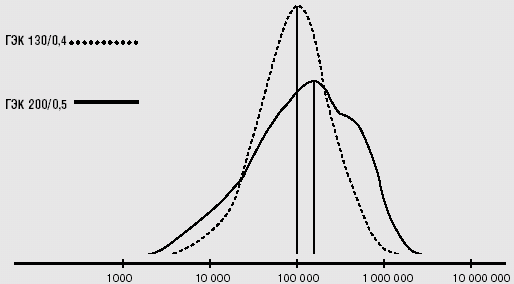
ГЭК 130/0 Волювен - это среднемолекулярный гидро-ксиэтилкрахмал со следующими физикохимическими характеристиками: MB in vitro 130 + 20 кДа, степень замещения 0,4, отношение С2/С6 более 8. ГЭК 130 был разработан для улучшения фармакокинетики и распределения MB препарата ГЭК 200/0,5 Haes-steril (рисунок 2). В частности, это изменение должно привести к ослаблению накопления препарата в плазме крови и тканях после многократного введения, а также, вероятно, к ослаблению его влияния на свертывание крови. Для достижения этой цели распределение MB было сужено путем уменьшения доли высокомолекулярной фракции, что привело к увеличению доли среднемолекулярной фракции, большинство молекул которой имеют размер выше порога почечной фильтрации. Более низкая степень замещения, чем у Haes-steril, обуславливает усиленное метаболическое расщепление.47,48 Однако относительно высокое соотношение С2/С6 частично компенсирует этот эффект. В целом, ожидалось, что эти изменения ускорят метаболическое выведение Волювена, сохраняя его фармакодинамические характеристики такими же, как у Haes-steril.
Фармакокинетические свойства Волювена исследовались после однократного и многократного введения. В открытом рандомизированном исследовании с параллельным участием групп6, в котором участвовали 24 здоровых добровольца, были изучены фармакокинетические показатели ГЭК 130/0,4 после однократного введения в виде 6% или 10% раствора. Анализ результатов показал быстрое выведение ГЭК из плазмы крови (ы). Средняя концентрация приближалась к нулю через 24 часа. Время полувыведения препарата в виде 6% раствора в начальной и конечной фазах выведения составило соотв. 0,75 час и 12,8 час. Клиренс препарата в 10% растворе был несколько выше, чем в 6% растворе (соотв. 30,8 и 25,6 мл/мин). Это различие, по-видимому, не имеет клинического значения. Полимеры ГЭК гидролизуются а-амилазой плазмы крови и тканей до более мелких молекул. 10 MB in vivo обоих препаратов был примерно одинаковым и составлял около 65 кДа. Мелкие молекулы ГЭК быстро выводятся. Порог почечной фильтрации составляет 50 кДа. Аналогичный порог фильтрации ранее показан и для других типов ГЭК. После введения ГЭК 130/0,4 в 6% растворе и в 10% растворе выведение с мочой за 72 часа составляет соотв. 62% и 68%. Следует отметить, что выведение препаратов за первые 24 часа минимально. Небольшое количество ГЭК, возможно, сохраняется в тканях. При исследовании накопления ГЭК в тканях крыс с использованием меченного ГЭК установлено, что накопление ГЭК 130/0,4 на 50-75% меньше, чем накопление Haes-steril (рисунок 4).
Для изучения фармакокинетических характеристик и безопасности 130/0,4 (10%) было спланировано соответствующее открытое несравнительное исследование с участием добровольцев, которым ежедневно в течение 10 последовательных дней вводили 500 мл ГЭК. Каждая инфузия длилась 30 минут. Как и ожидалось, исходя из исследований однократного применения препарата, ГЭК быстро выводился из плазмы крови. На 1-й и 10-й дни введения препарата в моче обнаруживалось соотв. 69 и 70% введенной дозы. Время полувыведения, рассчитанное путем фармакокинетического моделирования, в двух фазах выведения составило 1,1 час и 8,3 часа. Расчетный клиренс в плазме крови в 1-й и 10-й дни введения составил соотв. 23,9 и 22,0 мл/мин. Это различие недостоверно. В заключение можно сказать, что клинически значимого накопления ГЭК 130/0,4 (10%) в плазме крови не обнаружено. Эти данные существенно отличаются от тех, что были получены ранее для других типов ГЭК.
Для оценки фармакодиамики ГЭК 130/0,4 было проведено открытое нерандомизированное клиническое исследование с участием 12 здоровых добровольцев, которым вводили препарат два раза. Целью этого исследования была оценка влияния ГЭК 130/0,3 в виде 6% или 10% раствора на объем крови и плазмы крови. В первом случае добровольцам вводили 500 мл ГЭК 130/0,4 (10%) как дополнительную гиперволемическую нагрузку, а во втором случае сначала создавали умеренную гиповолемию путем флеботомии и отбора 500 мл крови, а затем вводили 500 мл ГЭК 130/0,4 (6%). Гиперволемическое введение ГЭК 130/0,4 (10%) привело к увеличению объема плазмы крови; относительный объем крови и плазмы крови увеличился в среднем на 20% (максимум на 32%). Среднее максимальное увеличение объема плазмы крови по сравнению с исходным составило 1,13 литра через 0,75 часа после инфузии. Увеличение объема крови наблюдалось в течение 6 часов после инфузии. Во втором случае добровольцам вводили ГЭК 130/0,4 для компенсации умеренной гиповолемии. Среднее максимальное увеличение объема плазмы крови по сравнению с исходным составило 0,70 литра через 30 минут после инфузии. Относительный объем крови и плазмы крови увеличился в среднем на 7% (максимум на 21%). Увеличение объема плазмы крови было сопоставимо с объемом введенного препарата, продолжалось 6 часов и затем возвращалось к исходному уровню.
По сравнению с другими типами ГЭК, ГЭК 130/0,4 выводится очень быстро. Начальная фаза выведения из плазмы крови происходит в течение 30-45 минут, а конечная - в течение примерно 12 часов. Поэтому можно предположить, что при многократном введении не происходит клинически значимого накопления препарата. Несмотря на быстрое выведение и низкую концентрацию ГЭК 130/0,4 (6% и 10%) в плазме крови, увеличение объема плазмы крови длится дольше, чем ожидалось. Это может объясняться более высоким количеством молекул среднего размера, что повышает коллоидное осмотическое давление in vivo. Кроме того, ожидается, что меньший средний молекулярный вес молекул, находящихся в плазме крови, обусловит меньшее влияние на свертывание крови.
Было проведено исследование для оценки частоты случаев гиповолемии у больных, подвергающихся операциям резекции тканей с возможностью переливания крови. Учитывая возможную потребность в переливании крови, проводился предоперационный отбор собственной крови больного. Одновременно с отбором крови больным вводили соответствующее количество ГЭК 130/0,4 или ГЭК 200/0,5, причем последний считается стандартным средством для таких ситуаций. Эта ситуация моделирует лечение слабой длительной потери крови и также соответствует острому нормоволемическому разбавлению крови, которое обычно проводится непосредственно перед операцией для экономии запасов крови больного. Важно отметить, что расчетный объем крови в двух группах больных был одинаков. В процессе исследования не выявлено различия между группами больных по основному регистрируемому показателю, т.е. частоте развития гиповолемии и клинических симптомов.
Было также проведено клиническое исследование с участием больных, подвергавшихся кардиологическим операциям. Это исследование было сконцентрировано на возможности применения высоких доз ГЭК 130/0,4 для поддержания объема крови в ходе операций. Максимально допустимая доза препарата составляла 3000 мл, что превышает разрешенную в настоящее время в большинстве стран ЕС максимальную суточную дозу ГЭК 200/0,5 (6%). При необходимости введения большего количества ГЭК вводили Haes-steril 6% или раствор нефракционированных белков плазмы крови. Для обеспечения свертывания крови в любое время разрешалось вводить свежезамороженную плазму (СЗП). Основным показателем эффективности являлся общий объем коллоидного раствора, необходимый для поддержания объема крови. Введение коллоидов осуществляли по заранее определенной схеме, включавшей весь период операции. Решение о введении коллоида принимали на основании мнения исследователя, учитывая показатели гемодинамики и баланс жидкости. При использовании ГЭК 130/0,4 по сравнению с ГЭК 200/0,5 общий введенный объем коллоида был немного выше (соотв. 2913 и 2884 мл, отличие недостоверно). 12 больных получили ГЭК 130/0,4, в количестве более 33 мл/кг веса тела/сут, или более 2 г/кг/сут. Максимальная введенная доза составила 42,9 мл/кг/сут. Что касается баланса жидкости, то у больных, получавших ГЭК 200/0,5, по сравнению с ГЭК 130/0,4 был больше объем введенной жидкости, и объем выведенной жидкости был тоже больше. Таким образом, суммарный баланс жидкости в двух группах больных был сопоставим. Анализ гемодинамики показал сходные характеристики в двух группах больных. Изучение показателей свертывания крови не выявило большого различия между группами, за исключением более выраженного удлинения частичного протромбинового времени при применении 200/0,5, более выраженного послеоперационного повышения концентрации фактора Виллебранда при применении ГЭК 130/0,4, а также ослабления агрегации тромбоцитов при применении 200/0,5, которое при применении ГЭК 130/0,4 не наблюдалось. Эти результаты подтверждают идею о том, что ГЭК 130/0,4 слабее влияет на гемостаз, чем ГЭК 200/0,5. В заключение, можно утверждать, что в данных клинических условиях оба исследуемых препарата одинаково эффективны в течение длительного времени.
Было также проведено другое рандомизированное исследование с двойным слепым контролем для сравнения эффективности ГЭК 130/0,4 и ГЭК 200/0,5 как плазмозамещающих препаратов у больных, подвергавшихся крупным ортопедическим операциям с ожидаемым объемом потери крови более 2000 мл. В исследование было включено 52 больных, которые были равномерно распределены в две группы, получавшие разные ГЭК. Согласно полученным результатам, исследуемые препараты (ГЭК 130 и ГЭК 200) применялись в одинаковых количествах (соотв. 1958 и 1962 мл). Однако объем введения альбумина больным, получавшим ГЭК 200/0,5, был значительно выше. Кроме того, один больной получал коммерческий ГЭК 200/0,5. Таким образом, общий объем введенных коллоидов у больных, получавших ГЭК 130/0,4 и ГЭК 200/0,5, составил соотв. 2019 мл и 2188 мл. Измерение концентрации и молекулярного веса ГЭК в плазме крови в течение 24 часов, как и ожидалось, показало более низкий MB in vivo и более быстрое выведение ГЭК 130/0,4 по сравнению с ГЭК 200/0,5. Эти данные сви детельствуют о том, что благодаря более низкому MB in vivo Волювен при более низкой концентрации в крови может обеспечивать такое же увеличение объема плазмы крови, как и Haes-steril.
Рисунок 5.
Замещение объема крови в процессе крупных ортопедических операций: новый гидроксиэтил-крахмал ГЭК 130/0,4 может снижать потерю крови
|
Общая потеря крови (мл) |
Эритроцитарная масса (мл) |
|
|
ГЭК 130 |
2151 + 1496 |
888 + 787 |
|
ГЭК 200 |
2821 + 2306 |
1221 + 1201 |
Потеря крови и потребность в переливании крови в процессе ортопедических операций у больных, получавших ГЭК 130/0,4 или ГЭК 200/0,5. Тенденция не достигает уровня статистической значимости
Наконец, было проведено многоцентровое рандомизированное исследование применения ГЭК в условиях ортопедических операций. В этом исследовании участвовали 100 больных с ожидаемым объемом потери крови более 2000 мл.
Больных случайным образом распределяли в группы, получавшие Волювен или Haes-steril. Это исследование подтвердило эквивалентность двух препаратов по показателю эффективности замещения объема крови (соотв. 1960 и 1928 мл). У больных, получавших Волювен, по сравнению с Haes-steril в послеоперационном периоде был значительно выше уровень фактора Виллебранда, а у больных, получавших Haes-steril, было удлинено частичное протромбиновое время, в то время, как у больных, получавших Волювен, этот показатель оставался нормальным. Интересно, что у больных, получавших Волювен, по сравнению с Haes-steril наблюдалась тенденция к меньшей потере крови (соотв. 2151 + 1496 мл и 2821 + 2306 мл). Эта тенденция не достигала уровня статистической значимости и сопровождалась более низкой потребностью в переливании растворов (рисунок 5).
ЗАКЛЮЧЕНИЕ
Гидроксиэтилкрахмалы - это синтетические коллоиды, обладающие фармакологическими свойствами, наиболее близкими к свойствам природных коллоидов. Имеются данные, подтверждающие возможность применения гидроксиэтилкрахмалов у больных, находящихся в отделениях реанимации и интенсивной терапии. Благоприятный эффект этих препаратов, по-видимому, больше связан с их влиянием на процесс воспаления, чем с создаваемым ими коллоидным осмотическим давлением. При анализе риск/выгода применения гидроксиэтилкрахмалов следует также учитывать их побочные эффекты. При использовании гидроксиэтилкрахмалов с низким MB in vivo побочные эффекты немногочисленны. Раствор гидроксиэтилкрахмала третьего поколения Волювен, по-видимому, имеет некоторые четкие преимущества перед препаратом Haes-streril. При одинаковом увеличении объема плазмы крови накопление этого препарата в плазме крови и тканях значительно снижено. Также существенно слабее нарушается свертывание крови и наблюдается тенденция к меньшей потере крови и потребности в переливании кровезаменителей.
Основные положения
1. Гидроксиэтилкрахмал - это полимер глюкозы, характеризуемый средним молекулярным весом, степенью гидроксиэтилирования и соотношением С2/С6.
2. MB in vivo зависит от исходного MB, степени гидро-ксиэтилирования и соотношения С2/С6. Чем выше значения этих трех параметров, тем выше MB in vivo
3. MB in vivo является основным показателем для оценки коллоидного осмотического давления, фармакокинетики, накопления в плазме крови и тканях, а также побочного действия на свертывание крови и функции почек.
4. Гидроксиэтилкрахмалы с низким MB in vivo (Haes-steril или Heafusine) оказывают слабое влияние или не влияют на гемостаз даже при многократном введении в течение 10 дней.
5. При применении практически всех коллоидов, включая желатины, декстраны, крахмалы и концентрированный альбумин, отмечены случаи острой гиперонкотической почечной недостаточности. В случае крахмалов развитие этого синдрома теоретически может усиливаться при повторном введении гидроксиэтилкрахмалов с высоким MB in vivo.
6. Иммунологическая инертность гидроксиэтилкрахмалов очень высока. Частота аллергических реакций при их применении ниже, чем при применении декстранов и желатинов.
7. ГЭК 130/0,4 Волювен - это среднемолекулярный гидроксиэтилкрахмал со следующими физико-химическими характеристиками: MB in vitro 130 + 20 кДа, степень замещения 0,4, отношение С2/С6 более 8.
8. Волювен, по-видимому, имеет некоторые важные преимущества перед препаратом Haes-streril. При одинаковом увеличении объема плазмы крови накопление этого препарата в плазме крови и тканях значительно снижено. Также существенно слабее нарушается свертывание крови и наблюдается тенденция к меньшей потере крови и потребности в переливании кровезаменителей.
