Применение нимесулида в педиатрической практике: кто «за»?
СтатьиИ.П. Никишина1, С.Р.Родионовская1, В.А.Малиевский2, Г.В.Перчаткина3, И.Н.Цымбал3, А.Н.Шаповаленко1
1ГУ Институт ревматологии РАМН (г. Москва); Республиканская детская клиническая больница МЗ республики Башкортостан (г. Уфа), 3Детская клиническая больница №38 - центр экологической педиатрии федерального медико-биологического агентства России (г. Москва).
Цель настоящего исследования: ретроспективный анализ эффективности и безопасности длительного применения нимесулида у детей с ювенильными артритами.
Материал и методы. Исследование выполнено на базе трех учреждений ревматологического профиля, включило 647 больных с различными нозологическими формами ювенильных артритов, получавших препарат нимесулида (Найз®) в дозах 3-5 мг/кг.
Результаты. 25,7% пациентов были в возрасте 1,5-5 лет; 36,6% - в возрасте 6-11 лет; 37,7% - 12-18 лет. 61% больных получали нимесулид в сочетании с базисными препаратами, в т.ч. 42,5% - метотрексатом. Продолжительность непрерывного приема составила 1-65 месяцев, 80% пациентов принимали препарат более 3 месяцев, а 25% -более 1 года. Эффективность нимесулида у 81% больных была сопоставима с эффектом других НПВП. Побочные реакции зарегистрированы у 25 больных (3,8%), преимущественно аллергические и диспептические симптомы. Только у 2 больных отмечалась умеренная гиперферментемия.
Заключение. Полученные данные, свидетельствующие об оптимальном профиле эффективность/безопасность нимесулида при длительном приеме у детей, позволяют рассматривать препарат как предпочтительную альтернативу в ряду НПВП.
Ключевые слова: нестероидные противовоспалительные препараты, нимесулид, ювенильные артриты, безопасность фармакотерапии в педиатрии.
Введение.
В настоящее время, когда благодаря очевидным успехам современной науки синтезируется много высокоэффективных лекарственных средств и аптечный рынок интенсивно пополняется новыми продуктами отечественной и зарубежной фармацевтической промышленности, первостепенное значение при выборе препарата приобретают аспекты безопасности фармакотерапии, особенно в педиатрии. Вопросам мониторирования и предупреждения побочных эффектов лекарственных средств посвящено большое количество серьезных научных исследований, в том числе эпидемиологических, а также публикаций, представляющих эмоциональную оценку авторов. Примером таких дискуссий в зарубежной, а теперь и в отечественной медицинской литературе явились публикации, посвященные применению нимесулида [1,2,3,4,5,6,7,8,9,10,11]. Наряду с объективной информацией и тщательным анализом отдельных наблюдений серьезных побочных реакций, развившихся преимущественно у лиц пожилого возраста [1,2,7,12,13], стали появляться высказывания, прямо противоречащие научным данным. Так, в недавно вышедшем номере отечественного педиатрического журнала [9] нимесулид был назван «самым токсичным из всех нестероидных противовоспалительных препаратов», что никак не может соответствовать принципам доказательной медицины.
Нестероидные противовоспалительные препараты (НПВП) - большая группа лекарственных средств, нашедших свое широкое применение в различных областях медицины благодаря уникальному сочетанию противовоспалительного, жаропонижающего и анальгетического действия. Показаниями к применению НПВП у детей являются различные состояния, сопровождающиеся болью, лихорадкой и воспалением при инфекционных заболеваниях, болезнях и травматических повреждениях, невралгиях, альгодисменорее, головной и зубной боли, а также использование в качестве компонента предоперационной и послеоперационной анальгезии. Примечательно, что НПВП могут традиционно использоваться в педиатрической практике и вне перечисленных показаний, так, например, известно, что ранее индометацин применялся в неонатальном периоде у детей с открытым артериальным протоком. Среди несколько неожиданных позитивных эффектов НПВП, обнаруженных сравнительно недавно, способность НПВП подавлять митотическую активность клеток и сдерживать развитие плоскоклеточного рака. Тем не менее, к числу основных «желательных» действий НПВП можно отнести только три -противовоспалительный, жаропонижающий и анальгетический эффект. Именно эти фармакологические свойства НПВП, доказанные на стадии предрегистрационных клинических испытаний, являются основанием для регистрации этих лекарственных средств к применению в клинической практике и исключение какого-либо из показаний должно иметь достаточно весомые мотивы.
Врачами практически всех медицинских специальностей широко используются НПВП в качестве эффективного симптоматического средства, но только ревматологи и педиатры, занимающиеся лечением ревматических заболеваний у детей, обладают уникальным опытом и исчерпывающей информацией о применении НПВП в клинической практике. Только при ревматических заболеваниях НПВП применяются в высоких дозах, длительно (в течение многих месяцев и лет), часто в условиях полипрагмазии и у больных, имеющих полиорганное поражение. Трудно представить, чтобы именно у этой категории больных переносимость НПВП была лучше, чем у изначально здоровых детей, получавших НПВП с симптоматической целью в невысоких дозах, однократно или в течение очень непродолжительного времени. В этой связи сведения о профиле безопасности нимесулида у детей с ревматическими заболеваниями, особенно ювенильными артритами, может дать обоснованный ответ на вопрос, действительно ли нимесулид является очень токсичным препаратом, чтобы обсуждать необходимость «срочно отозвать лицензию»[9], либо такие требования не имеют достаточных оснований. Вышеизложенное свидетельствует об актуальности проведения ретроспективного анализа эффективности и переносимости нимесулида при длительном применении у детей с ювенильными артритами, что и послужило целью настоящего исследования.
Материал и методы исследования.
Исследование было выполнено на базе трех учреждений, где осуществляется лечение ревматических заболеваний у пациентов детского возраста: 1)детского отделения (руководитель отделения проф. Н.Н. Кузьмина) ГУ Института ревматологии РАМН (ГУ ИР), 2) кардиоревматологического отделения (зав. отделением Р.М. Салимова) Республиканской детской клинической больницы МЗ республики Башкортостан (РДКБ РБ), 3)отделения болезней крови и ревматических заболеваний (зав. отделением к.м.н. И.Н.Цымбал) Детская клинической больницы №38 - центр экологической педиатрии федерального медико-биологического агентства России (ДКБ38). Исследование проводилось путем изучения медицинской документации и анкетирования врачей (всего в анкетировании приняло участие 15 врачей указанных учреждений) и включило данные о 647 больных, получавших препарат нимесулида с торговым названием Найз® (д-р Редди'с Лабораторис Лтд.). В ГУ ИР - в исследование были включены все больные, проходившие стационарное лечение и впоследствии наблюдавшиеся амбулаторно, а также большинство «диспансерного» контингента пациентов (всего 426 больных); в РДКБ РБ - все пациенты, вошедшие в республиканский регистр больных ювенильными артритами (всего 101); в ДКБ38 - все больные, получавшие лечение в отделении (всего 120).
Изучению были подвергнуты данные о возрасте больных, диагнозе ревматического заболевания, фармакологическом анамнезе (сведения о сопутствующей терапии базисными препаратами; предшествующем приеме других НПВП и спектре вызванных ими побочных реакций), диапазоне используемых доз, продолжительности приема препарата, причинах его отмены, всех неблагоприятных реакциях, развившихся на фоне приема Найза®.
Результаты исследования.
В результате проведенного анализа было установлено, что среди 647 пациентов, получавших Найз, 166 (25,7%) были в возрасте 1,5-5 лет; 237 (36,6%) - в возрасте 6-11 лет; 241 (37,7%) - 12-18 лет; с некоторыми различиями в возрастном составе больных в разных учреждениях (рисунок 1). Распределение больных в зависимости от конкретных нозологических форм ювенильных артритов представлено в таблице 1. Если в ГУ ИР и РДКБ РБ существенную долю из всех пациентов составляли больные ювенильным ревматоидным артритом, наиболее тяжелым суставным заболеванием детского возраста, характеризующимся полиартикулярным, часто генерализованным поражением суставов и высокой частотой системных проявлений, то среди пациентов ДКБ38 наиболее многочисленной была группа больных реактивными артритами.
Таблица 1.
Распределение больных по нозологическим формам ювенильных артритов
| Диагноз ревматического заболевания | Количество больных (%) | |||
| ГУ ИР | РДКБ РБ | ДКБ38 | ВСЕГО | |
| Ювенильный ревматоидный артрит | 159 (37,3 %) | 41 (40,6 %) | 15 (12,5 %) | 215 (33,3 %) |
| Ювенильный хронический артрит/ ювенильные спондилоартриты | 236 (55,4 %) | 60 (59,4 %) | 49 (40,8 %) | 345 (53,3 %) |
| Реактивные артриты | 31 (7,3% ) | 0 | 56 (46,7 %) | 87 (13,4 %) |
Рисунок 1.
Возрастной состав больных ювенильными артритами, получавших терапию нимесулидом (Найзом®) 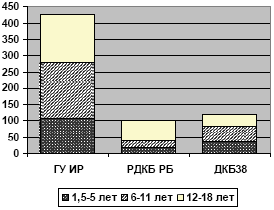
Обращают внимание некоторые особенности фармакологического анамнеза, представленные в таблице 2, в частности, очень высокий процент пациентов, получавших одновременно с нимесулидом базисную терапию, в т.ч. такой гепатотоксичный препарат как метотрексат. Кроме того, довольно часто (у каждого 5-го пациента) в анамнезе регистрировались побочные эффекты других НПВП (аллергические реакции, гастропатии, гепатопатии, декомпенсация бронхиальной астмы, гематурия, цефалгии, головокружение) преимущественно на фоне приема диклофенака натрия, индометацина, ибупрофена, кетопрофена, пироксикама.
Таблица 2.
Фармакологический анамнез больных, получавших терапию нимесулидом (Найзом®)
Количество больных (%) |
||||
| ГУ ИР | РДКБ РБ | ДКБ38 | ВСЕГО | |
Терапия базисными препаратами одновременно с приемом нимесулида
|
256 (60,1 %) 187 (43,9 %) |
92 (91,1 %) 68 (67,3 %) |
46 (38,3 %) 20 (16,7 %) |
394 (60,9 %) 275 (42,5 %) |
Предшествующий терапии нимесулидом прием других НПВП в т.ч. побочные эффекты других НПВП |
297 (69,7 %) 102 (23,9 %) |
60 (59,4 %) 13 (12,9 %) |
44 (36.7 %) 19 (15.8 %) |
401 (62%) 134 (20,7 %) |
У ряда больных отмечались серьезные коморбидные состояния, способные оказать потенциально неблагоприятное влияние на переносимость нимесулида: язвенная болезнь желудка и 12-перстной кишки или множественные эрозии гастродуоденальной зоны - у 38 пациентов; выявление антигена вирусного гепатита В или С - у 14 больных; бронхиальная астма - у 25.
Подавляющее большинство больных принимали нимесулид (Найз®) в достаточно высоких дозах более 4 мг/кг, особенно пациенты ГУ ИР и ДКБ38 (рисунок 2). Продолжительность непрерывного приема нимесулида (Найза®) варьировала в диапазоне от 1 до 65 месяцев (медиана 8 месяцев), при этом 80% пациентов принимали препарат более 3 месяцев, а 25% - более 1 года (рисунок 3). Согласно оценке лечащих врачей эффективность нимесулида (Найза®) у 81% больных была сопоставима с эффектом ранее применяемых других НПВП или выше таковой (рисунок 4). У подавляющего большинства детей терапия нимесулидом продолжается до настоящего времени или была отменена вследствие достижения стойкого положительного эффекта. Только у 20 больных (3,1%) причиной отмены препарата стала его недостаточная эффективность и у такого же количества больных - побочные эффекты. Всего побочные реакции в нашем исследовании были зарегистрированы у 25 больных, т.е. с частотой 3,8% (таблица 3).
Таблица 3.
Побочные реакции на фоне терапии нимесулидом (Найзом®)
| Характер побочных реакций | ГУ ИР | РД КБ РБ | ДКБ 38 | ВСЕГО | Причина отмены |
| Кожные аллергические реакции | 2 | 2 | 3 | 7 | 7 |
| Диспептические жалобы | 5 | 2 | 3 | 10 | 7 |
| Повышение трансаминаз (до 2,5 норм) | 2 | 0 | 0 | 2 | 2 |
| Изменения показателей периферической крови | 1 | 0 | 1 | 2 | 2 |
| Отечный синдром, тенденция к олигурии | 4 | 0 | 0 | 4 | 2 |
| ВСЕГО: | 14 | 4 | 8 | 25 | 20 |
Рисунок 2.
Распределение больных в зависимости от применявшейся дозы нимесулида (Найза®) 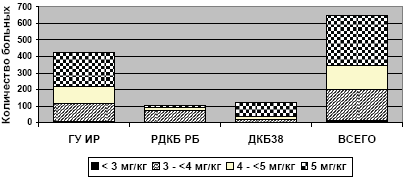
Рисунок 3.
Продолжительность непрерывного приема нимесулида (Найза®)
А)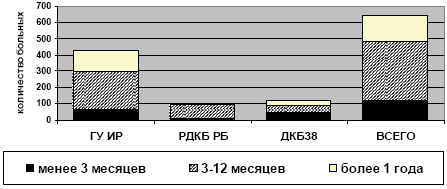
Б)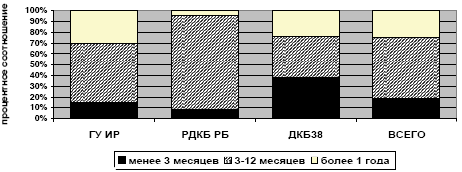
Рисунок 4.
Сопоставление эффективности нимесулида (Найз®) с эффективностью предшествующего приема других НПВП у 401 пациента по оценке врача 
Спектр побочных реакций включал: умеренные диспептические явления преимущественно на прием суспензии, при этом не отмечено развития эрозий и язв слизистой оболочки желудка и 12-перстной кишки. У двух детей зарегистрировано небольшое (1,5-2,5 раза) повышение трансаминаз, причем у одного ребенка с тяжелым системным вариантом ювенильного ревматоидного артрита после нормализации уровня печеночных ферментов прием препарата был возобновлен с хорошей переносимостью. Следует подчеркнуть, что не было обнаружено гиперферментемии у всех 14 детей, инфицированных вирусами гепатита В и С. Минимальный отечный синдром с тенденцией к олигурии при нормальных анализах мочи, уровне креатинина крови и клубочковой фильтрации, был отмечен у 4 детей (девочек подросткового возраста).
В одном наблюдении отмечалась гематологическая реакция в виде тенденции к лейкопении, анемии и выраженного палочкоядерного сдвига без нейтрофилеза. Еще в одном наблюдении была зарегистрирована умеренная анемия, связь которой с приемом Найза® представлялась маловероятной. Напротив, у одного пациента с системным вариантом ювенильного ревматоидного артрита, перенесшего в анамнезе тяжелый агранулоцитоз на фоне применения диклофенака в сочетании с однократным внутримышечным введением анальгина, длительный (более 2 лет) прием Найза® не сопровождался развитием каких-либо побочных реакций.
За исключением отечного синдрома, выявлявшегося исключительно у девочек-подростков, ассоциаций в частоте развития побочных реакций с полом и возрастом пациентов не установлено.
Все неблагоприятные реакции были быстро обратимыми, устранялись при необходимости отменой препарата и не требовали применения дополнительных средств.
Обсуждение.
Представленный нами ретроспективный анализ эффективности и безопасности нимесулида при длительном применении у детей с ювенильными артритами показывает очевидную необоснованность серии публикаций, посвященных применению нимесулида и определяющих этот препарат как «опасный» и «самый токсичный» из НПВП [9]. Полученные нами данные показывают, что даже в условиях очень длительного непрерывного приема, полипрагмазии и серьезных коморбидных состояний (язвенная болезнь, инфицированность вирусами гепатита В или С, бронхиальная астма) частота развития неблагоприятных эффектов на фоне терапии Найзом® была низкой, а серьезных побочных реакций не наблюдалось.
Определенный интерес представляет случай гематологических изменений, аналогичный наблюдавшимся нами ранее у пациентов, получавших терапию сульфасалазином. Можно предположить, что этот феномен имеет общие патогенетические механизмы, поскольку нимесулид является производным сульфонанилида и, по-видимому, имеет сходные с сульфасалазином побочные эффекты вследствие наличия генетически детерминированного биохимического дефекта и, возможно, медленного типа ацетилирования [2].
Поскольку за последние 2 года отечественная медицинская литература, доклады и лекции на солидных научных форумах изобилуют предостережениями о ассоциированным с приемом нимесулида риске развития фулминантного гепатита, необходимо дать рациональное объяснение полученным нами данным. Почему у детей, получавших нимесулид в дозах 4-5 мг/кг в течение многих месяцев и лет и в сочетании с гепатотоксичным метотрексатом, в том числе инфицированных вирусом гепатита В или С, практически не наблюдалось случаев гепатоксичности? Если исключить такие «ненаучные» объяснения, что природа мудрее нас и если лекарственный препарат действительно необходим, то он хорошо переносится, то ответ, на наш взгляд, может быть только один. При ревматических заболеваниях боль, воспаление и лихорадка является симптомом известного заболевания. Напротив, распространенная в педиатрической практике лихорадка неясного генеза, также как и лихорадка при вирусных инфекциях без соответствующей верификации возбудителя, часто является следствием недиагностированного заболевания, и в случае развития серьезных осложнений, проще объяснить их побочным действием лекарств, чем признанием в том, что генез заболевания остался нераспознанным.
Ответ на следующий вопрос также принципиален для понимания сущности и происхождения беспрецедентной для нашей страны дискуссии о потенциальной токсичности лекарственного препарата - почему в фокусе этих дискуссий оказался нимесулид?
Нимесулид был выпущен на мировой фармацевтический рынок швейцарской компанией разработчиком Helsinn Healthcare в 1985 году, т.е. до начала «эры селективных ЦОГ-2 ингибиторов». Вскоре благодаря революционному научному открытию механизма действия НПВП, заключающемуся в ингибиции фермента циклооксигеназы (ЦОГ), блокирующей синтез простагландинов и, соответственно, их патологических (ЦОГ-2) и физиологических (ЦОГ-1) эффектов, были синтезированы ряд принципиально новых НПВП - селективных ЦОГ-2 ингибиторов со значительно лучшим профилем переносимости, особенно гастроэнтерологической. К этому моменту оказалось, что нимесулид обладает свойствами селективности в отношение ЦОГ-2, невольно составив конкуренцию новым, специально синтезированным с учетом механизма избирательной ингибиции ЦОГ дорогостоящим препаратам, а обладателями лицензии на производство нимесулида стали крупнейшие мировые фармацевтические компании (в т.ч. практически все компании, производящие селективные ЦОГ-2 ингибиторы).
С другой стороны, в связи с практически полным прекращением использования в мировой клинической практике препаратов, содержащих метамизол натрия (анальгина), а также появления многочисленных сообщений о неблагоприятных побочных реакциях на фоне приема ацетаминофена (парацетамола) [14,14,16], все чаще для достижения обезболивающего и жаропонижающего эффекта стали применяться НПВП, в т.ч. нимесулид.
Стремительно возрастающая доля нимесулидов на фармацевтическом рынке НПВП не могла не вызвать обеспокоенности конкурирующих за этот рынок фармацевтических компаний. Возможно из-за этого только с 2000 года спустя 15 лет (!) после разработки и появления нимесулида в аптечной сети, развернулась активная дискуссия среди врачей и организаторов здравоохранения по поводу целесообразности применения нимесулида из-за его потенциальной гепатотоксичности. Ареной для этих дискуссий стали популярные медицинские издания, сначала зарубежные, а теперь и российские, причем анализ публикуемой информации не всегда можно признать объективным. Сторонники ограничения использования нимесулидов в педиатрической практике в качестве аргумента нередко приводят ссылки на литературные источники, в названиях которых присутствуют ключевые слова «гепатотоксичность нимесулидов», хотя содержательная часть статьи свидетельствует об обратном. В качестве примера можно привести очень масштабное исследование, выполненное в Италии Traversa G. С соавт. и опубликованное в печатном варианте и на интернет-сайте BMJ в 2003 под названием «Cohort study of hepatotoxity associated with nimesulide and other nonsteroidal anti-inflammatory drugs» [4]. Исследование было посвящено изучению популяционной частоты гепатотоксических реакций, связанных с приемом нимесулида и других НПВП и охватило 397537 больных, которым были назначены НПВП, а всего проанализировано 2 млн. назначений за период с 1997 по 2001 гг. Суммарная частота гепатопатий составила 29,8 на 100 тыс. пациентов-лет и ассоциировалась в большей степени с другими НПВП (диклофенаком - 39,2 на 100000 пациентов-лет; кеторолаком - 66,8; ибупрофеном - 44,6), чем с нимесулидом (35,3 на 100000 пациентов-лет).
Весьма примечательно, что за 15 лет коммерческого использования нимесулида с 1985 по 2001 гг. была получена информация только о 195 случаях неблагоприятных реакций (из них 123 - серьезных) при том, что этот препарат получало около 304 миллионов пациентов, а частота гепатопатий, возникших на фоне лечения нимесулидом составила 0.1 на 100000. Еще более удивительным является факт, что с 1985 до 1998 г. было известно только о 25 случаях гепатопатий, ассоциированных с приемом нимесулида, а в последующие 3 года это число возросло на 170 случаев [1,6]. Подобная закономерность может объясняться либо обостренным и вниманием к данной проблеме, либо какими-то иными причинами. В числе последних нелишним следует считать то обстоятельство, что последние годы ознаменовались бурным всплеском заболеваемости вирусными гепатитами, причем все более многочисленным и разнообразным становится спектр гепатотропных вирусных агентов, а их массовая диагностика далека до приемлемого уровня.
О явном преувеличении масштабов проблемы НПВП-индуцированных гепатопатий свидетельствуют объективные данные ведущих специалистов-гепатологов [16], по мнению которых НПВП фактически находятся на последнем месте в ряду причин лекарственных поражений печени и во много раз уступают в частоте развития гепатопатий таким распространенным лекарственным средствам как антибиотики, противотуберкулезные и противосудорожные средства. Кроме того, известно, что НПВП-индуцированные гепатопатии относятся к редким непредсказуемым идиосинкразическим побочным эффектам и в значительно большей степени зависят от других факторов, (т.ч. генетических, инфекционных, алиментарных, полипрагмазии, употребления алкоголя и т.д.), нежели от собственно механизма действия НПВП [1,2,4,6,16]. По сравнению с риском развития НПВП-индуцированных гастропатий, которые, как стало известно в последние годы актуальны не только для взрослых ревматологических больных, но и для детей [17,18], риск НПВП-ассоциированного поражения печени минимален. Из этого соотношения следует, что при выборе НПВП преимущества за селективными ЦОГ-2 ингибиторами, в том числе нимесулидом.
Возможное (но не очевидное) гепатотоксическое действие нимесулидов, в частности, описанные в литературе несколько примеров острого гепатита у взрослых пациентов, получавших нимесулид, оказалось в центре внимания детских врачей благодаря серии статей, размещенной на интернет-сайте BMJ. Отдельные материалы этой серии, касающиеся применения нимесулида у детей представляются достаточно тенденциозными, неубедительными и излишне эмоциональными. Так, например, в публикации [10] K. Saha из Университетского медицинского центра в Огайо, США звучит призыв прекратить применение нимесулидов у детей, хотя предлагаемый в качестве альтернативы ацетаминофен (парацетамол) вполне сопоставим с нимесулидом по частоте упоминаемых в литературе гепатологических побочных реакций. В России сторонники ограничения применения нимесулида в педиатрической практике [8,9] ссылаются на то, что нимесулид не зарегистрирован к применению у детей в США и многих странах Европы, что нельзя считать достаточно весомым аргументом. Следует подчеркнуть, что самый распространенный в России НПВП диклофенак натрия также практически не используется у детей с ревматическими заболеваниями в большинстве стран Европы и Северной Америки [18]. Чаще всего в педиатрической практике в Европейских странах используется напроксен - препарат, который не имеют возможности использовать российские педиатры, поскольку существующие на отечественном фармацевтическом рынке в настоящее время препараты напроксена ограничены в применении у детей до 16 лет и не имеют «детских» лекарственных форм. Относительно спектра применения НПВП в педиатрической практике в США уместно заметить, что в ходе дискуссии на Конгрессе педиатров России в феврале 2005 года известнейший американский профессор педиатр и детский ревматолог из Нью-Йорка T.Lehman, отвечая на вопрос о применении нимесулида у детей, сказал, что чаще всего использует из НПВП индометацин. Кроме того, известно, что наиболее популярным из НПВП препаратом для применения у детей в США до сих пор является аспирин, гепатотоксичность которого не вызывает сомнений. Причем, если в отношении нимесулида неблагоприятные гепатологические реакции зафиксированы у взрослых, то развитие синдрома Рейе (тяжелого нарушения функции печени, сопровождающегося ацидозом и энцефалопатией на фоне приема аспирина) наблюдается практически исключительно у детей. Следует также отметить, что в этой же серии статей-откликов на сайте BMJ (BMJ.com) фигурируют и прямо противоположного содержания заметки под названиями «Defending Nimesulide Use!» («Защитим использование нимесулида!») и «Science or Commerce?» («Наука или Коммерция?»), где приводятся данные о, как минимум, 50 наблюдениях развития синдрома Рейе в результате применение не аспирина, а других лекарственных средств и чаще всего парацетамола. По-видимому, в патогенезе синдрома Рейе, как и других серьезных побочных реакций, немаловажную роль играют процессы, связанные с лекарственными взаимодействиями и ответом организма на активную репликацию определенных вирусов. Эти данные подтверждают очевидные факты о том, что практически любой лекарственный препарат, даже самый безопасный может выступить в роли того последнего (но не самого главного) в сложной патогенетической цепи звена, приводящего к неблагоприятным последствиям. Именно поэтому решение о выборе лекарственного препарата в конкретной клинической ситуации должен принимать только грамотный, осведомленный о всех потенциальных последствиях и рисках врач, а безрецептурный прием НПВП возможен только в течение очень ограниченного периода времени и только с использованием препаратов и тех невысоких доз (ацетаминофен 15 мг/кг, ибупрофен 7,5-10 мг/кг), которые признаны безопасными ВОЗ. Именно подтверждение этого положения и было сформулировано на заседании Московского Городского Общества Терапевтов 30.11.2004, которое часто цитируется как аргумент против применения нимесулида. На том общественном мероприятии не было представлено ни одного аргумента против применения нимесулида у детей, хотя содержательная часть дискуссии и то, что такое обсуждение состоялось на заседании общества терапевтов, а не педиатров (например, кардиоревматологической секции) позволяет предположить, что была запланирована иная более категоричная в отношении нимесулида формулировка.
Нельзя согласиться с высказыванием известного профессора-педиатра о том, что «в России имеет место довольно агрессивная рекламная кампания по применению нимесулида...», поскольку нимесулид является рецептурным препаратом и его реклама в средствах массовой информации (СМИ) в отличие от безрецептурных парацетамола и ибупрофена невозможна, поскольку прямо противоречит Российскому законодательству. Надо отметить, что и в научной медицинской литературе публикаций, посвященных применению нимесулида у детей крайне мало и назвать агрессивными можно только те из них, что призывают «срочно отозвать лицензию на лекарственные формы для детей» [9]. Автор прямо противоречит методологическому подходу, представленному им же в другой статье того же номера журнала «Педиатрическая фармакология» [19], посвященной вакцинопрофилактике детских инфекций, где сообщения о случаях развития аутоиммунных заболеваний в хронологической связи с рекомбинантной противовирусной вакциной (патогенетически вполне объяснимое, особенно для ревматологов) предлагается подвергать тщательному научному анализу, а для пропаганды вакцинации привлекать СМИ.
С позиций доказательной медицины данные контролируемых клинических испытаний являются надежным аргументом того, что эффективность нимесулида чаще оказывается выше, чем у парацетамола и ибупрофена, при сопоставимой частоте побочных реакций [15,20,21,22,23,24,25,26]. Например, |в электронных базах данных (Cochrane, PubMed, Toxnet) представлены сведения о 16 контролируемых клинических испытаниях нимесулида у 1254 детей в возрасте от 22 до 140 месяцев, в 9 исследованиях препаратом сравнения выступал парацетамол [20]. В подавляющем большинстве контролируемых клинических испытаний показаниями к назначению являлась лихорадка, а в одном исследовании нимесулид применялся для облегчения симптомов ОРВИ у больных бронхиальной астмой, при которой применение других НПВП противопоказано.
Признанная ВОЗ безопасность парацетамола и ибупрофена послужила основанием для безрецептурного отпуска этих препаратов во многих (но не во всех) странах в первую очередь потому, что эти препараты должны были выступить в качестве альтернативы метамизолу натрия, производство которого было прекращено практически во всех странах (но не в России). Каждый практикующий врач должен понимать, что достоинства лекарственных препаратов почти всегда являются продолжением недостатков и наоборот. Так, ацетаминофен и ибупрофен являются самыми короткодействующими из жаропонижающих и противовоспалительных средств, что обуславливает с одной стороны их относительную безопасность, а с другой стороны в ряде ситуаций - недостаточную эффективность в плане продолжительности действия.
В амбулаторных условиях при обеспечении адекватного врачебного контроля и в стационаре нет никаких оснований ограничивать врача в праве выбора эффективного лекарственного средства, если препарат зарегистрирован к применению у детей и в качестве показания зарегистрировано его жаропонижающее свойство.
Следует подчеркнуть, что список разрешенных к применению у детей НПВП ограничен и включает лекарственные средства, достаточно скомпрометировавшие себя высокой частотой неблагоприятных побочных реакций, особенно НПВП-индуцированных гастропатий. Длительное время считалось, что тяжелые эрозивно-язвенные поражения верхних отделов ЖКТ не характерны для детей и только по мере активного внедрения эндоскопического метода исследования ЖКТ в повседневную ревматологическую практику стало очевидным, что НПВП-гастропатии развиваются в детском возрасте практически с той же частотой (20-30%) [17,18], что у взрослых. Рациональный подход к выбору НПВП для длительного приема у детей с ревматическими заболеваниями предусматривает предпочтение препаратам с меньшей ульцерогенностью и в этом смысле преимущества селективных ЦОГ-2 ингибиторов неоспоримы.
В перечень НПВП, регистрация которых допускает их использование у детей с незначительными возрастными ограничениями, входят ибупрофен, индометацин и только 2 препарата нимесулида (Найз® и Нимулид®), разрешенных к применению с 2-летнего возраста. Отдельные лекарственные формы диклофенака натрия в зависимости от конкретного торгового названия разрешены к применению у детей старше 6, 12, 15 или 18 лет. Селективный ЦОГ-2 ингибитор мелоксикам разрешен к применению у детей старше 15 лет, многие новые НПВП - только после 18 лет. В этой связи уместно отметить, что препарат Найз® в 2004 году успешно прошел процедуру перерегистрации, а за предшествующие 5 лет его использования на отечественном фармацевтическом рынке не было зарегистрировано серьезных неблагоприятных побочных реакций, индуцированных этим препаратом.
Заключение.
Анализ данных литературы и успешный опыт длительного применения у детей с ювенильными артритами позволяет рассматривать Найз® на сегодняшний день, как одну из предпочтительных альтернатив в ряду НПВП, объективно оценивая все свидетельства «за» и «против» его применения у детей.
Среди аргументов в пользу использования Найза® у детей:
1) основания, регламентирующие возможность применения у детей, начиная с 2-летнего возраста;
2) существование лекарственных форм, предназначенных для детей и обеспечивающих возможность оптимального дозирования;
3) достаточная эффективность в качестве противовоспалительного средства у детей с ревматическими заболеваниями
4) преимущественная ингибиция ЦОГ-2, обеспечивающая меньшую по сравнению с «традиционными» НПВП гастротоксичность и нефротоксичность;
5) установленное для нимесулидов антигистаминное и антибрадикининовое действие, позволяющее рассматривать препарат как «препарат выбора» у детей с аллергической предрасположенностью и бронхиальной астмой;
6) доказанный на экспериментальных моделях хондропротективный эффект нимесулида, актуальный для детского возраста с учетом повышенной уязвимости хрящевой ткани ребенка в условиях незавершенности костеообразования.
Это ни в коей мере не противоречит необходимости взвешенного и осторожного подхода к назначению нимесулидов в педиатрической практике с учетом потенциальных рисков медикаментозной терапии, особенно в условиях полипрагмазии и коморбидных состояний, обеспечение надлежащей процедуры врачебного мониторирования безопасности лечения и тщательный анализ всех случаев неблагоприятных побочных реакций. В ответ на поставленный в названии статьи вопрос можно утверждать, что за применение нимесулида у детей выступают ревматологи, т.е. те, кто наиболее в этом вопросе компетентен, так как среди всех представителей педиатрических специальностей обладают наиболее серьезным опытом использования НПВП в повседневной практике. Библиография
1. Каратеев А.Е., Насонова В.А. НПВП-ассоциированная гепатопатия: проблема нимесулидов. Научно-практическая ревматология. 2003, №4, с. 87-91.
2. Boelsterli U.A. Mechanisms of NSAID-induced hepatotoxity. Focus on nimesulide. Drug Safety 2002; 25, 633-648.
3. Fusetti G., Magni E., Armandola M. Tolerability of nimesulide. Epidemiological data. Drugs. 1993; 46, suppl. 1; 277-280.
4. Traversa G., Bianchi C., Da Cas R. et al. Cohort study of hepatotoxity associated with nimesulide and other nonsteroidal anti-inflammatory drugs. BMJ, 2003, 327, 18-22.
5. Conforti A., Leone R, Moretti U, et al. Adverse drug reactions related to the use of NSAIDs with a focus on nimesulide: results of spontaneous reporting from a Northern Italian area. Drug Saf. 2001; 24: 1081-1090.
6. Rainsford KD, Relationship of nimesulide safety to its pharmacokinetics; assessment of adverse reactions. Rheumatology 1999; 38; Suppl.1;4-10
7. Merlani G, Fox M, Oehen HP, et al. Fatal hepatotoxicity secondary to nimesulide. Eur J Clin Pharmacol 2001; 57; 321-326
8. Таточенко В.К. Ребенок с лихорадкой. Лечащий врач. 2005, 1, с.16-20.
9. Таточенко В.К. Опасный жаропонижающий препарат для детей. Педиатрическая фармакология. 2006; 1; с.71-71.
10. Saha K. Use of nimesulide in Indian children must be stopped. BMJ, 2003; 326, 713.
11. Kumar S. Drug linked to child deaths is still available in India. BMJ, 2003; 326,70.
12. Van Steenbergen W, Peeters P, De Bondt J, et al. Nimesulide- induced acute hepatitis; evidence from six cases. J Hepatol, 1998; 29;135-141
13. Weiis P, Mouallem M, Bruck R, et al. Nimesulide induced hepatitis and acute liver failure. Isr Med Assoc J 1999; 1;89-91
14. Clarc WG. Antipyretic therapy: clinical trials 1990 through 1995. In: Mackowiak PA (ed) Fever; basic mechanisms and management, 2nd ed. 1997. Lippincolt raven, Philadelphia, pp 295302
15. Ulukol B, Koksal Y, Cin S. Assessment of the efficacy and safety of paracetamol, ibuprofen and nimesulide in children with upper respiratory tract infections. Eur J Clin Pharmacol 1999; 55; 615-618.
16. Полунина Т.Е. Лекарственные поражения печени. Лечащий врач, 2005, 3, с.8-13.
17. Комелягина Е.Г. Структура гастродуоденальной патологии у детей с ювенильными артритами: клинико-эндоскопическая и морфологическая характеристика. Автореф.... канд. мед. наук. М.- 2004, 21 с.
18. Cassidy J.T., Petty R.E. Textbook of pediatric rheumatology. / Churchill Livingstone, New York etc., - 2001, p. 90-101.
19. Семенов Б.Ф., Таточенко В.К. Иммунопрофилактика детских инфекций: итоги и перспективы. Педиатрическая фармакология. 2006; 1; с.41-44.
20. Gupta P., Sachdev H.P.S. Safety of oral use of nimesulide in children: systematic review of randomized controlled trials. Indian Pediatrics. 2003; 40; 17; p.518-531.
21. Catti A, Monti T. Treatment of infants with acute upper respiratory tract inflammation. A double-blind comparison between nimesulide and paracetamol suppositories. Clinical Trials Journal 1990; 27; 327-335.
22. Gianiorio P, Zappa R., Sacco O., et al. Antipyretic and anti- Inflammatory Efficacy of Nimesulide vs Paracetamol in the Symptomatic treatment of Acute respiratory Infections in Children, Drugs 1993; 46 (Suppl. 1) 204-207.
23. Kapoor SK, Scharma J, Batra B, et al. Comparison of antipyretic effect of nimesulide and paracetamol in children attending a secondary level hospital. Indian Pediatr 2002; 39; 473-477.
24. Lecomte J., Monti T., Pochodradsky M.G., Antipyretic effects of nimesulide in paediatric practice: a double-blind sudy. Current Medical research and opinion; 1991; 12, 296-300.
25. Polidori G., Titti G., Pieragostini P., et al. A Comparison of Nimesulide and paracetamol in the treatment of fever due to inflammatory diseases of the upper respiratory tract in children. Drugs 1993;46 (Suppl 1); 231-233.
26. Ugazio AG, Guarnaccia S, Berardi M, Renzetti I (1993) Clinical and pharmacokinetic study of nimesulide in children. Drugs 46 [suppl] : 215-218
