Метформин пролонгированного высвобождения - новый стандарт лечения сахарного диабета типа 2
СтатьиОпубликовано в журнале:
«ЭНДОКРИНОЛОГИЯ»; № 1; 2015; стр. 19-26.
А.С. Аметов, М. А. Прудникова
ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздрава России, Москва
На сегодняшний день метформин занимает центральное место во всех актуальных рекомендациях по управлению сахарным диабетом типа 2 (СД2). Учитывая эпидемический характер распространенности заболевания, число пациентов, получающих метформин, неуклонно растет день ото дня. В статье описываются клеточные и молекулярные механизмы действия метформина, преимущества его выбора в качестве сахароснижающей терапии у пациентов с СД2, приводятся доводы в пользу использования метформина для профилактики СД2, рассматривается возможность назначения метформина пациентам с умеренными нарушениями функции печени и почек. Недавно была разработана новая лекарственная форма препарата замедленного высвобождения. На фоне приема метформина замедленного высвобождения в 2 раза снижается риск развития желудочно-кишечных расстройств и значительно возрастает приверженность пациентов лечению. В статье приводятся преимущества и недостатки применения пролонгированной формы в сравнении с метформином немедленного высвобождения.
Ключевые слова: сахарный диабет типа 2, метформин, метформин замедленного высвобождения, метформин и рак, фармакокинетика метформина
Prolonged-release Metformin - New Standard Of Medical Care In Type 2 Diabetes Mellitus
A.S. Ametov, M.A. Prudnikova
Russian Medical Academy of Post-graduate Education, Moscow
Metformin is a drug of choice in all existing recommendations of the management of type 2 diabetes today. The number of patients receiving metformin progressively increasing day by day. This article describes the cellular and molecular mechanisms of action of metformin, metformin benefits of choosing as glucose-lowering therapy in patients with type 2 diabetes mellitus, argues the use of metformin for the prevention of type 2 diabetes, the possibility of the use of metformin in patients with moderate impairment liver and kidney function. Recently, a new formulation extended release of the drug has developed. Metformin extended release twice reduces the risk of gastro-intestinal disorders and significantly improves patient compliance. The article presents the advantages and disadvantages of the use of long-acting forms in comparison with metformin immediate release.
Key words: type 2 diabetes mellitus, metformin, extended release metformin, metformin and cancer, pharmacokinetics of metformin
Уровень распространенности сахарного диабета типа 2 (СД2) непрерывно растет, опережая все существующие прогнозы. Согласно эпидемиологическим данным Международной федерации диабета, в 2014 г. СД страдал каждый 12-й житель планеты. К 2035 г. ожидается увеличение числа заболевших до 592 млн человек [1].
Эпидемический характер распространения заболевания послужил поводом для разработки четких алгоритмов управления СД2. Препаратом выбора во всех актуальных на сегодняшний день клинических рекомендациях является метформин - препарат, применяемый для лечения нарушений углеводного обмена вот уже более полувека.
Клеточные и молекулярные механизмы действия метформина
Согласно современным представлениям о клеточных и молекулярных механизмах действия препарата, наибольшую активность метформин проявляет в печени. Захват препарата гепатоцитами опосредован активностью транспортера органических катионов 1.
Ранее полагали, что способность снижать уровень глюкозы в крови обусловлена активацией АМФ-активируемой протеинкиназы, но сейчас доказано, что антигипергликемическое действие метформина связано с высокоспецифичным ингибированием комплекса 1 митохондриальной дыхательной цепи переноса электронов (рис. 1) [2].
Рис. 1. Комплекс 1 дыхательной цепи переноса электронов митохондрий - основная мишень действия метформина [2] 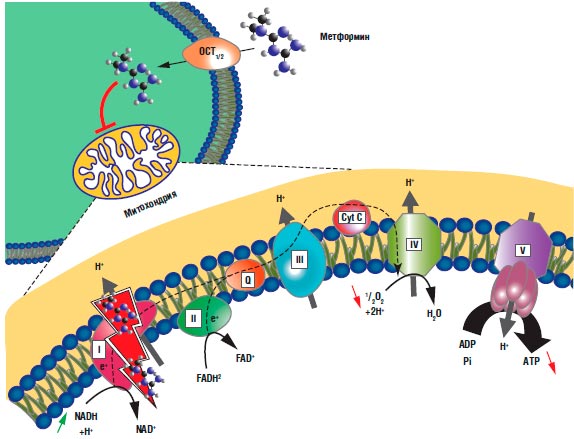
Однако негликемические эффекты метформина (в том числе кардиопротективный, антиатерогенный, гиполипидемический) проявляются именно в результате активации АМФК, что приводит к переключению клетки из анаболического состояния в катаболическое путем закрытия синтетических путей потребления АТФ и восстановления энергетического баланса в клетке, в результате чего подавляются синтез глюкозы, липидов, белков и клеточный рост. При этом стимулируется окисление глюкозы и жирных кислот [3]. Кроме того, на фоне приема метформина увеличивается количество общего циркулирующего в крови глюкагоноподобного пептида-1 (ГПП-1), чем, вероятно, и обусловлена способность препарата снижать массу тела [4].
Метформин в современных рекомендациях по управлению сахарным диабетом типа 2
В настоящее время метформин занимает центральное место во всех актуальных рекомендациях по управлению СД2.
Так, в согласованном алгоритме Американской и Европейской диабетических ассоциаций (ADA/EASD) 2012 г. настоятельно рекомендуется использовать метформин в качестве средства первой линии (при отсутствии противопоказаний или непереносимости), сразу при постановке диагноза СД2, в дополнение к коррекции образа жизни, диетическим рекомендациям и физическим упражнениям. Предпочтение, отдаваемое этому лекарственному средству, не случайно: эффективность и безопасность метформина имеют огромную доказательную базу, стоимость его невысока, но особенно привлекательна способность препарата снижать риск развития кардиоваскулярных осложнений. Метформин в виде монотерапии снижает уровень HbA1c на 1-1,5%. В том случае, если с помощью монотерапии метформином не удается достичь целевых показателей гликемии, в алгоритме ADA/EASD рекомендован переход на комбинированную терапию двумя пероральными сахароснижающими препаратами (ПССП), причем одним из них должен быть метформин (рис. 2) [5].
Рис. 2. Место метформина в актуальных рекомендациях по управлению сахарным диабетом типа 2 на примере согласованного алгоритма ADA/EASD [5]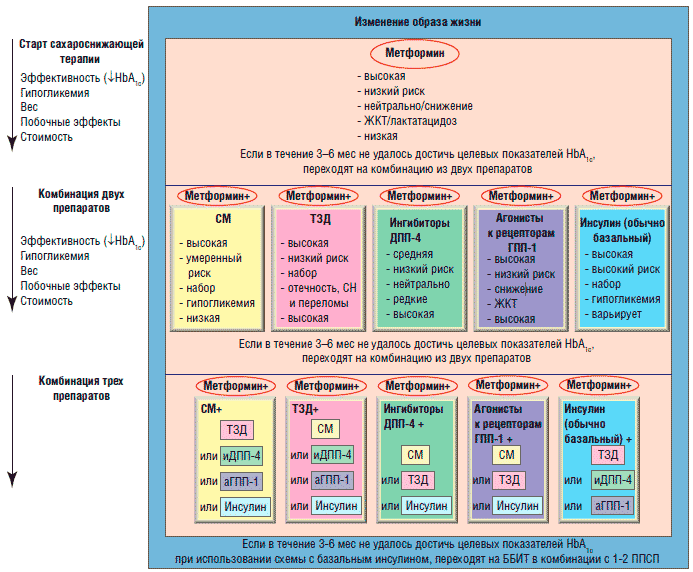
В 2014 г. Американская диабетическая ассоциация выпустила новые рекомендации, но и в них метформин остается самым предпочтительным лекарственным средством для старта сахароснижающей терапии у пациентов с СД2 (уровень доказательности A) [6].
В актуальных на сегодняшний день отечественных Алгоритмах специализированной медицинской помощи больным СД 2013 г. выбор терапии на старте лечения зависит от исходного уровня HbA1c. Метформин в качестве монотерапии рекомендуется использовать при HbA1c 6,5-7,5%, причем в качестве альтернативы ему предлагаются только дорогостоящие препараты инкретинового ряда.
При уровне HbA1c 7,6-9,0% в российских алгоритмах рекомендована комбинированная терапия с указанием на то, что «к наиболее рациональным комбинациям относятся сочетания метформина (базового препарата, снижающего инсулинорезистентность) и препаратов, стимулирующих секрецию инсулина» (рис. 3).
В числе дополнительных преимуществ метформина в отечественных рекомендациях указываются его доступность в составе фиксированных комбинаций препаратов и способность снижать риск развития инфаркта миокарда у лиц с СД и ожирением [7].
Рис. 3. Рациональные комбинации сахароснижающих препаратов на основании отечественных Алгоритмов специализированной медицинской помощи больным сахарным диабетом 2013 г. [7] 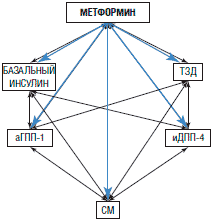
Таким образом, на сегодняшний день метформин при отсутствии противопоказаний и хорошей переносимости является неотъемлемой составной частью терапии СД2 на всех этапах лечения.
Метформин в профилактике сахарного диабета типа 2
Одной из наиболее перспективных областей применения метформина является профилактика СД2. В исследованиях Diabetes Prevention Program (DPP) и Diabetes Prevention Program Outcomes Study (DPPOS) назначение метформина снижало риск развития диабета в меньшей степени, чем модификация образа жизни (31 против 58%). Однако среди женщин с гестационным диабетом в анамнезе терапия метформином приводила к снижению риска развития СД2 на 50% [8]. Кроме того, по результатам дальнейшего наблюдения длительностью 10 лет прием метформина оказался самым экономичным способом профилактики СД2 [9].
Согласно уже упомянутым алгоритмам Американской диабетической ассоциации 2014 г., метформин рекомендован для профилактики диабета у лиц с нарушением толерантности к глюкозе (уровень доказательности A), нарушением гликемии натощак (уровень доказательности Е), с уровнем HbA1c 5,7-6,4% (уровень доказательности Е), а также лицам с ИМТ> 35 кг/м2 в возрасте до 60 лет и женщинам с гестационным диабетом в анамнезе (уровень доказательности A) [6]. В отечественных рекомендациях 2013 г. также допускается назначение метформина лицам с очень высоким риском развития СД в дозах 250-850 мг 2 раза в день (в зависимости от переносимости) особенно это касается лиц моложе 60 лет с ИМТ >30 кг/м2 при отсутствии противопоказаний [7]. Как следствие, применение метформина является надежным и недорогим способом профилактики СД среди пациентов группы риска.
Метформин и ожирение
Согласно данным ВОЗ (2008), около 35% взрослых людей во всем мире страдают от ожирения или избыточной массы тела (ИМТ >25 кг/м2). В частности в Российской Федерации от избыточной массы тела страдают 29,8% женщин и 18,4% мужчин. Это примерно четвертая часть населения, которая подвержена высокому риску развития сердечно-сосудистых заболеваний и нарушений углеводного обмена.
Выбор лекарственных препаратов для снижения массы тела крайне скуден, и метформин в их число формально не входит. Однако в целом ряде исследований показано, что на фоне приема данного препарата наблюдается достоверное снижение массы тела. Так, в метаанализе 31 исследования, проведенного с 1966 по 2006 г. и включившего суммарно данные 4570 пациентов, прием метформина приводил к снижению ИМТ в среднем на 5,3% при средней продолжительности приема 1,8 года [10].
Отчасти способность метформина снижать массу тела обусловлена увеличением плазменных уровней ГПП-1 на фоне его приема. Kappe и соавт. показали, что метформин улучшает секрецию ГПП-1 L-клетками in vitro, поэтому в плазме пациентов, длительно получающих метформин, как правило, отмечаются повышенные уровни ГПП-1 [11].
Кроме того, есть данные о том, что метформин способствует более здоровому распределению жировой клетчатки в организме, в первую очередь снижая долю висцерального жира [12]. Лечение ожирения является одной из наиболее привлекательных для клинициста областей применения метформина, что подтверждает повсеместная практика назначения препарата для снижения массы тела off-label.
Метформин и рак
В ряде доклинических и клинических исследований, связанных с применением метформина, было задокументировано снижение уровня онкологической смертности, что привело к волне интереса к антионкогенным свойствам препарата.
В частности интересен метаанализ 47 независимых исследований и 65 540 случаев рака у пациентов с СД2. Согласно его результатам, на фоне приема метформина риск развития рака любой локализации снижался на 31% [суммарный относительный риск 0,69; 95% доверительный интервал (ДИ) 0,52-0,90], общая смертность от рака снижалась на 34% (суммарный относительный риск - 0,66, 95% ДИ 0,54-0,81; I2=21%) [13].
Способность метформина снижать уровень инсулина в крови, вероятно, играет ключевую роль в его противоопухолевой активности, так как инсулин обладает митогенным эффектом, а для опухолевых клеток характерны высокие уровни рецептора к инсулину, что указывает на потенциальную чувствительность к анаболическим свойствам данного гормона. Кроме того, у метформина есть прямые инсулиннезависимые противоопухолевые эффекты: на фоне его приема увеличиваются соотношение фосфоинозитол-3-киназа/mТОR (mammalian target of rapamycin - протеин-киназа серин-треониновой специфичности), экспрессия транспортера органического катиона-1/2/3, экспрессия LKB1 (liver kinase B1), экспрессия TSC2 (Tuberous Sclerosis Complex 2).
Применение метформина у лиц с онкологическими заболеваниями является перспективным направлением развития современной науки, однако требуются дальнейшие исследования в этой области.
Метформин и хроническая болезнь почек
Пациенты с СД и хронической болезнью почек (ХБП) требуют особого внимания в связи с изменением фармакокинетики и фармакодинамики лекарственных средств и многократно увеличивающимся на этом фоне риском гипогликемии. Проблема заключается и в том, что чаще всего данные пациентов с ХБП исключаются из исследований, поэтому информация о безопасности и эффективности лекарственных препаратов у данной категории пациентов чаще всего отсутствует.
Ранее считалось, что метформин категорически противопоказан пациентам с умеренными и тяжелыми нарушениями функции почек (скорость клубочковой фильтрации -СКФ<60 мл/мин) в связи с высоким риском развития лактатацидоза. Однако в настоящее время это противопоказание пересмотрено, и, согласно новым данным, метформин может назначаться пациентам с СД и ХБП при СКФ>30 мл/мин (по версии некоторых авторов, >45 мл/мин). А вот при использовании препаратов сульфонилмочевины, глинидов и инсулина у данной категории пациентов следует быть крайне осторожными в связи с высоким риском развития гипогликемии [14].
Так, в актуальных британских рекомендациях допускается использование метформина в качестве препарата выбора у лиц с СКФ>30 мл/мин, но при условии частого мониторинга функции почек и коррекции дозы метформина. Канадская диабетическая ассоциация в своих рекомендациях ограничивает дозу метформина для лиц с СКФ 30-60 мл/мин до 850 мг/день [15].
В актуальных российских рекомендациях по управлению СД 2013 г. рекомендовано использование метформина при СКФ>45 мл/мин, но при условии коррекции дозы и контроля показателей, отражающих функцию почек [7].
Таким образом, не подлежит сомнению, что при умеренном снижении функции почек метформин может и должен оставаться препаратом выбора у пациентов с СД2.
Метформин и кардиоваскулярные исходы
Сердечно-сосудистые заболевания продолжают занимать лидирующее положение в структуре смертности пациентов с СД2.
Исследование United Kingdom Prospective Diabetes Study (UKPDS) стало первым, в котором было показано улучшение клинических исходов у пациентов с СД на фоне приема метформина. В нем приняли участие 5102 пациента, которые наблюдались более 20 лет. Согласно полученным результатам, у лиц с избыточной массой тела метформин снижал риск развития ассоциированных с диабетом клинических исходов на 32%, число смертей, связанных с диабетом, - на 42% и общую смертность - на 36% [16]. Даже спустя 10 лет после завершения основного этапа исследования у пациентов, получавших метформин, риск развития ассоциированных с диабетом клинических исходов был ниже на 21%, инфаркта миокарда - на 33%, смерти от любых причин -на 27% [17].
Кардиопротективное действие метформина, вероятно, обусловлено целым рядом эффектов, оказываемых препаратом на сердечную мышцу и сосудистую стенку.
Положительное влияние метформина на эндотелиальную функцию нашло подтверждение в нидерландском исследовании 2013 г., согласно результатам которого прием препарата достоверно снижал уровень таких повреждающих факторов, как фактор Виллебранда, sVCAM-1, тканевой активатор плазминогена, ингибитор активатора плазминогена-1, растворимый Е-селектин, С-реактивный белок, и снижал сердечно-сосудистую заболеваемость и смертность на 34% [18]. В эксперименте на животных моделях было показано, что метформин улучшает метаболизм в сердечной мышце (нормализуя соотношение окисляемых жирных кислот к глюкозе) [19].
Еще совсем недавно не вызывало сомнений, что метформин категорически противопоказан лицам с хронической сердечной недостаточностью в связи с высоким риском развития лактатацидоза. Однако данные недавнего метаанализа, включившего 9 исследований и 34 000 пациентов, свидетельствуют о том, что это противопоказание может быть пересмотрено. Согласно его результатам, метформин достоверно снижает уровень смертности у пациентов с сердечной недостаточностью по сравнению с препаратами сульфонилмочевины [23 против 37%; относительный риск (ОР) 0,80; ДИ 0,74-0,87] [20].
Метформин и повышение уровня печеночных трансаминаз
Неалкогольный стеатогепатит (неалкогольная жировая болезнь печени, жировой гепатоз) занимает центральное место в структуре патологии печени у лиц с метаболическими нарушениями и диагностируется почти у 1/3 взрослого населения в развитых странах. У пациентов с СД2 жировой гепатоз развивается примерно в 4 раза чаще, чем в общей популяции [21].
Ключевую роль в патогенезе стеатогепатита играет инсулинорезистентность, именно поэтому в основе его лечения, помимо модификации образа жизни, лежит назначение препаратов, повышающих чувствительность клеток к инсулину. Среди практикующих эндокринологов существует пагубная практика отмены метформина даже при незначительном превышении нормы уровней АЛТ и АСТ, что с точки зрения гепатолога категорически неверно. Как правило, при жировом гепатозе наблюдается небольшое повышение печеночных трансаминаз - до 3 норм, до этого уровня использование метформина в управлении СД2 не только допустимо, но и необходимо для лечения неалкогольного стеатогепатита [22].
Метформин пролонгированного высвобождения - новые технологии в клинической практике
До недавнего времени очевидные преимущества метформина частично нивелировались высокой частотой развития побочных эффектов со стороны пищеварительного тракта, что приводило к отказу от приема препарата. Это послужило поводом для разработки новой лекарственной формы - метформина замедленного высвобождения (extended-release).
Для того чтобы обеспечить всасывание препарата преимущественно в верхних отделах пищеварительного тракта, в таблетке метформина пролонгированного действия была использована система «гель внутри геля» (GelShield Diffusion System). Метформин содержится в гранулах гидрофильного полимерного матрикса внутренней фазы, которые распределены внутри наружного полимерного матрикса (рис. 4).
Рис. 4. Структура таблетки метформина пролонгированного высвобождения 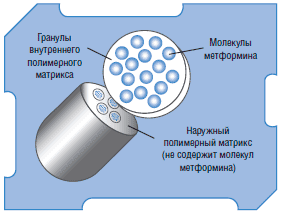
После попадания в желудок верхний гелевый слой впитывает влагу и набухает, в то время как гранулы, содержащие активное вещество, постепенно диффундируют через гелевый барьер, что обеспечивает дозированное высвобождение препарата в верхние отделы кишечника. Более ровный профиль действия с увеличением Tmax (время достижения максимальной концентрации препарата в крови) до 7 ч приводит к снижению частоты развития побочных эффектов на старте терапии с 19,83% случаев при использовании обычных форм метформина до 9,23% случаев при использовании новой формы метформина замедленного высвобождения (р=0,04) [23]. Кроме того, в этом случае можно принимать препарат 1 раз в день, что существенно повышает приверженность терапии.
Однако следует иметь в виду и предупреждать пациентов, что неактивная часть таблетки метформина замедленного высвобождения выводится в неизмененном виде. Иначе это может привести к ошибочным выводам и немотивированному отказу от использования данной лекарственной формы.
Сахароснижающий эффект метформина пролонгированного действия сравним с таковым у метформина немедленного высвобождения. В двойном слепом рандомизированном исследовании, в рамках которого пациенты с недавно диагностированным СД2 получали обычную форму метформина или метформин пролонгированного действия в течение 24 нед, метформин пролонгированного высвобождения снижал HbA1c немного сильнее (-1,06%), чем форма препарата немедленного высвобождения [24].
Метформин пролонгированного высвобождения и триглицериды: есть ли проблема?
В ряде исследований было показано ухудшение показателей липидного обмена в виде небольшого повышения уровня триглицеридов на фоне приема метформина замедленного высвобождения при отсутствии значительного влияния на уровень общего холестерина, ЛПНП или ЛПВП (см. таблицу) [24-26].
Изменение уровня триглицеридов на фоне лечения метформином замедленного и немедленного высвобождения
| Fujioka K. и соавт. (2003), 24 нед лечения | Метформин немедленного высвобождения 500 мг/день | Метформин пролонгированного действия 1000 мг/день | Метформин пролонгированного действия 1500 мг/день |
| Среднее изменение уровня триглицеридов, мг/дл | +1 | +34 | +42 |
| Fujioka K. и соавт. (2006), 16 нед лечения | Метформин немедленного высвобождения 500 мг/день | Метформин пролонгированного действия 1000 мг/день | Метформин пролонгированного действия 1500 мг/день |
| Среднее изменение уровня триглицеридов от исходного, мг/дл | -7 | +16 | +33 |
| Среднее изменение уровня триглицеридов по сравнению с показателями группы плацебо, ммоль/л | ? | +23 | +40 |
| Schwartz S. и соавт. (2006) | Метформин немедленного высвобождения 1500 мг/день | Метформин пролонгированного действия 1500 мг/день | Метформин пролонгированного действия 2000 мг/день |
| Триглицериды, мг/дл: | |||
| - исходный уровень | 186±29,3 | 199±27,7 | 216,2±29,3 |
| - конечный уровень | 181,7±12,2 | 201,2±12,1 | 206,8±12,3 |
Основной механизм и клиническая значимость повышения уровня триглицеридов на фоне лечения метформином пролонгированного действия до сих пор не определены. Однако, как показано в таблице, динамика уровня триглицеридов на фоне приема препарата замедленного действия незначительна, а в исследовании S. Schwartz и соавт. (2006) носит положительный характер.
Заключение
Метформин в течение многих лет является неотъемлемым компонентом терапии СД2, занимая центральное место во всех актуальных клинических рекомендациях по его лечению.
Метформин пролонгированного высвобождения, обладая всеми преимуществами обычной формы препарата, лишен значительной части его недостатков. На фоне его приема отмечаются снижение частоты побочных эффектов со стороны желудочно-кишечного тракта и улучшение приверженности лечению. Сведения о том, что на фоне приема пролонгированной формы препарата повышается уровень триглицеридов, противоречивы и требуют дальнейшего изучения.
Сведения об авторах
Аметов Александр Сергеевич - доктор медицинских наук, профессор, заведующий кафедрой эндокринологии и диабетологии ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздрава России (Москва)
Прудникова Марина Александровна - врач-эндокринолог, аспирант кафедры эндокринологии и диабетологии ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздрава России (Москва)
ЛИТЕРАТУРА
1. Diabetes atlas IDF 2014. 5th ed.
2. Benoit V., Bruno G., Nieves S.G. et al. Cellular and molecular mechanisms of metformin: an overview // Clin. Sci. (Lond.). - 2012. - Vol. 122, N 6. - P. 253-270.
3. Аметов А.С. Сахарный диабет 2 типа. Проблемы и решения. - 2-е изд. - М.: ГЭОТАР-Медиа, 2013. - С. 226246.
4. Maida A., Lamont B.J., Cao X., Drucker D.J. Metformin regulates theincretin receptor axis via a pathway dependent on peroxisome proliferator-activated receptor-(alpha) in mice // Diabetologia. - 2011. - Vol. 54, N 2. - P. 339-349.
5. Management of Hyperglycemia in Type 2 Diabetes: A Patient-Centered Approach Position Statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD) // Diabetes Care. -2012 June. - Vol. 35, N 6. - P. 1364-1379.
6. Standards of Medical Care in Diabetes - 2014 American Diabetes Association doi: 10.2337/dc14-S014 // Diabetes Care. -2014 Jan. - Vol. 37, suppl. 1. - P. S14-S80.
7. Алгоритмы специализированной медицинской помощи больным сахарным диабетом / Под ред. И.И. Дедова, М.В. Шестаковой. - 6-й вып. - М., 2013.
8. Ratner R.E., Christophi C.A., Metzger B.E. et al., Diabetes Prevention Program Research Group. Prevention of diabetes in women with a history of gestational diabetes: effects of metformin and lifestyle interventions // J. Clin. Endocrinol. Metab. - 2008. - Vol. 93. - P. 4774-4779.
9. Diabetes Prevention Program Research Group. The 10-year cost-effectiveness of lifestyle intervention or metformin for diabetes prevention: an intent-to-treat analysis of the DPP/DPPOS // Diabetes Care. - 2012. - Vol. 35. - P. 723730.
10. Krentz A.J. Management of type 2 diabetes in the obese patient: current concerns and emerging therapies // Curr. Med. Res. Opin. - 2008. - Vol. 24. N 2. - P. 401-417.
11. Kappe C., Patrone C., Holst J.J., Zhang Q. Metformin protects against lipoapoptosis and enhances GLP-1 secretion from GLP-1-producing cells // J. Gastroenterol. - 2013. - Vol. 48, N 3. - P. 322-332.
12. Kurukulasuriya R., Banerji M.A., Chaiken R., Lebovitz H. Selective decrease in visceral fat is associated with weight loss during metformin treatment in African Americans with type 2 diabetes // Diabetes. - 1999. - Vol. 48. - P. A315.
13. Gandini S., Puntoni M., Heckman-Stoddard B.M. et al. Metformin and Cancer Risk and Mortality: A Systematic Review and Meta-analysis Taking into Account Biases and Confounders // Cancer Prev. Res. (Phila.). - 2014. - Vol. 7, N 9. -P. 867-885.
14. Ioannidis I. Diabetes treatment in patients with renal disease: Is the landscape clear enough? // World J. Diabetes. - 2014 Oct 15. - Vol. 5, N 5. - P. 651-658. doi: 0.4239/wjd.v5.i5.651.
15. Inzucchi S.E., Lipska K.J., Mayo H. et al. Metformin in patients with type 2 diabetes and kidney disease: a systematic review // JAMA. - 2014. - Vol. 312, N 24. - P. 26682675.
16. UK Prospective Diabetes Study (UKPDS) Group. Effect of intensive blood-glucose control with metformin on complications in overweight patients with type 2 diabetes (UKPDS 34). UK Prospective Diabetes Study (UKPDS) Group // Lancet. - 1998. - Vol. 352. - P. 854-865.
17. Мельникова О.Г. Британское проспективное исследование сахарного диабета (UKPDS) — результаты 30-летнего наблюдения больных сахарным диабетом 2 типа // Сахар. диабет. - 2008. - № 4. - С. 90-91.
18. Jager J., Kooy A., Schalkwijk C. et al. Long-term effects of metformin on endothelial function in type 2 diabetes: a randomized controlled trial // J. Intern. Med. - 2014 Jan. -Vol. 275, N 1. - P. 59-70.
19. Benes J., Kazdova L., Drahota Z. et al. Effect of metformin therapy on cardiac function and survival in a volume-overload model of heart failure in rats // Clin. Sci. (Lond.). - 2011. -Vol. 121. - P. 29-41.
20. Eurich D.T., Weir D.L., Majumdar S.R. et al. Comparative safety and effectiveness of metformin in patients with diabetes mellitus and heart failure: systematic review of observational studies involving 34,000 patients // Circ. Heart Fail. -2013 May. - Vol. 6, N 3. - P. 395-402.
21. Cohen J.C., Horton J.D., Hobbs H.H. Human fatty liver disease: old questions and new insights // Science. - 2011. -Vol. 332. - P. 1519-1523.
22. Буеверов А.О. Безопасность метформина с точки зрения гепатолога // Ожирение и метаболизм. — 2010. -Вып. 2. - С. 73-76.
23. Blonde L., Dailey G.E., Jabbour S.A. et al. Gastrointestinal tolerability of extended-release metformin tablets compared to immediate-release metformin tablets: results of a retrospective cohort study // Curr. Med. Res. Opin. - 2004. -Vol. 20, N 4. - P. 565-572.
24. Schwartz S., Fonseca V., Berner B. et al. Efficacy, tolerability, and safety of a novel once-daily extended-release metformin in patients with type 2 diabetes // Diabetes Care. - 2006. - Vol. 29, N 4. — P. 759-764.
25. Fujioka K., Brazg R.L., Raz I. et al. Efficacy, dose-response relationship and safety of once-daily extended-release metformin (glucophage(registered trademark) XR) in type 2 diabetic patients with inadequate glycaemic control despite prior treatment with diet and exercise: Results from two double-blind, placebo-controlled studies // Diabetes Obes. Metab. - 2005. - Vol. 7, N 1. - P. 28-39.
26. Schwartz S., Fonseca V., Berner B. et al. Efficacy, tolerability, and safety of a novel once-daily extended-release metformin in patients with type 2 diabetes // Diabetes Care. - 2006. - Vol. 29, N 4. - P. 759-764.
27. Fujioka K., Pans M., Joyal S. Glycemic control in patients with type 2 diabetes mellitus switched from twice-daily immediate-release metformin to a once-daily extended-release formulation // Clin. Ther. - 2003. - Vol. 25, N 2. - P. 515529.
