Патогенетическое лечение Актовегином нейроишемического болевого синдрома в нижних конечностях при сахарном диабете
СтатьиОпубликовано в журнале:
«РУССКИЙ МЕДИЦИНСКИЙ ЖУРНАЛ» Эндокринология; ТОМ 17; № 10; 2009; стр. 8-11.
Д.м.н. И.В. Гурьева, И.В. Бегма, к.м.н. И.В. Кузина, А.Н. Бегма, О.В. Светлова
Федеральное бюро медико-социальной экспертизы, РМАПО
Сахарный диабет 2 типа (СД 2) в настоящее время является наиболее распространенным эндокринным заболеванием. По данным статистических исследований, им страдает около 4% населения (Государственный регистр сахарного диабета). В России число лиц с нарушением углеводного обмена приближается к 8 млн. Наряду со столь высокой распространенностью СД 2 является одной из основных причин ранней инвалидизации и смертности больных трудоспособного возраста. Данная категория пациентов имеет высокий риск ампутации нижних конечностей при гангрене, развившейся на фоне артериальной недостаточности [1,2]. Атеросклеротический процесс у страдающих сахарным диабетом развивается в более раннем возрасте и захватывает большую протяженность периферического артериального русла, чем в общей популяции [3,5].
Наиболее важным клиническим проявлением атеросклероза является перемежающаяся хромота (ПХ), встречающаяся почти у каждого третьего пациента. ПХ характеризуется болью в одной или обеих ногах при ходьбе, которая может значительно ограничивать способность пациента к передвижению, но обычно значительно ослабевает в покое [8]. Кроме того, при ПХ нередко наблюдаются судороги и выраженная слабость в ногах, также провоцируемые ходьбой.
Нарушение периферического кровотока при сахарном диабете, как правило, сочетается с периферической сенсомоторной невропатией, которая накладывает некоторые особенности на течение и клиническую картину периферического атеросклероза: нарушение микроциркуляции в коже, влияние на скорость заживления язв, снижение «защитных функций» и сопротивления тканей по отношению к травмам [4]. Это обусловливает особую подверженность тканей стоп при диабете к формированию хронических язв и нарушенной способности к заживлению при сочетании нейропатии, ишемии и инфекции, которые являются основными факторами риска диабетической язвы и ампутации.
В настоящее время в комплексной терапии больных сахарным диабетом, помимо препаратов, использующихся для компенсации углеводного обмена, применяются некоторые лекарственные средства, воздействующие на факторы риска. Существует не так много медикаментозных способов воздействия на увеличение дистанции безболевой ходьбы: с этой целью изучается использование статинов, антикоагулянтов, антитромботических средств, а также препаратов, улучшающих функцию эндотелия. Большой интерес вызывает использование в комплексном лечении любых форм диабетической стопы препарата Актовегин. Актовегин представляет собой высокоочищенный депротеинизированный гемодиализат телячьей крови, который получают методом ультрафильтрации. Препарат содержит органические низкомолекулярные соединения весом не более 5000 Дальтон.
В нашей клинике Актовегин используется в комплексном лечении больных СД, страдающих поражением нижних конечностей. На основании нашего опыта применения препарата встал вопрос об обобщении, анализе, дальнейшем изучении и теоретическом обосновании показаний к использованию Актовегина для лечения данных осложнений сахарного диабета.
Целью пилотного рандомизированного открытого сравнительного 8-недельного исследования явилась оценка влияния препарата Актовегин на состояние ишемического синдрома в нижних конечностях (перемежающей хромоты), периферической гемодинамики, перекисного окисления, углеводного обмена у больных СД 2 типа, имеющих нейроишемическую форму поражения нижних конечностей, в сравнении с сулодексидом. Сулодексид входит в группу низкомолекулярных гепаринов и содержит гепариноидную и дерматансульфатную фракции, оказывая антитромботическое действие, снижая содержание фибриногена и влияя на гемореологические характеристики крови. В связи с этим данный препарат в последние годы нашел широкое применение в терапии перемежающей хромоты [2], а потому был выбран в качестве препарата сравнения в данном пилотном исследовании.
Материалы и методы исследования
В исследование были включены 26 пациентов СД 2 и 1 типа (14 женщин и 12 мужчин) в возрасте от 58 до 75 лет (средний возраст 64,3±1,2 года). Длительность заболевания диабетом была от 2 до 23 лет (14,8±1,7 лет). Уровень HbA1c составил 7,6±1,25%. В исследование включались пациенты, имеющие хроническую артериальную недостаточность легкой и умеренной степени (ХАН II по Лериш-Фонтейну, индекс лодыжка/плечо по данным ультразвуковой допплерографии ниже 0,9) без язвенного поражения стоп. Пациенты были рандомизированы в две группы лечения: Актовегином (n=12) и сулодексидом (n=14) (табл. 1). Пациенты получали раствор Актовегина в течение 14 дней в виде внутривенных капельных инфузий (2000 мг 1 раз в сутки) с последующим переходом на пероральный прием 1200 мг в сутки (в 3 приема) в течение 6 недель. Сулодексид также применяли в виде внутривенных капельных инфузий (1200 ЛЕ препарата в сутки) в течение 2 недель с последующим периодом 6-недельного перорального приема (1000 ЛЕ в 2 приема).
Таблица 1. Сравнительная характеристика больных в подруппах лечения Актовегином и сулодексидом: средняя (стандартное отклонение) |
||
| Показатели | Группа сулодексида (n=14) |
Группа Актовегина (n=12) |
| СД1/СД2 | 1/13 |
1/11 |
| Возраст | 63,9 (8,0) |
64,4 (7,4) |
| Длительность СД | 12,1 (5,3) |
12,8(6,7) |
| НЬА1с | 8,8 (2,9) |
8,1 (1,4) |
| ЛПИ | 0,8(0,1) |
0,8(0,1) |
| Макс. время ходьбы (сек/мин.) | 285(127,5)/4,7 |
255(141,1)/4,2 |
| НДС | 14,5(3,6) |
14,1(3,7) |
Состояние периферического артериального кровотока оценивали по ультразвуковой допплерографии, функциональную способность к ходьбе - по данным тредмил-теста (протокол Gardner) c определением максимального времени до возникновения боли при ходьбе на тредмиле перед началом лечения, затем после окончания инфузионного периода (2 недели) и в конце исследования. Состояние системы гемостаза оценивалось по уровню активированного частичного тромбопластинового времени, протромбина, фибриногена, антитромбина и МНО. Определяли также уровень оксидативного стресса (малоновый диальдегид) и антиоксидативной активности плазмы по уровню ферментов глютатионпероксидазы, супероксиддисмутазы, общей антиоксидантной активности сыворотки крови. Оценка степени диабетической невропатии проводилась методом подсчета нейропатического дисфунционального счета (НДС). Определение транскутанного напряжения кислорода проводилось методом чрескожной оксиметрии (TcpO2) перед началом и в конце исследования.
Результаты исследования и обсуждение
В двух группах лечения было показано увеличение максимального времени безболевой ходьбы (PWT) при проведении тредмил-теста после окончания периода инфузии, а затем перорального приема препарата через 8 недель лечения (табл. 2). Абсолютные значения прироста PWT сотавили в среднем 378,2±43,8 с в группе сулодексида и 435,9±53,2 с в группе Актовегина к концу 8-недельного периода лечения, однако эффект Актовегина по абсолютному приросту не отличался от такового у сулодексида. По величине относительного прироста времени безболевой ходьбы эффект Актовегина значительно превышал эффект сулодексида в конце лечения (95,1% против 38,1%, p<0,05, Mann-Whitney U test). Выраженность нейропатии была достаточно значительна в начале лечения и достоверно уменьшилась в обеих группах через 8 недель терапии (табл. 2).
Таблица 2. Время максимальной дистанции ходьбы до появления боли (PWT) и нейропатического дефицита (NDS) в процессе лечения Актовегином и сулодексидом (M±m) |
|||
Показатели |
0 недель |
2 недели |
8 недель |
| PWT Актовегин, с | 275,8±42,7 |
354,1±48,9, p<0,05 против 0 недели |
435,9±53,2 p<0,01 против 0 недели |
| PWT сулодексид, с | 281,3±34,1 |
337,5±39,5 |
378,2±43,8 p<0,05 против 0 недели |
| NDS Актовегин | 14,1±1,2 |
- |
10,4±1,3 p<0,05 |
| NDS сулодексид | 14,8±1,2 |
- |
12,4±1,4 p<0,05 |
| Абс. прирост Актовегин PWT, с | - |
- |
160,1±21,9 |
| Абс. прирост сулодексид PWT, с | - |
- |
84,9±44,5 |
| Отн. прирост Актовегин | - |
- |
98,1% |
| Отн. прирост сулодексид | - |
- |
38,1% |
Средний уровень ТсрО2 составил 45,0±4,3 мм в начале исследования, достоверно не изменившись в конце лечения. Уровень фибриногена и факторов свертывания, а также показателя оксидативного стресса и антиоксидантной защиты также достоверно не изменялись в двух группах за 8-недельный период лечения. Не было обнаружено статистически достоверных изменений гликированного гемоглобина в процессе терапии.
Обоснование применения Актовегина в исследовании обусловлено его способностью стимулировать обмен веществ в клетках [11,12]. В экспериментальных исследованиях было показано, что под воздействием Актовегина клетки различных тканей увеличивают потребление кислорода и глюкозы путем активации пируватдегидрогеназы [13,14]. Это приводит к повышению энергетического статуса клеток и интенсификации их метаболизма. Инсулиноподобное действие Актовегина осуществляется за счет инозитолфосфоолигосахаридов, активизирующих транспортеры глюкозы в плазматической мембране. Инсулиноподобный механизм действия Актовегина отличается от механизма действия собственно инсулина, так как стимулируемые им липогенез, липолиз и транспорт глюкозы не ингибируются при использовании антиинсулиновых антител. Кроме того, Актовегин не влияет на фосфорилирование инсулиновых рецепторов и их взаимодействие с инсулином.
Традиционно Актовегин используется для лечения церебральной патологии и дегенеративных заболеваний [15-17]. Выраженный клинический эффект высоких доз Актовегина при лечении осложненных форм СД был отмечен многими отечественными и зарубежными авторами [1,6,7]. Показано, что Актовегин способен улучшать состояние периферических нервов, включая увеличение скорости нервного проведения и уменьшение механической аллодинии. Кроме того, препарат улучшает качество жизни после 24 недель приема у пациентов с диабетической болевой невропатией [18]. Отмечена эффективность лечения больных СД и периферическими ангио- и невропатиями [18]: уменьшение болевого синдрома в ногах, увеличение прогулочного расстояния, улучшение скорости проведения возбуждения по нервам. Проведение пилотных исследований в хирургических клиниках при включении Актовегина в комплекс лечения больных с синдромом диабетической стопы (хронические язвы, гнойно-некротические процессы) демонстрируют возможность стимуляции процесса заживления язвенных дефектов при лечении Актовегином, что вполне объяснимо с точки зрения патофизиологического воздействия препарата [9,10].
Заключение
Таким образом, в результате проведенного нами открытого сравнительного исследования продемонстрировано, что последовательное лечение Актовегином в виде инфузий в дозе 2000 мг 1 раз в сутки с переходом на поддерживающий прием Актовегина в таблетках в дозе 1200 мг с сутки в 3 приема в течение 6 недель (всего 8 недель лечения) достоверно увеличивает дистанцию безболевой ходьбы у больных СД с перемежающей хромотой. При этом достоверно увеличивается время до появления болевых ощущений и утомляемости в ногах уже через 2 недели от начала лечения после окончания инфузионного курса и продолжает нарастать после 6 недель курса таблетированного лечения. Аналогичная тенденция отмечена у пациентов, получающих сулодексид. Однако ответ на лечение Актовегином выражен более отчетливо по сравнению с сулодексидом и превосходит по эффективности относительного прироста времени возникновения боли при ходьбе на тредмиле (рис. 1). Также наблюдается статистически достоверное улучшение диабетической невропатии по шкале невропатического дисфункционального счета (рис. 2). Возможно, эффективность лечения может возрастать с увеличением его длительности.
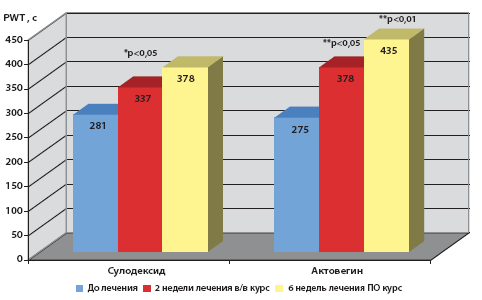
Рис. 1. Актовегин и сулодексид увеличивают максимальное время ходьбы до боли (Mean, p vs 0 – Wilkoxon test)
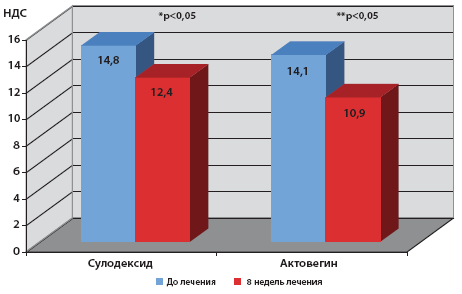
Рис. 2. Актовегин и сулодексид уменьшают сенсорную невропатию (Mean, p vs 0 – Wilkoxon test)
Полученные в нашем исследовании результаты согласуются с имеющимися литературными данными об улучшении проявлений симптомной периферической невропатии и ангиопатии у больных СД при лечении Актовегином. У препарата большой клинический опыт применения в разных странах, в том числе и в России [14-18]. Несомненно, эффективность препаратов с различным механизмом действия в терапии болевого синдрома ишемического генеза должна изучаться и далее.
ЛИТЕРАТУРА:
1. Балаболкин М.И., Клебанова Е.М., Креминская В.М. Микроангиопатия - одно из сосудистых осложнений сахарного диабета // Consilium medicum. - 2000. -Т. 2. • №5. .-С 34-37.
2. Бреговский В.Б.//Матер.Конф. "Роль гликозоаминогликанов (ГАГ) в лечении сосудистых осложнений сахарного диабета" - Санкт-Петербург, 1996. - С. 17.
3. Гурьева И.В. Профилактика, лечение, медико-социальная реабилитация и организация междисциплинарной помощи при синдроме диабетическрй стопы. Автореферат дисс…докт.мед наук. -40 с.
4. Гурьева И.В., Кузина И.В., Воронин А.В., Комелягина Е.Ю., Мамонтова Е.Ю. Синдром диабетической стопы. - М. - 2000. - 40 с.
5. Дедов И.И., Анциферов М.Б., Галстян Г.Р. и др. Синдром диабетической стопы: клиника, диагностика, лечение. М., 1998.
6. Львова Л. В. В центре внимания// Провизор. -2003. - № 6.
7. Любарский М.С., Смагин А.А., Хабаров Д.В., Ракитин А.А., Титова Л. В. Возможности экстракорпоральных методов в лечении трофических язв // Матер. VIII Всеросс. съезда анестезиологов - реаниматологов. -2002.
8. Светухин A.M., Прокудина М.В. Комплексное хирургическое лечение больных.
9. Оболенский В.Н. Комплексное лечение больных с синдромом диабетической стопы. Фарматека 2008.-№8.- С. 49-52.
10. Дубошина К.С., Яйлаханян К.С. Лечение больных с синдромом диабетической стопы в хирургической клинике. РМЖ2008.том16.-№5-С1-3
11. Sch fer G, Lamprecht W. Zur Wirkung von Blutextrakten auf die Mitochondrienatmung und die oxydative Phosphorylierung. Arzneimittelforschung 15: 757-759, 1965.
12. Kuninaka T, Senga Y, Senga H, Weiner M. Nature of enhanced mitochondrial oxidative metabolism by a calf blood extract. J Cell Physiol 146: 148-155, 1991.
13. Obermaier-Kusser B, Muhlbacher C, Mushack J, Seffer E, Ermel B, Machicao F. Further evidence for a two-step model of glucose-transport regulation. Inositol phosphate oligosaccharides regulate glucose-carrier activity. Biochem J 261:699-705, 1989.
14. Jacob S, Dietze GJ, Machicao F, Kuntz G, Augustin HJ. Improvement of glucose metabolism in patients with type II diabetes after treatment with a hemodialysate. Arzneimittelforschung 46: 269-272, 1996.
15. Kanowski S, Kinzler E, Lehmann E, Schweizer A, Kuntz G. Confirmed clinical efficacy of Actovegin® in elderly patients with organic brain syndrome. Pharmacopsychiat 28:125-33, 1995.
16. Herrmann WM, Bohn-Olszewsky WJ, Kuntz G. Infusionstherapie mit Actovegin bei Patienten mit prim rer degenerativer Demenz vom Alzheimer-Type und Multiinfarkt-Demenz. Ergebnisse einer prospektiven, Placebokontrollierten Doppelblindstudie bei station ren Patienten. Z Geriatrie 5: 46-55, 1992.
17. Saletu B, Gr nberger J, Linzmayer L, Anderer P, Semlitsch HV. EEG brain mapping and psychometry in age-associated memory impairment after acute and 2-week infusions with the hemoderivative Actovegin: double-blind, placebo-controlled trials. Neuropsychobiology 24: 135-148, 1990-1991.
18. Jensen W, Beck ? Treatment of the diabetic polyneuropathy. A controlled double blind study. Med Welt 38: 838-841, 1987.
