Глюкофаж Лонг: максимальное использование эффектов сахароснижающего препарата первой линии
СтатьиОпубликовано в журнале:
CONSILIUM MEDICUM, Том 13, No 12
О.Ю.Сухарева, М.В.Шестакова
ФГБУ Эндокринологический научный центр Минздравсоцразвития РФ
Реалиями ежедневной клинической практики врача-эндокринолога являются постоянное увеличение числа новых случаев сахарного диабета типа 2 (СД 2), существенное омоложение заболевания, наличие в большинстве случаев проблемы избыточной массы тела, а также других соматических отягощений (наиболее часто – сердечно-сосудистой патологии). Выбор оптимального препарата у полиморбидного пациента зачастую оказывается совсем не прост, так как помимо ожидаемого сахароснижающего эффекта требуется учесть индивидуальные особенности пациента, его сопутствующие заболевания, а также принять во внимание имеющиеся показания и противопоказания к применению различных сахароснижающих средств. Более того, принятие решения об оптимальном варианте лечения усложняется возможностью выбора из нескольких классов сахароснижающих препаратов с различными механизмами действия (а с учетом наличия нескольких препаратов в отдельных группах и возможных сочетаний количество вариантов стремительно умножается).
На сегодняшний день для лечения СД 2 в Российской Федерации применяются:
- бигуаниды (метформин);
- препараты сульфонилмочевины (СМ) и глиниды;
- ингибиторы дипептидилпептидазы-4 (ДПП-4);
- агонисты/аналоги глюкагоноподобного пептида-1 (ГПП-1);
- тиазолидиндионы (ТЗД), в РФ и Европе – только пиоглитазон;
- ингибиторы α-глюкозидаз (акарбоза);
- инсулин и его аналоги (в том числе в виде готовых смесей).
Оптимизировать выбор врача и способствовать избранию наиболее оправданной лечебной тактики призваны международные консенсусы, рекомендации и алгоритмы [1, 2]. Однако получение новой информации (иногда меняющей представления о целях лечения), внедрение новых групп лекарственных препаратов, появление серьезных ограничений в отношении ранее использовавшихся средств периодически диктует необходимость обновления имеющихся рекомендаций.
В 2011 г. Российская ассоциация эндокринологов (РАЭ) провела большую работу, итогом которой стал собственный рекомендательный документ – Консенсус по инициации и интенсификации сахароснижающей терапии СД 2 [3].
Основой Консенсуса РАЭ стали следующие положения:
- приоритет индивидуального подхода к каждому пациенту (определение индивидуальных целей лечения с учетом возраста, наличия осложнений, риска гипогликемий);
- стратификация терапевтической тактики в зависимости от исходного уровня метаболического контроля;
- эффективность и безопасность в качестве определяющих факторов при выборе сахароснижающей терапии.
Резюмируя содержание консенсуса РАЭ, необходимо выделить следующие позиции:
- Определение индивидуального целевого значения контроля гликемии по уровню гликированного гемоглобина НbА1с. Выбор зависит от возраста пациента или ожидаемой продолжительности жизни, длительности заболевания, наличия сосудистых осложнений, риска развития гипогликемий (табл. 1).
- Стратификация терапевтической тактики в зависимости от исходного уровня HbA1c.
- При исходном HbA1c 6,5–7,5% достижение индивидуальных целевых значений гликемии возможно при использовании монотерапии. Если при монотерапии достичь поставленных целей не удается, то далее применяется комбинированное лечение (2 или 3 препарата). Препараты 1-го ряда: средства с минимальным риском гипогликемий и отсутствием негативного влияния на массу тела. Метформин; ингибиторы ДПП4; агонисты рецепторов ГПП-1.
- При исходном HbA1c 7,6-9,0% следует сразу начинать с комбинированной терапии (2 препарата). При неэффективности возможно сочетание 3 препаратов или начало инсулинотерапии.
- При исходном HbA1c более 9,0% при выраженной клинической симптоматике следует назначить инсулинотерапию (возможно в комбинации с пероральными сахароснижающими препаратами). При отсутствии симптомов декомпенсации в дебюте возможно назначение комбинации 2 или 3 сахароснижающих препаратов, при этом основой такой комбинации должны стать препараты СМ.
- При назначении комбинации 2 или 3 препаратов (в том числе инсулина) необходимо помнить о нерациональных сочетаниях, т.е. которые противопоказаны или не приносят дополнительного эффекта (табл. 2).
- В любой комбинации 2 или 3 препаратов рекомендуется использование метформина при отсутствии противопоказаний.
- Изменение (интенсификация) ранее назначенной терапии: мониторинг эффективности лечения по уровню НbА1с рекомендуется осуществлять каждые 3 мес; интенсификация лечения при недостижении индивидуальных целей НbА1с должна быть выполнена не позднее чем через 6 мес; безопасность и эффективность являются приоритетами в выборе лечения.
Таблица 1. Индивидуализированный выбор целей терапии по HbA1c (Консенсус РАЭ 2011 г.)
| Состояние пациента | Возраст | ||
| Молодой | Средний | Пожилой и/или ожидаемая продолжительность жизни | |
| Нет тяжелых осложнений и/или риска тяжелой гипогликемии | |||
| Есть тяжелые осложнения и/или риск тяжелой гипогликемии | |||
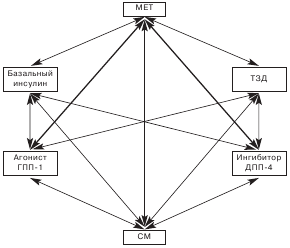
Таблица 2. Нерациональные комбинации сахароснижающих препаратов (Консенсус РАЭ 2011 г.)
| 1. СМ + глинид | 4. ТЗД + инсулин |
| 2. Агонист ГПП-1 + ингибитор ДПП-4 | 5. Ингибитор ДПП-4 или агонист ГПП-1 + глинид |
| 3. 2 препарата СМ | 6. Инсулин короткого действия + ингибитор ДПП-4, или антагонист ГПП-1, или глинид, или СМ |
Таким образом, в РФ в 2011 г. впервые появился согласительный документ по ведению столь непростой когорты пациентов, как больные с впервые установленным диагнозом «сахарный диабет типа 2». Его главным принципом является дифференцированный подход к каждому пациенту с выбором индивидуальных целей терапии для разных категорий больных.
Сердечно-сосудистая безопасность терапии СД 2
Во многом необходимость выбора индивидуальных целей лечения продиктована уроками, извлеченными из исследований ACCORD, VADT, ADVANCE [4–6], которые были призваны дать ответ на крайне важный вопрос: как влияет интенсивный контроль гликемии на риск макрососудистых осложнений у больных СД 2?
После печально известной приостановки сахароснижающей ветви исследования ACCORD из-за увеличения смертности в группе интенсивного контроля по сравнению с группой традиционного лечения были предприняты многочисленные попытки проанализировать и объяснить полученные результаты. Помимо предполагаемой связи между увеличением смертности и тяжелыми гипогликемиями, внимание привлекли следующие факты [7]:
 Ставшее знаковым исследование UKPDS, где у пациентов с впервые установленным диагнозом СД 2 изучались эффекты интенсивной и традиционной терапии, показало: у лиц с избыточной массой тела, получавших терапию метформином, через 10 лет наблюдения в группе интенсивного контроля гликемии получено снижение риска инфаркта миокарда на 39%, любой конечной точки, связанной с диабетом, – на 32%, смерти, связанной с диабетом, – на 42%, смертности от всех причин – на 36% [9]. Результаты UKPDS оказали существенное влияние на последующие представления о тактике лечения пациентов с СД 2 и обусловили закрепление метформина в качестве препарата выбора во всех международных рекомендациях. В качестве исследуемого препарата метформина в UKPDS применялся оригинальный препарат метформина Глюкофаж®.Однако не менее важными представляются результаты продолженного 10-летнего наблюдения за участниками UKPDS. В результате, несмотря на то, что различия в уровне гликированного гемоглобина HbA1c нивелировались уже через 1 год (не предпринималось никаких попыток поддерживать прежний режим приема препаратов), были подтверждены существенные долгосрочные преимущества в группе исходного интенсивного контроля гликемии по сравнению с традиционным лечением. Так, среди лиц, получавших лечение препаратами СМ/инсулином, относительное снижение риска сохранялось через 10 лет для любой связанной с диабетом конечной точки (на 9%), микрососудистых осложнений (на 24%), снижения риска инфаркта миокарда (на 15%) и смерти от любой причины (на 13%). В группе исходного лечения метформином (Глюкофаж®) статистически значимое снижение риска для этих событий составило: для любой конечной точки, связанной с диабетом – на 21%, инфаркта миокарда – на 33%, смерти от любой причины – на 27%). Это позволило говорить в дальнейшем о существующем «эффекте памяти» и подчеркнуть важность адекватного сахароснижающего лечения сразу с момента установления диагноза.Кардиопротективные механизмы действия метформинаСуществует несколько механизмов, посредством которых метформин может влиять на улучшение сердечно-сосудистых исходов [10–14]:
Ставшее знаковым исследование UKPDS, где у пациентов с впервые установленным диагнозом СД 2 изучались эффекты интенсивной и традиционной терапии, показало: у лиц с избыточной массой тела, получавших терапию метформином, через 10 лет наблюдения в группе интенсивного контроля гликемии получено снижение риска инфаркта миокарда на 39%, любой конечной точки, связанной с диабетом, – на 32%, смерти, связанной с диабетом, – на 42%, смертности от всех причин – на 36% [9]. Результаты UKPDS оказали существенное влияние на последующие представления о тактике лечения пациентов с СД 2 и обусловили закрепление метформина в качестве препарата выбора во всех международных рекомендациях. В качестве исследуемого препарата метформина в UKPDS применялся оригинальный препарат метформина Глюкофаж®.Однако не менее важными представляются результаты продолженного 10-летнего наблюдения за участниками UKPDS. В результате, несмотря на то, что различия в уровне гликированного гемоглобина HbA1c нивелировались уже через 1 год (не предпринималось никаких попыток поддерживать прежний режим приема препаратов), были подтверждены существенные долгосрочные преимущества в группе исходного интенсивного контроля гликемии по сравнению с традиционным лечением. Так, среди лиц, получавших лечение препаратами СМ/инсулином, относительное снижение риска сохранялось через 10 лет для любой связанной с диабетом конечной точки (на 9%), микрососудистых осложнений (на 24%), снижения риска инфаркта миокарда (на 15%) и смерти от любой причины (на 13%). В группе исходного лечения метформином (Глюкофаж®) статистически значимое снижение риска для этих событий составило: для любой конечной точки, связанной с диабетом – на 21%, инфаркта миокарда – на 33%, смерти от любой причины – на 27%). Это позволило говорить в дальнейшем о существующем «эффекте памяти» и подчеркнуть важность адекватного сахароснижающего лечения сразу с момента установления диагноза.Кардиопротективные механизмы действия метформинаСуществует несколько механизмов, посредством которых метформин может влиять на улучшение сердечно-сосудистых исходов [10–14]: - Препарат является инсулиновым сенситайзером и, улучшая чувствительность тканей к инсулину, снижает сердечно-сосудистые риски, ассоциированные с инсулинорезистентностью, гиперинсулинемией и глюкозотоксичностью.
- Улучшает липидный профиль (снижение уровней общего холестерина, липопротеидов низкой плотности, триглицеридов).
- Снижает массу тела.
- Улучшает фибринолитические свойства, улучшает микроциркуляцию и снижает риск внутрисосудистых тромбозов.
- Снижает степень оксидативного стресса и апоптоза, нейтрализует конечные продукты гликирования.
- Снижает экспрессию молекул адгезии на эндотелиоцитах (в результате снижается адгезия лейкоцитов к эндотелию), а также дифференцировку клеток воспаления в макрофаги и дальнейшее поглощение макрофагами липидов, что уменьшает степень выраженности атеросклеротическоих процессов.
 Улучшение переносимости метформина пролонгированного действия Проведено несколько исследований, показывающих, что использование метформина пролонгированного действия (Глюкофаж Лонг) улучшает переносимость, сохраняя при этом прежнюю сахароснижающую эффективность. Для оценки улучшения переносимости со стороны ЖКТ L.Blonde и соавт. ретроспективно оценили данные пациентов с СД 2, которые в течение 1 года до включения в исследование получали метформин в любой лекарственной форме [20]. В анализе принимали участие 468 пациентов: 158 использовали метформин немедленного высвобождения и 310 получали метформин пролонгированного действия (из них 213 человек когда-либо ранее получали метформин немедленного высвобождения, 65 человек получали пролонгированную форму впервые и 32 человек ранее принимали другие сахароснижающие препараты). В группе метформина пролонгированного действия 25% больных (каждый 4-й участник!) стали принимать его именно из-за выраженных гастроинтестинальных НЯ на фоне приема обычных форм метформина. Соответственно, в этой группе по определению были сконцентрированы лица с заведомой чувствительностью к метформину со стороны ЖКТ. Тем не менее, частота любых гастроинтестинальных НЯ была сопоставима между группами лечения метформином пролонгированного действия и метформином немедленного высвобождения (11,94 против 11.39%, р=0,86). Частота отдельных гастроинтестинальных НЯ (диарея, тошнота, диспепсия, боли в животе, запоры, рвота и т.д.) так же не различалась. Дополнительно проводился анализ в отдельно выделенной когорте из 205 пациентов, которые до назначения метформина пролонгированного действия принимали обычные формы метформина в течение 1 года. На фоне приема обычной формы любые НЯ со стороны ЖКТ отмечались у 26,3% больных, тогда как после смены на лекарственную форму пролонгированного (Глюкофаж Лонг) действия в 2 раза реже – у 11,7% (р=0,0006). Сходным образом изменилась частота развития диареи (наиболее частого НЯ): у 18,05% участников «до» в сравнении с 8,29% «после» смены терапии на Глюкофаж Лонг (р=0,0084). Поскольку НЯ со стороны ЖКТ весьма частое явление именно при инициации терапии метформином, эти события были отдельно проанализированы у лиц, впервые получавших разные лекарственные формы препарата. В результате при старте терапии с обычных форм метформина (т.е. немедленного высвобождения) гастроинтестинальные явления в течение 1 года лечения встречались достоверно чаще (в 19,83% случаев) по сравнению с метформином пролонгированного действия – в 9,23% случаев (р=0,04).L.Donelly и соавт. ретроспективно проанализировали соблюдение схемы терапии с использованием баз данных пациентов, проживающих в округе Тейсайд (Великобритания), которые получали лечение метформином [21]. Метформин в стандартной лекарственной форме получали 10 772 пациента, метформин пролонгированного действия – 137 пациентов. В целом соблюдение схемы терапии было выше в группе препарата пролонгированного действия (80%) по сравнению с пациентами, принимавшими стандартную форму препарата (72%), (р=0,0026). У 40 пациентов (с достаточным количеством данных для анализа соблюдения терапии), у которых имела место смена терапии с обычной формы препарата на форму пролонгированного действия, соблюдение схемы лечения повысилось почти на 30% (с 62 до 81%, р Сходные данные по применению Глюкофажа Лонг получили M.Feher и соавт., проанализировав результаты 2 проспективных и 2 ретроспективных клинических наблюдений (n=95) у лиц с непереносимостью метформина немедленного высвобождения [22]. Переносимость новой формулы отмечалась у 62–100% участников, при этом показатели углеводного обмена улучшились или не изменились.Сахароснижающая эффективность метформина пролонгированного действияВажно, что в случае метформина пролонгированного действия (Глюкофаж Лонг) улучшение переносимости не сопровождается уменьшением антигипергликемического действия. К.Fujioka и соавт. оценили эффективность и безопасность метформина продленного действия в 2 протоколах (двойных слепых рандомизированных плацебоконтролируемых исследованиях) у пациентов с неудовлетворительным гликемическим контролем на фоне диетотерапии и физических нагрузок [23].В протоколе 1 (240 пациентов) применение метформина пролонгированного действия снижало HbA1с по сравнению с плацебо на 0,7% за 12 нед и на 0,8% – за 24 нед (все p В протоколе 2 (742 пациента) оценивалась эффективность различных дозировок метформина пролонгированного действия в течение 16 нед. Показано дозозависимое сахароснижающее действие метформина пролонгированного действия с максимальной эффективностью в дозировке 1500–2000 мг/сут. При использовании однократной дозы 500 мг HbA1с по сравнению с плацебо снижался на 0,6%, 1000 мг – на 0,7%, 1500 мг – на 1,0% и 2000 мг – на 1,0%. Эффективность метформина пролонгированного действия 2000 мг 1 раз в день и 1000 мг 2 раза в день была сопоставима (1,0% и 1,2% соответственно). Уровень HbA1с менее 7,0% при приеме метформина пролонгированного действия был достигнут у 36% участников по сравнению с 10% в группе плацебо. Метформин пролонгированного действия (Глюкофаж Лонг) в этих 2 исследованиях хорошо переносился; гастроинтестинальные побочные эффекты при его приеме встречались чаще, чем в группах контроля, но очень мало пациентов (как принимавших метформин, так и получавших плацебо) вышли из исследований по этой причине (1,3% против 1,3% в протоколе 1 и 1,6% против 0,9% в протоколе 2).ЗаключениеПринцип максимально индивидуализированной и безопасной тактики ведения больных является основой Консенсуса РАЭ по инициации и интенсификации терапии СД 2, принятого в 2011 г.Метформин, вследствие доказанных в долгосрочных исследованиях кардиоваскулярных преимуществ, а также отсутствия негативного влияния на массу тела и минимального риска гипогликемий является препаратом 1-й линии на старте терапии СД 2. Кроме того, использование метформина рекомендуется в любой комбинации 2 или 3 препаратов на любом этапе лечения при отсутствии противопоказаний.Появление новой лекарственной формы метформина пролонгированного действия (Глюкофаж Лонг) с удобной схемой титрации (увеличение дозы препарата до эффективной на 500 мг 1 раз в 7–10 дней) и приемом 1 раз в сутки позволяет существенно снизить нежелательные гастроинтестинальные проявления и повысить приверженность к лечению.Список использованной литературы
Улучшение переносимости метформина пролонгированного действия Проведено несколько исследований, показывающих, что использование метформина пролонгированного действия (Глюкофаж Лонг) улучшает переносимость, сохраняя при этом прежнюю сахароснижающую эффективность. Для оценки улучшения переносимости со стороны ЖКТ L.Blonde и соавт. ретроспективно оценили данные пациентов с СД 2, которые в течение 1 года до включения в исследование получали метформин в любой лекарственной форме [20]. В анализе принимали участие 468 пациентов: 158 использовали метформин немедленного высвобождения и 310 получали метформин пролонгированного действия (из них 213 человек когда-либо ранее получали метформин немедленного высвобождения, 65 человек получали пролонгированную форму впервые и 32 человек ранее принимали другие сахароснижающие препараты). В группе метформина пролонгированного действия 25% больных (каждый 4-й участник!) стали принимать его именно из-за выраженных гастроинтестинальных НЯ на фоне приема обычных форм метформина. Соответственно, в этой группе по определению были сконцентрированы лица с заведомой чувствительностью к метформину со стороны ЖКТ. Тем не менее, частота любых гастроинтестинальных НЯ была сопоставима между группами лечения метформином пролонгированного действия и метформином немедленного высвобождения (11,94 против 11.39%, р=0,86). Частота отдельных гастроинтестинальных НЯ (диарея, тошнота, диспепсия, боли в животе, запоры, рвота и т.д.) так же не различалась. Дополнительно проводился анализ в отдельно выделенной когорте из 205 пациентов, которые до назначения метформина пролонгированного действия принимали обычные формы метформина в течение 1 года. На фоне приема обычной формы любые НЯ со стороны ЖКТ отмечались у 26,3% больных, тогда как после смены на лекарственную форму пролонгированного (Глюкофаж Лонг) действия в 2 раза реже – у 11,7% (р=0,0006). Сходным образом изменилась частота развития диареи (наиболее частого НЯ): у 18,05% участников «до» в сравнении с 8,29% «после» смены терапии на Глюкофаж Лонг (р=0,0084). Поскольку НЯ со стороны ЖКТ весьма частое явление именно при инициации терапии метформином, эти события были отдельно проанализированы у лиц, впервые получавших разные лекарственные формы препарата. В результате при старте терапии с обычных форм метформина (т.е. немедленного высвобождения) гастроинтестинальные явления в течение 1 года лечения встречались достоверно чаще (в 19,83% случаев) по сравнению с метформином пролонгированного действия – в 9,23% случаев (р=0,04).L.Donelly и соавт. ретроспективно проанализировали соблюдение схемы терапии с использованием баз данных пациентов, проживающих в округе Тейсайд (Великобритания), которые получали лечение метформином [21]. Метформин в стандартной лекарственной форме получали 10 772 пациента, метформин пролонгированного действия – 137 пациентов. В целом соблюдение схемы терапии было выше в группе препарата пролонгированного действия (80%) по сравнению с пациентами, принимавшими стандартную форму препарата (72%), (р=0,0026). У 40 пациентов (с достаточным количеством данных для анализа соблюдения терапии), у которых имела место смена терапии с обычной формы препарата на форму пролонгированного действия, соблюдение схемы лечения повысилось почти на 30% (с 62 до 81%, р Сходные данные по применению Глюкофажа Лонг получили M.Feher и соавт., проанализировав результаты 2 проспективных и 2 ретроспективных клинических наблюдений (n=95) у лиц с непереносимостью метформина немедленного высвобождения [22]. Переносимость новой формулы отмечалась у 62–100% участников, при этом показатели углеводного обмена улучшились или не изменились.Сахароснижающая эффективность метформина пролонгированного действияВажно, что в случае метформина пролонгированного действия (Глюкофаж Лонг) улучшение переносимости не сопровождается уменьшением антигипергликемического действия. К.Fujioka и соавт. оценили эффективность и безопасность метформина продленного действия в 2 протоколах (двойных слепых рандомизированных плацебоконтролируемых исследованиях) у пациентов с неудовлетворительным гликемическим контролем на фоне диетотерапии и физических нагрузок [23].В протоколе 1 (240 пациентов) применение метформина пролонгированного действия снижало HbA1с по сравнению с плацебо на 0,7% за 12 нед и на 0,8% – за 24 нед (все p В протоколе 2 (742 пациента) оценивалась эффективность различных дозировок метформина пролонгированного действия в течение 16 нед. Показано дозозависимое сахароснижающее действие метформина пролонгированного действия с максимальной эффективностью в дозировке 1500–2000 мг/сут. При использовании однократной дозы 500 мг HbA1с по сравнению с плацебо снижался на 0,6%, 1000 мг – на 0,7%, 1500 мг – на 1,0% и 2000 мг – на 1,0%. Эффективность метформина пролонгированного действия 2000 мг 1 раз в день и 1000 мг 2 раза в день была сопоставима (1,0% и 1,2% соответственно). Уровень HbA1с менее 7,0% при приеме метформина пролонгированного действия был достигнут у 36% участников по сравнению с 10% в группе плацебо. Метформин пролонгированного действия (Глюкофаж Лонг) в этих 2 исследованиях хорошо переносился; гастроинтестинальные побочные эффекты при его приеме встречались чаще, чем в группах контроля, но очень мало пациентов (как принимавших метформин, так и получавших плацебо) вышли из исследований по этой причине (1,3% против 1,3% в протоколе 1 и 1,6% против 0,9% в протоколе 2).ЗаключениеПринцип максимально индивидуализированной и безопасной тактики ведения больных является основой Консенсуса РАЭ по инициации и интенсификации терапии СД 2, принятого в 2011 г.Метформин, вследствие доказанных в долгосрочных исследованиях кардиоваскулярных преимуществ, а также отсутствия негативного влияния на массу тела и минимального риска гипогликемий является препаратом 1-й линии на старте терапии СД 2. Кроме того, использование метформина рекомендуется в любой комбинации 2 или 3 препаратов на любом этапе лечения при отсутствии противопоказаний.Появление новой лекарственной формы метформина пролонгированного действия (Глюкофаж Лонг) с удобной схемой титрации (увеличение дозы препарата до эффективной на 500 мг 1 раз в 7–10 дней) и приемом 1 раз в сутки позволяет существенно снизить нежелательные гастроинтестинальные проявления и повысить приверженность к лечению.Список использованной литературы1. Nathan DM, Buse JB, Davidson MB et al. American Diabetes Association; European Association for the Study of Diabetes. Medical management of hyperglycemia in type 2 diabetes: a consensus algorithm for the initiation and adjustment of therapy. A consensus statement of the American Diabetes Association and the European Association for the Study of Diabetes. Diabetes Care 2009; 32: 193–203.
2. Rodbard HW, Jellinger PS, Davidson JA еt al. Statement by an American Association of Clinical Endocrinologists / American College of Endocrinology Consensus Panel on Type 2 Diabetes Mellitus: An Algorithm for Glycemic Control. Endocr Pract 2009; 15 (6): 540–59.
3. Дедов И.И., Шестакова М.В., Аметов А.С. и др. Проект «Консенсус совета экспертов Российской ассоциации эндокринологов (РАЭ) по инициации и интенсификации сахароснижающей терапии сахарного диабета типа 2». Сахарный диабет. 2011; 4 (53): 6–16.
4. Miller ME, Byington RP, Goff DC Jr et al (Action to Control Cardiovascular Risk in Diabetes Study Group). Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med 2008; 358: 2545–59.
5. Duckworth W, Abraira C,Moritz T et al (VADT Investigators). Glucose control and vascular complications in veterans with type 2 diabetes [published correction appears in N Engl J Med 2009; 361: 1024–5, 1028]. N Engl J Med 2009; 360: 129–39.
6. Patel A, MacMahon S, Chalmers J et al (ADVANCE Collaborative Group). Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes. N Engl J Med 2008; 358: 2560–72.
7. Skyler JS, Bergenstal R, Bonow RO. A position statement of the American Diabetes Association and a scientific statement of the American College of Cardiology Foundation and the American Heart Association. Intensive Glycemic Control and the Prevention of Cardiovascular Events: Implications of the ACCORD, ADVANCE and VA Diabetes Trials. Diabetes Care 2009; 32: 187–92.
8. Center for Drug Evaluation and Research. Guidance for industry diabetes mellitus: evaluating cardiovascular risk in new antidiabetic therapies to treat type 2 diabetes [Internet] 2008. Available from http://www.fda.gov/ downloads/Drugs/GuidanceComplianceRegulatoryInformation/Guidances/ucm071 627.pdf.
9. UK Prospective Diabetes Study (UKPDS) Group. Effect of intensive blood-glucose control with metformin on complications in overweight patients with type 2 diabetes (UKPDS 34). Lancet 1998; 352, 854–65.
10. Wiernsperger NF. Metformin: intrinsic vasculoprotective properties. Diabetes Technol Ther 2000; 2: 259–72.
11. Leverve XM, Guigas B, Detaille D et al. Mitochondrial metabolism and type-2 diabetes: a specific target of metformin. Diabetes Metab 2003; 29: 6S88–6S94.
12. Grant PJ. Beneficial effects of metformin on haemostasis and vascular function in man. Diabetes Metab 2003; 29: 6S44–6S52.
13. Beisswenger P, Ruggiero-Lopez D. Metformin inhibition of glycation processes. Diabetes Metab 2003; 29: 6S95–6S103.
14. Смирнова О.М. Применение метформина в настоящем и будущем. Cons. Med. 2010; 12: 10–7.
15. Oates MS, Snah RR, Idle JR et al. Influence of oxidation polymorphism on phenformin kinetics and dynamics. Clin Pharmacol Ther 1983; 34: 827–34.
16. Rousse R, Travert F, Pasquet B. Metformin Use and Mortality Among Patients With Diabetes and Atherothrombosis. Arch Intern Med 2010; 170 (21): 1892–9.
17. Lipska K, Bailey C, Inzucci S. Use of metformin in the setting of mild-to moderate renal insufficient. Diabetes Care 2011; 34: 1431–7.
18. Donnan PT, MacDonald TM, Morris AD. Adherence to prescribed oral hypoglycaemic medication in a population of patients with Type 2 diabetes: a retrospective cohort study. Diabet Med 2002; 19: 279–84.
19. Timmins P, Donahue S, Meeker J, Marathe P. Steady-state pharmacokinetics of a novel extended-release Metformin formulation. Clin Pharmacokinet 2005; 44 (7): 721–9.
20. Blonde L, Dailey GE, Jabbour SA et al. Gastrointestinal tolerability of extended-release metformin tablets compared to immediate-release metformin tablets: results of a retrospective cohort study. Curr Med Res Opin 2004; 20 (4): 565–72.
21. Donnelly LA, Morris AD, Pearson ER. Adherence in patients transferred from immediate release metformin to a sustained release formulation: a population-based study. Diabetes, Obesity and Metabolism 2009; 11: 338–42.
22. Feher M, Al-Murat M, Brake J et al. Tolerability of prolongedrelease metformin (Glucophage® SR) in individuals intolerant to standard metformin – results from four UK centres. Br J Diabetes Vasc Dis 2007; 7: 225–8.
23. Fujioka K, Brazg RL, Raz I et al. Efficacy, dose-response relationship and safety of once-daily extended-release metformin (Glucophage XR) in type 2 diabetic patients with inadequate glycaemic control despite prior treatment with diet and exercise: results from two double-blind, placebo-controlled studies. Diabetes, Obesity and Metabolism 2005; 7: 28–39.
