Место ингибиторов протонной помпы в профилактике стрессовых повреждений желудочно-кишечного тракта у больных в критических состояниях
Статьи Опубликовано в журнале:«ХИРУРГИЯ»; № 1; 2009; стр. 64-69.
О.М.Антоненко
Консультативно-диагностическое отделение «ЭТИРК»
Несмотря на проводимые в последнее время исследования и профилактические мероприятия, остается актуальной проблема возникновения кровотечения из верхних отделов желудочно-кишечного тракта (ЖКТ) у больных в критическом состоянии. Клиническое значение кровотечений определяется высокими показателями летальности, которые на протяжении последних лет устойчиво сохраняются на уровне 5-10%. Наиболее частой причиной кровотечений из верхних отделов ЖКТ являются острые эрозивно-язвенные поражения желудка и двенадцатиперстной кишки у пациентов в критических состояниях, в том числе и в послеоперационном периоде. Это грозное осложнение - закономерное следствие развившихся мультисистемных нарушений, которое принципиально ухудшает прогноз жизни пациента. Так, по данным ряда авторов (В.А.Кубышкин, К.ВШишин и др.) в послеоперационном периоде эрозивно-язвенное поражение гастродуоденальной зоны на вскрытии обнаруживается в 24% случаев, а при тотальной эзофагогастродуоденоскопии - у 50-100% прооперированных больных. Следует отметить, что до 74%, т.е. у 3 из 4 больных, острые эрозии и язвы осложняются кровотечением.
Сам термин «стрессовые острые повреждения гастродуоденальной слизистой» (ОПГС) является собирательным и обозначает эрозивно-язвенное поражение слизистой оболочки желудка и/или ДПК, развившееся у больного в критическом состоянии. Патогенез ОПГС универсален и практически не зависит от особенностей основного заболевания. Установлено, что ОПГС развивается в результате пептического (кислотного) повреждения слизистой оболочки на фоне глубокой ишемии с угнетением всех механизмов гастропротекции: секреции бикарбонатов, муцина, пролиферации желудочного эпителия.
У больных, перенесших оперативное вмешательство, в развитии ОПГС также нельзя исключить влияние гипопротеинемии, анемии, резорбции эндотоксинов, а также последствий анестезии. Тем не менее, многие исследователи настаивают на том, что ОПГС следует рассматривать как острое, ассоциированное с гиперацидностью повреждение гастродуоденальной слизистой оболочки, при котором первичным этиологическим фактором является не хеликобактерный гастрит, как при пептической язве, не длительный прием нестероидных противовоспалительных препаратов (НПВП), как при НПВП-гастропатии, а тяжесть основного заболевания вне зависимости от его этиологии. Тяжесть состояния приводит к гипотонии, ишемии гастродуоденальной слизистой оболочки, которая, в свою очередь, вызывает обратную диффузию Н+, ацидоз, истощение буферных систем, гибель клеток эпителия, приводящие к повреждению целостности слизистой оболочки. Большинство авторов отдают предпочтение концепции ишемического повреждения слизистой оболочки ЖКТ на фоне неадекватного кровоснабжения стенки желудка и ДПК. Результатом стрессорных воздействий является развитие стойкого спазма сосудов чревной зоны с нарушением артериальной перфузии и венозного оттока. Данное состояние приводит к застою крови в слизисто-подслизистом слое желудка и ДПК, локальной гемоконцентрации с последующим возникновением микротромбозов. В дальнейшем восстановление регионарного кровообращения после длительной гипоперфузии приводит к неоклюзионному нарушению спланхнического кровотока, усугублению нарушений оксигенации и создает благоприятные условия для повреждения слизистой оболочки ЖКТ.
Именно на этом фоне в условиях ишемии слизистой оболочки естественная нейтрализация соляной кислоты становится недостаточной, и даже при обычном уровне кислотной продукции развивается ацидоз слизистой оболочки, которая легко подвергается повреждающему воздействию пепсина даже при нормальной кислотной продукции желудка и возникновению эрозий и язв (см. рис. 1).
Рис. 1 Схема развития стрессовых повреждений ЖКТ у больных в критических состояниях.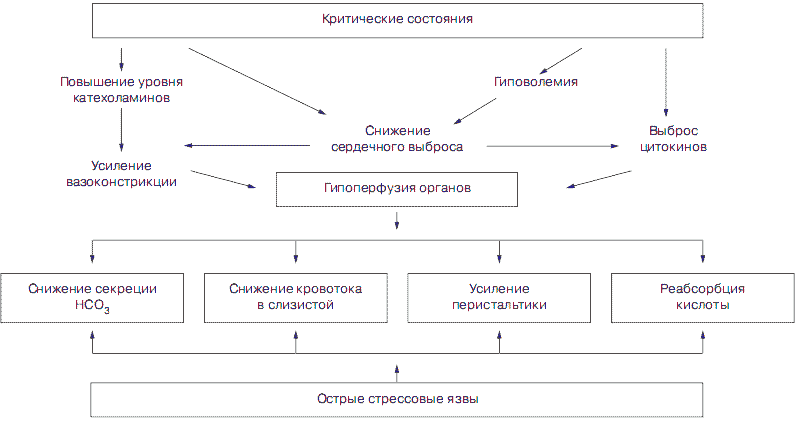
Однако при комбинированной оценке кислотообразующей функции желудка у больных в критических состояниях и послеоперационном периоде (суточное рН мониторирование, титрование) выявлен феномен гиперсекреции соляной кислоты в течение 1-й недели с максимальным подъемом на 3-5-е сутки, что клинически соответствовало манифестации эрозивно-язвенного поражения слизистой оболочки ЖКТ и развития кровотечений.
Как правило, ОПГС бывают множественными, располагаются преимущественно на малой кривизне, реже - в дне и в антральном отделе желудка. Характер повреждений варьирует от поверхностных эрозий до глубоких язв слизистой оболочки желудка и ДПК, часто - множественных и занимающих значительную поверхность слизистой оболочки. Диаметр острых язв обычно не превышает 1 см.
ОПГС необходимо предполагать у любого больного с гипотонией, дыхательной недостаточностью и нарушением перфузии внутренних органов. Установлено, что у пациентов с гипотонией, сепсисом, ожогами, черепно-мозговой травмой и людей, перенесших обширное хирургическое вмешательство, ОПГС развиваются в 40-100% случаев. Однако риски, связанные с ОПГС, обусловлены не собственно частотой этого поражения, а возможностью развития у находящихся в критическом состоянии больных массивного желудочно-кишечного кровотечения (ЖКК), лечение которого исходя из тяжести пациента, представляет весьма трудную и нередко неэффективную задачу. Летальность при ЖКК у критически больных достигает, по разным данным, 50-80%. В то же время определить, насколько распространены ОПГС среди пациентов, находящихся в критическом состоянии, практически невозможно, поскольку для этого требуется проведение эндоскопии всем пациентам отделений интенсивной терапии. Так, при острых формах ишемической болезни сердца, реальную частоту гастродуоденальных поражений отражают результаты отечественного клинико-морфологического исследования, в ходе которого ОПГС были выявлены у 10% умерших от инфаркта миокарда (ИМ).
Впрочем, большинство исследователей согласны с тем, что на самом деле ЖКК у критически больных развиваются гораздо чаще, чем выявляются. По данным С.В.Колобова и соавт. (2002 г.), у больных с ИМ состоявшееся ЖКК в 30% случаев приводит к острой постгеморрагической анемии. При этом известно, что анемия у больных ИМ в 1,5 раза повышает риск госпитальной смерти и в 4 раза - риск массивного ЖКК. В свою очередь, при ЖКК в 2 раза возрастает риск летального исхода (RR-1-4), а сроки лечения в отделении интенсивной терапии удлиняются в среднем на 4-8 дней. Не связанными между собой факторами наиболее высокого риска развития ЖКК у критически больных вне зависимости от основного заболевания являются дыхательная недостаточность, коагулопатия, искусственная вентиляция легких (ИВЛ) более 48 ч (табл. 1; рис. 2).
Таблица 1.
Факторы риска развития стресс-повреждений желудка
Рис. 2. Частота развития кровотечений в зависимости от количества факторов риска (ФР) у пациентов, получавших и не получавших антисекреторную терапию.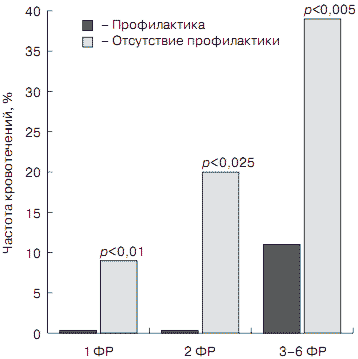
ЖКК при ОГПС носит характер паренхиматозного, часто развивается на 2-5-е сутки после госпитализации больного в отделение интенсивной терапии и начинается бессимптомно. В редких случаях оно сопровождается рвотой с кровью (гематемезис) и черным дегтеобразным стулом (мелена).
Рвота с кровью отмечается обычно при значительной по объему кровопотере (более 500 мл) и, как правило, всегда сопровождается меленой. Артериальное пищеводное кровотечение характеризуется рвотой с примесью неизмененной крови. При желудочном кровотечении в результате взаимодействия гемоглобина с соляной кислотой и образования хлорида гематина рвотные массы имеют вид кофейной гущи. Правда, при выраженной гипохлоргидрии, а также в тех случаях, когда желудочное кровотечение бывает профузным, рвотные массы сохраняют примесь неизмененной крови.
Мелена нередко сопутствует рвоте с кровью, но может наблюдаться и без нее. Мелена характерна для кровотечений из ДПК, но нередко встречается и при более высоко расположенных источниках кровотечения, особенно если оно происходит достаточно медленно. В большинстве случаев мелена обнаруживается не ранее чем через 8 ч после начала кровотечения, причем кровопотери объемом 50-80 мл может быть уже достаточным для ее появления.
К общим симптомам (непрямым признакам) кровотечений из верхних отделов ЖКТ относятся общая слабость, головокружение, ощущения шума в ушах и потемнения в глазах, одышка, тахикардия. В ряде случаев непрямые симптомы ЖКК могут предшествовать возникновению мелены и рвоты с кровью или выступать на передний план в клинической картине. Если выделение алой крови с калом обусловлено кровотечением из нижних отделов ЖКТ, то непрямые симптомы (тахикардия, головокружение, общая слабость и др.) возникают после гематохезии, а не предшествуют ее появлению. Однако в подавляющем большинстве случаев кровотечение протекает бессимптомно
Лечение стрессовых повреждений ЖКТ
Исходя из принципа - «предупредить всегда легче, чем лечить», пациент, соответствующий одному или нескольким критериям риска возникновения стресс-язв гастродуоденальной зоны, нуждается в проведении комплекса профилактических мероприятий (табл. 2). . Согласно доказательным исследованиям абсолютными показаниями для проведения профилактики развития стрессовых язв (эрозий) являются ИВЛ/острая дыхательная недостаточность (ОДН), гипотензия, обусловленная септическим шоком, и коагулопатия (ДВС-синдром). Установлено, что профилактика стресс-язв ЖКТ снижает риск развития ЖКК и не увеличивает частоту развития нозокомиальной пневмонии.
Профилактика стрссерных поражений ЖКТ включает:
Коррекцию гипоперфузии и локальной ишемии гастродуоденальной зоны проводят, используя:
Гастропротекторы
Гастропротекторы включают группу средств, действующих непосредственно на слизистую оболочку желудка и снижающих или препятствующих повреждающему воздействию на нее химических или физических факторов. Используют гастропротекторы для сохранения структуры и основных функций слизистой оболочки и ее компонентов (особенно эндотелия сосудов, обеспечивающих микроциркуляцию в слизистой оболочке). Наиболее изученным препаратом этой группы является сукралфат. При рН<4,0, т.е. в кислой среде, происходит полимеризация препарата, образуется клейкое вещество, которое интенсивно покрывает язвенную поверхность. Язвенную поверхность гель прочно покрывает примерно на 6 ч. Кроме того, препарат стимулирует эндогенный синтез простагландинов, что повышает устойчивость слизистой оболочки желудка к воздействию соляной кислоты. Поскольку соляная кислота является активатором полимеризации сукралфата, нельзя комбинировать последний с антацидами, блокаторами H2-рецепторов и ингибиторами протонной помпы (ИПП).
В ряде случаев используют висмутсодержащие препараты, обладающие цитопртективным действием и способностью уменьшать активность пепсина.
Антациды
По нейтрализующей HCl-активности антациды располагаются следующим образом: магния окись> алюминия гидроокись > кальция карбонат > магния трисиликат > натрия гидрокорбнат. Для достижения адекватной нейтрализации соляной кислоты необходим прием препаратом с интервалом в 2-3 ч. Быстродействующие антациды - натрия гидрокарбонат и кальция карбонат - при взаимодействии с соляной кислотой образуют углекислоту, что вследствие растяжения желудка и повышения в нем давления увеличивает опасность регургитации и аспирации желудочного содержимого в трахею (развитие СОПЛ), а также может быть причиной вторичного увеличения выделения соляной кислоты. Кроме того, все антацидные средства не имеют антипепсиновой активности и не снижают секрецию соляной кислоты, следовательно, не эффективны при кровотечении из стресс-язв и эрозий. Пероральный прием препарата не возможен у больных находящихся на ИВЛ, с угнетенным сознанием. Не приемлем одновременный прием ряда лекарственных препаратов совместно с антацидами, которые нарушают всасывание этих лекарственных средств. Эти ограничения не позволяют использовать антациды в отделениях интенсивной терапии.
Блокаторы Н2-рецепторов
Блокаторы Н2-рецепторов являются конкурентными антагонистами гистамина. В России применяют циметидин, ранитидин, фамотидин. Наиболее выраженно их эффект проявляется в виде угнетения секреции соляной кислоты париетальными клетками желудка. Эти препараты способны значительно блокировать базальную секрецию. Однако активность Н2-блокаторов в отношении стимулированной секреции намного ниже, чем у ИПП. Стимуляция гистамином Н2-рецепторов через аденилат-циклазу повышает содержание циклического аденозин-монофосфата (цАМФ) в париетальных клетках желудка, что сопровождается повышением их секреторной активности. Увеличение цАМФ происходит и в тучных клетках, базофилах, Т-лимфоцитах, клетках миокарда, центральной нервной системы. К сожалению, у 7% госпитализированных больных отмечаются побочные реакции при назначении блокаторов гистаминовых рецепторов (беспокойство, дезориентация, делирий, галлюцинозы). Очевидно, что у больных, находящихся в отделении интенсивной терапии, многие из которых имеют ту или иную степень энцефалопатии, эти побочные эффекты являются нежелательными. Применение блокаторов Н2-рецепторов может привести к отрицательному хроно- и инотропному эффектам, экстрасистолии и атриовентрикулярной блокаде. Особое значение имеет отрицательное действие блокаторов на тромбоциты, так как вызываемая ими тромбоцитопения является дополнительным фактором поддержания коагулопатии. Кроме того, при применении Н2-блокаторов развивается феномен «усталости рецепторов» (эффект тахифилаксии), что сопровождается быстрой потерей ими антисекреторной активности [2, 10]. Это требует увеличения дозы применяемого препарата, а следовательно, повышает риск развития побочных эффектов.
ИПП
ИПП способны удерживать внутрижелудочный рН>4 на протяжении суток и, обладая самой высокой антисекреторной активностью среди разных классов препаратов, уменьшающих секрецию соляной кислоты, вызывают наименьшее число нежелательных побочных явлений. По своей химической структуре ИПП относятся к классу замещенных пиридин-метил-сульфинил-бензимидазолов, отличающихся между собой радикалами в пиридиновом и бензимидазольном кольцах.
ИПП блокируют последний этап синтеза соляной кислоты - работу фермента Н+, К+-АТФазы (протонной помпы) париетальной клетки желудка, обеспечивая активное, мощное и длительное подавление кислотной продукции вне зависимости от природы стимулирующего фактора. Это выгодно отличает ИПП от других антисекреторных средств (блокаторов Н2-гистаминовых рецепторов и М-холинорецепторов), которые блокируют лишь один из многих механизмов кислотной секреции. ИПП обеспечивают оптимальный уровень снижения секреции и длительное сохранение достигнутого эффекта (более 18 ч).
Механизм действия ИПП состоит из стадий абсорбции бензимидазола, его концентрирования в секреторных канальцах париетальных клеток, активации под действием соляной кислоты и связывания с SH-группами Н+, К+-АТФазы. ИПП являются слабыми основаниями, поэтому способны накапливаться в организме только в участках с высокой кислотностью. Они избирательно концентрируются в секреторных канальцах париетальной клетки в форме сульфонамида, стабильного только при рН 1, который не может покинуть эту зону, так как не способен в форме постоянного катиона проникать сквозь биологические мембраны.
ИПП являются наиболее мощными блокаторами желудочной секреции. Они угнетают выработку желудочной секреции соляной кислоты до 100%, причем ввиду необратимости взаимодействия с ферментами (характерно для омепразола) эффект сохраняется в течение нескольких дней. Антисекреторный эффект ингибиторов Н+, К+-АТФазы определяется количеством ингибитора, накопившегося в канальцах париетальной клетки, и периодом полужизни протонного насоса. Длительность действия разных ИПП при использовании равных доз у больных с уровнем интрагастральной рН<2,0 практически одинакова. Повышение дозы препаратов приводит к увеличению его концентрации и усилению антисекреторного эффекта. Следует отметить несоответствие временных характеристик фармакокинетики и фармакодинамики. Максимальная антисекреторная активность лекарственного вещества отмечается, когда препарата уже нет в плазме. ИПП присущ феномен функциональной кумуляции, т.е. в силу необратимости ингибирования протонной помпы идет накопление эффекта, а не препарата. После отмены препарата восстановление продукции соляной кислоты происходит на 4-5-й день после ресинтеза фермента. Важно отметить отсутствие феномена «отдачи» после отмены препаратов этой группы.
Поскольку для образования действующей формы ИПП необходима кислая среда, оптимальная эффективность достигается при приеме препарата за 30 мин до еды. Влияние на внутрижелудочную секрецию ИПП значительно выше, чем у Н2-блокаторов всех поколений. Частота заживления дуоденальных язв при его курсовом назначении приближается к 100%.
Метаболизм ИПП происходит в печени при участии двух изоформ цитохрома Р-450 - CYP2C19 и СУРЗА. Процесс элиминации ИПП зависит от генетической гетерогенности гена, кодирующего эти изоформы цитохрома Р-450. Вариабельность гена CYP2C19 является причиной различий, как в фармакокинетике, так и в фармакодинамике у лиц, принимающих ИПП. Наличие мутаций гена CYP2C19 приводит к увеличению периода полувыведения, площади под кривой «концентрация-время», максимальной концентрации и уменьшению клиренса ИПП.
Наиболее часто используемыми в медицинской практике представителями ингибиторов кислотопродукции на современном этапе являются омепразол, пантопразол, рабепразол и эзомепразол (рис. 3).
Рис. 3. Больная Б., 63 года. Фармакологическая проба с пантопразолом при проведении пролонгированной рН-метрии. Латентный период - 2,49 ч; продолжительность антисекреторного действия - 16 ч 50 мин; время рН>4 - 13,8 ч.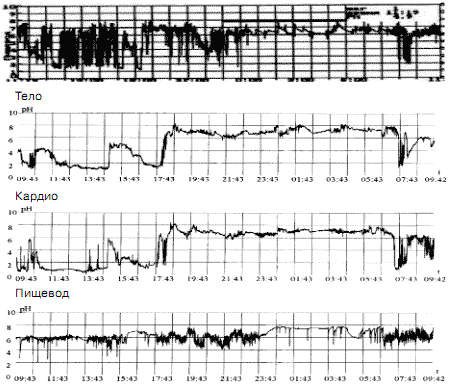
Пантопразол (препарат Контролок) представляет собой высокоэффективный ИПП.
Режим дозирования препарата - болюсно или внутривенная инфузия - определяется индивидуально и зависит от уровня факторов риска развития стрсс-повреждений ЖКТ. При минимальной степени риска показано однократное внутривенное введение 40 мг препарата или непрерывная инфузия со скоростью 2 мг/ч. Если степень риска высока - 2-кратное внутривенное введение по 40 мг или непрерывно со скоростью 4 мг/ч. Согласно результатам ряда метаанализов клинических исследований, терапия ИПП больных в критическом состоянии для профилактики эрозивно-язвенного поражения верхних отделов ЖКТ приводит к снижению потребности в трансфузионой терапии, продолжительности госпитализации и частоты возникновения и рецидивов ЖКК.
Некоторыми авторами высказано опасение, что повышение внутрижелудочного pH может усиливать бактериальную колонизацию в ротоглотке и быть фактором риска развития нозокомиальной пневмонии. Однако это предположение многими исследованиями не подтверждается: риск развития нозокомиальной пневмонии при применении ИПП не увеличивается. Важно, чтобы при этом не было увеличения риска аспирации. Колонизация бактерий в желудке редко приводит к патологической колонизации бактерий в ротоглотке, и риск развития нозокомиальной пневмонии при применении ИПП не увеличивается
Заключение
Стресс-повреждения верхнего отдела ЖКТ играют важную роль в патогенезе и исходах у больных в критических состояниях. Высокая частота возникновения стрессорных язв и эрозий гастродуоденальной зоны, уровень летальности при ЖКК требуют обязательного проведения профилактической терапии больных в критических состояниях. Профилактика должна носить комплексный характер, направленный на поддержание и оптимизацию всех факторов, обеспечивающих структурную и функциональную целостность ЖКТ. Ведущее место здесь по праву пренадлежит высокоэффективным антисекреторным препаратам - ИПП. Важную роль играет возможность парентерального ведения отдельных представителей это группы лекарственных средств, учитывая особенности фармакотерапии больных в критических состояниях. Своевременое и адекватное начало профилактической терапии поможет уменьшить летальность больных в отделениях интенсивной терапии.
Литература 1. Осипов И.С., Скрябин О.Н., Вербицкий ВГ. Профилактика и лечение стресс-язв у больных с полиорганной недостаточностью после хирургических вмешательств и термических травм. Полиорганная недостаточность при шокогенных травмах и острых хирургических заболеваниях органов брюшной полости. СПб, 1992; 42-6.
2. Водолагин ВД. Клиника, диагностика и лечение эрозии желудка и двенадцатиперстной кишки. Клин. мед. 1990; 9: 102-11.
3. Зильбер АП. Медицина критических состояний: общие проблемы. Петрозаводск: Издательство ПГУ, 1995.
4. Патологическая физиология. Под ред. А.Д.Адо, М.А.Адо, ВИ.Пыцкого и др. М.: Триада-Х, 2000.
5. Гельфанд Б.Р., Гурьянов ВА, Мартынов АН. Вестн. интенсивн. тер. 2002; 4: 20-4.
6. Гельфанд Б.Р. и др. Профилактика стресс-язв у больных в критических состояниях. Методические рекомендации РАСХИ. М, 2004.
7. Гостищев ВК., Евсеев М.А Антисекреторная терапия как составляющая часть консервативного гемостаза при острых гастродуоденальных язвенных кровотечениях. Хирургия. 2005; 8: 52-7.
8. Гостищев ВК., Евсеев МА.. Гастродуоденальные кровотечения язвенной этиологии. Руководство для врачей. М., 2008.
9. Исаков В.А. Ингибиторы протонного насоса: их свойства и применение в гастроэнтерологии. М.: ИКЦ «Академкнига», 2001.
10. Литвицкий П.Ф. Патофизиология. М.: ГЭОТАР-Мед, 2002; 1: 752.
11. Гостищев ВК., Евсеев М.А Значение антисекреторной терапии в лечении острых гастродуоденальных язвенных кровотечений. РМЖ. 2004; 12 (24).
12. Degtiareva II, Khatib Z, Lodianaia EV et al. The prevention of stress-related postoperative and drag-induced erosive-ulcerative lesions of the upper digestive tract. Lik Sprava 1995; 3-4: 61-4.
13. Cook DJ, Fuller HD, Guyatt GH et al. Risk factors for gastrointestinal bleeding in critically ill patients: Canadian Crit. Care Trials Groups. N Engl J Med 1994; 330:397-81.
14. Geus WP. Are there indications for intravenous acid-inhibition in the prevention and treatment of upper GI bleeding? Scand J Gastroenterol 2000; Suppl. 232: 10-20.
15. Laterre PF, Horsmans Y. Intravenous omeprazole in critically ill patients: a randomized, crossover study comparing 40 with 80 mg plus 8 mg/hour on intragastric pH. Crit Care Med 2001; 29 (10): 1931-5.
16. Simoens M, Gevers AM, Rutgeerte P. Endoscopic therapy for upper gastrointestinal hemorrhage: A state of the art. Hepatogastroenterology 1999; 46: 737-45.
17. Barkun А, Bandou M, Marshall JK. Consensus recommendations for managing patients with nonvariceal upper gastrointestinal bleeding. Ann Intern Med 2003; 139 (10): 843-57.
18. Kantorova I, Svoboda P., Scheer P et al. Stress ulcer prophylaxis in critically ill patients: а randomized controlled trial. Hepatogastroenterology 2004; 51 (57): 757-61.
19. Moriitomo H, Nagahata V, Urakawa T et el. The mechanism of development of acuta gastric ulceration. Nippon Eeka Gakkai Lasshi 1995; 96 (1): 1-9.
20. Leontiadis GI, Sharma VK, Howden CW. Systematic review and meta-analysis: proton-pump inhibitor treatment for ulcer bleeding reduces transfusion requirements and hospital stay--results from the Cochrane Collaboration. Aliment Pharmacol Ther 2005; 22 (3): 169-74.
21. Leontiadis GI, Sharma VK, Howden CW. Systematic review and meta-analysis: enhanced efficacy of proton-pump inhibitor therapy for peptic ulcer bleeding in Asia--a post hoc analysis from the Cochrane Collaboration. Aliment Pharmacol Ther 2005; 21 (9): 1055-61.
