Воздействие препаратов гидроксиэтилкрахмала на тромбоэластографию у больных мужского пола в предоперационном периоде
СтатьиОпубликовано в журнале:
Вестник службы крови России. »» № 4 декабрь 2004
The effects of hydroxyethyl starch solutions on thromboelastography in preoperative male patients
M. Фелферниг, А. Франц, П. Бройнлих, К. Форингер и С. А Коцек-Лангенекер
Отделение анестезиологии и реанимации, Венский университет, медицинский факультет,
Вена, Австрия
Acta Anaesthesiol Scand 2003; 47; 70-73
Обоснование исследования: Тромбоэластография (TEG) показывает, что действие препаратов гидроксиэтилкрахмала (HES) уменьшает ретракцию сгустка и увеличивает время коагуляции. Применение препаратов гидроксиэтил крахмала, проявляющих минимальные побочные эффекты на коагуляцию, является предпочтительным для увеличения объема плазмы в периоперационном периоде. Сравнение влияния in vivo крупно-, средне- и низкомолекулярных препаратов гидроксиэтилкрахмала на тромбоэла-стографию ранее представлено не было.
Методы: Осуществлялся забор крови до и после внутривенной инфузии (10 мл/кг) физиологического раствора, гидроксиэтилкрахмал 70/0.5/4 (молекулярный вес в кДа / степень замещения / соотношение С2:С6), гидроксиэтилкрахмал 130/0.4/9 или гидроксиэтилкрахмал 450/0.7/4.6 у 50 пациентов без патологии системы гемостаза. После рекальцифика-ции проводилась тромбоэластография в 360 мкл цельной крови с 1% раствором целита, активированного цитратом.
Результаты: Препарат гидроксиэтилкрахмала 450/0.7/4.6 увеличивал время реакции, что свидетельствовало о нарушении плазматического звена системы коагуляции. Тромбоэластографические параметры, определяющие функциональную активность тромбоцитов, включая угол альфа, максимальную амплитуду и время коагуляции, ухудшались после введения препаратов гидроксиэтилкрахмала 450/0.7/4.6 и 70/0.5/4. Препараты гидроксиэтилкрахмала 200/0.6/9.4 и 130/0.4/9 нарушали тромбоцитар-ный гемостаз лишь частично, снижая два или один тромбоцитарных тромбоэластографических параметра.
Выводы: Введение препарата гидроксиэтилкрахмала 450/0.7/4.6 нарушает тромбоэластографические параметры в большей мере, чем другие исследованные препараты гидроксиэтилкрахмала, в то время как гидроксиэтилкрахмал 130\0.4\9 имеет минимальное воздействие. Необходимо проведение дальнейших исследований для изучения клинической значимости наших данных.
Ключевые слова: коагуляция, гидроксиэтил-кархмал, тромбоэластография.
В настоящее время растет уверенность в наличии возможных побочных эффектов препаратов гидроксиэтилкрахмала, используемых для увеличения объема плазмы. Их влияние на коагуляцию крови рассматривается как в экспериментальных работах, in vitro (1-7), так и in vivo (7-9), после внутривенной инфузии. Влияние данных препаратов носило дозо-зависимый эффект (4,5). В последних исследованиях тромбоэластография (TEG) используется для виско-эластических измерений коагуляции во время гемо-дилюции искусственными коллоидами (1-7). Тромбоэластография является чувствительным методом для быстрой оценки статуса плазматического и клеточного гемостаза в тех ситуациях, когда во время операций используются большие количества растворов гидроксиэтилкрахмала (8,10,11). Более того, существуют доказательства, что использование тромбо-эластографии способно предотвратить развитие клинически значимых кровотечений. Обнаружено, что препараты гидроксиэтилкрахмала уменьшают ретракцию сгустка (максимальная амплитуда) и скорость образования сгустка (угол а), а также увеличивают время реакции и коагуляции (r и к) в 16-60 % гемоди-люции (2-8). Подобный паттерн тромбоэластографии показывает наличие гемодилюционной коагулопатии и дисфункции тромбоцитов (10). Сравнение эффектов препаратов гидроксиэтилкрахмала с различной молекулярной массой in vivo с помощью тромбоэластографии также ранее не было представлено. Ранее мы показали, что препарат гидроксиэтилкрахмала 130/0.4/9 (молекулярная масса в кДа / степень замещения / соотношение С2:С6) в меньшей мере подавляет экспрессию активированного гликопротеина 2b-За на мембране тромбоцита, чем другие препараты гидроксиэтилкрахмала (13,14). Целью настоящего исследования, проводимого in vivo, заключалась в проверке предположения, что: гидроксиэтилкрахмал 130/0.4/9 в сравнении с гидроксиэтилкрахмалами 450\0.7\4.6, 200\0.6\9.4 и 70\0.5\4 в меньшей степени нарушает параметры тромбоэластограммы.
Методы.
Пробы крови были взяты у 50 относительно здоровых пациентов мужского пола, подготовленных к таким плановым операциям, как паховое грыжесечение и артроскопия коленного сустава. Все участники эксперимента принадлежали к европеоидной расе, некурящие и в течение 14 дней не принимали каких-либо лекарственных препаратов. Общее число выбранных участников составило 50, и все пациенты с большим желанием хотели участвовать в предполагаемом эксперименте. Исключающими критериями являлись данные анамнеза о наличии кровотечений, почечная дисфункция и заболевания печени. Пациенты воздерживались от приема еды в течение 10 часов, и им не проводилась премедикация перед этим проспективным, рандомизированным и двойным-слепым исследованием. Данное исследование получило поддержку институтского редакционного совета и информированное согласие каждого из 50 участников.
Используя генерированные компьютером таблицы для рандомизации, пациенты были случайным образом разделены в течение 30 минут им проводилась внутривенная тест-инфузия одного из препаратов в дозе 10 мл/кг: 0.9% физиологический раствор (n=10), гидроксиэтилкрахмал 70/0.5/4 (n=10; Экспа-фузин® 6%, Фрезениус Фарма, Австрия, Гамбург; Грац. Австрия), гидроксиэтилкрахмал 130/0.4/9 (п=10; Волювен® 6%, Фрезениус Фарма, Австрия, Гамбург), гидроксиэтилкрахмал 200/0.6/9.4 (п=10; Элохест® 6%, Фрезениус Фарма, Австрия, Гамбург), или гидроксиэтилкрахмал 450/0.7/4.6 {п=10; Плазма-стерил® 6%, Фрезениус Фарма, Австрия, Гамбург). Все препараты гидроксиэтилкрахмала одобрены и доступны в Европе в виде 6% растворов, на 0.9% физиологическом растворе. Образцы крови были взяты как до, так и сразу после контрольной внутривенной инфузии. Забор крови происходил путем венепункции без стаза, из антекубитальной вены, контрлате-рально по отношению к инфузионному доступу, в силиконовые трубки - Вакутейнеры® (Бэктон Дикин-сон. Разефорд, Нью Джерси), содержащие в себе 3,8% цитрата натрия(9;1 v/v) после ликвидации первых 3 мл. Образцы были обработаны в течение 3-х минут. Все образцы крови были получены до введения анестезии при оперативном вмешательстве. Это было предпринято с целью исключения воздействия на коагуляцию анестезии и операции самой по себе.
В настоящем исследовании использовался метод тромбоэластографии как наиболее широко используемый для оценки коагуляционного статуса пациента во время операции, Для проведения тромбоэластографии 340 мкл 1% раствора целита, активированного цитратом, рекальцификацировали введением с 20м 0.2 мол/л кальция хлорида. Проводили анализ при 37° С (Тромбоэластограф®, Хемоскоуп, Мортон Грув, Скоки, Иллинойс). Основной принцип тромбоэластографии описан выше (10). Были зафиксированы следующие параметры тромбоэластографии: время реакции (г), отражающее функцию факторов коагуляции; время коагуляции (к), на которое влияют не только факторы свертывания, но также фибриноген, число и функция тромбоцитов; максимальная амплитуда, отражающая ретракцию сгустка как одну из функций фибриногена и тромбоцитов; и, наконец, угол а, который, как и максимальная амплитуда, находится под влиянием тромбоцитов и фибриногена
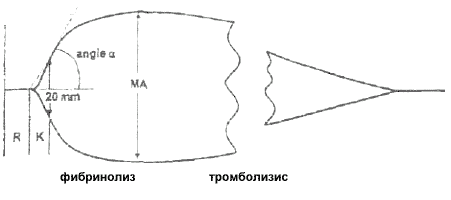
Рисунок 1.
Тромбоэластография. Нормативные параметры: время реакции (r)=1-9мм, максимальная амплитуда (МА)=45-53мм, угол a=45-53 °
Силовой анализ показал, что размер группы в 10 пациентов обеспечит достоверность более 80 % в плане определения различий по максимальной амплитуде, по меньшей мере, с одной стандартной девиацией (СД) между группами гидроксиэтилкрахма-лов 450/0.7/4.6 и 130/0.4/9. Все данные были обработаны для нормального распределения при использованием теста Колмогорова-Смирнова. Влияние внутривенной тест-инфузии на переменные тромбоэластографии было изучено при помощи t-теста. Несоответствия между группами проанализировано с помощью одностороннего анализа параметров, вслед за тестом Дункана, применяемом в сравнительном анализ. Полученные данные рассматриваются как средняя ± стандартное отклонение. Р<0.05 считался статистически достоверным.
Результаты.
Демографические сведения и исходные параметры тромбоэластограммы сравнивались в разных группах (Таблица 1). В исходных параметрах тромбоэластограммы у исследуемых пациентов и в контрольной группе добровольных участников эксперимента значительной разницы не наблюдалось. Внутривенная инфузия физиологического раствора не оказала значительного влияния на параметры тромбоэластографии.
Таблица 1.
Начальные параметры коагуляции.
|
Группа |
Физ.рас-р |
HES 450/0.7/4.6 |
HES 200/0.6/9.4 |
HES 130/0.4/9 |
HES70/0.5/4 |
|
Возраст |
40±15 |
41 ± 14 |
48±14 |
40±11 |
43±14 |
|
Вес (кг) |
77±8 |
86±14 |
80±11 |
86±13 |
89±22 |
|
Вес (см) |
179 ± 6 |
177±6 |
178±7 |
178±4 |
176±9 |
|
Время реакции (мм) |
10.8 ± 3.4 |
9.5±4.5 |
10.4±3.5 |
10.2±3.6 |
9.6±1.4 |
|
Время коаг. (мм) |
5.6±2.3 |
5.7±4.1 |
5.2±3.4 |
.8±1.2 |
4.2±1.3 |
|
Макс. ампл-да (мм) 60±5 |
60±5 |
64±8 |
64±4 |
68±7 |
|
|
Угол а(°) |
56±13 |
56±12 |
59±14 |
56±11 |
60±8 |
Данные рассматриваются как средняя ± СД НЕS=гидроксиэтилкрахмал (молекулярный вес в кДа / степень замещения / коэффициент С2:С6).
Таблица 2.
Воздействие контрольной внутривенной инфузии (10мл) Физ.рас-ра,HES 450/0.7/4.6; HES 200/0.6/9.4;HES 130/0.4/9; HES70/0.5/4 на тромбоэластографические параметры.
|
Группа |
Физ.рас-р |
HES 450/0.7/4.6 |
HES 200/0.6/9.4 |
HES 130/0.4/9 |
HES70/0.5/4 |
|
Время реакции (мм) |
1.1±1.7 |
4.0±4.0*^ |
1.8±3.9 |
1.4±2.4 |
1.6±3.3 |
|
Время коаг. (мм) |
-0.31±4.6 |
2.4±2.8*^ |
0.9±3.9 |
0.6±1.0 |
1.1±1.3*^ |
|
Макс. ампл-да (мм) |
-0.4±3.0 |
-7.3±4.7 |
-6.9±3.7*^ |
-6.4±4.3*^ |
-9.6±7.9*^ |
|
Угол а(°) |
4.4±14 |
-7.0±6.7*^ |
-5.3±7.8*^ |
-5.1±8.4 |
-8.4±3.5*^ |
Приводимые данные абсолютно измененные по сравнению с начальным уровнем (средняя ±СД). Р<0.05, *в сравнении с начальным уровнем, ^в сравнении с группой физиологического раствора, #в сравнении со всеми остальными группами.
НЕS=гидроксиэтилкрахмал (молекулярный вес в кДа/степень замещения / коэффициент С2:С6).
Инфузия гидроксиэтилкрахмала 130/0.4/9 в сравнении с начальным уровнем (Р<0.05) уменьшила максимальную амплитуду, Инфузия гидроксиэтил-крахмала 200/0.6/9.4 уменьшила не только максимальную амплитуду, но и угол а (Р<0.05). Среди исследованных препаратов гидроксиэтилкрахмала снижение максимальной амплитуды и угла а 'было зафиксировано после инфузии гидроксиэтилкрахмала 70\0.5\4. Внутривенное введение HES 70/0.5/4 также увеличивает время коагуляции до статистически достоверного (Р<0.05). Инфузия гидроксиэтилкрахмала 450/0.7/4.6, увеличивая как время реакции, так и время коагуляции, уменьшая максимальную амлитуду по сравнении с начальным уровнем (Р<0.05). Разница максимальной амплитуды между группой гидроксиэтилкрахмала 450/0.7/4.6 и другими группами в пост-инфузионный период являлась статистически достоверной (Р<0.05).
Обсуждение.
Настоящее исследование показывает, что параметры тромбоэластографии (максимальная амплитуда, угол а и время коагуляции к), свидетельствующие о функции тромбоцитов, значительно ухудшались после внутривенной инфузии относительно здоровым пациентам мужского пола, подготовленных к плановым операциям, препаратов гидроксиэтилирах-мала 450/0.7/4.6 и 70/0.5/4 в дозе 10 мл/кг в течение 30 минут. Наоборот, инфузия гидроксиэтилкрахмала 200/0.6/9.4 снижает лишь максимальную амплитуду и угол а, тогда как введение гидроксиэтилкрахмала 130/0.5/9 влияет только на максимальную амплитуду. Данный вывод соответствовал результатам наших предыдущих исследований, заключавшихся в том, что антитромбоцитарное воздействие гидроксиэтилкрахмала 130/0.4/9 как in vivo, так и in vitro проявляется в меньшей степени по сравнении с другими препаратами гидроксиэтилкрахмала (13,14). Молекулы гидроксиэтилкрахмала способны препятствовать воздействию тромбоцитов на ретракцию сгустка, вызывая тромбоцитопению вследствие пассивной дилю-ции (1), прямого подавления функции тромбоцитов (7, 13-15), и влияний на плазматическое звено системы гемостаза, например, на фактор Виллебранда (16,17). Мы обнаружили значительную разницу в сокращении максимальной амплитуды между пациентами, получающими гидроксиэтилкрахмал 450/0.7/4.6 и пациентами всех других групп (Таблица 2). Вывод, что большая молекулярная масса гидроксиэтилкрах-мала нарушает параметры тромбоэластографии в большей степени, чем средне- и низкомолекулярные препараты гидроксиэтилкрахмала, совпадает с нашими предыдущими заключениями (5,17). Показано, что разница в воздействии препаратов гидроксиэтилкрахмала на процесс коагуляции заключается в их средней молекулярной массе (1, 17, 18) и их фармакокинетике, зависящей от степени замещения (19), определяемой как среднее число гидроксиэтиловых групп на долю глюкозы и соотношение С2:С6 (20). Данное соотношение заключается в замещении гидроксиэтиловых групп величинами молекул глюкозы С2 и Сб.
В настоящем исследовании in vivo доказано, что негативное воздействие среднемолекулярного препарата гидроксиэтилкрахмала 200/0.6/9.4 на параметры тромбоэластографии происходит в большей мере, чем влияние низкомолекулярного препарата гидроксиэтилкрахмала 130/0.4/9 (Таблица 2). Интересным явился факт, что более сильная угнетающая способность выявлена у препаратов гидроксиэтилкрахмала 70/0.5/4 с более низкой молекулярной массой, чем у препаратов гидроксиэтилкрахмала 130/0.4/9, который является также низкомолекулярным (Таблица 2). По данным Конрада и др., полученных на анализаторе Sonoclot, гидроксиэтилкрахмал 70/0.5/3.2 оказывает влияние на ретракцию сгустка в большей мере, чем гидроксиэтилкрахмал 200/0.6/9.4 (Таблица 2). Препарат гидроксиэтилкрахмала с низким молекулярным весом 70/0.5/4 нарушает процесс коагуляции в большей степени, чем гидроксиэтил крахмал 200/0.6/9.4 (Таблица 2). Данный вывод подтверждает предыдущий эксперимент, проводимый in vitro, но не совпадает с последней поубликацией (1), в которой утверждается, что гидроксиэтилкрахмал 70/0.5/3.1 in vivo нарушает коагуляцию, сравнительно меньше, чем гидроксиэтилкрахмал 200\0.5\4.6. Причина данного несоответствия по всей вероятности находит, объяснение в разнице молекулярной массы, степени и соотношения замещения гидроксиэтилкрахмала 200/0.5/4.6 в сравнении с 200/0.6/9.4 (20). К сожалению, выявление факторов, определяющих ан-тикоакулянтные свойства препаратов гидроксиэтилкрахмала с различным молярным замещением, но сходным молекулярным весом все еще признается экономически невыгодным.
В заключение необходимо отметить, что в результате тромбоэластографического анализа у пациентов мужского пола показано, что препарат гидроксиэтилкрахмала 130/0.4/9 в меньшей степени нарушает параметры тромбоэластограммы, чем другие растворы гидроксиэтилкрахмала. Разница может оказаться незначительной, но она возрастает при гемо-дидюции альбумином или препаратами гидроксиэтилкрахмала (2). Наше исследование не ставило своей задачей оценку такого клинического исхода как смертность, возникшую в результате развития индуцированных гидроксиэтилкрахмалом нарушений параметров тромбоэластографии. Необходимы дальнейшие рандомизированные, контролируемые исследования, взаимосвязи доза - ответ, особенностей индивидуальных реакций и оценка клинической значимости полученных результатов.
Волювен® - Досье препарата
