Функциональное состояние щитовидной железы в процессе лечения амиодароном
Статьи C.П. Голицын, С.А. Бакалов, Н.Ю. Свириденко, Н.М. Платонова, Н.В. Молашенко, С.Е. СердюкПредыдущий раздел | Оглавление | Следующий раздел
3. ФУНКЦИОНАЛЬНОЕ СОСТОЯНИЕ ЩИТОВИДНОЙ ЖЕЛЕЗЫ В ПРОЦЕССЕ ЛЕЧЕНИЯ АМИОДАРОНОМ
У большинства больных, принимающих амиодарон, сохраняется эутиреоз. Тем не менее у некоторых пациентов может развиться гипотиреоз или тиреотоксикоз. Частота нарушений функции щитовидной железы, по данным зарубежных авторов, колеблется от 2 до 24%, в большинстве случаев от 14 до 18%. Тиреотоксикоз на фоне приема амиодарона часто наблюдается в районах с недостаточным поступлением йода, в то время как гипотиреоз наиболее распространен в йодобеспеченных регионах. В исследованиях, проведенных в зонах с умеренно-низким потреблением йода (Западная Тоскания, Италия) и нормальным потреблением йода (Массачусетс, США), распространенность ТА составила около 10% в Италии и 2% в США, в то время как гипотиреоз встречался в 5 и 22% соответственно.
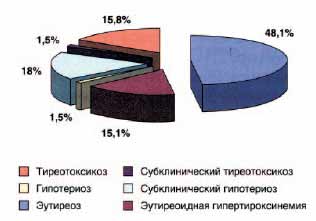
По нашим данным, у лиц старшей возрастной группы (средний возраст 60 лет), проживающих в районе легкого и умеренного йодного дефицита, наиболее часто на фоне приема амиодарона выявлялся субклинический гипотиреоз (18%) и манифестный тиреотоксикоз (15,8%), реже - явный гипотиреоз (1,5%) и субклинический тиреотоксикоз (1,5%). Эутиреоидное состояние сохранялось у 48,1% больных ив 15,1% случаев выявлялась эутиреоидная гипертироксинемия (рис. 6). При этом у пациентов с исходной сопутствующей патологией ЩЖ общая частота тиреотоксикоза и гипотиреоза, развившихся на фоне приема амиодарона была выше, чем у пациентов без патологии ЩЖ-и составила 49 и 25% соответственно (рис. 7).
Рис. 7. Функциональное состояние щитовидной железы у пациентов, принимающих амиодарон в течение 12-164 месяцев
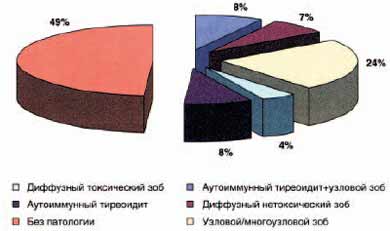
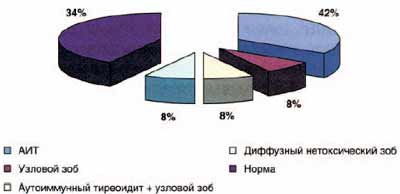
Следует отметить, что у лиц, получающих амиодарон, сопутствующая патология щитовидной железы выявлялась в 51,2% случаев, причем большую часть составили пациенты с узловым и многоузловым зобом (рис. 8). Высокая распространенность тиреоидной патологии характерна для иоддефицитных районов, к которым относится Москва и Московская область.
Рис. 8. Структура патологии щитовидной железы у пациентов, принимающих амиодарон в течение 12-164 месяцев
3.1. ДИНАМИКА УРОВНЯ ТИРЕОИДНЫХ ГОРМОНОВ И ТТГ У ЭУТИРЕОИДНЫХ ЛИЦ НА ФОНЕ ПРИЕМА АМИОДАРОНА
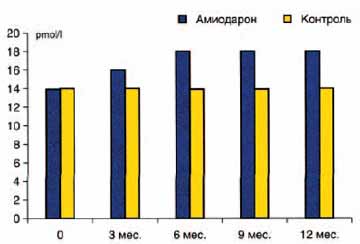
Функциональные тесты, оценивающие состояние щитовидной железы у пациентов, получающих амиодарон, имеют другой диапазон нормальных значений, чем у эутиреоидных лиц, не принимающих препарат. Установлено, что у 1/3 пациентов в процессе лечения амиодароном наблюдается повышение уровня общего и свободного Т4, рТ3, уменьшение уровня Т3. Это обусловлено подавлением активности 5-дейодиназы I типа, нарушающим конверсию Т4 в Т3 в периферических тканях, особенно в печени. Динамика уровня св. Т4 на фоне приема амиодарона представлена на рис. 9. Подавление активности 5-дейодиназы может сохраняться на протяжении нескольких месяцев и после отмены препарата. Кроме того, препарат снижает проникновение тиреоидных гормонов в клетки периферических тканей. В конечном итоге оба механизма способствуют развитию доброкачественной формы эутиреоидной гипертироксинемии, с повышенным уровнем общего и св. Т4, рТ3, нормальным или субнормальным Т3. Несмотря на повышенный уровень, у пациентов не отмечается признаков тиреотоксикоза.
Рис. 9. Динамика показателей св. Т4 у пациентов без патологии щитовидной железы (n=84), принимающих амиодарон (контроль - пациенты с ИБС не принимающие амиодарон, n=40)
В нашем исследовании эутиреоидная гипертироксинемия наблюдалась у 20 человек (15,1%). Уровень ТТГ составил 1,3 мЕ/л [1; 2], св. Т4 - 23,9 пмоль/л [22,4; 25,9], св. Т3-5,6 пмоль/л [5; 6,4].
В настоящее время эутиреоидная гипертироксинемия рассматривается как лабораторный феномен, развивающийся на фоне приема амиодарона. Это состояние не требует медикаментозной коррекции, а диагноз тиреотоксикоза не должен базироваться на одном только обнаружении повышенного уровня тироксина у больных, получающих амиодарон.
По нашим данным, развитие эутиреоидной гипертироксинемии не приводит к утрате амиодароном антиаритмической эффективности и рецидивам предшествующих нарушений сердечного ритма. Пациенты должны оставаться под динамическим наблюдением с периодическим мониторированием функционального состояния щитовидной железы.
В процессе лечения амиодароном у ряда больных может произойти изменение уровня ТТГ в сыворотке крови без клинических проявлений нарушения функции щитовидной железы. Повышение концентрации ТТГ у клинически эутиреоидных пациентов, зависит как от дозы, так и длительности приема препарата. Так, при ежедневном приеме 200-400 мг амиодарона уровень ТТГ обычно находится в пределах нормы. При более высокой дозе препарата увеличение концентрации ТТГ может произойти в первые месяцы приема с последующим возвращением к норме (таблица 5).
Таблица 5. Возможные изменения уровня тиреоидных гормонов и ТТГ у эутиреоидных пациентов в процессе лечения амиодароном
| Показатель | Длительность терапии менее 3 месяцев | Длительность терапии более 3 месяцев |
| Т4 или св. Т4 | норма или повышен | повышен на 40% от исходного |
| Т3 или св. Т3 | понижен | понижен или нормальный |
| рТ3 | повышен | повышен |
| ТТГ | норма или повышен | норма |
3.2. ТИРЕОТОКСИКОЗ, ВЫЯВЛЯЕМЫЙ НА ФОНЕ ПРИЕМА АМИОДАРОНА
Тиреотоксикоз на фоне приема амиодарона наиболее часто встречается в йоддефицитных регионах (например, Европа) и преимущественно развивается у мужчин (соотношение полов составляет 3:1). ТА может развиться как в первые месяцы, так и через несколько лет лечения. Благодаря накоплению препарата и его метаболита в тканях, а также их медленному выведению из организма ТА может развиться даже через несколько месяцев после отмены препарата. На сегодняшний день нет четких критериев, позволяющих предсказать развитие ТА у пациентов. Наличие сопутствующей патологии щитовидной железы - узлового зоба с накоплением радиоактивного препарата в зоне узла - может являться фактором риска развития ТА.
3.2.1. ПАТОГЕНЕЗ АМИОДАРОН-АССОЦИИРОВАННОГО ТИРЕОТОКСИКОЗА
Патогенез ТА сложен и полностью не изучен. Заболевание встречается у лиц как с исходной патологией щитовидной железы, так и без таковой. В исследованиях, проведенных в районах с умеренным дефицитом йода, среди пациентов с ТА диффузный зоб определялся в 29% случаев, узловой зоб в 38%, а в оставшихся 33% щитовидная железа была без патологических изменений.
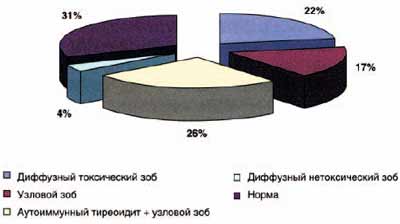
По нашим данным, среди пациентов с ТА, проживающих в районе легкого и умеренного йодного дефицита (Москва и Московская область), преобладали лица с измененной щитовидной железой (61%), в основном с узловыми зобами и аутоиммунным поражением щитовидной железы (рис. 10).
Рис. 10. Структура патологии щитовидной железы у лиц с тиреотоксикозом, развившимся на фоне приема амиодарона
Необходимо отметить, что гуморальный аутоиммунитет играет небольшую роль в развитии ТА.
Считается, что в основе патогенеза тиреотоксикоза на фоне приема амиодарона лежат два основных механизма, согласно которым выделяют два типа амиодарон-ассоциированного тиреотоксикоза:
1. Амиодарон-ассоциированный тиреотоксикоз 1 типа (ТА 1 типа) развивается в основном у лиц с исходной патологией в щитовидной железе, включая узловой зоб, автономию или субклинический вариант диффузного токсического зоба. ТА 1 типа аналогичен феномену иодиндуцированного тиреотоксикоза, который встречается у лиц с эндемическим зобом при длительном приеме йода, поэтому частота встречаемости ТА 1 типа в зонах йодного дефицита значительно выше, чем других форм ТА. Йод, высвобождаемый из препарата, приводит к повышению синтеза тиреоидных гормонов в существующих зонах автономии в железе.
2. Амиодарон-ассоциированный тиреотоксикоз 2 типа (ТА 2 типа) описан у пациентов без предшествующих или сопутствующих заболеваний ЩЖ и связан с развитием деструктивных процессов в железе, причиной которых является действие самого амиодарона, а не только йода (т. е. форма лекарственного тиреоидита), и выходом ранее синтезированных гормонов в кровоток. У пациентов, перенесших деструктивный тиреотоксикоз, позже может развиться гипотиреоз, особенно в ответ на прием фармакологических доз йода.
ТА смешанного типа - форма тиреотоксикоза, сочетающая черты ТА I и ТА 2 типов. Как правило, такой диагноз ставится ретроспективно, в ходе исследования послеоперационного материала ткани щитовидной железы или исходя из клиники заболевания (тяжесть тиреотоксикоза, отсутствие эффекта от приема тиреостатиков).
3.2.2. КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ И ДИАГНОСТИКА АМИОДАРОН-АССОЦИИРОВАННОГО ТИРЕОТОКСИКОЗА
Благодаря антиадренергической активности амиодарона и его блокирующего влияния на конверсию Т4 в Т3, классические симптомы тиреотоксикоза - зоб, потливость, тремор рук, потеря веса - могут быть выражены незначительно или вовсе отсутствовать. В клинической картине, как правило, доминируют сердечнососудистые и психические расстройства. Больные предъявляют жалобы на учащенное сердцебиение, одышку при физической нагрузке, утомляемость. При осмотре у больных фиксируется тахикардия, увеличение разницы пульсового давления, систолический шум.
Токсическое действие тиреоидных гормонов на центральную нервную систему приводит к развитию тиреотоксической энцефалопатии, которая проявляется нервной возбудимостью, эмоциональной лабильностью, нарушением сна. Однако у больных пожилого возраста, как правило, доминируют противоположные признаки: психическая заторможенность, апатия, отсутствие аппетита, слабость, адинамия, депрессия, что может затруднять диагностику ТА.
Серьезную опасность представляет именно действие избытка тиреоидных гормонов на сердечно-сосудистую систему: ухудшение течения аритмий, стенокардии у больных ИБС. Повышенная чувствительность кардиомиоцитов к адренергической стимуляции при тиреотоксикозе может увеличивать частоту желудочковых аритмий, особенно у больных с предшествующей сердечной патологией. Тиреоидные гормоны непосредственно влияют на электрофизиологические свойства предсердных миоцитов. Укорачивая их рефрактерный период, они способствуют формированию условий для повторного входа волны возбуждения и возникновению фибрилляции предсердий. При нераспознанном и длительно существующем тиреотоксикозе может развиться синдром дилатационной кардиомиопатии, проявляющийся снижением насосной функции сердца и появлением сердечной недостаточности.
Ухудшение течения существующих аритмий у пациентов, принимающих амиодарон, является показанием для обследования функционального состояния щитовидной железы.
Диагностика тиреотоксикоза основывается на определении уровня ТТГ в сыворотке с помощью радиоиммунометрического анализа третьего поколения. Снижение уровня ТТГ ниже нижней границы нормы свидетельствует о развитии тиреотоксикоза. При манифестном тиреотоксикозе снижение уровня ТТГ сопровождается повышением уровня св. Т4, нормальным или повышенным уровнем св. Т3. При субклиническом варианте уровни св. Т4 и св. Т3 остаются в пределах нормы. Исследование св. Т3 проводят в том случае, если уровень св. Т4 не превышает нормальных величин.
3.2.3. ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА АМИОДАРОН-АССОЦИИРОВАННОГО ТИРЕОТОКСИКОЗА 1 И 2 ТИПОВ
Для клинициста важно дифференцировать две формы ТА для выбора правильной тактики ведения пациентов.
Как было сказано выше, ТА I типа развивается на фоне существующих или предшествующих заболеваний щитовидной железы. Помимо изменений уровня тиреоидных гормонов, ТТГ и определения повышенного титра тиреоидных антител (в случаях манифестации ДТ3), ТА 1 типа характеризуется нормальным или повышенным захватом радиоактивного йода (рис.11), умеренно повышенным уровнем ИЛ-6. При УЗИ с доплерографией выявляются признаки сопутствующей патологии: узлового зоба или ДТ3 с нормальным или повышенным кровотоком (рис. 12а).
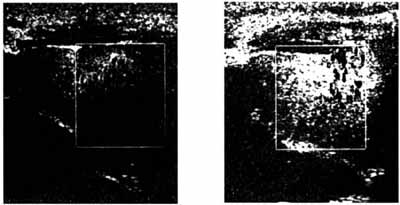
Рис. 11. Сцинтиграфия ЩЖ с Тс99: распределение РФП в обеих долях неравномерное. В нижнем сегменте левой доли накопление РФП повышено - функционирующий узел
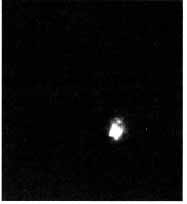
Рис. 12а. Экограмма пациентки П., 50 лет, с тиреотоксикозом, развившимся на фоне приема кордарона. Выявлено: снижение эхогенности ткани ЩЖ и отсутствие повышения кровотока (выделено рамкой)
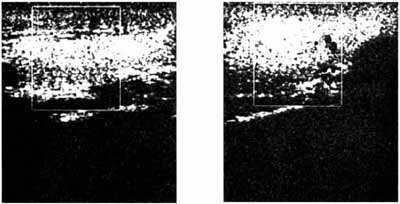
ТА 2 типа развивается на фоне интактной железы. Главная клиническая особенность этой формы - тяжесть тиреотоксикоза, в том числе развитие болевых форм, клинически похожих на подострый тиреоидит. При исследовании с радиоактивным йодом отмечается снижение накопления препарата в железе. В биоптате щитовидной железы, полученном при тонкоигольной биопсии или после хирургического вмешательства, выявляется большое количество коллоида, инфильтрация макрофагами, деструкция тиреоцитов. При УЗИ с доплерографией часто наблюдается отсутствие или снижение кровотока в щитовидной железе (рис. 12б). Уровень антител к ТПО, ТГ, рецептору ТТГ не превышают нормальных значений.
Рис. 12б. Экограмма ЩЖ пациента И., 55 лет, с тиреотоксикозом, развившимся на фоне приема кордарона. У пациента многоузловой зоб с аутоиммунным поражением ткани ЩЖ. Выявлено: повышение кровотока в ЩЖ (выделено рамкой)
В литературе обсуждается роль повышенной концентрации ИЛ-6 как маркера этого состояния, однако в нашем исследовании мы не обнаружили существенных различий в уровне ИЛ-6 и косвенно.
Кроме этих двух форм в практике клинициста могут встречаться смешанные варианты течения этого осложнения с чертами ТА I и 2 типов. Сводные данные об отличии двух форм представлены в таблице 6.
Таблица 6. Особенности амиодарон-ассоциированного тиреотоксикоза 1 и 2 типов
| ТА 1 ТИПА | ТА 2 ТИПА | |
| Исходная патология ЩЖ | Есть | Нет |
| Пальпация ЩЖ | Узловой или диффузный зоб | Норма или небольшой зоб,чувствительный при пальпации |
| Цветовое доплеровское картирование при УЗИ ЩЖ | Кровоток выражен умеренно | Кровоток отсутствует |
| Патогенетический механизм | Избыточный синтез и секреция тиреоидных гормонов | Избыточное высвобождение тиреоидных гормонов |
| Терапия | Тиреостатики | ГСК как монотерапия или в комбинации с тиреостатиками |
| Влияние избытка йода после тиреотоксической фазы | Вероятен йодиндуцированный гипотиреоз | Вероятен йодиндуцированный гипотиреоз |
Примечание: ГКС - глюкокортикостероиды
3.2.4. АНТИАРИТМИЧЕСКАЯ ЭФФЕКТИВНОСТЬ АМИОДАРОНА НА ФОНЕ АМИОДАРОН-АССОЦИИРОВАННОГО ТИРЕОТОКСИКОЗА
Тиреоидные гормоны оказывают многообразное действие на сердечно-сосудистую систему, путем как прямого связывания Т3 с рецепторами кардиомиоцитов, так и опосредованного влияния через активацию симпатической нервной системы.
При тиреотоксикозе происходит ускорение фазы диастолической деполяризации, потенциала действия клеток синусового узла, неравномерное укорочение рефрактерных периодов предсердных миоцитов, что обуславливает возникновение электрической гетерогенности миокарда предсердий. Происходит также укорочение рефрактерного периода АВ-узла, повышается чувствительность к адренергической стимуляции, что может провоцировать возникновение наджелудочковых аритмий, прежде всего фибрилляции предсердий, а также желудочковых нарушений ритма сердца, особенно у больных с органической патологией миокарда.
В нашем исследовании основным и наиболее ранним проявлением амиодарон-ассоциированного гипертиреоза явилась потеря антиаритмической эффективности амиодарона во всех случаях. У пациентов с пароксизмами желудочковой тахикардии и мерцательной аритмией, отмечалось рецидивирование нарушений ритма сердца. У больных с желудочковой экстрасистолией по результатам суточного мониторирования ЭКГ отмечалось увеличение общего количества парных желудочковых экстрасистол и пробежек желудочковой тахикардии на 61,7, 83,5 и 85% соответственно, по сравнению с показателями, регистрировавшимися до развития гипертиреоза.
У 87,5% наших больных коррекция гипертиреоза успешно проводилась на фоне продолжающейся терапии амиодароном. Во всех этих случаях отмена препарата оказалась невозможной в связи с наличием у больных жизнеугрожающих нарушений ритма сердца либо в связи с резистентностью к ранее использовавшейся антиаритмической терапии.
И только в 12,5% случаев коррекция функции щитовидной железы проводилась в условиях отмены амиодарона, в связи с отсутствием витальных показаний к применению препарата и возможностью использования других антиаритмических средств после достижения эутиреоза.
Компенсация гипертиреоза в условиях продолжающегося приема амиодарона у всех больных с пароксизмами желудочковой тахикардии и мерцательной аритмией сопровождалась исчезновением приступов. У больных с желудочковой экстрасистол ней при тех же условиях коррекции гипертиреоза, по данным суточного мониторирования ЭКГ, и было зафиксировано достоверное снижение количества желудочковых эктопических комплексов. Общее количество желудочковых экстрасистол снизилось в среднем на 39,7%, парных желудочковых экстрасистол на 74,9%. У всех пациентов было отмечено полное устранение пробежек желудочковой тахикардии.
Таким образом, необходимо подчеркнуть, что развитие амиодарон-ассоциированного гипертиреоза в отличие от эутиреоиднои гипертироксинемии сопряжено с утратой антиаритмической эффективности амиодарона, а его коррекция с ее восстановлением.
Рецидивирование нарушений ритма сердца у больных, принимающих амиодарон, должно служить основанием для внеочередного мониторирования функции щитовидной железы с целью исключения гипертиреоза, единственным проявлением которого они могут являться.
3.2.5. ЛЕЧЕНИЕ АМИОДАРОН-АССОЦИИРОВАННОГО ТИРЕОТОКСИКОЗА
Компенсация тиреотоксикоза, развившегося на фоне приема амиодарона, сопряжена со многими трудностями и требует индивидуального подхода в каждом случае. Для лечения тиреотоксикоза применяют тионамиды, глюкокортикоиды, плазмаферез, радиойодтерапию, оперативное лечение, за рубежом - блокатор поступления йода в щитовидную железу - перхлорат калия.
Так как интратиреоидное содержание йода у пациентов с ТА высокое, для подавления синтеза тиреоидных гормонов рекомендуется применение больших доз антитиреоидных препаратов (тирозол, мерказолил, метизол 40-80 мг или пропицил 400-800 мг). Сроки медикаментозной компенсации удлиняются. Эутиреоз, как правило, восстанавливается через 6-12 недель. Доза тиреостатика должна снижаться после лабораторной компенсации тиреотоксикоза (нормализация уровня св. Т4).
Схема 1. Алгоритм лечения амиодарон-ассоциированного тиреотоксикоза
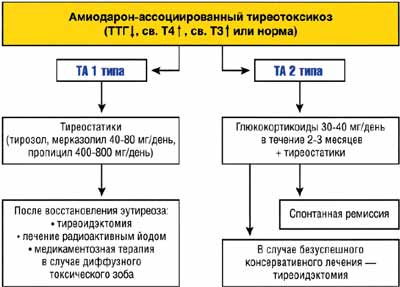
Длительная терапия высокими дозами тионамидов обычно необходима пациентам, которые продолжают получать амиодарон по жизненным показаниям. Ряд авторов предпочитают продолжать терапию поддерживающими дозами тиреостатиков в течение всего периода лечения антиаритмиком (т. е. пожизненно) для того, чтобы поддержать полный или частичный блок синтеза тиреоидных гормонов.
Одним из главных фактов патогенеза ТА 2 типа, особенно возникшего у лиц без предшествующих изменений щитовидной железы, предполагается развитие деструктивного тиреоидита и выход ранее синтезированных гормонов в кровоток. В такой ситуации предлагается использовать глюкокортикоиды. Преднизолон назначается в дозе 30-40 мг/сут. Курс лечения может продолжаться до 3 месяцев, так как описаны случаи возобновления симптомов тиреотоксикоза при попытке снизить дозу препарата.
В случае развития гипотиреоза у пациентов, перенесших ТА 2 типа, к лечению добавляется L-тироксин.
При тяжелом течении амиодарон-ассоциированного тиреотоксикоза (обычно при сочетании 2 форм) используют комбинацию тионамида и глюкокортикоида. У некоторых пациентов комбинированная лекарственная терапия может быть неэффективна, что требует хирургического вмешательства. Оперативное лечение обычно проводится в случае невозможности достижения компенсации заболевания после длительного (около 6 месяцев) курса медикаментозной терапии или при сочетании амиодарон-ассоциированного тиреотоксикоза с узловым зобом. Несмотря на риск тиреотоксического криза во время анестезии и хирургического вмешательства в мире накоплен опыт лечения таких больных, показавший, что субтотальная резекция щитовидной железы позволяет быстро добиться ремиссии тиреотоксикоза и продолжить антиаритмическую терапию. При крайне тяжелом состоянии используют плазмаферез.
В районах с пограничным йодным дефицитом пациентам с диффузным или узловым зобом, имеющим нормальное или повышенное поглощение радиоизотопа, при отсутствии эффекта от консервативной терапии показано лечение радиоактивным йодом.
Как было отмечено выше, амиодарон назначается при тяжелых, жизнеугрожающих аритмиях, часто рефрактерных к другой терапии. Отмена препарата в такой ситуации может быть недопустима по жизненным показаниям. Поэтому в лечебной практике в случае невозможности прекращения приема антиаритмика компенсацию тиреотоксикоза проводят на фоне продолжающейся терапии амиодароном. Более того, поскольку препарат и его метаболит ДЭА вызывают развитие «местного гипотиреоза», парадоксально, но это защищает сердце от действия избытка тиреоидных гормонов, поэтому отмена препарата может усилить токсическое действие тиреоидных гормонов на сердце. В литературе описаны случаи успешного ведения пациентов с тиреотоксикозом без отмены амиодарона, поэтому в каждом конкретном случае решение о смене антиаритмического препарата должно приниматься индивидуально в союзе кардиолога и эндокринолога. Ряд авторов предполагают, что даже в тех случаях, когда планируется отмена препарата, пациенты должны принимать амиодарон, пока тиреотоксикоз не будет полностью компенсирован.
3.3. ГИПОТИРЕОЗ, ВЫЯВЛЯЕМЫЙ НА ФОНЕ ПРИЕМА АМИОДАРОНА
Распространенность гипотиреоза на фоне приема амиодарона колеблется в пределах от 6% в странах с низким потреблением йода до 13% с высоким потреблением йода. Наиболее часто гипотиреоз встречается у пожилых и женщин, распространенность тиреоидной патологии среди которых особенно высока (отношение полов 1,5:1).
Поданным нашего исследования среди пациентов с амиодарон-ассоциированным гипотиреозом органическая патология щитовидной железы выявлена в 70,8% случаев (в основном аутоиммунный тиреоидит) (рис. 13).
Рис. 13. Структура патологии щитовидной железы у лиц с гипотиреозом, развившимся на фоне приема амиодарона
У лиц с сопутствующим аутоиммунным тиреоидитом лечение амиодароном, как правило, ускоряет развитие гипотиреоза. Амиодарон-ассоциированный гипотиреоз может быть транзиторным или постоянным, последний почти всегда связан с предшествующими нарушениями в щитовидной железе. Гипотиреоз обычно манифестирует рано, но иногда и после 18 месяцев лечения.
Рис. 13. Структура патологии щитовидной железы у лиц с гипотиреозом, развившимся на фоне приема амиодарона
3.3.1. ПАТОГЕНЕЗ АМИОДАРОН-АССОЦИИРОВАННОГО ГИПОТИРЕОЗА
Возникновение гипотиреоза объясняется длительным блоком органификации йода в щитовидной железе вследствие нарушения «ускользания» от эффекта Вольфа-Чайкова. По современным представлениям, основной механизм, обеспечивающий «ускользание» от ингибирующего влияния эффекта Вольфа-Чайкова, - блокирование поступления йода в щитовидную железу за счет снижения активности Na/I-симпортера, что приводит к уменьшению интратиреоидного содержания элемента. Этот процесс позволяет восстановить органификацию йода в железе, несмотря на высокое содержание элемента в плазме. Однако во время терапии амиодароном интратиреоидное содержание йода очень высоко, несмотря на блокированный транспорт элемента. Следовательно, существуют дополнительные механизмы накопления йода в железе при приеме амиодарона. Предполагается, что амиодарон, благодаря своей липофильности, попадает внутрь клеток и внутри тиреоцитов из препарата высвобождается йод. Кроме того, амиодарон оказывает токсическое влияние на щитовидную железу, приводя к уменьшению количества тиреоцитов, что в комбинации с высвобождением большого количества йода снижает функциональную активность железы.
Наиболее часто ГА встречается у пациентов с сопутствующим аутоиммунным тиреоидитом. У пациентов без органической патологии щитовидной железы и нормальным уровнем антител к ТГ и ТПО как причины ГА рассматриваются: скрытые дефекты органификации йода и синтеза тиреоидных гормонов на фоне приема фармакологических доз йода и развитие деструкции тиреоцитов с уменьшением числа функционирующих клеток.
3.3.2. КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ И ДИАГНОСТИКА АМИОДАРОН-АССОЦИИРОВАННОГО ГИПОТИРЕОЗА
В клинической картине ГА отмечаются классические признаки: утомляемость, сухость кожи, зябкость, запоры, сонливость, ухудшение внимания, отечный синдром, брадиаритмии и др. Субклинический вариант гипотиреоза может протекать бессимптомно, но возможны признаки легкой тиреоидной недостаточности (изменения в эмоциональной сфере, ухудшение памяти, депрессия) в сочетании с нарушениями липидного обмена (повышение ЛПНП, коэффициентов охс/ЛПВП, ЛПНП/ЛПВП и снижение ЛПВП). Депрессия при сГА характеризуется чувством паники и более «бедным» ответом на лечение антидепрессантами. Считается, что субклинический гипотиреоз не является причиной развития депрессии, но он может снижать порог развития депрессивных состояний и затруднять коррекцию этих нарушений. Со стороны сердечно-сосудистой системы у лиц с субклиническим гипотиреозом и ИБС может отмечаться обострение коронарной недостаточности, а также тенденция к повышению показателей диастолического артериального давления по сравнению с пациентами в эутиреозе. Среди других признаков, встречающихся у пациентов с субклиническим гипотиреозом, можно отметить развитие гипохромной анемии, миалгии, снижение ахиллова рефлекса.
Жалобы больных, как правило, связываются с гипотиреозом только после обнаружения гормональных изменений, но у 25-50% пациентов их можно выявить при целенаправленном расспросе.
Диагностика гипотиреоза основана на определении сниженного уровня свободного Т4 и повышенного уровня ТТГ либо изолированного повышения ТТГ при субклиническом гипотиреозе. Уровень Т3 не является надежным индикатором, так как у эутиреоидных пациентов, принимающих амиодарон, он может быть низким, а при гипотиреозе - в пределах нормы.
3.3.3. АНТИАРИТМИЧЕСКАЯ ЭФФЕКТИВНОСТЬ АМИОДАРОНА НА ФОНЕ АМИОДАРОН-АССОЦИИРОВАННОГО ГИПОТИРЕОЗА
Поданным нашего исследования среди пациентов с амиодарон-ассоциированным гипотиреозом органическая патология щитовидной железы выявлена в 70,8% случаев (в основном аутоиммунный тиреоидит) (рис. 13).
3.3.4. ЛЕЧЕНИЕ АМИОДАРОН-АССОЦИИРОВАННОГО ГИПОТИРЕОЗА
Амиодарон-ассоциированный гипотиреоз может быть устранен двумя путями: отменой амиодарона либо подбором заместительной терапии тиреоидными гормонами при продолжающемся приеме препарата. После отмены амиодарона эутиреоз обычно восстанавливается, но на это могут потребоваться месяцы в связи с длительным периодом выведения лекарства. На практике в подавляющем большинстве случаев отмена амиодарона невозможна, так как препарат применяется по жизненным показаниям, особенно для лечения тяжелых желудочковых тахиаритмий. В таких случаях лечение амиодароном обычно продолжают и пациентам назначается L-тироксин для снижения уровня ТТГ до верхней границы нормы. Рекомендуется начинать заместительную терапию тиреоидными гормонами с минимальных доз 12,5-25 мкг в сутки с постепенным повышением ее с интервалом 4-6 недель до эффективной под контролем ТТГ, ЭКГ или мониторирования ЭКГ по Holter, не допуская при этом декомпенсации кардиальной патологии или развития аритмии.
При субклиническом течении гипотиреоза вопрос о заместительной терапии решается индивидуально. В зависимости от возраста, наличия или отсутствия ИБС. Назначение L-тироксина может быть показано при сопутствующем нарушении липидного профиля, депрессии, причем подбирается минимально эффективная доза для коррекции выявленных нарушений. Уровень ТТГ является главным параметром при мониторинге заместительной терапии. Пациент должен оставаться под наблюдением с целью оценки динамики состояния на фоне лечения первые 6 недель, а затем каждые 3 месяца. При отсутствии изменений в лабораторных показателях липидного спектра и клинической симптоматики - препарат отменяют.
- Показанием к назначению терапии левотироксином пациентам с сопутствующей кардиальной патологией и субклиническим гипотиреозом является уровень ТТГ выше 10 мЕд/л для профилактики развития клинического гипотиреоза и дислипидемии.
- Показанием к назначению терапии левотироксином пациентам с сопутствующей кардиальной патологией и субклиническим гипотиреозом при уровне ТТГ менее 10 мЕд/л является наличие дислипидемии.
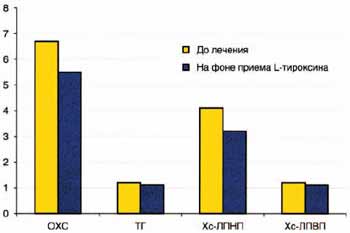
По нашим данным, назначение заместительной терапии L-тироксином при субклиническом гипотиреозе по индивидуальным показаниям у лиц старшей возрастной группы с использованием минимально эффективных доз препарата позволяет улучшить показатели липидного спектра крови. Доза L-тироксина у наших больных составила 37,5 мкг (25; 50 мкг), средний уровень ТТГ 3,3 мЕд/л [2,9; 4,2], компенсация достигалась в среднем через 6 месяцев (4,0; 9,0). На фоне лечения произошло достоверное снижение показателей общего холестерина и Хс-ЛПНП (рис. 14).
Рис. 14. Структура патологии щитовидной железы у лиц с гипотиреозом, развившимся на фоне приема амиодарона
В случаях, когда отмена амиодарона невозможна, заместительную терапию проводят на фоне продолжения приема антиаритмика. При отсутствии показаний к проведению заместительной терапии пациентам с субклиническим гипотиреозом, развившимся на фоне приема амиодарона, показано динамическое наблюдение: определение ТТГ 1 раз в 6 месяцев.
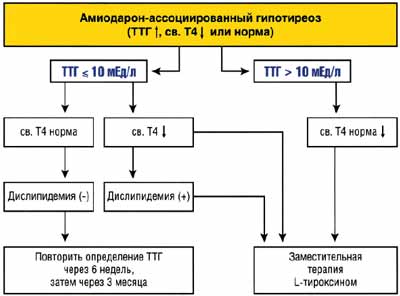
Схема 2. Алгоритм лечения амиодарон-ассоциированного гипотиреоза
Предыдущий раздел | Оглавление | Следующий раздел
Комментарии
ПРАКТИКА ПЕДИАТРА
