Лечение ОРВИ и гриппа в амбулаторнополиклинической практике: Результаты международной наблюдательной неинтервенционной программы «Эрмитаж»
СтатьиОпубликовано в журнале:
Терапия №8 (18) 2017
Н.А. Геппе1, С.Т. Валиева2, Н.А. Фараджева2, М.Р. Оганян3, Г.Т. Мырзабекова4, М.А. Жанузаков4, А.К. Катарбаев5, Л.Н. Скучалина6, Н.С. Айткулуев7, Д.Д. Кабаева8, Ф.О. Раупов9, Г.А. Ибадова10, Ф.С. Шамсиев10, Ш.И. Наврузова11, Ш.А. Хусинова12, Р.А. Нурмухамедова13, С.Т. Абдрахманова6
1 ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, г. Москва, Россия
2 Азербайджанский государственный институт усовершенствования врачей им. Азиза Алиева, г. Баку, Азербайджан
3 Ереванский государственный медицинский университет им. Мхитара Гераци, г. Ереван, Армения
4 Казахский медицинский университет непрерывного образования, г. Алматы, Казахстан
5 Казахский государственный медицинский университет им. С.Д. Асфендиярова, г. Алматы, Казахстан
6 Медицинский университет Астана, г. Астана, Казахстан
7 Кыргызско-российский славянский университет им. Б.Н. Ельцина, г. Бишкек, Кыргызстан
8 Национальный центр охраны материнства и детства, г. Бишкек, Кыргызстан
9 Республиканский учебно-клинический центр семейной медицины, г. Душанбе, Таджикистан
10 Ташкентский институт усовершенствования врачей, г. Ташкент, Узбекистан
11 Бухарский государственный медицинский институт, г. Бухара, Узбекистан
12 Самаркандский государственный медицинский институт, г. Самарканд, Узбекистан
13 Ташкентский институт усовершенствования врачей, г. Ташкент, Узбекистан
Острые респираторные вирусные инфекции (ОРВИ), включая грипп, относятся к наиболее распространенным заболеваниям в детской и взрослой популяциях. Несмотря на широкий выбор средств, для лечения данной патологии актуальным остается поиск препаратов, сочетающих в себе универсальную противовирусную активность, доказанные эффективность и безопасность, а именно возможность применения у пациентов из групп риска, в том числе при аллергических заболеваниях. Целью исследования являлось изучение практики применения препарата на основе антител в релиз-активной форме к интерферону-γ, CD4+ рецептору и гистамину (Эргоферон) в амбулаторных условиях, в том числе при позднем начале лечения, а также у пациентов с отягощенным аллергологическим анамнезом. В исследование включались данные детей и взрослых пациентов, наблюдавшихся амбулаторно с диагнозом грипп/ОРВИ, для лечения которых применялся Эргоферон. Продолжительность и схема терапии определялись непосредственно врачом, результаты оценивались ретроспективно. Исследование проводилось с участием врачей общей практики из Азербайджана, Армении, Грузии, Казахстана, Киргизии, Монголии, Таджикистана и Узбекистана; период проведения – эпидемиологический сезон 2016-2017 гг. Были обработаны данные 8411 человек, в том числе 6005 детей и 2069 взрослых, 337 – без уточнения возраста. У 706 пациентов отмечались проявления аллергии в виде аллергического ринита/риносинусита, атопического дерматита/экземы, бронхиальной астмы. Длительность заболевания до разрешения всех симптомов заболевания составила в среднем 4,84±1,53 дня; у пациентов, начавших лечение в первый день заболевания – 4,79±1,44 дня (FNOVA, фактор «день начала терапии» χ²=31,15, df=3, p<0,001). Несмотря на значимость раннего начала лечения, разница длительности всех симптомов заболевания у пациентов, начавших лечение в 1-е и 4-е сутки, составила всего 0,39 сут (9,4 ч). Сделан вывод, что терапевтическая эффективность Эргоферона, обладающего комбинированным противовирусным, противовоспалительным и антигистаминным действием, проявляется в быстром купировании симптомов ОРВИ и гриппа при любых сроках начала терапии независимо от возраста пациентов, в том числе у лиц с сопутствующими аллергическими заболеваниями.
Ключевые слова: ОРВИ, грипп, сопутствующие аллергические заболевания, бронхиальная астма, Эргоферон.
Для цитирования: Геппе Н.А., Валиева С.Т., Фараджева Н.А., Оганян М.Р., Мырзабекова Г.Т., Жанузаков М.А., Катарбаев А.К., Скучалина Л.Н., Айткулуев Н.С., Кабаева Д.Д., Раупов Ф.О., Ибадова Г.А., Шамсиев Ф.С., Наврузова Ш.И., Хусинова Ш.А., Нурмухамедова Р.А., Абдрахманова С.Т. Лечение ОРВИ и гриппа в амбулаторно-поликлинической практике: результаты международной наблюдательной неинтервенционной программы «Эрмитаж». Терапия. 2017;8(18):63-78
Treatment of ARVI and grippe in ambulatory-plyclinical practice: Results of international observing noninterventional programme «Ermitage»
N.A. Geppe1, S.T. Vаliyeva2, N.А. Farajova2, M.R. Ohanyan3, G.T. Myrzabekova4, M.A. Zhanuzakov4, A.K. Katarbayev5, L.N. Skuchalina6, N.S. Aitkuluyev7, D.D. Kabaeva8, F.О. Raupov9, G.A. Ibadova10, F.S. Shamsiev10, Sh.I. Navruzova11, Sh.A. Khusinova12, R.A. Nurmukhamedova13, S.T. Abdrakhmanova6
1 I.M. Sechenov first Moscow state medical university of the Ministry of Health of Russia, Moscow, Russia
2 Azerbaijan state advanced training institute for doctors named after A. Aliyev, Baku, Azerbaijan
3 Yerevan state medical university after Mkhitar Heratsi, Armenia
4 Kazakh medical university of recurrent education, Almaty, Kazakhstan
5 S.D. Asphendiyarov Kazakh state medical university, Almaty, Kazakhstan
6 Astana medical university, Astana, Kazakhstan
7 B.N. Yeltsin Kyrgyz-Russian slavic university, Bishkek, Kyrgyzstan
8 National Center Of Maternity and Childhood Protection, Bishkek, Kyrgyzstan
9 Republican Training and Clinical Family Medicine Center, Dushanbe, Tadjikistan
10 Tashkent Institute of Postgraduate Medical Education , Tashkent, Uzbekistan
11 Bukara state medical institute, Bukhara, Uzbekistan
12 Samarkand state medical institute, Samarkad, Uzbekistan
13 Tashkent medical refresher institute, Tashkent, Uzbekistan
Acute respiratory viral infections (ARVI) along with influenza are the most common diseases both in adult and pediatric practices. Nowadays there are a lot of different medications to cure this condition, but it's still urgent to find some new drugs, which have a universal antiviral activity and also have proved effectiveness and safety, especially in case of treating patients with different allergic pathologies. The aim of the study was to evaluate the practical use of the drug based on release-active antibodies to interferone-γ,CD4+receptor and histamine (Ergoferon) in ambulatory practice, including cases of late-start treatment and cases with allergic status of patients. Data of pediatric and adult patients who were ambulatory observed with influenza/ARVI diagnosis and used Ergoferon were included into the research. The physician set duration and scheme of the therapy. The received results were estimated retrospectively. The research was carried out with general practitioners from Azerbaijan, Armenia, Georgia, Kazakhstan, Kyrgyzstan, Mongolia, Tajikistan and Uzbekistan; period of observation – epidemiological season 2016-2017. 8411 patients (6005 infants, 2069 adults, 337 without specifications of the age) took part in the research. 706 patients had such allergy manifestations as allergic rhinitis/sinusitis, atopic dermatitis/eczema, bronchial asthma. The duration of the disease before the resolution of all the symptoms was on average 4.84±1.53 days; patients who started treatment from the first day of disease the duration was 4.79±1.44 days (ANOVA, factor «the day of the start of therapy» χ²=31.15, df=3, p <0.001). Although the early-start treatment is important, the difference between the duration of all symptoms of the disease in both groups was only 0.39 day (9.4 hours). Therefore the conclusion has been made that Ergoferon has combined antiviral, anti-inflammatory and antihistamine effect only in case of prompt relief of ARVI and influenza symptoms in different terms of the beginning of the therapy independently of the age of patients, and including patients with an allergic status.
Key words: ARVI, influenza, accompanying allergic diseases, bronchial asthma, Ergoferon.
For citation: Geppe N.A., Vаliyeva S.T., Farajova N.A., Ohanyan M.R., Myrzabekova G.T., Zhanuzakov M.A., Katarbayev A.K., Skuchalina L.N., Aitkuluyev N.S., Kabaeva D.D., Raupov F.O., Ibadova G.A., Shamsiev F.S., Navruzova Sh.I., Khusinova Sh.A., Nurmukhamedova R.A., Abdrakhmanova S.T. Treatment of ARVI and grippe in ambulatory-polyclinical practice: results of international observing non-interventional programme "Ermitage". Therapy. 2017;8(18):63-78
Актуальность
Острые респираторные вирусные инфекции (ОРВИ), включая грипп, относятся к наиболее распространенным заболеваниям в детской и взрослой популяциях. В среднем за год ребенок болеет ОРВИ от 4 до 10 раз, взрослый – от 2 до 4 раз. Пик заболеваемости приходится на ранний детский возраст. Несмотря на то что возбудителями респираторных инфекций являются различные вирусы (более 200 видов), лекарственные средства с прямым противовирусным действием разработаны только для вируса гриппа, на долю которого приходится в эпидемический сезон не более 30% случаев в структуре ОРВИ [1, 2].
Вместе с тем в настоящее время отмечается рост числа штаммов вируса гриппа, резистентных к этиотропной терапии, а также снижение эффективности ингибиторов нейраминидазы (в частности, при вирусе гриппа H7N9), в том числе при использовании в высоких дозах [3, 4]. В условиях реальной амбулаторно-поликлинической практики определение типа возбудителя и его чувствительности к терапии нередко затруднительно, что обусловливает использование препаратов с универсальной противовирусной активностью. Другими важными критериями выбора лекарственного средства является его безопасность и возможность применения у детей, пациентов с сопутствующими заболеваниями, из групп риска, в том числе при аллергических заболеваниях, для которых характерны затяжное течение ОРВИ, замедленный ответ на терапию и частое развитие осложнений [5].
Этим требованиям отвечает препарат Эргоферон, созданный на основе релиз-активных антител (Р-А АТ) к интерферону γ (ИФН-γ), CD4 рецептору и гистамину. Противовирусное действие Эргоферона реализуется за счет влияния на систему ИФН в сочетании с активацией процессов распознавания вирусов системой CD4 [6]. Совместное применение Р-А АТ к ИФН-γ и Р-А АТ к CD4 активирует универсальные механизмы противовирусной защиты, играющие ключевую роль в развитии иммунного ответа независимо от типа вируса, обеспечивая усиленное противовирусное действие. Р-А АТ к гистамину модифицируют гистамин-зависимую активацию периферических и центральных Н1-рецепторов, приводя к уменьшению сосудистой проницаемости, сокращению длительности и выраженности катаральных симптомов и аллергических реакций [7].
Клинические исследования продемонстрировали эффективность и безопасность Эргоферона в лечении ОРВИ и гриппа, его хорошую переносимость и высокую приверженность терапии этим препаратом как взрослых пациентов, так и детей. Широкое применение Эргоферона связано с возможностью лечения ОРВИ и гриппа, в том числе у детей раннего возраста, независимо от этиологии, у больных из групп риска (с аллергическими заболеваниями, соматической патологией, хроническими бронхолегочными заболеваниями) [8-13]. Тем не менее масштабных исследований по изучению эффективности и безопасности препарата Эргоферон в условиях амбулаторной практики у пациентов данных категорий не было, что послужило основанием для проведения международной наблюдательной программы «ЭРМИТАЖ».
Цель исследования состояла в изучении практики применения препарата Эргоферон в условиях амбулаторной практики и получении дополнительных данных по эффективности и безопасности препарата Эргоферон в лечении гриппа/ ОРВИ у взрослых и детей в амбулаторных условиях, в том числе при позднем начале терапии (через 48 и 72 ч от начала заболевания), а также у пациентов с отягощенным аллергологическим анамнезом.
Материал и методы
Дизайн исследования
Неинтервенционная ретроспективная наблюдательная программа.
Критерии соответствия
В исследование включались данные детей от 6 мес до 18 лет и взрослых пациентов старше 18 лет с диагнозом грипп/ОРВИ, аксиллярной температурой выше 37,4 °С, наличием как минимум одного симптома интоксикации и/или катарального симптома длительностью от 12 ч до 3 сут к моменту обращения к врачу, для лечения которых был назначен препарат Эргоферон. Продолжительность терапии препаратом Эргоферон определялась непосредственно врачом на основании опыта применения препарата, общего клинического впечатления и переносимости лечения в соответствии с зарегистрированными показаниями, в терапевтической дозировке, указанной в инструкции по медицинскому применению.
Условиями программы не было предусмотрено обязательного инструментального или лабораторного обследования пациента для включения его данных в анализируемую выборку.
Условия проведения исследования
Обработаны данные 8411 человек, наблюдавшихся амбулаторно на протяжении эпидемиологического сезона 2016-2017 гг.; врач – участник программы – переносил данные пациентов в индивидуальную регистрационную карту (ИРК). В наблюдательной программе приняли участие 519 врачей общей практики (педиатры, терапевты и семейные врачи) из 8 стран: Азербайджана, Армении, Грузии, Казахстана, Киргизии, Монголии, Таджикистана и Узбекистана. Набор пациентов производился в произвольной демографической и национальной пропорции.
Отступления от дизайна
Несмотря на то что критериями включения были регламентированы рамки продолжительности заболевания не более трех суток до момента обращения к врачу, в процессе обработки результатов выяснилось, что часть пациентов обращалась за помощью на 4-е сутки заболевания и позже. Акцентируя важность получения информации о результатах терапии ОРВИ/гриппа в условиях реальной врачебной практики, данные этих пациентов также были включены в общий анализ и рассчитывались отдельно.
Описание медицинского вмешательства
Неинтервенционный характер данной наблюдательной программы не подразумевал какого-либо вмешательства в назначаемую врачом терапию. Исследуемый препарат Эргоферон (таблетки для рассасывания) назначался по схеме, описанной в инструкции: 8 табл. в 1-й день лечения (в первые 2 ч по 1 табл. каждые 30 мин, потом еще 3 приема через равные промежутки времени); со вторых суток и далее по 1 табл. 3 раза в день до полного выздоровления.
Первичный критерий эффективности – длительность симптомов ОРВИ/гриппа от начала лечения Эргофероном до их разрешения: температура ≤37 °С в течение 24 ч (без последующего повышения в течение периода наблюдения), отсутствие катаральных проявлений и симптомов интоксикации.
Вторичные критерии эффективности включали оценку длительности повышенной температуры тела (>37 °С), симптомов интоксикации, симптомов со стороны носа и горла (заложенность/ выделения из носа боль в горле и др.), а также определение доли пациентов, у которых отмечено ухудшение течения заболевания (развитие осложнений ОРВИ, в том числе требующих назначения антибиотиков и/или госпитализации) за период наблюдения.
Анализ в группах
Пациенты распределялись в 2 группы: дети от 6 мес до 18 лет и взрослые ≥18 лет. Для получения дополнительных данных по эффективности и безопасности применения Эргоферона при лечении гриппа/ОРВИ у пациентов с отягощенным аллергологическим анамнезом были выделены 2 подгруппы пациентов (взрослых и детей) с аллергией.
Этическая экспертиза
Международная наблюдательная программа «ЭРМИТАЖ» получила одобрение Независимого междисциплинарного Комитета по этической экспертизе клинических исследований.
Статистический анализ
Для анализа данных использовался следующий набор методов и подходов. Анализ времени до наступления события: по методу Каплана-Майера для оценки функции рисков и средних времен (survival analysis). Для анализа влияния выделенных факторов, а также значимости ковариат использовался дисперсионный анализ ANOVA/ANCOVA в рамках метода Кокса (Cox proportional hazards model). Категориальные переменные, не подразумевающие порядка, описывались с помощью частотных таблиц. Анализ проводился с помощью ANOVA/ANCOVA для мультиномиальной регрессии. Категориальные переменные, подразумевающие порядок, описывались как с помощью частотных таблиц, так и с помощью мер центральной тенденции (среднее) и масштаба (стандартное отклонение). Анализ проводился в рамках ANOVA/ ANCOVA для ординальной регрессии в смысле среднего значения величины. Для биномиальных величин использовалась логистическая модель, анализ проводился для вероятностей наступления заданного события. Общий уровень ошибки контролировался в рамках коррекции по методу Бенджамини-Хохберга (Hochberg procedure). Статистический анализ проводился только для полных случаев ввиду типа исследования (неполные/отсутствующие данные игнорировались в тех методах, в которых они не являются легальным значением переменной). Преобразование и статистическая обработка данных производились в программных средах R 3.3.2 и SAS 9.4.
Результаты исследования
Характеристика групп
Из 8411 пациентов участников данной программы 71,4% составили дети (n=6005; 49,2% – мальчики, 48,1% – девочки, 1,5% – без уточнения пола по данным ИРК) и 24,6% (n=2069) – взрослые (42,8% – мужчины, 55,5% – женщины, 1,8% – без уточнения пола по данным ИРК). В 337 ИРК (4,0%) отсутствовало указание возраста пациента. Средний возраст детей составил 6,8±4,6 года (от 6 мес до 18 лет), взрослых – 36,8±14,1 года (от 18 до 90 лет).
У большинства пациентов (91,7%, n=7716) диагностировалось ОРВИ, в 7,0% (n=595) – грипп, чаще у взрослых, чем у детей: 8,5 против 5,9%; в 1,3% ИРК диагноз отмечен не был. Единичные случаи заболеваний были обусловлены другими вирусными инфекциями: ветряная оспа – 0,1%, краснуха – 0,1%.
Распределение пациентов в группах, в зависимости от тяжести заболевания, было неоднородным (ANOVA, фактор «возраст» p <0,0001). Доля пациентов с ОРВИ легкой степени тяжести составила 27,7% среди детей и 23,5% среди взрослых, доля пациентов с ОРВИ средней степени тяжести в обеих группах была одинаковая – 64,5%; тяжелое течение заболевания встречалось у 3,2% взрослых против 1,4% детей (ANOVA, фактор «возраст» χ²=24,15, df=1,p <0,0001).
Количество пациентов с аллергией составило 8,4% (n=706), среди них 68,1% (n=481) детей и 26,2% (n=185) взрослых. У 5,5% пациентов (n=40) с аллергией отсутствовало уточнение возраста. Чаще всего под аллергией подразумевался аллергический ринит/риносинусит – 78,8% (n=379) у детей и 80,5% (n=149) у взрослых, атопический дерматит/экзема – 10,6% (n=51) и 9,2% (n=17), бронхиальная астма (БА) – 7,8% (n=37) и 8,6% (n=16), а также их сочетание – 2,9% (n=14) и 1,6% (n=3) соответственно.
Подавляющее большинство пациентов (95,0% детей и 92,8% взрослых) обратились за медицинской помощью и начали лечение в первые 3 дня заболевания. Чаще всего обращались за помощью на второй день заболевания: 52,9% детей и 47,4% взрослых; реже в первый день (23,3 и 24,3%) и на третий день (18,9 и 21,2% соответственно). Начало лечения в более поздние сроки (4-й день и позже) отмечено у 3,6% детей и у 5,6% взрослых. У 2,6% пациентов сроки начала лечения не установлены. Согласно проведенному статистическому анализу, взрослые обращались за медицинской помощью и начинали лечение в более поздние сроки (ANOVA, фактор «возраст» χ²=25,8; df=4;p <0,001), а пациенты с аллергией, напротив, обращались к врачу несколько раньше (ANOVA, фактор «аллергия» χ²=12,265; df=4; p=0,0154 [после коррекции по методу Бенджамини-Хохберга р=0,0251]).
Все пациенты, участвовавшие в программе, получали Эргоферон. Средняя длительность приема Эргоферона составила 5,48±1,32 дня и значимо не различалась у детей и взрослых. У 49,1% больных ОРВИ (n=4129) препарат назначался в виде монотерапии, у 50,9% (n=4282) – совместно с другими средствами. Монотерапия Эргофероном чаще назначалась пациентам без аллергии (точный тест Фишера, p <0,0001), а также с легкой и средней тяжестью заболевания (multinomial ANOVA, χ²=260,13; df=2; p <0,0001).
Среди пациентов, которые получали лечение Эргофероном в комбинации с другими лекарственными средствами, 36,1% (n=1547) получали 1 дополнительный препарат, 32,0% (n=1369) – 2, 21,0% (n=899) – 3, а 10,9% – 4 и более. Количество дополнительно назначаемых препаратов повышалось по мере увеличения возраста (ANOVA, фактор «возраст», p <0,00001). Наиболее часто назначали лекарственные средства для лечения патологии органов дыхания (АТХ группа R) – 53,0%, противомикробные средства для системного использования (АТХ группа J) – 17,0%, а также анальгетики и антипиретики (АТХ группа N) – 14,0%. Реже применялись средства для коррекции расстройств костно-мышечной системы (АТХ группа М) – 9,7%, средства для восстановления микрофлоры кишечника, обмена веществ, а также пищеварительные ферменты (АТХ группа А) – 6,2%. Среди препаратов группы R деконгестанты и назальные препараты для местного применения (R01) назначались в 33,9% случаев, отхаркивающие и противокашлевые препараты (R05) – в 24,8%, препараты для лечения заболеваний горла (R02) – в 22,6%, антигистаминные средства (R06) – в 12,0%, препараты для лечения обструктивных заболеваний дыхательных путей (R03) – в 4,4%, другие препараты для лечения заболеваний дыхательной системы (R07) – в 2,3%. Пациенты с тяжелым течением заболевания получали антибактериальную терапию чаще других больных (40,3% детей и 42,7% взрослых), со средней тяжестью несколько реже (18,0% детей и 17,5% взрослых), а с легкой степенью тяжести еще реже (5,2% детей и 3,2% взрослых; ANOVA фактор «тяжесть заболевания» χ²=567, df=2,р <0,001). Среди всех пациентов, получавших антибактериальную терапию, дети и взрослые с аллергией составили 10,6 и 11,5% соответственно.
Пациенты с аллергией получали меньшее количество препаратов сопутствующей терапии, большая часть которых была представлена антигистаминными средствами и препаратами для лечения обструктивных заболеваний дыхательных путей (ANOVA, фактор «аллергия» χ²=167,7, df=4, p <0,00001). В среднем дети с аллергией получали не более двух дополнительных препаратов, а взрослые с аллергией – не более трех (ANOVA, фактор «возраст-аллергия», p=0,0003).
Оценка первичного критерия эффективности
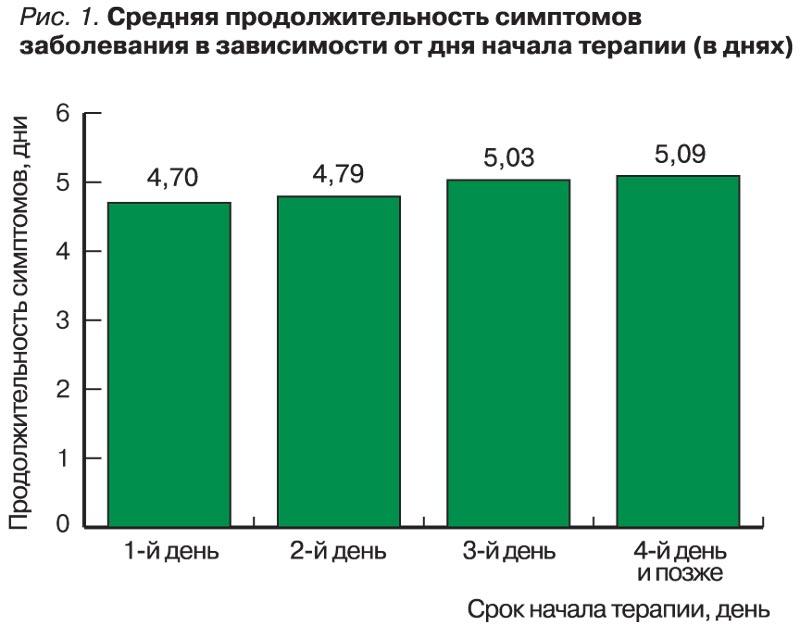
Длительность заболевания от начала лечения Эргофероном до разрешения всех симптомов заболевания (нормализация температуры ≤37 °С в течение 24 ч без последующего повышения в течение периода наблюдения, отсутствие интоксикационного и катарального синдромов) в среднем составила 4,84±1,53 дня. У пациентов, начавших лечение в первый день заболевания, продолжительность всех симптомов заболевания составила 4,70±1,58 дня, а на 2-й, 3-й, 4-й день и позже – 4,79±1,44, 5,03±1,58 и 5,09±1,74 дня соответственно (ANOVA, фактор «день начала терапии» χ²=31,15, df=3, p <0,001; рис. 1). Несмотря на значимость раннего начала лечения, разница в длительности всех симптомов заболевания у пациентов, начавших лечение в 1-е и 4-е сутки, составила всего 0,39 сут (9,4 ч).
У пациентов с аллергией сроки до разрешения симптомов удлинялись (ANOVA, фактор «аллергия» χ²=6,35, df=1, p=0,01; фактор «день начала терапии» χ²=62,059, df=4, p=0,0001 [после коррекции по методу Бенджамини-Хохберга р=0,0251]; табл. 1).
Таблица 1. Значения зависимой переменной (время до разрешения всех симптомов заболевания) от различных факторов в соответствии с подходом Least Squares Means у пациентов с аллергией
| Фактор | χ² | df | p-value |
| Возраст | 2,55 | 1 | 0,11 |
| Аллергия | 6,35 | 1 | 0,01 |
| День начала терапии | 62,059 | 4 | <0.0001 |
| Возраст – аллергия | 3,4 | 1 | 0,06 |
| Возраст – день начала терапии | 8,065 | 4 | 0,09 |
| Аллергия – день начала терапии | 3,649 | 4 | 0,455 |
| Возраст – аллергия – день начала терапии | 6,93 | 4 | 0,13 |
Продолжительность симптомов интоксикации в среднем составила 2,33±1,0 дня. Через 1 день от начала лечения Эргофероном симптомы интоксикации купировались у 16,6% пациентов, через 2 дня – у 65,7%, через 3 дня – у 90,1% и через 4 дня – у 97,1%.
Продолжительность симптомов со стороны носа и горла была в среднем 2,9±1,23 дня. Количество пациентов с купированием симптомов со стороны носа (заложенность/выделения из носа) через 1 день терапии составило 8,8%, а горла (боли/першение в горле) – 12,2%; через 2 дня – 41,0 и 42,3%; через 3 дня – 74,8 и "70,4%; через 4 дня – 89,8 и 89,2%; через 5 дней – 97,6 и 96,9% соответственно.
Средняя продолжительность симптомов заболевания у пациентов разных возрастных групп и в зависимости от наличия/отсутствия аллергии представлена в табл. 2.
Таблица 2. Средняя продолжительность симптомов заболевания в подгруппах
| Симптомы | Аллергия | Нет аллергии | Статистика | ||||
| Дети | Взрослые | Дети | Взрослые | Фактор «возраст» | Фактор «аллергия» | Фактор «возраст-аллергия» | |
| Лихорадка | 2,11±0,43 | 2,3±0,07 | 1,99±0,01 | 1,95±0,02 | χ²=0,62, df=1, р=0,43 | χ²=19,5, df=1, р<0,0001 | χ²=5,02, df=1, р=0,0251 |
| Интоксикация | 2,4±0,05 | 2,6±0,11 | 2,31±0,01 | 2,35±0,02 | χ²=2,91, df=1, р=0,087 | χ²=11,99, df=1, р<0,0001 | χ²=1,84, df=1, р=0,17 |
| Заложенность/ выделяемое из носа | 3,04±0,07 | 3,05±0,12 | 2,91±0,02 | 2,82±0,03 | χ²=2,01, df=1, р=0,155 | χ²=12,54, df=1, р=0,0004 | χ²=1, df=1, р=0,31 |
| Боли/першение в горле | 3,09±0,07 | 3,23±0,13 | 2,93±0,02 | 2,75±0,03 | χ²=13,5, df=1, р<0,0001 | χ²=22,05, df=1, р<0,0001 | χ²=7,097, df=1, р=0,007 |
Примечание. Данные представлены как M±SE (среднее арифметическое значение ± стандартизированная ошибка среднего).
Наименьшая продолжительность лихорадки отмечалась у пациентов без аллергии, не зависела от возраста и составила 1,95±0,02 дня у детей и 1,99±0,01 дня у взрослых (ANOVA, фактор «возраст» χ²=0,62, df=1, р=0,43). У пациентов с аллергией продолжительность лихорадки была значимо больше: 2,11±0,43 дня у детей и 2,3±0,07 дня у взрослых (ANOVA, фактор «аллергия» χ²=19,5, df=1, р <0,0001; фактор «возраст-аллергия» χ²=5,02, df=1, р=0,0251). Наименьшая продолжительность интоксикации (2,31±0,01 и 2,35±0,02 дня) отмечалась у детей и взрослых без аллергии; у детей и взрослых с аллергией симптомы интоксикации сохранялись несколько дольше, составив 2,4±0,05 и 2,6±0,11 дня (ANOVA, фактор «аллергия», χ²=11,99, df=1, р <0,0001; фактор «возраст» χ²=2,91, df=1, р=0,087; фактор «возраст-аллергия» χ²=1,84, df=1, р=0,17).
У пациентов без аллергии быстрее купировались проявления со стороны носа, средняя продолжительность данного симптома составила 2,91±0,02 и 2,82±0,03 дня у детей и взрослых без аллергии (ANOVA, фактор «возраст», χ²=2,01, df=1, р=0,155), а для пациентов с аллергией – 3,04±0,07 и 3,05±0,12 дня соответственно (ANOVA, фактор «аллергия» χ²=12,54, df=1, р=0,0004; рис. 3, 4).
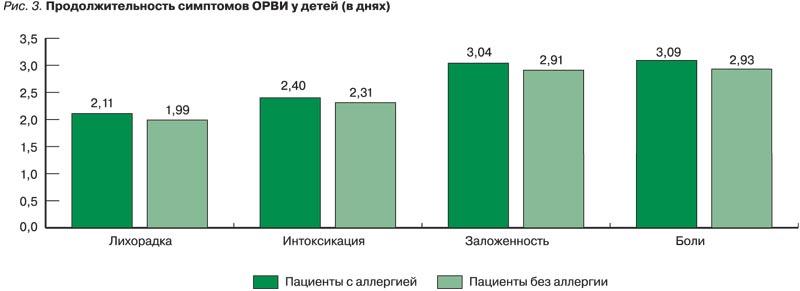
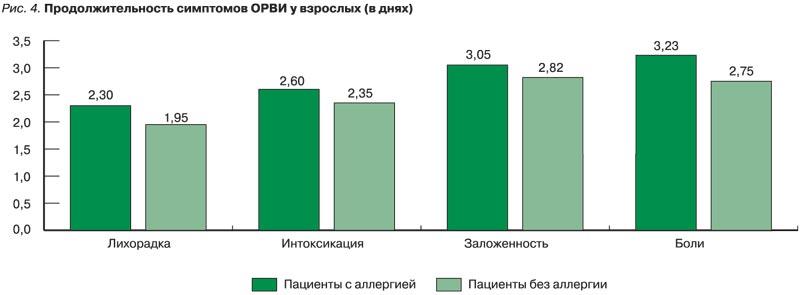
Время купирования симптомов со стороны горла у пациентов с аллергией было более продолжительным и составило 3,09±0,07 дня для детей и 3,23±0,13 дня для взрослых. У пациентов без аллергии данные показатели составляли 2,93±0,02 и 2,75±0,03 дня для детей и взрослых соответственно (ANOVA, «фактор аллергия» χ²=22,05, df=1, р <0,0001; «фактор возраст» χ²= 13,5, df=1, р <0,0001; фактор «возраст-аллергия» χ²=7,097, df=1, р=0,007). Среди взрослых с БА (n=16) обострение, возникшее на фоне ОРВИ, было зарегистрировано у 1 пациента. Среди детей с БА (n=37), принимающих Эргоферон, обострений БА на фоне ОРВИ отмечено не было (рис. 3, 4).
У пациентов с тяжелым течением заболевания (84 детей и 67 взрослых) время до разрешения всех симптомов заболевания составило 5,88±0,22 дня у детей и 6,15±0,25 дня у взрослых (ANOVA, фактор «возраст» χ²=0,213, df=1, р=0,643). Среднее время купирования лихорадки составило 3,56±0,26 и 2,46±0,17 дня (ANOVA, фактор «возраст» χ²=12,135, df=1, р=0,0005), интоксикации – 3,52±0,27 и 2,91±0,185 дня (ANOVA, фактор «возраст» χ²=3,46, df=1, р=0,063), симптомов со стороны носа – 4,73±0,65 и 3,79±0,31 дня (ANOVA, фактор «возраст» χ²=5,176, df=1, p=0,023); симптомов со стороны горла – 5,41±0,4 и 4,37±0,41 дня (ANOVA, фактор «возраст» χ²=4,42, df=1, р=0,0355) для детей и взрослых соответственно.
Антибактериальная терапия
Общее количество пациентов, получавших антибактериальную терапию, составило 1241 (14,8%) человек, при этом 71,0% из них (n=881) получили антибактериальные препараты (АБП) уже в первый день лечения (до начала приема Эргоферона либо совместно с ним). Системные АБП на второй и последующий дни лечения Эргофероном были назначены 279 (3,3%) пациентам. Число больных, которым потребовалась госпитализация на фоне проводимой терапии, составило 36 человек (0,4%). Показания для госпитализации служили бронхит (3 детей), пневмония (7 детей и 1 взрослый), острый ларинготрахеит (1 ребенок и 3 взрослых), а также обострение БА (1 взрослый) и хронической обструктивной болезни легких (ХОБЛ; 1 взрослый); в 20 случаях показания к госпитализации уточнены не были.
Врачами АБП назначались по поводу острого бронхита (5,1%), тонзиллита – (4,3%,) ларингита/ ларинготрахеита – 2,3%, ОРВИ – 1,8%, пневмонии – 0,5%, отита – 0,2%, ринита/синусита – 0,2%, обострения ХОБЛ – 0,2%, лимфаденита – 0,1%. Редко встречалось назначение АБП у пациентов с БА – 0,1%, ветряной оспой – 0,1%, краснухой – 0,1%, обострением пиелонефрита – 0,04%, энтеритом – 0,04% и эндометритом – 0,04%.
Эффективность терапии
В большинстве случаев (68,1%) эффективность терапии Эргофероном оценивалась врачами как высокая, в 30,8% – как удовлетворительная, и только 0,7% врачей отметили недостаточную эффективность лечения или отсутствие эффекта. В общей сложности 98,9% врачей признали терапию Эргофероном эффективной. В 0,4% случаев оценить эффект терапии не представлялось возможным ввиду отсутствия данных. Статистический анализ показал отсутствие различий эффективности терапии в разных возрастных группах пациентов (ANOVA, фактор «возраст» χ²=1,43, df=1, р=0,23).
Безопасность терапии
Нежелательные явления (НЯ) были отмечены у 7 пациентов (0,1%), в одном случае в виде лекарственной крапивницы, в 6 других случаях их описание отсутствовало. У 2 пациентов НЯ отмечены как несвязанные с приемом Эргоферона, в 5 остальных случаях – без уточнения причинно-следственной связи. К НЯ не относили бактериальные осложнения, потребовавшие назначения АБП, так как эти данные учитывались при анализе критериев эффективности. У 451 пациента отсутствовали данные по нежелательным явлениям.
Обсуждение
Согласно литературным данным, сроки выздоровления пациентов при ОРВИ и гриппе в популяции в среднем не превышают 7 дней и значительно сокращаются на фоне применения противовирусной терапии. По данным Кохрейновского обзора Jefferson T. (2014) с использованием 20 рандомизированных клинических исследований (РКИ) осельтамивира (с участием 9623 пациентов) и 26 РКИ занамивира (14 628 пациентов), влияние ингибиторов нейраминидазы на течение гриппа проявлялось в сокращении сроков лечения с 7 до 6,3 дня (16,8 ч) для осельтамивира и с 6,6 до 6,0 дней для занамивира у взрослых пациентов. У детей с гриппом применение занамивира не приводило к значимому сокращению сроков лечения [14]. В.Х. Фазылов (2016), представляя результаты многоцентрового международного наблюдательного исследования FLU-EE с участием более 18 тыс. взрослых пациентов с ОРВИ и гриппом, приводит данные, что 77,2% больных выздоравливают через 6 сут терапии, а у пациентов с тяжелым течением гриппа и ОРВИ сроки лечения составляют 7-8 дней [15]. По данным двойного слепого плацебо-контролируемого РКИ (Шульдяков А.А., 2015), сроки выздоровления при лечении ОРВИ и гриппа у детей в возрасте 13-17 лет на фоне приема имидазолилэтана-мида пентандиовой кислоты (ИЭПК) составили 5,21±1,84 сут, а на фоне плацебо – 6,25±1,43 сут [16].
Результаты, полученные в наблюдательной программе «ЭРМИТАЖ», показали, что препарат Эргоферон оказывает существенное влияние на течение ОРВИ и гриппа, не уступая другим противовирусным средствам, но в отличие от них эффективность терапии Эргофероном не зависит от этиологии ОРВИ.
Средняя продолжительность разрешения всех симптомов заболевания от начала лечения Эргофероном составила в среднем 4,84±1,53 дня, у пациентов с гриппом – 4,73±0,06 дня. Сроки исчезновения симптомов гриппа при терапии Эргофероном сопоставимы с результатами лечения осельтамивиром, что ранее также было показано в сравнительном РКИ [12]. Несущественная разница в продолжительности лечения ОРВИ и гриппа в данном случае может быть обусловлена отсутствием обязательной диагностики возбудителя по условиям программы и постановкой этиологического диагноза на основании клинической картины заболевания, как это часто бывает в условиях реальной амбулаторно-поликлинической практики.
Сроки начала лечения оказывали влияние на продолжительность терапии. Так, у пациентов, начавших лечение на 1-й день заболевания, продолжительность лечения Эргофероном составила 4,70±1,58 дня, тогда как у начавших лечение на 4-й день заболевания и позже она составляла 5,09±1,74 дня. Несмотря на значимость раннего начала лечения (ANOVA, фактор «день начала терапии» χ²=62,059, df=4, p <0,0001), максимальная разница продолжительности терапии у пациентов, начавших лечение в разные сроки, составила всего 0,39 сут (9,36 ч). Таким образом, противовирусное действие препарата Эргоферон, усиленное за счет одновременного воздействия на систему ИФН и CD4+ рецепторы, обеспечивает выраженный клинический эффект даже при позднем начале терапии.
Сроки купирования симптомов ОРВИ, согласно различным литературным источникам, могут колебаться в широких пределах. По данным L. Deckx (2016), продолжительность отдельных симптомов ОРВИ может составлять менее 3 дней [17], а по данным М. Thompson (2013), они могут сохраняться значительно дольше, до 2 нед и более (в частности, признаки бронхиолита и кашель у детей отмечаются до 20-25 дней) [18].
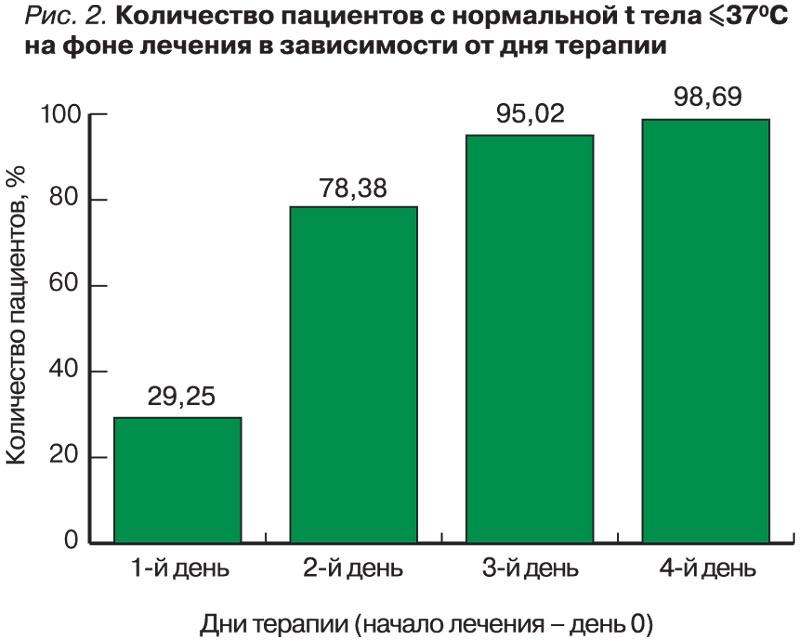
Результаты наблюдательной программы показали, что продолжительность лихорадки на фоне терапии препаратом Эргоферон составила в среднем 1,99±0,87 дня, при этом у трети пациентов (29,3%) лихорадка отсутствовала уже по окончании первого дня терапии. Доля больных с нормальной температурой тела через 2 дня лечения составила 78,4%, через 3 и 4 дня – 95,0 и 98,7% соответственно. Сопоставимые сроки купирования лихорадки при ОРВИ и гриппе у детей 7-12 лет отмечались на фоне применения ИЭПК: 42 ч, или 1,75 сут на фоне лечения по сравнению с 54,48 ч, или 2,27 суток на фоне плацебо. Доли пациентов с нормализацией температуры тела составили на 1-е сутки 15,5% при приеме ИЭПК и 9% при приеме плацебо, на 2-е сутки 49,0 и 33,5%, на 3-е сутки 82,6 и 62,6%, на 4-е сутки 92,3 и 84,5%, на 5-е сутки 97,4 и 91,6% соответственно [19]. Более длительные сроки разрешения лихорадки были продемонстрированы для других препаратов, применяемых для лечения ОРВИ. О.В. Кладова (2012) приводит данные о средней продолжительности лихорадки у детей с ОРВИ, принимавших умифеновир в течение 2,8 дня [20]. По данным В.Х. Фазылова, купирование лихорадки при ОРВИ у взрослых на фоне приема сополимера натрийкарбоксиметилцеллюлозы и госсипола [21] было отмечено на 3-й день терапии у 51,3% пациентов, к 6-му дню – у 98,8% [15].
Продолжительность симптомов интоксикации при лечении Эргофероном в среднем составила 2,33±1,0 дня. Купирование симптомов интоксикации после 1-го дня лечения отмечалось у 16,6% пациентов, через 2 дня – у 65,7% и у 90,1% – через 3 дня лечения. По данным литературы, средние сроки исчезновения интоксикационного синдрома на фоне приема ИЭПК были несколько продолжительнее – 3,21 сут, а доли пациентов с купированием данного синдрома после первых дней лечения – меньше, составив 3,9, 36,1 и 58,7% пациентов к окончанию 1, 2 и 3-го дней соответственно [19].
Комбинированный состав препарата Эргоферон, позволяющий воздействовать в том числе на патогенетический механизм развития заболевания за счет уменьшения проявлений воспаления и гистамин-зависимых реакций, способствовал быстрому купированию катаральных проявлений, средняя продолжительность которых составила 2,9±1,23 дня. Количество пациентов с жалобами на выделения из носа, боли и першение в горле уменьшалось, начиная с 1-го дня терапии. К началу 2-го дня терапии катаральные проявления со стороны носа и горла отсутствовали у 8,8 и 12,2% пациентов соответственно. На 3-й день от начала лечения их количество увеличилось в 3,5-4,5 раза, составив 41,0% с отсутствием симптомов со стороны носа и 42,3% с отсутствием симптомов со стороны горла. В последующие дни отмечалось дальнейшее нарастание положительной динамики, и через 5 дней терапии катаральные проявления со стороны носа и горла были полностью купированы у 97,6 и 96,9% пациентов соответственно.
Подобные данные отмечались в программе FLU-EE, где симптомы со стороны носа (ринит) и горла (зуд в горле, кашель) отсутствовали у 40,0 и 60,7% пациентов на 3-й день и у 95,6 и 98,7% на 6-й день терапии соответственно [15]. Более длительные сроки купирования катаральных симптомов наблюдались при применении ИЭПК у детей с ОРВИ – препарат способствовал сокращению продолжительности катаральных симптомов до 5,82±1,55 дня по сравнению с плацебо (6,48±1,24 дня) [16], а доля пациентов с отсутствием катаральных симптомов на 2-е сутки лечения составила 1,9%, на 3-и сутки – 8,4%, на 4-е – 21,3% и на 5-е – 52,9% [19].
Продолжительность клинических проявлений инфекционного заболевания обусловлена в первую очередь сроками персистирования возбудителя в организме [22]. Терапевтический эффект препарата Эргоферон, проявляющийся быстрым купированием симптомов гриппа и ОРВИ, обусловлен в том числе ускорением элиминации возбудителя, что подтверждается ранее проведенными исследованиями. Результаты экспериментальных работ показали, что Эргоферон обладает сопоставимым с осельтамивиром эффектом в отношении вируса гриппа А (H3N2); оба препарата снижали репликацию вируса в легких животных более чем в 10 раз как через 2, так и через 4 сут [23]. В двуцентровом проспективном открытом клиническом рандомизированном исследовании было показано, что лечение ОРВИ Эргофероном способствовало увеличению доли «вируснегативных» пациентов до 76% к 3 дню лечения [24].
Пациенты с БА
Известно, что у пациентов с аллергической патологией частота возникновения ОРВИ выше, а само заболевание характеризуется затяжным течением, сниженной или замедленной реакцией на существующие схемы лечения и частым развитием осложнений [5]. Имеются данные о неэффективности осельтамивира при лечении гриппа у детей с БА [14]. Применяя для лечения ОРВИ имеющиеся в распоряжении врачей на сегодняшний день препараты, следует помнить о возможности возникновения аллергических реакций у детей с БА, особенно при использовании жидких лекарственных форм (сиропов) [25].
Наличие у Эргоферона противовоспалительного и антигистаминного действия в совокупности с благоприятным профилем безопасности и возможностью сочетания с другими лекарственными средствами объясняет его выбор в качестве средства для лечения ОРВИ и гриппа у пациентов с аллергическими заболеваниями. Имеется описанный ранее опыт применения Эргоферона при лечении ОРВИ у детей с БА [8]. Клиническая эффективность лечебно-профилактической схемы приема препарата проявлялась в значимом снижении количества эпизодов ОРВИ, вирус-индуцированных обострений БА, а также тенденцией к более легкому течении ОРВИ при ее возникновении, что сочеталось с хорошей переносимостью и отсутствием аллергических реакций на препарат.
Согласно результатам, полученным в ходе наблюдательной программы «ЭРМИТАЖ», продолжительность основных симптомов заболевания у пациентов с аллергией была несколько больше, чем без аллергии (ANOVA, фактор «аллергия», p <0,0001). Быстрее всего нормализовалась температура тела (2,11 и 2,3 сут у детей и взрослых соответственно), чуть позже были купированы симптомы интоксикации (2,4 и 2,6 сут), катаральные симптомы в среднем продолжались 3 сут, лишь симптомы со стороны горла у взрослых несколько дольше – 3,23 сут (ANOVA, фактор «возраст» χ²=13,5, df=1, р <0,0001). Вместе с тем продолжительность клинических проявлений ОРВИ/гриппа у детей с аллергией превышала таковую у детей без аллергии максимум на 0,19 сут (4,6 ч), а у взрослых максимум на 0,48 сут (11,5 ч). Терапия Эргофероном сопровождалась отсутствием индуцированных ОРВИ обострений БА у детей (единичный случай обострения БА наблюдался в группе взрослых пациентов). Полученные результаты не уступают данным сравнительного проспективного исследования с применением ИЭПК в лечении пациентов с инфекционным обострением БА (Дзюблик А.Я., 2013). Терапевтическая эффективность препарата заключалась в достоверном сокращении продолжительности лихорадки, симптомов интоксикации (с 6 до 5 дней), катаральных симптомов (с 7 до 6 дней), а также частоты развития бактериальных осложнений (с 20 до 4,9%) по сравнению с группой стандартной терапии без применения противовирусных средств [26].
Осложнения
В ходе проведения данной наблюдательной программы было обнаружено, что 14,75% (n=1241) пациентов дополнительно получали антибактериальную терапию. Похожие данные были получены в программе FLU-EE, где частота назначения АБП в среднем составила 13,4%, а при позднем обращении количество их назначений возрастало более чем в 2 раза – до 31,6% [15]. Большая часть пациентов, получавших АБП (71,0%, n=881), начинали прием с 1-го дня лечения Эргофероном или раньше, что было обусловлено поздними сроками обращения, тяжелым течением заболевания, а также необоснованными назначениями АБП с профилактической целью. По данным Кохрейновского обзора (Spurling G.K., 2017), назначение АБП при ОРВИ с профилактической целью является неоправданным и не способствует уменьшению осложнений по сравнению с более поздним их назначением, кроме того, более позднее назначение позволяет сократить общее число выписанных АБП в 3 раза [27]. Согласно рекомендациям Американского колледжа врачей (The American College of Physicians – ACP) и Центров по контролю и профилактики заболеваний США (Centers for Disease Control and Prevention – CDC), показаниями для назначения АБП при ОРВИ являются сохранение симптомов ОРВИ в течение ≥10 дней; высокая температура тела (>39 °С) и гнойное отделяемого из носа либо лицевые боли, продолжающиеся как минимум 3 дня подряд; повторное ухудшение на фоне текущего ОРВИ продолжительностью 5 дней [28]. Помимо повышения риска возникновения НЯ, обусловленных действием АБП, широкое их назначение при ОРВИ способствует развитию антибиотикорезистентности микроорганизмов [27].
Наиболее высокая частота развития осложнений при ОРВИ, особенно в эпидемические периоды, описана Т.И. Гаращенко и Ф.И. Ершовым (2001), которые оценивают ее в 20-30%, подразумевая под осложнениями риниты, фарингиты, тонзиллиты, ларингиты, трахеиты, бронхиты, пневмонии (первичные вирусные и вторичные бактериальные), а также синуситы, обострения хронических заболеваний легких, сердечно-сосудистой системы, почек и мочевыводящих путей [29]. В зарубежных публикациях чаще обращается внимание на серьезные осложнения ОРВИ, такие как острый тонзиллит, мастоидит после острого среднего отита и пневмонию. Риск развития пневмонии наиболее высок среди пациентов старшего возраста (≥65 лет) и достигает 4% случаев, а у детей встречается реже, в 0,04-1,3% случаев [30]. В процессе лечения пациентов программы «ЭРМИТАЖ» пневмония была отмечена в 0,5% случаев, что можно расценивать как низкую частоту осложнений в сравнении с приведенными литературными данными. Почти 2% назначений АБП были у пациентов, у которых врачами-участниками программы назофарингит расценивался как осложнение основного заболевания без подтверждения бактериальной природы либо сопровождался диагнозом ОРВИ. В целом количество НЯ, зарегистрированных на фоне приема Эргоферона, было меньше, чем при течении ОРВИ и гриппа без применения противовирусной терапии, согласно литературным данным.
Выводы
- Препарат Эргоферон эффективен для лечения гриппа и ОРВИ любой этиологии, во всех возрастных группах, в том числе у пациентов с сопутствующими аллергическими заболеваниями.
- Сроки купирования основных синдромов гриппа и ОРВИ (лихорадочного, интоксикационного, катарального) на фоне терапии Эргофероном в среднем не превышали трех дней.
- Терапевтический эффект препарата Эргоферон развивается быстро, у 29,3% пациентов к окончанию первого дня лечения лихорадочный синдром был полностью купирован.
- Препарат Эргоферон эффективен при позднем (после 48 ч от начала заболевания) старте терапии гриппа и ОРВИ любой этиологии. В случае раннего начала терапии (в первые 24 ч заболевания) сроки лечения сокращаются максимально на 9 ч по сравнению с более поздним назначением Эргоферона.
- Применение препарата Эргоферон для лечения ОРВИ и гриппа у пациентов с сопутствующими аллергическими заболеваниями было эффективным и не приводило к увеличению лекарственной нагрузки.
- Использование Эргоферона значительно сокращает количество, а в половине случаев (49%) позволяет полностью исключить прием средств для симптоматической терапии ОРВИ и гриппа, что делает терапию более безопасной и экономически выгодной.
- Применение препарата Эргоферон сопровождалось низкой частотой развития бактериальных осложнений.
- Препарат Эргоферон безопасен и хорошо переносится пациентами. Редкие НЯ, отмеченные в процессе лечения, не имели причинно-следственной связи с приемом препарата.
- Практически все врачи (98,9%) оценили терапию препаратом Эргоферон как эффективную.
Заключение
Результаты неинтервенционной наблюдательной программы «ЭРМИТАЖ» показали, что терапевтическая эффективность Эргоферона, обладающего комбинированным противовирусным, противовоспалительным и антигистаминным действием, проявляется в быстром купировании симптомов ОРВИ и гриппа на любых сроках начала терапии у пациентов независимо от возраста, в том числе у пациентов с сопутствующими аллергическими заболеваниями. Использование препарата Эргоферон в амбулаторно-поликлинической практике позволяет эффективно и безопасно лечить грипп и ОРВИ любой этиологии, что сопровождается уменьшением частоты бактериальных осложнений, сокращает лекарственную нагрузку на пациента. Указанные результаты прослеживаются во всех странах-участниках проекта, независимо от климата и географического положения.
Источник финансирования
Данная наблюдательная программа проводилась при поддержке компании ООО «НПФ «Материа Медика Холдинг». Научными консультантами являлись МОО «Педиатрическое респираторное общество», а также национальные координаторы стран-участников программы.
Литература
- Гриневич А.И., Матяш В.И. Этиопатогенетические профилактика и лечение гриппа и ОРВИ: новые возможности. Укр. мед. часопис. 2011;22:1-7. [Grinevich A.I., Matyash V.I. Etiopathogenetic prevention and treatment of grippe and ARVI: new opportunities. Ukr. med. chasopis. 2011;22:1-7.]
- Заплатников А.Л., Кондюрина Е.Г., Елкина Т.Н., Бурцева Е.И., Грибанова О.А., Пирожкова Н.И., Мингалимова Г.А., Тюленева И.О., Трушакова С.В., Мукашева Е.А. Многоплановая оценка схем терапии острых респираторных инфекций в условиях рутинной педиатрической практики. Антибиотики и химиотерапия. 2016;61(5-6):8-20. [Zaplatnikov A.L., Kondjurina E.G., Elkina T.L., Burtzava E.I., Gribanova O.A., Pirozhkova N.I., Mingalimova G.A., Tjuleneva I.O., Trushakova S.V., Mukasheva E.A. Multipoint estimation of therapeutical schemes for acute respiratory infections in routine pediatric practice conditions. Antibiotics and chemotherapy. 2016;61(5-6):8-20.]
- Kiso M., Iwatsuki-Horimoto K., Yamayoshi S., Uraki R., Ito M., Nakajima N., Yamada S., Imai M., Kawakami E., Tomita Y., Fukuyama S., Itoh Y., Ogasawara K., Lopes T.J.S., Watanabe T., Moncla L.H., Hasegawa H., Friedrich T.C., Neumann G., Kawaoka Y. Emergence of Oseltamivir-Resistant H7N9 Influenza Viruses in Immunosuppressed Cynomolgus Macaques. J. Infect. Dis. 2017;21 6(5):582-93.
- Gubareva L.V., Sleeman K., Guo Z., Yang H., Hodges E., Davis C.T., Baranovich T., Stevens J. Drug Susceptibility Evaluation of an Influenza A(H7N9) Virus by Analyzing Recombinant Neuraminidase Proteins. J. Infect. Dis. 2017;216(4):566-74.
- Косяков С.Я. Острые респираторные инфекции в практике оториноларинголога. Медицинский совет. 2013;7:26-31. [Kosyakov S.Ya. Acute respiratory infections in otolaryngologist's practice. Cosilium medicum. 2013;7:26-31.]
- Инструкция по медицинскому применению препарата Эргоферон, 16.11.17. URL:sites.reformal.ru/grls.rosminzdrav. ru/ [Instruction for Ergoferon medical use, 16.11.17. URL:sites.reformal.ru/grls.rosminzdrav.ru/]
- Шиловский И.П. Применение комбинированных препаратов в лечении респираторных вирусных инфекций. Медицинский совет. 2016;17:50-4. [Shilovsky I.P. Use of combined medicaments for respiratory viral infections' treatment. Consilium medicum. 2016;17:50-4.]
- Сабитов А.У., Ершова А.В. Оптимизация лечения острой респираторной вирусной инфекции у детей с бронхиальной астмой. Практическая медицина. 2015;2(87):85-90. [Sabitov A.U., Ershova A.V. Treatment optimization of acute respiratory viral infection in pediatric patients with bronchial asthma. Practical medicine. 2015;2(87):85-90.]
- Мордык А.В., Иванова О.Г., Антропова В.В., Ситникова С.В., Нагибина Л.А. Лечение и профилактика острых респираторных вирусных инфекций у больных туберкулезом органов дыхания в условиях противотуберкулезного стационара. Справочник поликлинического врача. 2017;1:14-9. [Mordyk A.V., Ivanova O.G., Antropova V.V., Sitnikova S.V., Nagibina L.A. Treatment and prevention of acute respiratory viral infections in patients with respiratory organs tuberculosis in antituberculosis hospital conditions. Manual of outpatient doctor. 2017;1:14-9.]
- Кондюрина Е.Г., Бурцева Е.И., Трушакова С.В., Мукашева Е.А., Виноградова А.А., Елкина Т.Н., Зеленская В.В. Оценка эффективности противовирусной терапии у детей с острым обструктивным бронхитом. Лечащий врач. 2017;1:65-70. [Kondjurina E.G., Burtzeva E.I., Trushakova S.V., Mukasheva E.A., Vinogradova A.A., Elkina T.N., Zelenskaya V.V. Estimation of the efficacy of antiviral therapy in pediatric patients with acute obstructive bronchitis. Practical physician. 2017;1:65-70.]
- Averyanov A., Andrianova A. The efficacy and safety of new combined medicinal product in the treatment of influenza: The results of a multicenter randomized comparative clinical trial. Eur. Respir. J. 2013;42(57):1496.
- Rafalsky V., Averyanov A., Bart B., Minina E., Putilovskiy M., Andrianova E., Epstein O. Efficacy and safety of Ergoferon versus oseltamivir in adult outpatients with seasonal influenza virus infection: a multicenter, open-label, randomized trial. Int. J. Infect. Dis. 2016;51:47-55.
- Горелова Е.А., Олисова О.Ю., Усенко Д.В. Исходы и пути оптимизации лечения ротавирусной инфекции у детей с атопическим дерматитом. Инфекционные болезни. 2016;14(1):80-5. [Gorelova E.A., Olisova O.Ju., Usenko D.V. Results and ways of optimization for rotaviral infection treatment in infants with atopic dermatitis. Infectious diseases. 2016;14(1):80-5.]
- Jefferson T., Jones M.A., Doshi P., Del Mar C.B., Hama R., Thompson M.J., Spencer E.A., Onakpoya I., Mahtani K.R., Nunan D., Howick J., Heneghan C.J. Neuraminidase inhibitors for preventing and treating influenza in healthy adults and children. Cochrane Database Syst. Rev. 2014;1:CD008965.
- Фазылов В.Х., Ситников И.Г., Силина Е.В., Шевченко С.Б., Можина Л.Н., Замятина Г.А., Еганян Г.А., Гроппа Л.Г., Корсантия Б.М. Лечение ОРВИ и гриппа в рутинной клинической практике (результаты многоцентрового международного наблюдательного исследования FLU-EE). Терапевтический архив. 2016;11:61-8. [Fazylov V.Kh., Sitnikov I.G., Silina E.V., Shevchenko S.B., Mozhina L.N., Zamyatina G.A., Yeganyan G.A., Groppa L.G., Korsantiya B.M. ARVI and grippe treatment in routine clinical practice (results of FLU-EE multicenter international observational study). Therapeutic archive. 2016;11:61-8.]
- Шульдяков А.А., Ляпина Е.П., Кузнецов В.И., Зрячкин Н.И., Ситников И.Г., Перминова ОА, Анохин В.А., Фаткуллина Г.Р. Новые возможности терапии острых респираторных вирусных инфекций у детей. Вопросы практической педиатрии, 2015;10(5):21-8. [Shuldyakov A.A., Lyapina E.P., Kuznetzov V.I., Zryachkin N.I., Sitnikov I.G., Perminova O.A., Anokhin V.A., Phatkullina G.R. New oppotrunities of the therapy of acute respiratory viral infections in pediatric patients. Aspects of practical pediatrics. 2015;10(5):21-8.]
- Deckx L., De Sutter A.I., Guo L., Mir N.A., van Driel M.L. Nasal decongestants in monotherapy for the common cold. Cochrane Database Syst. Rev. 2016;10:CD009612.
- Thompson M., Vodicka T.A., Blair P.S., Buckley D.I., Heneghan C., Hay A.D Duration of symptoms of respiratory tract infections in children: systematic review. BMJ.2013;347:f7027.
- Геппе Н.А., Теплякова Е Д, Шульдяков А.А, Ляпина Е.П., Перминова О.А., Мартынова Г.П., Ситников, Анохин И.Г., Фаткуллина В.А., Романенко Г.Р., Сависько В.В., Кондюрина А.А., Балыкова Е.Г. Инновации в педиатрии: оптимальный клинический эффект при лечении ОРВИ у детей препаратом комплексного действия. Педиатрия. 2016;95(2):96-103. [Geppe N.A., Teplyakova E.D., Shuldyakov A.A., Lyapina E.P., Perminova O.A., Martynova G.P., Sitnikov I.G., Anokhin V.A., Phatkullina G.R., Romanenko V.V., Savysko A.A., Kondjurina E.G., Balykova L.A. Innovations in pediatrics: optimal clinical effect in the treatment of ARVI in infants by combined medication drug. Pediatrics. 2016;95(2):96-103.]
- Кладова О.В. Профилактика и лечение частых респираторных заболеваний у детей с ослабленным иммунитетом. Детские инфекции. 2012. Спецвыпуск:26-31. [Kladova O.V. Prevention and treatment of frequently occuring respiratory diseases in blunt immunity infants. Infections of pediatric age. 2012. Special issue:26-31.]
- Описание изобретения к патенту 2238122. 16.1 1.2017. URL:www1.fips.ru/fips_servl/fips_servlet umber=2238122&TypeFile=html. [Description of the invention to the patent 2238122. 16.1 1.2017. URL:www1.fips.ru fips_servl/fips_servlet?DB=RUPAT&DocNumber=2238122&TypeFile=html.]
- Ison M.G., de Jong M.D., Gilligan K.J., Higgs E.S., Pavia A.T., Pierson J., Hayden FG. End points for testing influenza antiviral treatments for patients at high risk of severe and lifethreatening disease. J. Infect. Dis. 2010;201:1654-62.
- Емельянова А.Г., Мысливец М.А., Никифорова Н.В., Борщева А.А., Барыкина Д.В., Дон Е.С., Горбунов Е.А., Яковлева Н.Н., Скарнович М.О., Скарнович М.А., Мазурков О.Ю., Тарасов С.А., Шишкина Л.Н. Эффективность эргоферона в отношении вируса гриппа АЛ-13№: данные доклинического исследования in vivo. XXIII Российский национальный конгресс «Человек и лекарство». Москва.11-14 апреля, 2016:230. [Emelyanova A.G., Myslivetz M.A., Nikiphorova N.V., Borscheva A.A., Barykina D.V., Don E.S., Gorbunov E.A., Yakovleva N.N., Skarnovitch M.A., Mazurkov O.Ju., Tarasov S.A., Shishkina L.N. Efficacy of ergoferon to АЛ-13№ grippe virus: the data of in vivo preclinical trial. XXIII Russian National Congress " Man and medicine". Moscow. 11-14th of April, 2016:230.]
- Заплатников А.Л., Кондюрина Е.Г., Елкина Т.Н., Бурцева Е.И., Грибанова О.А., Пирожкова Н.И., Мингалимова Г.А., Тюленева И.О., Трушакова С.В., Мукашева Е.А. Многоплановая оценка схем терапии острых респираторных инфекций в условиях рутинной педиатрической практики. Антибиотики и химиотерапия. 2016;61(5-6):8-20. [Zaplatnikov A.L., Kondjurina E.G., Elkina T.L., Burtzeva E.I, Gribanova O.A., Pirozhkova E.I., Mingalimova G.A., Tjuleneva I.O., Trushakova S.V., Mukasheva E.A. Multisided estimation of the schemes of acute respiratory infections' therapy in routine pediatric practice conditions. Antibiotics and chemotherapy. 2016;61(5-6):8-20.]
- Кондюрина Е.Г., Елкина Т.Н., Зеленская В.В. ОРВИ и бронхиальная астма. Лечащий врач. 2005;9:28-32. [Kondjurina E.G., Elkina T.N., Zelenskaya V.V. ARVI and bronchial asthma. Practical physician. 2005;9:28-32.]
- Дзюблик А.Я., Симонов С.С., Ячник В.А. Клиническая эффективность и безопасность противовирусного препарата Ингавирин в комплексном лечении больных с обострением бронхиальной астмы, ассоциированным с ОРВИ. Пульмонология. 2013;6:43-50. [Dzjublik A.Ya., Simonov S.S., Yachnik V.A. Clinical efficacy and safety of Ingavirin antiviral medicament in the complex treatment of ARVI-associated bronchial asthma exacerbation patients. Pulmonology. 2013;6:43-50.]
- Spurling G.K., Del Mar C.B., Dooley L., Foxlee R., Farley R. Delayed antibiotic prescriptions for respiratory infections. Cochrane Database Syst. Rev. 2017;9:CD004417.
- Harris A.M., Hicks L.A., Qaseem A. Appropriate Antibiotic Use for Acute Respiratory Tract Infection in Adults: Advice for High-Value Care From the American College of Physicians and the Centers for Disease Control and Prevention. Ann. Intern. Med. 2016;164(6):425-34.
- Гаращенко Т.И., Ершов Ф.И. Возможен ли контроль острых респираторных заболеваний у детей? (Новый взгляд на старую проблему). Актуальные вопросы оториноларингологии детского возраста и фармакотерапия болезней ЛОР-органов. Юбилейный сборник научных трудов. Москва; 2001. [Garaschenko T.I., Ershov F.I. Is it possible to control acute respiratory diseases in infants? (New viewpoint at the old problem). Actual aspects of pediatric otolaryngology and pharmacotherapy of otolaryngological organs' diseases. Jubilee collection of scientific works. Moscow; 2001.]
- Petersen I., Johnson A.M., Islam A., Duckworth G., Livermore D.M., Hayward A.C. Protective effect of antibiotics against serious complications of common respiratory tract infections: retrospective cohort study with the UK General Practice Research Database. BMJ. 2007;10;335(7627):982.
Сведения об авторах:
Наталья Анатольевна Геппе, д.м.н., профессор, зав. кафедрой детских болезней ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России. Адрес: Россия, 119991, г. Москва, ул. Трубецкая, д. 8.
Санубар Таги к. Валиева, к.м.н., доцент кафедры педиатрии Азербайджанского государственного института усовершенствования врачей им. Азиза Алиева, г. Баку. Адрес: Азербайджан, AZ1012, г Баку, Тбилисский пр-т, 3165-й квартал, Ясамальский район.
Натаван Алыш гызы Фараджева, д.м.н., профессор кафедры терапии Института усовершенствования врачей им. Азиза Алиева, г. Баку. Адрес: Азербайджан, AZ1012, г Баку, Тбилисский пр-т, 3165-й квартал, Ясамальский район.
Марина Рудольфовна Оганян, к.м.н., доцент кафедры семейной медицины Ереванского государственного медицинского университета им. Мхитара Гераци. Адрес: Армения, 0025, г. Ереван, ул. Корьюна, д. 2.
Гулшара Туребековна Мырзабекова, д.м.н., доцент, зав. кафедрой педиатрии Казахского медицинского университета непрерывного образования, г. Алматы. Адрес: Казахстан, г. Алматы, ул. Манаса, д. 34.
Мурат Ахметович Жанузаков, д.м.н., профессор, зав. кафедрой терапии и пульмонологии Казахского медицинского университета непрерывного образования, г. Алматы. Адрес: Казахстан, г. Алматы, ул. Манаса, д. 34.
Адыл Каирбекович Катарбаев, д.м.н., профессор, зав. кафедрой детских инфекционных болезней Казахского государственного медицинского университета им. С.Д. Асфендиярова, г. Алматы. Адрес: Казахстан, г. Алматы, ул. Толе би, д.94.
Любовь Николаевна Скучалина, д.м.н., профессор, профессор кафедры детских болезней № 2 АО «Медицинский университет Астана». Адрес: Казахстан, г. Астана, ул. Бейбитшилик, д. 49-А.
Нарынбек Сабыркулович Айткулуев, к.м.н., доцент кафедры инфекционных болезней Кыргызско-российского славянского университета им Б.Н. Ельцина, г. Бишкек. Адрес: Киргыстан, 720035, г. Бишкек, ул. Льва Толстого, д. 70.
Динара Джамалбековна Кабаева, к.м.н., с.н.с., зав. отделением острой респираторной патологии Национального центра охраны материнства и детства, г. Бишкек. Адрес: Кыргызстан, 720038, г. Бишкек, ул. Тоголок Молдо, д. 1/2.
Фирдавс Орифович Раупов, к.м.н., ассистент кафедры семейной медицины Республиканского учебно-клинического центра семейной медицины, г. Душанбе. Адрес: Таджикистан, г. Душанбе, ул. Нарзикулова, д. 8, д. 80.
Гульнара Алиевна Ибадова, д.м.н., профессор, зав. кафедрой инфекционных и паразитарных заболеваний детского возраста Ташкентского института усовершенствования врачей. Адрес: Узбекистан, г. Ташкент, ул. Паркент, д. 51.
Фазлитдин Сайфутдинович Шамсиев, д.м.н., профессор, зав. кафедрой педиатрии факультета усовершенствования врачей Ташкентского института усовершенствования врачей. Адрес: Узбекистан, г. Ташкент, ул. Паркент, д. 51.
Шакар Истамовна Наврузова, д.м.н., профессор, зав. кафедрой детских болезней Бухарского государственного медицинского института. Адрес: Узбекистан, 200118,г. Бухара, пр. Навои, д. 1.
Шоира Акбаровна Хусинова, к.м.н., доцент, зав. кафедрой общей практики/семейной медицины факультета последипломного образования Самаркандского государственного медицинского института. Адрес: Узбекистан, г. Самарканд, ул. А. Темура, д. 18.
Рохатой Абдушариповна Нурмухамедова к.м.н., доцент кафедры повышения квалификации врачей общей практики Ташкентского института усовершенствования врачей. Адрес: Узбекистан, г. Ташкент, ул. Паркентская, д. 51.
Сагира Токсанбаевна Абдрахманова, д.м.н., зав. кафедрой детских болезней № 2 АО «Медицинский университет Астана». Адрес: Казахстан, г. Астана, ул. Бейбитшилик, д. 49А.
About the autors:
Natalya A. Geppe, MD, professor, head of the department of childhood diseases of I.M. Sechenov First Moscow state medical university of the Ministry of Health of Russia. Address: 119991, Russia, Moscow, 8 Trubetzkaya St.
Sanubar T. Vаliyeva, PhD, assistant professor of the Department of pediatrics of Azerbaijan State Advanced Training Institute for Doctors Aziz Aliev medical refresher institute, Baku. Address: Azerbaijan, AZ1012, Tbilisi Ave. 3165 quarter, Yasamal district, Baku.
Natavan A. Farajova, MD, professor Azerbaijan state advanced training institute for doctors named after A. Aliyev, Department of therapy. Address:Azerbaijan, Baku, 3165 Tbilisi ave, AZ 1012.
Marina R. Ohanyan, MD, assistant professor of the Family Medicine Department of Yerevan State Medical University after M. Heratsi. Address: Armenia, 0025, Yerevan, Korjun Str. 2.
Gulshara T. Myrzabekova, MD, assistant professor, head of the Department of pediatrics of Kazakh medical university of recurrent education, Almaty. Address: Kazakhstan, Almaty, 34 Manasa St.
Murat A. Zhanuzakov, MD, professor, head of the Department of therapy and pulmonology of Kazakh medical university of recurrent education, Almaty. Address: Kazakhstan, Almaty, 34 Manasa St.
Adyl K. Katarbayev, MD, professor, head of the Department of pediatric infections of S.D. Asphendiyarov Kazakh state medical university, Almaty. Address: Kazakstan, Almaty, 94 Tole bi St.
Ljubov N. Skuchalina, MD, professor of the Department of pediatrics № 2 of medical university, Astana. Address: Kazakstan, Astana, 49-A Beibitshilik St.
Narynbek S. Aitkuluev, PhD, assistant professor of the Department of infectious diseases of B.N. Yeltsin Kyrgyz-Russian Slavic university, Bishkek. Address: Kyrgyzstan, 720035, 70 Lva Tolstogo St.
Dinara D. Kabaeva, PhD, head of the Department of acute respiratory pathology of National Center Of Maternity and Childhood Protection, Bishkek. Address: Kyrgyzstan, 720038, Bishkek, Togolok Moldo St.
Firdavs О. Raupov, PhD, assistant of family medicine Department of Republican Training and Clinical Family Medicine Center, Dushanbe. Address: Tadjikistan, Dushanbe, 80 Alinij St.
Gulnara A. Ibadova, professir, head of the Department of pediatric infectious diseases and parasitology of medical refresher faculty ofTashkent Institute of Postgraduate Medical Education . Address: Uzbekistan, Tashkent, 51 Parkent St.
Fazlitdin S. Shamsiev, MD, professor, head of the Department of pediatrics of medical refresher faculty of Tashkent medical refresher institute. Address: Uzbekistan, Tashkent, 51 Parkent St.
Shakar I. Navruzova, MD, professor, head of the Department of pediatric diseases of Bukara state medical institute. Address: Uzbekistan, 200118, Bukhara, 1 Navoi pr.
Shoira A. Khusinova, PhD, assistant professor of common practice/family medicine Department of postgraduate education faculty of Samarkand state medical institute. Address: Uzbekistan, Samarkand, 18 A. Temur St.
Rokhatoi A. Nurmukhamedova, PhD, assistant professor of the Department of upgrading qualification for common practice doctors of medical refresher faculty from Tashkent medical refresher institute. Address: Uzbekistan, Tashkent, 51 Parkent St.
Sagira T. Abdrakhmanova, MD., head of the Department of pediatrics № 2 of Astana medical university. Address: Kazakhstan, Astana, 49A Beibitshilik St.


