Результаты плацебоконтролируемого многоцентрового исследования “Актовегин по сравнению с плацебо у пациентов с диабетической полиневропатией”*
СтатьиИ.А. Строков
* Статья подготовлена по материалам указанного исследования, результаты которого представлены в недавней публикации журнала “Diabetes Care”: Ziegler D., Movsesyan L., Mankovsky B. et al. Treatment of symptomatic polyneuropathy with actovegin in type 2 diabetic patients // Diabetes Care. 2009. V. 32. № 8. P. 1479-1484.
Сахарный диабет (СД) становится наиболее серьезной угрозой для здоровья населения во всем мире. Согласно прогнозам, в мире число больных СД увеличится со 171 млн. в 2000 г. до 366 млн. в 2030 г. СД сопровождается повышением риска макрососудистых осложнений, таких как ишемическая болезнь сердца, инсульт, заболевания периферических сосудов. Кроме того, быстро увеличивается распространенность микрососудистых осложнений СД, таких как ретинопатия, нефропатия и диабетическая полиневропатия (ДПН).
Формирование ДПН обусловлено метаболическими нарушениями и изменением сосудов микроциркуляторного русла, в том числе эндоневральных сосудов, что формирует клеточную гипоксию и феномен “оксидативного стресса”. В этой связи в последние годы для лечения ДПН наиболее широко использовались различные антиоксиданты.
Вместе с тем возможность увеличения поступления кислорода в клетки и улучшения энергетического обеспечения их жизнедеятельности предоставляют антигипоксанты, из которых наиболее известным и широко применяемым является препарат Актовегин. Актовегин представляет собой высокоочищенный гемодиализат, получаемый методом ультрафильтрации из крови телят. Актовегин содержит аминокислоты, олигопептиды, нуклеозиды, продукты углеводного и жирового обмена, липиды, олигосахариды, электролиты и микроэлементы. Увеличение поглощения кислорода сосудистой стенкой при лечении Актовегином приводит к нормализации эндотелийзависимых реакций и снижению периферического сосудистого сопротивления. Важно, что Актовегин активизирует транспорт глюкозы внутрь клеток, улучшая энергообеспечение клеточных структур, что имеет большое значение при инсулинорезистентности у больных СД 2-го типа.
В экспериментальных исследованиях показано, что Актовегин уменьшает при сахарном диабете выраженность оксидативного стресса.
W. Jansen и E. Beck провели контролируемое клиническое исследование эффективности применения таблетированной формы Актовегина в дозе 1800 мг в день (по 600 мг 3 раза в день) у 35 больных СД 2-го типа и ДПН в течение 24 нед [1]. По сравнению с группой из 35 больных, получавших плацебо, в группе, получавшей Актовегин, наблюдалось достоверное снижение позитивной (жалобы больных) и негативной (неврологический дефицит) невропатической симптоматики.
Приведенные данные экспериментальных и клинических исследований, а также накопленный к настоящему времени значительный опыт применения Актовегина при диабетической полиневропатии в широкой клинической практике послужили основанием для подготовки и проведения широкомасштабного исследования “Актовегин по сравнению с плацебо у пациентов с диабетической полиневропатией” [2].
Дизайн исследования
Исследование “Актовегин по сравнению с плацебо у больных с диабетической полиневропатией” проводилось в 26 клинических центрах России, Украины и Казахстана. В окончательный анализ результатов исследования вошли 567 пациентов с сахарным диабетом 2-го типа, имевших симптоматику дистальной симметричной сенсорномоторной полиневропатии. Все больные были рандомизированы в группу лечения Актовегином и группу сравнения (группа плацебо). Пациенты обеих групп были сопоставимы по возрасту, сопутствующей патологии, получаемой сахароснижающей терапии (в том числе инсулином). Схема лечения в группах Актовегина и плацебо включала сначала 20 внутривенных инфузий (по 2000 мг 1 раз в день), затем прием таблеток Актовегина (по 1800 мг -3 таблетки по 200 мг 3 раза в день) в течение 140 дней (рис. 1). За время наблюдения у пациентов было 26 контрольных визитов. На каждом из этих визитов проводилось тестирование по шкалам невропатических симптомов и исследование порога вибрационной чувствительности. В качестве основного показателя состояния больных использовалась оценка по “Общей шкале невропатических симптомов” (TSS). Функциональное состояние периферических нервов оценивали по порогу вибрационной чувствительности (VPT). Вторичными показателями состояния больных были комбинированная шкала симптомов невропатии для нижних конечностей (NIS-LL) и оценка качества жизни по опроснику SF-36.
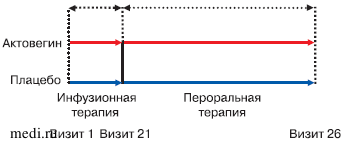 Рис. 1. Схемы терапии. Период инфузионной терапии: всего 20 инфузий (Актовегина или плацебо) 1 раз в сутки в течение 20-36 дней. Период пероральной терапии: Актовегин или плацебо в течение 140 ± 15 дней.
Рис. 1. Схемы терапии. Период инфузионной терапии: всего 20 инфузий (Актовегина или плацебо) 1 раз в сутки в течение 20-36 дней. Период пероральной терапии: Актовегин или плацебо в течение 140 ± 15 дней.
Шкала оценки общих симптомов невропатии
Шкала TSS (Total Symptom Score) включает четыре позитивных невропатических симптома: стреляющую боль, жжение, парестезии и онемение в стопах и/или голенях. Позитивная невропатическая симптоматика, оценка которой проводится по шкале TSS, - это наиболее часто отмечаемые симптомы у больных СД 2-го типа и дистальной полиневропатией. Оценка по шкале TSS является суммарной оценкой интенсивности и частоты всех четырех позитивных невропатических симптомов в баллах. Именно позитивная невропатическая симптоматика оказывает влияние на повседневную активность и нарушает качество жизни пациентов с сахарным диабетом и ДПН.
Изменение (уменьшение) баллов по шкале TSS считается наиболее важным, когда речь идет об улучшении состояния пациентов.
Анализ свидетельствует о положительном влиянии Актовегина на симптомы ДПН уже в течение периода инфузионной терапии (рис. 2). Эффект постепенно усиливался в период перорального приема препарата с появлением статистически значимой разницы между группами Актовегина и плацебо вскоре после окончания периода инфузионной терапии. По рекомендациям согласительного комитета разница между активной терапией и плацебо для изменения положительных сенсорных симптомов должна составлять не менее 0,83 балла. Оценка по шкале TSS в группе Актовегина достоверно улучшилась на 0,86 балла по сравнению с плацебо (от начала исследования до 160-го дня) (см. рис. 2).
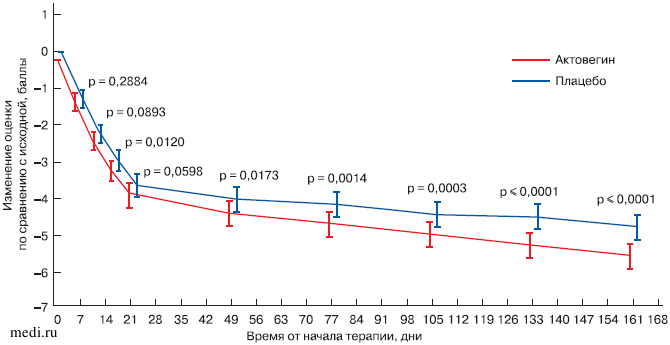 Рис. 2. Изменения оценки невропатических симптомов по шкале TSS.
Рис. 2. Изменения оценки невропатических симптомов по шкале TSS.
Порог вибрационной чувствительности
Определение порога вибрационной чувствительности (VPT - vibration perception threshold) относится к объективным количественным исследованиям чувствительности. Определение VPT проводили на биотензиометре.
Биотензиометр - это прибор, разработанный для простой и точной оценки ощущения порога вибрации. По сути, это “электрический камертон”, амплитуда которого зависит от величины подаваемого напряжения, в связи с чем уровень вибрации измеряется в вольтах. Чем ниже VPT, тем выше чувствительность. Амплитуду можно установить на любой заранее определенный уровень или постепенно повышать до достижения порога вибрационной чувствительности, и наоборот, снижать до тех пор, пока ощущение вибрации не исчезнет.
Для измерения порога вибрационной чувствительности биотензиометр помещали на следующие 5 точек в области обеих стоп: медиальную лодыжку, медиальную головку 1-й плюсневой кости, подушечку большого пальца стопы, латеральную головку 5-й плюсневой кости и бугристость 5-й плюсневой кости. Рассчитывали среднее значение для 5 точек на одной стопе. В каждом учреждении для тестирования всех пациентов применяли один и тот же прибор. Для включения пациента в исследование порог вибрационной чувствительности на каждой стопе должен был составлять ≤30 В.
Изначально средний порог вибрационной чувствительности был несколько ниже для группы Актовегина, чем для плацебо. К концу исследования среднее значение VPT в группе Актовегина снизилось по сравнению с исходным достоверно (р = 0,017) на большую величину (-3,6 В), чем в группе плацебо (-2,9 В). Таким образом, объективный показатель функционального состояния периферических нервов подтвердил, что отмечаемое пациентами уменьшение позитивной невропатической симптоматики имеет физиологическую основу в виде улучшения чувствительности и лечение Актовегином уменьшает риск развития диабетической стопы.
Комбинированная шкала симптомов невропатии нижних конечностей
Шкала NIS-LL (Neuropathy Impairment Score of Low Limbs) - это комплексный показатель неврологического статуса, который позволяет количественно оценить неврологический дефицит. По шкале оцениваются мышечная сила (сгибание/разгибание в тазобедренном и коленном суставах, тыльное/подошвенное сгибание в голеностопном суставе и разгибание/сгибание большого пальца стопы), сухожильные рефлексы (коленный и ахиллов), а также чувствительность различной модальности (тактильная, болевая, вибрационная и суставно-мышечное чувство).
Улучшение оценки по шкале NIS-LL (т.е. уменьшение общего количества баллов) к концу исследования по сравнению с исходными значениями было более значительным в группе Актовегина (рис. 3). 75% пациентов из группы лечения Актовегином показали абсолютное улучшение оценки по сравнению с группой плацебо на 2 балла (что считается клинически значимым).
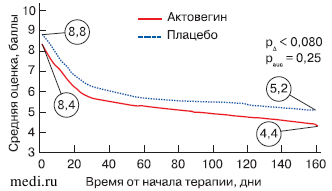 Рис. 3. Профили средней оценки по шкале NIS-LL в течение периода терапии.
Рис. 3. Профили средней оценки по шкале NIS-LL в течение периода терапии.
Отмечено достоверное уменьшение нарушений чувствительности (вибрационная, болевая, тактильная, суставно-мышечное чувство) (p < 0,005). Важно, что наблюдалось улучшение не только глубокой (проприоцептивной) чувствительности, которая проводится толстыми волокнами, но и поверхностной чувствительности, которая проводится тонкими волокнами. Таким образом, в группе Актовегина улучшалась чувствительность различных модальностей. Улучшение состояния больных по шкале NIS-LL подтверждает уменьшение неврологических проявлений ДПН при лечении Актовегином, что является прогностически важным показателем, особенно учитывая длительность наблюдения за больными.
Оценка качества жизни по опроснику SF-36
Опросник SF-36 служит валидизированным инструментом определения качества жизни, связанного со здоровьем, и позволяет оценить физическое, психологическое, социальное и психическое здоровье, общее восприятие здоровья, а также интенсивность боли и жизненную активность.
Опросник SF-36 состоит из следующих разделов: энергичность, физическое здоровье, физическая боль, общее восприятие здоровья, оценка физической активности, оценка эмоциональной активности, оценка социальной активности, психическое здоровье.
Перечисленные разделы объединяются в два измерения: физическое здоровье и психическое здоровье. Физическое здоровье включает функциональные параметры (ходьба, умывание, одевание), телесную боль, общее здоровье. Психическое здоровье включает жизненную энергию, социальное функционирование, уровень счастья (насколько радостно, подавленно или депрессивно чувствует себя пациент).
Психическое здоровье к концу исследования в группе Актовегина улучшилось достоверно (p = 0,027) в большей степени, чем в группе плацебо (рис. 4). Отмечалось также улучшение физического здоровья в группе лечения Актовегином, более значительное, чем в группе плацебо, однако эффект терапии к концу лечения не достиг статистической значимости (p = 0,101).
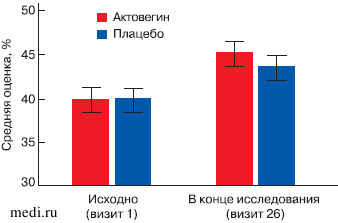 Рис. 4. Суммарная оценка качества жизни по опроснику SF-36 (психическое здоровье) в течение периода терапии.
Рис. 4. Суммарная оценка качества жизни по опроснику SF-36 (психическое здоровье) в течение периода терапии.
Уменьшение проявлений диабетической полиневропатии у больных СД 2-го типа на фоне лечения Актовегином сопровождалось улучшением качества жизни больных, что всегда является одной из задач проводимого лечения.
Выводы
Результаты исследования показали, что лечение Актовегином, сначала в виде внутривенных инфузий (2000 мг), а затем в виде таблетированной формы (1800 мг), достоверно уменьшает клинические проявления диабетической полиневропатии и улучшает качество жизни больных сахарным диабетом 2-го типа.
Последовательная внутривенная, а затем пероральная терапия Актовегином уменьшила симптомы невропатии, улучшила вибрационную чувствительность и сенсорную функцию у пациентов с СД 2-го типа и ДПН.
Показано значимое улучшение качества жизни в группе Актовегина по сравнению с плацебо (опросник SF-36, психическое здоровье).
Группы пациентов, получавших Актовегин и плацебо, имели сравнимый профиль безопасности.
Игорь Алексеевич Строков - канд. мед. наук, доцент кафедры нервных болезней лечебного факультета ММА им. И.М. Сеченова.
Список литературы
1. Jansen W., Beck E. // Die Medizinische Welt. 1987. V. 38. P. 838. (Пер. на рус. яз. в сб. “Опыт клинического применения актовегина в эндокринологии”. М., 2005. С. 11-20.)
2. Ziegler D. et al. // Diabetes Care. 2009. V. 32. P. 1479.
