 invar.ru
invar.ru

Cредство для естественного восстановления менструального цикла без гормонов
В его состав входит уникальная комбинация мио-инозитола, D-хиро-инозитола, марганца и фолиевой кислоты.
далее...
Новые возможности интегративной терапии пациенток с синдромом поликистозных яичников и нарушениями углеводного и липидного обмена. Результаты сравнительного исследования
СтатьиОпубликовано в журнале:
РМЖ. Мать и дитя. T.3, № 3, 2020
DOI: 10.32364/2618-8430-2020-3-3-169-173
Ю.Э. Доброхотова, И.А. Лапина, Т.Г. Чирвон, В.В. Таранов
ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, Москва, Россия
Резюме
Введение: первой линией лечения женщин с синдромом поликистозных яичников (СПКЯ) является назначение эстроген-гестагенных комбинированных оральных контрацептивов (КОК) в длительном режиме. Однако такая терапевтическая стратегия не влияет на метаболические нарушения, более выраженные у пациенток со вторым патогенетическим вариантом СПКЯ, что ведет к увеличению риска кардиометаболических осложнений.
Цель исследования: оценить влияние средства на основе мио- и D-хиро-инозитола в соотношении 5:1 на метаболические показатели у пациенток репродуктивного возраста со вторым патогенетическим вариантом СПКЯ и нарушением углеводного и липидного обмена.
Материал и методы: в рандомизированном проспективном исследовании приняли участие 60 женщин с СПКЯ и избыточной массой тела или ожирением. Пациентки 1-й группы (n=30) получали КОК в сочетании со средством, содержащим две изоформы инозитола в соотношении 5:1 (мио-инозитол 1000 мг и D-хиро-инозитол 200 мг). Во 2-й группе (n=30) женщины принимали только КОК. Оценивали показатели системы гемостаза, липидного профиля, уровень глюкозы плазмы натощак, а также индекс массы тела (ИМТ) и окружность талии до начала исследования и через 90 дней.
Результаты исследования: в 1-й группе у пациенток отмечено статистически значимое (p<0,05) улучшение показателей липидограммы: снижение уровня общего холестерина (Хс) (на 16,9%), триглицеридов (на 15,7%), Хс липопротеинов низкой плотности (на 17,8%) и увеличение уровня Хс липопротеинов высокой плотности (на 28,5%); снижение уровня фибриногена (на 15,8%) и глюкозы натощак (на 16,9%), тогда как во 2-й группе достоверных изменений анализируемых показателей зарегистрировано не было. Кроме того, в 1-й группе на фоне лечения отмечено уменьшение окружности талии (на 4,5%) и ИМТ (на 9,1%).
Заключение: включение в терапию пациенток с СПКЯ средства на основе мио- и D-хиро-инозитола в соотношении 5:1 представляется перспективным для профилактики у них кардиометаболических осложнений. Для подтверждения полученных результатов и дополнительной оценки свойств инозитолов рекомендуется проведение дальнейших, более масштабных исследований.
Ключевые слова: синдром поликистозных яичников (СПКЯ), лечение, профилактика, ожирение, метаболический синдром, липидограмма, инозитол, комбинированные оральные контрацептивы.
Для цитирования: Доброхотова Ю.Э, Лапина ИА, Чирвон Т.Г, Таранов В.В. Новые возможности интегративной терапии пациенток с синдромом поликистозных яичников и нарушениями углеводного и липидного обмена. Результаты сравнительного исследования. РМЖ. Мать и дитя. 2020;3(3):169-172. DOI: 10.32364/2618-8430-2020-3-3-169-173.
New prospects of the integrative therapy for polycystic ovary syndrome in women with the disorders of carbohydrate and lipid metabolism: a comparative study
Yu.E. Dobrokhotova, I.A. Lapina, T.G. Chirvon, V.V. Taranov
Pirogov Russian National Research Medical University, Moscow, Russian Federation
Abstract
Background: long-term combined estrogen-progestin oral contraceptive pills (COCPs) are the first-line treatment for polycystic ovary syndrome (PCOS). However, this therapeutic option does not affect metabolic disorders that are more severe in women with the second PCOS phenotype thus increasing the risk of cardiometabolic complications.
Aim: to assess the effect of myo-inositol and D-chiro-inositol at a 5:1 ratio on metabolic parameters in women of reproductive age with the second PCOS pathogenetic type and the disorders of carbohydrate and lipid metabolism.
Patients and Methods: 60 overweight and obese women with PCOS were enrolled in this randomized prospective study. Group 1 women (n=30) received COCP and a drug containing two isoforms of inositol at a 5:1 ratio (myo-inositol 1,000 mg plus D-chiro inositol 200 mg). Group 2 women (n = 30) received COCP only. Hemostasis, lipid panel, fasting glucose level, body mass index (BMI), and waist circumference were measured before and 90 days after treatment begins.
Results: in group 1, the significant (p<0.05) improvement of lipid parameters was reported as demonstrated by the reduction of the levels of total cholesterol (TC) by 16.9%, triglycerides by 15.7%, low-density lipoprotein cholesterol (LDL-C) by 17.8%, fibrinogen by 15.8%, and fasting glucose by 16.9% as well as the increase of high-density lipoprotein cholesterol (HDL-C) by 28.5%. Meanwhile, no significant changes were seen in group 2. Additionally, the reduction of waist circumference by 4.5% and BMI by 9.1% was reported in group 1.
Conclusions: a medication containing myo-inositol and D-chiro-inositol at a 5:1 ratio is promising for the prevention of cardiometabolic complications in women with PCOS. Further large studies of the investigated drug are needed to demonstrate its efficacy and to assess its properties.
Keywords: polycystic ovary syndrome (PCOS), treatment, prevention, obesity, metabolic syndrome, lipid panel, inositol, oral contraceptive pills.
For citation: Dobrokhotova Yu.E., Lapina I.A., Chirvon T.G., Taranov V.V. New prospects of the integrative therapy for polycystic ovary syndrome in women with the disorders of carbohydrate and lipid metabolism: a comparative study. Russian Journal of Woman and Child Health. 2020;3(3):170-172. DOI: 10.32364/2618-8430-2020-3-3-169-173.
Введение
Синдром поликистозных яичников (СПКЯ) – одно из самых распространенных гинекологических заболеваний, диагностическими критериями которого являются хроническая ановуляция, клинические или биохимические признаки гиперандрогении и наличие поликистозных яичников по данным УЗИ [1, 2]. Исследования последнего десятилетия показали, что некоторые пациентки с данным диагнозом имеют сниженную чувствительность к инсулину (инсулинорезистентность) независимо от наличия избыточной массы тела или ожирения. Ее обнаруживают примерно у 70-80% женщин с СПКЯ и центральным ожирением и у 15-30% худых женщин с СПКЯ [3, 4]. Это увеличивает риск нарушения углеводного обмена и развития сахарного диабета 2 типа у таких пациенток и влечет за собой кардиометаболические нарушения, которые ассоциированы с артериальной гипертензией, дислипидемией, висцеральным ожирением, гиперинсулинемией и нарушениями в системе гемостаза. Гиперандрогения и низкий уровень глобулинов, связывающих половые гормоны, также ассоциированы с увеличением риска кардиометаболических осложнений у женщин всех возрастных групп [3, 5].
В зависимости от клинической картины и с учетом метаболических характеристик выделяют два патогенетических варианта СПКЯ: первый – классический репродуктивный и второй – с высоким риском метаболических нарушений, называемый некоторыми авторами «метаболический репродуктивный синдром» [3].
Терапевтическая коррекция проявлений СПКЯ у пациенток, не планирующих беременность, направлена в первую очередь на устранение андрогенозависимых эстетических дефектов, таких как гирсутизм, себорея, акне, и условное восстановление менструального цикла. Первой линией лечения таких женщин является назначение эстроген-гестагенных комбинированных оральных контрацептивов (КОК) в длительном режиме. Однако такая терапевтическая стратегия не влияет на метаболические нарушения, более выраженные у пациенток со вторым патогенетическим вариантом СПКЯ, что ведет к увеличению риска кардиометаболических осложнений [2, 3].
В качестве элемента комплексной терапии перспективным у данной группы пациенток представляется применение инозитола в виде его активных стереоизомеров – мио-инозитола и D-хиро-инозитола. Обе изоформы способны повышать чувствительность тканей к инсулину. Мио-инозитол является предшественником инозитолтрифосфата (I3P) – посредника, который участвует в передаче сигнала от рецепторов тиреотропного гормона и фолликулостимулирующего гормона (ФСГ), а также инсулина. Он оказывает специфическое влияние на яичники, главным образом путем модуляции метаболизма глюкозы и передачи сигналов ФСГ. Кроме того, мио-инозитол может улучшать функцию яичников посредством изменения метаболизма стероидов через инсулиннезависимые пути. D-хиро-инозитол образуется из мио-инозитола при участии специфического фермента эпимеразы. Он участвует в опосредованной активации сигнального пути инсулина, а также препятствует увеличению продукции андрогенов. Активность обеих изоформ инозитола включает различные биологические механизмы, что приводит к синергическому усилению эффекта от их совместного применения [6-10].
Несколько мировых исследований убедительно показали положительное влияние инозитола на репродуктивную функцию, восстановление овуляции и менструального цикла у пациенток с СПКЯ. Однако не меньший интерес представляют динамика метаболических показателей при клиническом использовании инозитола, а также его роль в профилактике кардиометаболических осложнений СПКЯ.
Цель исследования: оценить влияние средства на основе мио- и D-хиро-инозитола в соотношении 5:1 на метаболические показатели у пациенток репродуктивного возраста со вторым патогенетическим вариантом СПКЯ и нарушением углеводного и липидного обмена.
Материал и методы
Проведено рандомизированное проспективное исследование с участием 60 женщин с верифицированным диагнозом СПКЯ и избыточной массой тела или ожирением. Исследование было одобрено локальным этическим комитетом. Перед началом исследования все пациентки подписывали информированное добровольное согласие.
Критерии включения в исследование: возраст 18-35 лет, верифицированный диагноз СПКЯ, прием КОК (в составе этинилэстрадиол 30 мкг), нарушение углеводного обмена (глюкоза плазмы натощак 5,6-6,0 ммоль/л), окружность талии более 80 см, нарушение жирового обмена (индекс массы тела (ИМТ) >27 кг/м²), отсутствие тяжелой соматической, эндокринной патологии (в т. ч. сахарного диабета).
Все женщины на момент начала исследования принимали КОК с дозировкой этинилэстрадиола 30 мкг от двух месяцев до 1 года.
У всех женщин диагноз СПКЯ был подтвержден ранее на основании клинических проявлений и характеристик менструального цикла, данных физикального обследования, биохимического анализа крови с определением уровня половых гормонов, а также ультразвукового исследования органов малого таза, в связи с чем и был назначен прием КОК.
С целью сравнительной оценки метаболических показателей и анализа эффективности применения комбинации мио-инозитола и D-хиро-инозитола (5:1) пациентки были распределены в 2 группы по 30 человек. Пациенткам 1-й группы (средний возраст 28,6±5,6 года) в дополнение к КОК было назначено средство, содержащее две изоформы инозитола (в одном саше – мио-инозитол 1000 мг и D-хиро-инозитол 200 мг), фолиевую кислоту и марганец, по 2 саше 1 р./сут (порошок из саше предварительно растворяли в стакане воды). Во 2-й группе женщины (средний возраст 29,4±4,8 года) принимали только КОК. Наблюдение осуществлялось в течение 90 дней. Наряду с медикаментозной терапией пациенткам были рекомендованы динамические физические нагрузки, коррекция образа жизни и питания.
Оценивали показатели системы гемостаза (тромбоциты, активированное частичное тромбопластиновое время (АЧТВ), международное нормализованное отношение (МНО), тромбиновое время, фибриноген), липидного профиля (общий холестерин (Хс), триглицериды, Хс липопротеинов высокой плотности (ЛПВП), Хс липопротеинов низкой плотности (ЛПНП), Хс липопротеинов очень низкой плотности (ЛПОНП), коэффициент атерогенности), уровня глюкозы плазмы натощак, а также ИМТ и окружности талии до начала исследования и через 90 дней. Кроме того, в 1-й группе оценивали побочные эффекты и нежелательные явления.
Статистическую обработку результатов исследования проводили с использованием методов параметрического и непараметрического анализа. Для накопления, корректировки, систематизации исходной информации и фиксации полученных результатов применяли электронные таблицы Microsoft Office Excel 2016. Статистический анализ проводили с использованием программы Statistica 13.3 (StatSoft. Inc, США). Первоначально оценивали характер распределения данных при помощи критерия Шапиро – Уилка и нормальных вероятностных графиков. Для определения однородности дисперсий по группам был использован критерий Левена. Если распределение подчинялось закону о нормальном распределении, применяли t-критерий Стьюдента, если нет – t-критерий Вилкоксона. Критерием статистической значимости различий принято значение p<0,05.
Результаты и обсуждение
Исходно группы были сопоставимы по изучаемым показателям. По результатам исследования установлено, что в 1-й группе пациенток добавление к терапии мио- и D-хиро-инозитола в соотношении 5:1 способствовало существенному снижению уровня общего Хс (на 16,9%), триглицеридов (на 15,7%), Хс ЛПНП (на 17,8%), коэффициента атерогенности (на 21,6%) и увеличению уровня Хс ЛПВП (на 28,5%). Во 2-й группе также отмечены изменения указанных параметров, однако изменения эти не были статистически значимыми (табл. 1). Также у пациенток 1-й группы было отмечено снижение уровня глюкозы натощак на 16,9%, что свидетельствует о выраженном влиянии на углеводный обмен (см. табл. 1).
Полученные данные позволяют предположить возможность коррекции нарушений углеводного и липидного обмена комбинацией мио- и D-хиро-инозитола в соотношении 5:1 для снижения риска кардиометаболических осложнений.
Концентрация фибриногена в 1-й группе уменьшилась на 15,8% в отличие от 2-й группы, где значение данного показателя не изменилось. Учитывая, что прием КОК пусть и незначительно, но повышает риск тромботических осложнений, данный терапевтический эффект изучаемого средства представляет дополнительный интерес в дальнейшем изучении его влияния на систему гемостаза. Динамика показателей АЧТВ, МНО, тромбоцитов и тромбинового времени в обеих группах не имела существенных различий (см. табл. 1).
Таблица 1. Показатели липидограммы, системы гемостаза и уровня глюкозы плазмы натощак у пациенток групп наблюдения (M±SD)
Table 1. Lipid profile, hemostasis, and fasting glucose level in both groups (M±SD)
| Показатель Parameters |
1-я группа Group 1 |
2-я группа Group 2 |
||
| до лечения before treatment |
через 90 дней after 90 days |
до лечения before treatment |
через 90 дней after 90 days |
|
| Общий Хс, ммоль/л / Total cholesterol, mmol/l | 5,79±0,35 | 4,92±0,28** | 5,65±0,45 | 5,37±0,31 |
| Триглицериды, ммоль/л / Triglycerides, mmol/l | 2,20±0,69 | 1,76±0,57* | 2,24±0,69 | 2,08±0,59 |
| Хс ЛПВП, ммоль/л / HDL-C, mmol/l | 0,89±0,55 | 1,36±0,45* | 0,92±0,53 | 0,96±0,55 |
| Хс ЛПНП, ммоль/л / LDL-C, mmol/l | 3,69±0,56 | 3,03±0,49** | 3,65±0,57 | 3,53±0,40 |
| Хс ЛПОНП, ммоль/л / VLDL-C, mmol/l | 1,59±0,60 | 1,30±0,56 | 1,67±0,59 | 1,51±0,59 |
| Коэффициент атерогенности / Atherogenic coefficient | 3,14±1,08 | 2,64±0,91 | 3,16±1,02 | 3,07±0,99 |
| Глюкоза, ммоль/л / Glucose, mmol/l | 5,81±0,12 | 4,89±0,27** | 5,80±0,11 | 5,79±0,11 |
| Тромбоциты, тыс. Ед/мкл / Platelets (Plt), 10³/μl | 297,4±13,4 | 295,2±13,7 | 289,2±14,4 | 286,2±14,1 |
| Фибриноген, г/л / Fibrinogen, g/l | 3,83±0,14 | 3,08±0,13** | 3,75±0,13 | 3,71±0,12 |
| МНО, ед. / INR, U | 0,92±0,09 | 0,95±0,12 | 0,91±0,07 | 0,93±0,11 |
| АЧТВ, с / Activated partial thromboplastin time (aPTT), sec | 28,90±0,63 | 29,64±0,57 | 27,34±0,59 | 28,91±0,53 |
| Тромбиновое время, с / Thrombin time, sec | 15,02±0,33 | 15,91±0,43 | 15,13±0,28 | 15,22±0,31 |
Примечание. Статистическая значимость различий по сравнению с исходным значением: *p<0,05; **p<0,01.
Note. Significant differences compared to baseline level: *p<0.05; **p<0.01.
Уменьшение окружности талии (на 4,5%) и ИМТ (на 9,1%) в 1-й группе на фоне лечения является дополнительным маркером положительного влияния на соматический статус пациенток с метаболическими нарушениями (рис. 1). Интересен тот факт, что средство демонстрирует более высокую эффективность при более выраженных метаболических нарушениях [7].
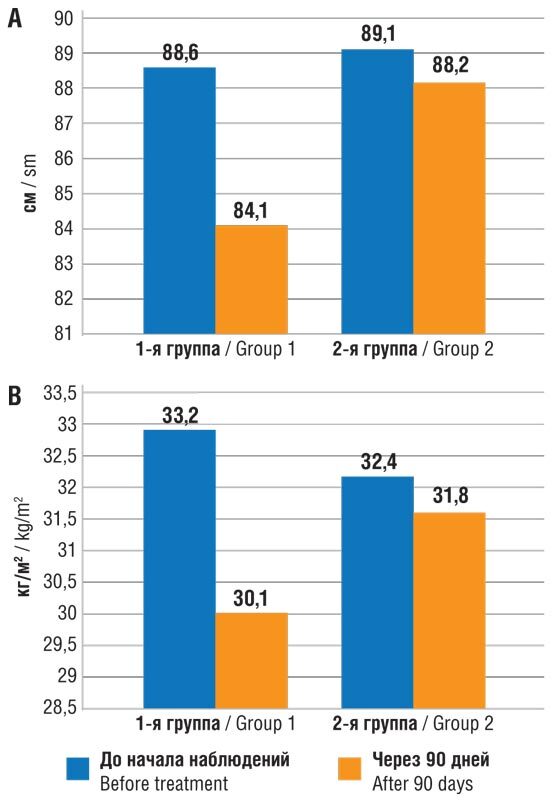 Рис. 1. Динамика окружности талии (А) и ИМТ (В) у пациенток групп наблюдения
Рис. 1. Динамика окружности талии (А) и ИМТ (В) у пациенток групп наблюдения
Fig. 1. Changes in waist circumference (A) and BMI (B) in both groups
Из побочных и нежелательных эффектов при приеме исследуемого средства были отмечены тошнота – у 2 (6,7%) пациенток, диарея – у 2 (6,7%) и аллергическая реакция в виде крапивницы у одной пациентки, которая прекратила прием инозитола, выбыла из исследования и не учитывалась при статистической обработке данных.
Заключение
Клиническое использование мио- и D-хиро-инозитола в соотношении 5:1 у пациенток с СПКЯ является новой, интегративной стратегией вне зависимости от репродуктивных планов. Изученное средство, сочетающее две активные формы инозитола в соотношении 5:1 (мио-инозитол 1000 мг и D-хиро-инозитол 200 мг), обладая высокой метаболической активностью, способствует улучшению параметров системы гемостаза, липидного профиля, углеводного обмена, а также снижению массы тела и уменьшению окружности талии. Для подтверждения полученных результатов и дополнительной оценки свойств инозитолов рекомендуется проведение дальнейших, более масштабных исследований.
Несмотря на то что в настоящее время применение инозитола при СПКЯ является экспериментальным, это направление в терапии следует считать перспективным не только в целях увеличения частоты овуляции и улучшения репродуктивной функции у пациенток, планирующих беременность, но и в целях улучшения показателей углеводного и липидного обмена и профилактики кардиометаболических осложнений у всех женщин с СПКЯ [7, 8].
Литература
- Regidor P.A., Schindler A.E., Lesoine B., Druckman R. Management of women with PCOS using myo-inositol and folic acid. New clinical data and review of the literature. Horm Mol Biol Clin Investig. 2018;34(2). pii: /j/hmbci.2018.34.issue-2/hmbci-2017-0067/hmbci-2017-0067.xml. DOI: 10.1515/hmbci-2017-0067.
- Rotterdam ESHRE/ASRM Sponsored PCOS Consensus Workshop Group. Revised 2003 consensus on diagnostic criteria and long term health risks related to polycystic ovary syndrome (PCOS). Hum Reprod. 2004;19(1):41-47. DOI: 10.1093/humrep/deh098.
- Genazzani A.D. Inositol as putative integrative treatment for PCOS. Reprod Biomed online. 2016;33(6):770-780. DOI: 10.1016/j. rbmo.2016.08.024.
- Pundir J., Psaroudakis D., Savnur P. et al. Inositol treatment of anovulation in women with polycystic ovary syndrome: a meta-analysis of randomised trials. BJOG. 2018;125(3):299-308. DOI: 10.1111/1471-0528.14754.
- Unfer V., Nestler J.E., Kamenov Z.A. et al. Effects of Inositol (s) in Women with PCOS: A Systematic Review of Randomized Controlled Trials. Int J Endocrinol. 2016;2016:1849162. DOI: 10.1155/2016/1849162.
- Crawford T.J., Crowther C.A., Alsweiler J., Brown J. Antenatal dietary supplementation with myo-inositol in women during pregnancy for preventing gestational diabetes. Cochrane Database Syst Rev. 2015;2015(12): CD011507. DOI: 10.1002/14651858.CD011507.pub2.
- Monastra G., Unfer V., Harrath A.H., Bizzarri M. Combining Treatment With Myo-Inositol and D-chiro-inositol (40:1) Is Effective in Restoring Ovary Function and Metabolic Balance in PCOS Patients. Gynecol Endocrinol. 2017;33(1):1-9. DOI: 10.1080/09513590.2016.1247797.
- Торшин И.Ю., Громова О. А., Калачева А.Г. и др. Мио-инозитол: микронутриент для «тонкой настройки» женской репродуктивной сферы. РМЖ. Мать и дитя. 2018;1(2):1-7. DOI: 10.32364/2618-8430-2018-1-2-148-155.
- Лапина И.А., Озолиня Л.А., Доброхотова Ю.Э. и др. Комплексная оценка влияния гликозаминогликанов на систему гемостаза у пациенток с синдромом поликистозных яичников. Вопросы гинекологии, акушерства и перинатологии. 2019;5:35-41. DOI: 10.20953/1726-1678-2019-5-35-41.
- Jeanes Y.M., Reeves S. Metabolic consequences of obesity and insulin resistance in polycystic ovary syndrome: diagnostic and methodological challenges. Nutr Res Rev. 2017;30(1):97-105. DOI: 10.1017/ S0954422416000287.
References
- Regidor P.A., Schindler A.E., Lesoine B., Druckman R. Management of women with PCOS using myo-inositol and folic acid. New clinical data and review of the literature. Horm Mol Biol Clin Investig. 2018;34(2). pii: /j/hmbci.2018.34.issue-2/hmbci-2017-0067/hmbci-2017-0067.xml. DOI: 10.1515/hmbci-2017-0067.
- Rotterdam ESHRE/ASRM Sponsored PCOS Consensus Workshop Group. Revised 2003 consensus on diagnostic criteria and long term health risks related to polycystic ovary syndrome (PCOS). Hum Reprod. 2004;19(1):41-47. DOI: 10.1093/humrep/deh098.
- Genazzani A.D. Inositol as putative integrative treatment for PCOS. Reprod Biomed online. 2016;33(6):770-780. DOI: 10.1016/j. rbmo.2016.08.024.
- Pundir J., Psaroudakis D., Savnur P. et al. Inositol treatment of anovulation in women with polycystic ovary syndrome: a meta-analysis of randomised trials. BJOG. 2018;125(3):299-308. DOI: 10.1111/1471-0528.14754.
- Unfer V., Nestler J.E., Kamenov Z.A. et al. Effects of Inositol (s) in Women with PCOS: A Systematic Review of Randomized Controlled Trials. Int J Endocrinol. 2016;2016:1849162. DOI: 10.1155/2016/1849162.
- Crawford T.J., Crowther C.A., Alsweiler J., Brown J. Antenatal dietary supplementation with myo-inositol in women during pregnancy for preventing gestational diabetes. Cochrane Database Syst Rev. 2015;2015(12): CD011507. DOI: 10.1002/14651858.CD011507.pub2.
- Monastra G., Unfer V., Harrath A.H., Bizzarri M. Combining Treatment With Myo-Inositol and D-chiro-inositol (40:1) Is Effective in Restoring Ovary Function and Metabolic Balance in PCOS Patients. Gynecol Endocrinol. 2017;33(1):1-9. DOI: 10.1080/09513590.2016.1247797.
- Torshin I.Yu., Gromova O.A., Kalacheva A.G. et al. Myo-inositol: micronutrient for “fine tuning” of the female reproductive sphere. Russian Journal of Woman and Child Health. 2018;1(2):148-155 (in Russ.). DOI: 10.32364/2618-8430-2018-1-2-148-155.
- Lapina I.A., Ozolinya L.A., Dobrokhotova Yu.E. et al. Complex assessment of the effect of glycosaminoglycans on the system of haemostasis in patients with polycystic ovary syndrome. Gynecology, Obstetrics and Perinatology. 2019;18(5):35-41 (in Russ.). DOI: 10.20953/1726-1678-2019-5-35-41.
- Jeanes Y.M., Reeves S. Metabolic consequences of obesity and insulin resistance in polycystic ovary syndrome: diagnostic and methodological challenges. Nutr Res Rev. 2017;30(1):97-105. DOI: 10.1017/S0954422416000287.
Сведения об авторах:
Доброхотова Юлия Эдуардовна – д.м.н., профессор, заведующая кафедрой акушерства и гинекологии лечебного факультета, ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-7830-2290.
Лапина Ирина Александровна – к.м.н., доцент кафедры акушерства и гинекологии лечебного факультета, ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-2875-6307.
Чирвон Татьяна Геннадьевна – аспирант кафедры акушерства и гинекологии лечебного факультета, ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-8302-7510.
Таранов Владислав Витальевич – клинический ординатор кафедры акушерства и гинекологии лечебного факультета, ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0003-2338-2884.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
About the authors:
Yuliya E. Dobrokhotova – Doct. of Sci. (Med.), Professor, Head of the Department of Obstetrics and Gynecology of Medical Faculty, Pirogov Russian National Research Medical University, 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0002-7830-2290.
Irina A. Lapina – Cand. of Sci. (Med.), associate professor of the Department of Obstetrics and Gynecology of the Medical Faculty, Pirogov Russian National Research Medical University, 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0002-2875-6307.
Tat’yana G. Chirvon – postgraduate student of the Department of Obstetrics and Gynecology of the Medical Faculty, Pirogov Russian National Research Medical University, 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0002-8302-7510.
Vladislav V. Taranov – resident of the Department of Obstetrics and Gynecology of the Medical Faculty, Pirogov Russian National Research Medical University, 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-00032338-2884.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
