 invar.ru
invar.ru

Cредство для естественного восстановления менструального цикла без гормонов
В его состав входит уникальная комбинация мио-инозитола, D-хиро-инозитола, марганца и фолиевой кислоты.
далее...
Заключение совещания экспертов «Обоснование применения средств на основе инозитола у пациенток с нарушениями менструального цикла»
Статьи14 ноября 2019 г. состоялось рабочее совещание экспертов, на котором обсуждались возможности новой биологически активной добавки (БАД) Дикироген® (ИНВАР) в сохранении женского здоровья.
Участники: Воронцова Анна Валерьевна, Гаспарян Сусанна Арташесовна, Громова Ольга Алексеевна, Джобава Элисо Мурмановна, Киселева Елена Юрьевна, Коротких Ирина Николаевна, Кулешов Виталий Михайлович, Обоскалова Татьяна Анатольевна, Пустотина Ольга Анатольевна, Сахаутдинова Индира Венеровна, Спиридонова Наталья Владимировна, Тапильская Наталья Игоревна, Тхостова Елизавета Борисовна
Е.Б. Тхостова. Биологически активные добавки: зачем, кому и почему?
Биологически активные добавки к пище – относительно новое направление в медицине, бурно развивающееся в последние два десятилетия. Существуют достоверно установленные связи между дефицитом определенных биологически активных веществ и риском возникновения той или иной патологии (1).
К БАД в российском медицинском сообществе отношение неоднозначное – от полного неприятия до излишне завышенных ожиданий. Хотя в развитых странах они весьма популярны (биологически активные добавки к пище принимают до 90% жителей Японии, до 80% - США, до 60% - Европы) (2).
Сегодня наше совещание посвящено обсуждению новой биологически активной добавки к пище – Дикироген.
Во многих странах потребление БАД очень распространено. Российская Федерация кардинально отличается по этому показателю: лишь 2-3% употребляют их регулярно и около 20% - от случая к случаю. Биодобавки оказывают более мягкий эффект и не могут заменить лекарственные препараты в лечении заболеваний. Их ценность заключается в способности корригировать недостаточное поступление в организм биологически активных веществ, необходимых для поддержания метаболизма.
Биологически активные добавки к пище (БАД) – концентраты натуральных природных пищевых и биологически активных веществ, выделенных из животного, минерального, растительного сырья, или полученных путем химического синтеза.
Единой классификации БАД не существует. Принято разделять БАД на две большие группы: нутрицевтики и парафармацевтики. Нутрицевтики используются для восполнения необходимых организму веществ, если их поступление с пищей недостаточно. Парафармацевтики более специфичны и способны оказывать влияние на функционирование органов и систем, регуляцию метаболизма; их можно применять как для профилактики, так и в составе комплексной терапии ряда состояний.
Оборот БАД на рынке РФ регулируется законодательством. Все БАД проходят обязательную государственную регистрацию. Требования, предъявляемые к БАД в настоящее время, включают соответствие производства высоким международным стандартам, тщательный контроль качества сырья и готового продукта, соответствие состава современным научным данным. Но, в отличие от лекарственных препаратов, требований обязательного проведения клинических исследований нет. Поэтому наличие таких исследований свидетельствует о высокой ответственности производителя и/или официального представителя БАД.
Дикироген® производится в Италии в соответствии со стандартами ISO (International Standards Organization), соответствует высоким требованиям, предъявляемым к качественным БАД. Он состоит из четырех компонентов: двух основных стереоизомеров инозитола (мио- и D-хиро-инозитола), усиленных фолиевой кислотой и марганцем (табл. 1).
Таблица 1. Химический состав биологически активной добавки к пище Дикироген®
| Биологически активные вещества | Содержание в 1 саше (4 г), не менее |
| Инозитол, мг (суммарно) | 1200 |
| Мио-инозитол, мг | 1000 |
| D-хиро-инозитол, мг | 200 |
| Фолиевая кислота, мкг | 200 |
| Марганец, мг | 5 |
В мировой литературе содержится большое количество исследований, посвященных применению мио- (МИ) и D-хиро-инозитола (ДХИ) и фолиевой кислоты в клинической практике. В частности, известны результаты итальянского рандомизированного плацебоконтролируемого исследования влияния БАД, содержащей мио-инозитол (МИ), ДХИ, фолиевую кислоту и марганец, на метаболические показатели у женщин (3).Высокий потенциал стереоизомеров инозитола в аспекте коррекции патологических состояний репродуктивной сферы вызывает большой интерес научного медицинского сообщества.
О.А. Громова. Инозитол, фолиевая кислота, марганец в фокусе репродуктивного здоровья
В 1848 г. немецким химиком Юлием Либихом из проростков пшеницы выделен инозитол (мио-инозитол). Инозитол - шестиатомный спирт. Он существует в 9 стереоизомерах, из которых в живой клетке преимущественно в форме МИ — более 91%. Содержание ДХИ в сыворотке составляет около 8%, остальных изомеров в сумме — 0,06%. Долгое время эту молекулу относили к витаминам группы В и называли витамином В8. За свойство поддерживать клеточный метаболизм его иногда называют «витамин молодости».
Большая часть инозитола синтезируется в организме. МИ и его производные также содержатся в продуктах питания: фруктах (апельсинах), дынях, бобовых, зерновых, орехах. Снижение поступления экзогенного инозитола может происходить в результате недостаточного потребления этих продуктов, нарушения его всасывания и употребления продуктов, нарушающих всасывание инозитола. Например, растворимый кофе, творог, крепкий алкоголь снижают кишечный биосинтез и всасывание инозитола.
ДХИ содержится в высоких концентрациях в некоторых продуктах — это кэроб (рожковое дерево), тыква фиголистная и хорошо нам известная гречневая крупа. Но его основная часть образуется в организме под действием фермента эпимеразы из МИ. Процесс эпимеризации двусторонний: в зависимости от потребности превращение может идти из МИ в ДХИ или наоборот. Нарушение механизма эпимеризации (МИ в ДХИ) влияет на функциональное состояние процессов, за которые отвечает ДХИ, в частности, на состоянии стероидогенеза.
В результате анализа 44 тыс. публикаций нами установлено, что основной функцией МИ и его производных является участие во внутриклеточной передаче сигнала. Например, сигналов от рецепторов инсулина, о расщеплении жиров, снижении уровня триглицеридов, холестерина в крови и от рецепторов репродуктивных гормонов. Известно 233 белка протеома, принимающих участие в передаче внутриклеточных сигналов посредством производных МИ. Но достоверная информация о специфическом участии в различных физиологических процессах пока имеется только для 120 инозитол-фосфат-зависимых белков .
Практически половина и них вовлечена в поддержание функционирования репродуктивной системы, развития эмбриона, нейропротекции в отношении плода, обеспечение активности сигнальных каскадов инсулина, что указывает на перспективность применения препаратов МИ в репродуктивной медицине.
Инозитолы присутствуют в клетках в свободной форме и в качестве компонентов мембранных фосфоинозитидов, выполняя самые разнообразные функции.
Фосфатидилинозитол является предшественником ряда соединений, которые образуют инозит 1,4,5 трифосфат - вторичный мессенджер мембранных рецепторов, который участвует в сигнальном механизме многих аутокоидов, гормонов и нейротрансмиттеров (4).
И МИ, и ДХИ-фосфоинозитиды способны влиять на внутриклеточные метаболические процессы, активируя ключевые ферменты окислительного и неокислительного метаболизма глюкозы (5, 6). МИ принимает участие в метаболизме, транспорте и расщеплении глюкозы и ее превращении в гликоген (7). ДХИ задействован в передаче сигналов инсулина и стимуляции ферментов, участвующих в регуляции метаболизма глюкозы (например, пируватдегидрогеназа фосфатазы (PDHP), протеинфосфатаза 2C (PP2C), инозитолфосфатгликан) (8) .
Предполагают, что МИ и ДХИ синергично участвуют в метаболизме глюкозы. В частности, МИ усиливает поглощение глюкозы клетками так как индуцирует транслокацию транспортера глюкозы в клеточную мембрану (9, 10). ДХИ стимулирует пируватдегидрогеназу и поддерживает выработку АТФ через цикл Кребса (9). Другими словами, МИ открывает, а ДХИ закрывает так называемое «инсулиновое окно». Более того, некоторые данные указывают на то, что ДХИ-гликаны специфически стимулируют секрецию инсулина в β-клетках поджелудочной железы (11).
Может возникнуть вопрос: если женщина хорошо питается и потребляет достаточное количество продуктов, содержащих инозитол, нужно ли ей принимать его дополнительно в составе БАД?
Традиционно такой пациентке для коррекции инсулинорезистентности назначают метформин. Этот препарат считается «золотым стандартом» в терапии инсулинорезистентности и рассматривается в качестве перспективного геропротектора (12). Как оказалось, метформин работает, используя ресурсы ДХИ, и без того малые у этой категории пациентов. Кроме того, при использовании метформина отмечаются такие явления как лактоацидоз, снижение уровня тестостерона, тиреотропного гормона.
Нами проведено очень интересное исследование, которое показывает, что на фоне приема МИ выравниваются: динамика уровня тестостерона, триглицеридов, инсулина и показатели уровня артериального давления. Динамика концентрации инсулина у пациенток с синдромом поликистозных яичников (СПКЯ) при глюкозотолерантном тесте на фоне приема МИ улучшается.
Концентрация МИ и его производных тканеспецифична. Например, в ногтевой пластинке он почти не определяется, а в фолликулярной жидкости зрелого фолликула к моменту овуляции его содержание очень высоко. Это связано с тем, что производные МИ взаимодействуют со специфическими белками, участвующими в функционировании репродуктивной системы и развитии эмбриона. Повышение концентрации МИ в фолликулярной жидкости в предовуляторном и овуляторном периодах необходимо для созревания фолликулов и является маркером хорошего качества ооцитов (13).
В процессе созревания ооцитов первостепенная роль производных МИ состоит в формировании кальций-опосредованных сигналов от рецептора гонадотропин-рилизинг-гормона (ГнРГ) (14,15), а также подготовки к успешной активации яйцеклетки в момент оплодотворения (16).
Инозитолы и фолаты действуют синергично, и наши исследования показали, что одни и те же белки используют в своей активности МИ и фолаты, в частности, регулирующие метилирование ДНК клеток.
В исследовании с участием 84 матерей, родивших ребенка с расщелиной неба и губы, в сравнении с группой 102 матерей новорожденных без дефектов, отмечены низкие уровни МИ в плазме крови матери (<13,5 мкмоль/л) и цинка в эритроцитах (<189 мкмоль/л). Эти показатели ассоциированы с повышенным риском врожденного порока развития (МИ: ОШ 3,0, 95% ДИ 1,2—7,4; цинк: ОШ 2,0, 95% ДИ 0,8—4,8). Дети с врожденными пороками развития также имели более низкие уровни МИ (<21,5 мкмоль/л) и эритроцитарного цинка (<118 мкмоль/л). Следовательно, совместное назначение активных фолатов и МИ целесообразно для предупреждения фолат-резистентных пороков (17).
Существует множество убедительных публикаций о влиянии инозитола на клинические и лабораторные показатели состояния женщин с СПКЯ. И, по-видимому, нам предстоит узнать и внедрить в клиническую практику еще множество интересных и полезных свойств инозитола и его производных.
Марганец (Mn) - четвертый компонент в составе средства Дикироген®. Какова его роль в организме, почему включение марганца в состав Дикирогена® так ценно?
Прежде всего, марганец входит в состав митохондриальной Mn-содержащей супероксиддисмутазы — фермента, который является мощным антиоксидантом, защищающим митохондрии от избыточного влияния свободных радикалов. Он необходим для роста сосудов, участвует в реализации вазодилатирующего каскада оксида азота (NO). Марганец входит в состав металлоферментов — аргиназы, гуанилат-циклазы, холинэстеразы и других.
Нашей группой выполнено исследование, в котором мы выявили, что железо реализует многие функции при участии Mn-зависимых белков. Марганец участвует в механизмах всасывания железа в кишечнике, утилизации железа в тканях, синтезе гемоглобина, антиоксидантной защите. Назначение только препаратов железа в ситуации дефицита марганца и инозитола не даст эффекта в лечении железодефицитной анемии.
С точки зрения фармакологических свойств марганец в составе средства Дикироген® представлен в форме марганца пидолата, что является оптимальной формой.
В заключение хочу еще раз подчеркнуть, что Дикироген® представляет собой очень интересную и перспективную композицию веществ в оптимальных дозах, которые подобраны с учетом синергизма компонентов, суточной потребности, особенностей кишечного всасывания, характера питания.
Н.И. Тапильская. Как использовать новое средство в клинической практике?
Сегодня у нас появился новый продукт. Какую нишу он должен занять в арсенале акушера-гинеколога? Все это мы сегодня обсуждаем на нашем экспертном совете.
Мне очень нравится, что, во-первых, инозитол хорошо себя зарекомендовал и хорошо изучен, а во-вторых, он безопасен и очень прост в применении. Практически 30% обращений по поводу нарушений менструального цикла на гинекологическом приеме — это пациентки с СПКЯ, а также женщины с ожирением.
Пациенты, которым показано назначение средства Дикироген®:
- планирующие беременность;
- имеющие нарушение менструального цикла в виде олиго- или ановуляции;
- имеющие низкий комплаенс приема комбинированных контрацептивов;
- женщины с синдромом предменструального напряжения (N94.3 по МКБ-10).
Трудно представить, что девушка-подросток, которой показано лечение эстроген-гестагенными препаратами, будет их принимать, если у нее нет выраженной дермопатии, угревой сыпи. В таких случаях также имеются показания к приему средства Дикироген®.
Давайте вдумаемся в эти цифры, коллеги: у каждой десятой женщины репродуктивного возраста есть СПКЯ, но каждой седьмой из их числа диагноз не устанавливается. СПКЯ идет под знаком нарушения менструального цикла, назначается лечение. Но желанная беременность так и не наступает. Почему? У пациентки попросту нет овуляции. Диагноз СПКЯ распространяется на возрастные категории и взрослых, и детей.
Метаанализ, включающий 266 исследований, показал, что у девочек-подростков с СПКЯ риск развития метаболического синдрома повышается в 2,7 раза и достигает 43,6%. В 5 раз чаще по сравнению с группой контроля встречается высокий уровень систолического и в 3,5 раза чаще — диастолического артериального давления. В 4,2 раза чаще отмечается повышенный уровень триглицеридов, в 5,3 раза чаще — центральное ожирение, в 1,3 раза чаще — повышенный уровень глюкозы натощак (18). Из-за небольшого размера изученных популяций и того факта, что часто несколько генов одновременно участвуют в патогенезе СПКЯ, генетическая основа этой патологии остается в значительной степени неизученной (19,20). Среди генетических причин указаны мутации в генах, участвующих в синтезе, транспорте и регуляции андрогенов (20), мутации в генах, регулирующих передачу сигналов гонадотропина, активацию фосфатидилинозитол-3-киназы (PI3-киназы), экспрессию транспортера глюкозы 4 (GLUT4) (21, 22, 23). Вот это — точки приложения МИ и ДХИ.
СПКЯ принято рассматривать как репродуктивный метаболический синдром, который представляет собой своеобразный образец смены парадигмы здоровья женщины. В молодости ее беспокоят нарушения менструального цикла, а затем начинает повышаться риск развития сердечно-сосудистых заболеваний, сахарного диабета 2-го типа, ожирения и рака эндометрия. Это тоже представляет собой одну из существенных ниш, которые может занять Дикироген® для применения с целью профилактики.
В настоящее время, наряду с Роттердамскими критериями, в диагностике применяется определение фенотипов СПКЯ, регламентированное в новых клинических рекомендациях (рис. 1).
 Рис. 1. Определение фенотипов синдрома поликистозных яичников, регламентированное в клинических рекомендациях.
Рис. 1. Определение фенотипов синдрома поликистозных яичников, регламентированное в клинических рекомендациях.
В фенотипах преобладают гиперандрогения, ожирение и инсулинорезистентность. Фенотип не является постоянным, он может меняться в течение жизни. Например, в стрессовой ситуации, при наборе веса женщина может переходить из легкого андрогенного избытка в тяжелый со всеми вытекающими отсюда последствиями.
В патогенезе СПКЯ ведущим триггером является инсулинорезистентность, вследствие чего происходят: повышение уровня лютеинизирующего гормона (ЛГ) и гиперсекреция андрогенов в яичниках, снижение уровня глобулина, связывающего половые стероиды, в надпочечниках повышение уровня фермента Р450с-17-гидроксилазы. Механизм активации этого фермента на сегодняшний день окончательно не выяснен. Но следствием является формирование СПКЯ.
Повышенный уровень циркулирующего инсулина у женщин с СПКЯ, наряду с высоким уровнем ЛГ, может остановить рост фолликулов, (23, 24). Гиперсекреция ЛГ у этих женщин может также приводить к ранней лютеинизации клеток гранулезы и раннему прекращению развития антрального фолликула (25, 26, 27). Более того, ЛГ может активировать преждевременные мейотические процессы, которые ухудшают качество ооцитов, тем самым способствуя эмбриональной анеуплоидии (28). Гиперинсулинемия приводит к изменению секреции ГнРГ и к ингибированию печеночного синтеза глобулина, связывающего половые гормоны (ГСПГ), что вызывает увеличение концентрации циркулирующих свободных андрогенов (29). Гиперандрогению могут вызывать и другие факторы, такие как избыток синтеза андрогенов в надпочечниках и наличие ферментативных дефектов яичникового и надпочечникового стероидогенеза (рис. 2) (30).
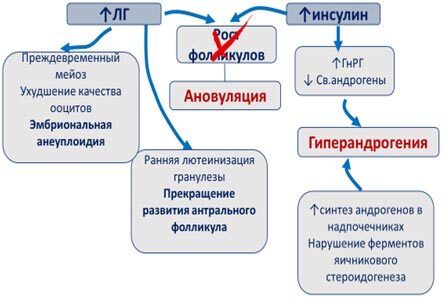 Рис. 2. Роль гиперинсулинемии и лютеинизирующего гормона в патогенезе синдрома поликистозных яичников (40).
Рис. 2. Роль гиперинсулинемии и лютеинизирующего гормона в патогенезе синдрома поликистозных яичников (40).
Ключевым нарушением действия инсулина на молекулярно-биологическом уровне считается пострецепторный дефект начальных этапов сигнальной трансдукции. При СПКЯ наблюдаются нарушения продукции мембранных переносчиков глюкозы, а также регуляции липогенеза. МИ и ДХИ, будучи медиаторами передачи клеточного сигнала, выступают регуляторами этих нарушений.
Еще одна большая группа пациентов — это женщины с ожирением. Установлено большое количество генов, ответственных за реализацию хронического рецидивирующего заболевания, которым является ожирение, хотя их роль до конца неизвестна. Но понимание механизмов влияния ожирения на репродуктивную систему хорошо изучено и отнесено к наиболее важным результатам развития репродуктологии в прошлом десятилетии.
В частности, сегодня у пациенток с ожирением активно изучается корреляция плохого качества ооцитов и митохондриальной недостаточности. В этом аспекте композиция, содержащая два изомера инозитола — МИ и ДХИ, и марганец, которые корригируют митохондриальную недостаточность, является очень актуальной, в том числе у женщин позднего репродуктивного возраста. Патогенез эндокринных нарушений при ожирении во многом схож с рассмотренным ранее, но в данной ситуации присоединяется еще и гиперлептинемия.
Лептин является цитокиновым рецептором группы факторов некроза опухоли и действует на отдельные трансмембранные рецепторы цитокинов, называемые рецепторами лептина, и участвует в следующих процессах:
- регуляция потребления пищи и энергетического баланса путем воздействия на центры гипоталамуса;
- регуляция овариального фолликулогенеза;
- стимуляция секреции ГнРГ из гипоталамуса, фолликулостимулирующего гормона (ФСГ) и ЛГ из гипофиза;
- повышение чувствительности к инсулину путем воздействия на секрецию β-клеточного инсулина;
- стимуляция активного транспорта глюкозы и синтеза гликогена;
- регуляция метаболизма жирных кислот;
- регуляция многих эндокринных функций, воспаления, иммунного ответа и ангиогенеза.
Лептин имеет очень узкое пороговое окно: снижение и повышение его уровня одинаково неблагоприятно. Почему? Потому что приводит к нарушению пульсирующей секреции ГнРГ с подавлением стероидогенеза яичников и нарушением ароматизации андрогенов в эстрогены в тека-клетках. Как следствие — нарушение репродуктивной функции. К этому добавляется активность ароматаз в жировой ткани, образование катехолэстрогенов, и в итоге — повышение риска развития рака эндометрия и рака молочной железы.
Лептин — цитокин, ключевой медиатор жировой ткани. Чем больше адипоцит по размеру и чем больше пролиферация адипоцитов, тем интенсивнее выработка провоспалительных цитокинов, в частности, продукция лептина, который регулируется и половыми стероидами, и тестостероном. Образуется порочный круг: избыточная продукция андрогенов, периферическая конверсия в клетках жировой ткани, повышение продукции лептина. Круг замкнулся: происходит нарушение овуляции и репродуктивной функции.
При ожирении соотношение эстрон/эстрадиол меняется в сторону повышения уровня эстрона, что предрасполагает к нарушению нормального функционирования механизма обратной связи. Гиперэстрогенемия сенсибилизирует гонадотрофы гипофиза к ГнРГ и снижает пороговый уровень овариального эстрадиола, необходимый для начала овуляторного подъема ЛГ. Гиперстимуляция незрелых фолликулов, вероятно, лежит в основе их кистозного перерождения.
Приведу довольно типичный пример из клинической практики гинеколога. Пациентка с СПКЯ, у которой имеются гиперандрогенемия, олиго- или ановуляция, поликистозная морфология яичников по данным ультразвукового исследования, ожирение II степени, нарушение толерантности к глюкозе и артериальная гипертензия I степени. Метформин может переносить плохо. На более дорогие методы денег нет. Гормональные контрацептивы противопоказаны. Думаю, что это как раз тот случай, когда будет рационально и безопасно рекомендовать ей Дикироген®.
Еще один клинический пример. Пациентка с ожирением, признаками гиперандрогении и гирсутизмом, гипертриглицеридемией, нарушением толерантности к глюкозе. Обратилась в связи с планированием беременности. Назначен прием Дикироген® с целью снижения веса в течение 3 мес. Отметим, что нормализация веса особенно важна, так как наличие ожирения у матери увеличивает относительный риск появления у плода таких пороков развития как:
- анэнцефалия;
- незаращение дужки позвонка (spina bifida);
- патология сердечной перегородки;
- расщелина губы и неба;
- гидроцефалия (31)
Применение средства Дикироген® показано на протяжении не менее 3 мес до планируемой беременности. Сочетание МИ, ДХИ и фолиевой кислоты в данном контексте очень удачно.
Следует учитывать вероятность вовлечения в описанные процессы стволовых клеток жировой ткани, которые способствуют поддержанию микроокружения опухоли (32). Устранение инсулинорезистентности при помощи инозитола прерывает патологическую цепочку избыточной эстроген-стимуляции эндометрия. Если говорить о клинических подходах к ведению пациенток с СПКЯ, при котором инсулинорезистентность и компенсаторно формирующаяся гиперинсулинемия являются ключевыми факторами, то применение МИ и ДХИ оказывает многокомпонентное действие, позволяя преодолеть инсулинорезистентность, снижая уровень андрогенов, улучшая качество ооцитов.
В протоколах экстракорпорального оплодотворения (ЭКО), особенно у пациенток старшей возрастной группы, мы обязательно включаем МИ на этапе прегравидарной подготовки с целью улучшения качества ооцитов.
По моему мнению, в скором времени в клинических рекомендациях этот аспект будет обязательно отражен, потому что накапливаются данные клинических исследований об обоснованности такого подхода.
В яичниках, в отличие от остальных тканей, резистентность к инсулину отсутствует, но при СПКЯ присутствует гиперандрогения, которая приводит к атрезии антральных фолликулов со всеми вытекающими отсюда последствиями. Здесь функция инозитола состоит в снижении гиперандрогении и устранении митохондриальной дисфункции. Отношение МИ/ДХИ определяется потребностью тканей и обусловлено ферментативной конверсией МИ в ДХИ, контролируемой NAD-NADH-зависимой эпимеразой.
Как показало плацебо-контролируемое исследование, на фоне 8-недельного приема ДХИ у женщин с СПКЯ произошло восстановление овуляции в 86% по сравнению с 27% в группе плацебо, р<0,001 (33).
Мета-анализ, включивший 6 исследований из 109 проанализированных публикаций, показал сопоставимую эффективность инозитола и метформина в нормализации углеводного обмена, снижении уровня андрогенов и ГСПГ. При применении метформина отмечалось в 5 раз больше побочных эффектов с более выраженными проявлениями: тошнота, диарея, лактоацидоз, общая слабость, боли в животе. Напротив, при приеме МИ— легкая тошнота, диарея, не требующие отмены препарата (34).
Мой опыт применения инозитола с целью восстановления овуляции также свидетельствует о хорошем эффекте. Восстанавливается овуляция, наступает беременность. Но я назначала инозитол для приема в течение не одного месяца, а восьми месяцев. Думаю, что оптимальный срок назначения должен составлять не менее 3 мес.
Приведу еще один пример. Пациентка с СПКЯ обратилась по поводу проведения ЭКО. Но я, как специалист, считаю, что данной пациентке с СПКЯ не показано ЭКО, ей необходимо улучшать качество ооцитов. Почему? Потому что, когда мы получаем 30 ооцитов при стимуляции суперовуляции, яйцеклетки, как правило, плохого качества и всего 1—2 эмбриона готовы к переносу, а еще есть риск получения анеуплоидного эмбриона. Таким образом, инозитол на сегодняшний день рассматривают, как одно из возможных потенциальных средств восстановления менструального цикла и овуляции. В недавних Клинических рекомендациях указано, что «инозитол (в любой форме) в настоящее время следует рассматривать как экспериментальную терапию при СПКЯ, и все новые данные об эффективности указывают на необходимость дальнейших исследований» (35).
Э.М. Джобава. Применение средства Дикироген® — пример реализации принципов персонализированной медицины
Хотелось бы поделиться мнением о модели медицины, отличной от привычной классической, — о персонализированной медицине. Персонализированная медицина — новая организационная модель, основанная на подборе индивидуальных лечебных, диагностических и профилактических методов, оптимально подходящих биохимическим, физиологическим и генетическим особенностям организма.
Целью этой модели является улучшение качества медицинской помощи.
В персонализированной медицине используется синдромальный подход, включающий в себя досимптоматическую идентификацию предрасположенности к развитию заболевания, разработку комплекса профилактических мер и подбор индивидуальных схем лечения на основе индивидуальных свойств генома, особенностей его реализации и специфики метаболизма у отдельного пациента.
Осознанное планирование беременности, прегравидарная подготовка под руководством специалиста отвечают принципам персонализированной медицины. Репродуктивный потенциал пары зависит от сочетания различных факторов, таких как возраст, образ жизни, наследственность, гормональный баланс, метаболомный баланс, инфекционный статус.
Научное сообщество убеждено в том, что весь континуум от преконцепционного периода до событий во время беременности, в частности нарушение питания, может повлиять на общий исход беременности и заложить у ребенка потенциальную основу развития заболеваний во взрослом возрасте путем программирования патофизиологии послеродового периода.
При условии соблюдения таких простых условий как: отказ от кофе, курения, алкоголя, умеренные физические нагрузки, нормализация массы тела, нормализация питьевого режима, сон не менее 7—8 ч в сутки, индивидуальная нутриентная программа поддержки, на 75% повышается вероятность наступления беременности и на 65% — шансы успешного вынашивания.
Большое внимание уделяется микробиоте как основе всех биохимических процессов в организме. На недавнем конгрессе о микробиоте в акушерской практике звучали сообщения о том, что от состояния микробиологического состава кишечника матери в значительной степени зависит развитие плода. Представлены очень интересные доклады о переносе ДНК яйцеклетки возрастной женщины в яйцеклетку молодой женщины с сохранением качества митохондрий. Это важно, потому что потом, после рождения ребенка, мы уже не в силах поменять качество митохондрий и устранить митохондриальную дисфункцию, если она имеется. Это еще раз доказывает важность планирования беременности и прегравидарной подготовки. Доказано также, что 80% микробиоты ребенка формируется на этапе беременности и только 20% в постнатальном периоде.
Все это говорит о том, насколько важно к планированию беременности относиться осознанно, корригируя возможные проблемы со здоровьем родителей, которые могут повлиять на формирование будущего ребенка. Используя синдромальный подход к диагностике, можно выделить ведущие симптомокомплексы со стороны женщины и мужчины (табл. 2).
Таблица 2. Ведущие симптомокомплексы со стороны женщины и мужчины, которые необходимо учитывать на этапе планирования беременности и прегравидарной подготовки
| Женщина | Мужчина |
| • Синдром доминирования эстрогенов
• Синдром истощения надпочечников • Синдром нарушенной кишечной проницаемости • Синдром инсулинорезистентности и гиперинсулинемии • Синдром снижения овариального резерва • Синдром гиперандрогении • Синдром хронического воспаления • Окислительный стресс • Дисфункция митохондрий |
• Синдром дефицита тестостерона
• Синдром истощения надпочечников • Синдром дефицита соматотропного гормона • Синдром нарушенной кишечной проницаемости • Синдром инсулинорезистентности и гиперинсулинемии • Синдром хронического воспаления • Окислительный стресс • Дисфункция митохондрий |
Основные направления нутрицевтической персонализированной стратегии в сохранении и повышении репродуктивного потенциала пары состоят в применении адаптогенов, антиоксидантов, антиандрогенов (для женщин), активаторов митохондрий, регуляторов баланса эстрогенов (для женщин), в нормализации углеводного обмена, аппетита, в назначении витаминов группы В, включая инозитол, минералов (магния, марганца, цинка, селена, хрома, меди), мелатонина, жирных кислот.
В многочисленных «естественных мерах», направленных на оптимизацию преконцепционного состояния здоровья матери и метаболического баланса, диетические добавки инозитола получили сильные и хорошо подтвержденные доказательства относительно положительного эффекта в улучшении глюкозного и липидного профилей у женщин с СПКЯ (36).
Хорошо известно, что МИ оказывает воздействие на функционирование сперматозоидов, регулируя осмолярность и объем семенной плазмы, экспрессию белков, необходимых для эмбриогенетического развития, и подвижность сперматозоидов. Достаточные концентрации МИ в питательной среде культуры клеток значительно увеличивают процент подвижных сперматозоидов как у здоровых людей, так и у пациентов с олигоастенотератозооспермией. Улучшение подвижности сперматозоидов обусловлено значительным увеличением митохондриального мембранного потенциала (37).
В открытом, проспективном, обсервационном исследовании с участием 3602 бесплодных женщин изучалось влияние МИ и фолиевой кислоты (прием в течение 2 мес) на качество ооцитов, скорость оплодотворения и качество эмбрионов у пациенток с СПКЯ. У 70% женщин восстановлена овуляция, у 15% (545) наступила беременность.
В рамках исследования выделена подгруппа женщин, которым проведен протокол ЭКО. Женщины группы А (n=14) получали МИ в сочетании с фолиевой кислотой, женщины группы B (n=15) — фолиевую кислоту и плацебо. У женщин группы А после 12-недельного курса МИ в сочетании с фолиевой кислотой уровень тестостерона уменьшился с 96,6 до 43,3 нг/мл, а прогестерона — увеличился с 2,1 до 12,3 нг/мл в среднем (p<0,05). Побочных эффектов у пациенток не было. Согласно полученным результатам, соотношение фолликул/извлеченный ооцит было явно лучше в группе МИ по сравнению с контрольной группой. Оплодотворено 58,4% (136 из 233) ооцитов, собранных в группе МИ, тогда как в группе плацебо оплодотворено только 43,6% (128 из 300) ооцитов. Качество ооцитов было лучше в группе МИ. По сравнению с группой, получавшей плацебо, извлечено больше метафаз II и I ооцитов по отношению к общему количеству ооцитов. В группе МИ отмечено больше эмбрионов I степени качества, чем в группе плацебо. Продолжительность стимуляции составила 9,7 дня (±3,3) у пациенток группы МИ и 11,2 (±1,8) дня — у пациенток группы плацебо, а количество использованных единиц ФСГ было ниже в группе МИ по сравнению с группой плацебо: 1750 ед. ФСГ в среднем по сравнению с 1850 ед. в контроле. Таким образом, МИ открывает оптимистичные перспективы лечения для пациенток с СПКЯ и бесплодием с точки зрения как эффективности, так и благоприятного профиля безопасности. Поскольку количество извлеченных ооцитов было меньше в группе МИ, можно предполагать, что риск синдрома гиперстимуляции у этих пациенток может быть снижен. Следовательно, прием МИ также перспективен в улучшении результатов ЭКО для пациенток с СПКЯ (38).
По данным проспективного рандомизированного исследования, целью которого было определить влияние МИ на качество ооцитов у пациенток с СПКЯ, проходящих циклы интрацитоплазматической инъекции сперматозоидов (ИКСИ), одна группа пациенток принимала МИ в сочетании с фолиевой кислотой, а другая — только фолиевую кислоту. У пациенток с СПКЯ применение комбинации МИ и фолиевой кислоты эффективнее, чем прием только фолиевой кислоты, уменьшало количество зародышевых пузырьков и дегенерированных ооцитов при получении яйцеклетки без ущерба для общего количества извлеченных ооцитов.
Этот подход, снижающий уровень эстрадиола при введении хорионического гонадотропина, по мнению авторов, может быть принят для снижения риска гиперстимуляции яичников у таких пациенток (13).
Сегодня уже отмечалось, что нарушение регуляции пути инозитола во время беременности может быть связано с фолат-резистентными дефектами нервной трубки эмбриона (ДНТ), которые представляют примерно 30% всех случаев этого порока развития с неясным патогенезом, возникающим в раннем эмбриогенезе, несмотря на правильное введение фолиевой кислоты в преконцепционном периоде. ДХИ оказался эффективнее в уменьшении ДНТ по сравнению с МИ (36). Получены превосходные результаты при назначении инозитола в преконцепционном периоде и во время беременности (15 из 17 беременностей) у 12 пар с повышенным риском фолат-резистентного ДНТ (39).
В заключение хочу еще раз подчеркнуть, что Дикироген® — это оптимальная комбинация двух изомеров инозитола, фолиевой кислоты и марганца, в которой учтены современные требования к биологически активным добавкам, и поэтому его можно считать эффективным дополнительным средством поддержания репродуктивного здоровья женщин.
А.В. Воронцова, Т.А. Обоскалова. Предварительные результаты апробации средства Дикироген® у пациенток с гиперандрогенией
В нашем центре проходит открытое проспективное исследование эффективности средства Дикироген® у пациенток с НМЦ на фоне СПКЯ. Цель исследования — изучить влияние Дикирогена® на состояние и гормональный статус женщин с гиперандрогенией.
Планируется включить в исследование 100 женщин с установленным диагнозом СПКЯ. Срок наблюдения 6 мес. Все женщины получают Дикироген® в режиме 2 саше в день в течение 24 нед.
К настоящему времени исследование закончили 37 пациенток. Поэтому проводить полноценный статистический анализ преждевременно, и мы можем представить только промежуточные данные.
Среди пациенток, закончивших исследование, доля женщин с нормальной длительностью МЦ увеличилась с 31% до 43% через 3 мес. и у 60% пациенток через 6 мес. (рис. 3). Положительный эффект в отношении кожных проявлений проявился к 3-му месяцу и продолжал нарастать к 6-му месяцу. У 25% больных отмечено полное исчезновение акне, а у 75% снизилась выраженность высыпаний. К концу наблюдения более чем у 40% женщин кожные высыпания исчезли полностью (рис. 4). У всех женщин отмечено более стабильное настроение. Из нежелательных явлений выявлена аллергическая реакция в виде кожного зуда у женщины, имевшей ранее подобную реакцию на поливитаминно-минеральный комплекс.
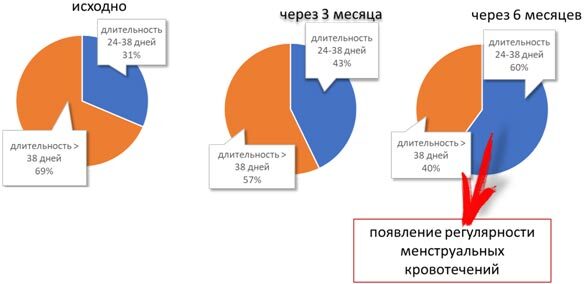 Рис. 3. Параметры менструального цикла на фоне приема средства Дикироген®
Рис. 3. Параметры менструального цикла на фоне приема средства Дикироген®
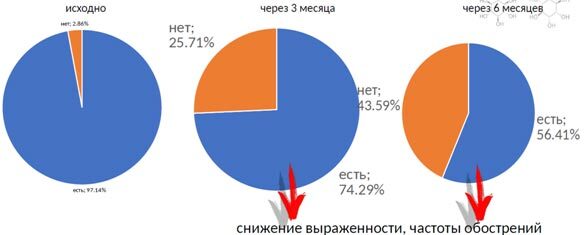 Рис. 4. Положительная динамика в отношении кожных проявлений у обследованных женщин на фоне приема средства Дикироген®
Рис. 4. Положительная динамика в отношении кожных проявлений у обследованных женщин на фоне приема средства Дикироген®
Таким образом, предварительные результаты исследования позволяют сделать заключение о положительном влиянии средства Дикироген® на параметры менструального цикла, выраженность кожных проявлений гиперандрогении, а также о благоприятном профиле безопасности.
Заключение
Дикироген® представляет собой оптимальную комбинацию двух изомеров инозитола, фолиевой кислоты и марганца, в которой учтены современные требования к биологически активным добавкам к пище. Вследствие этого Дикироген® будет эффективным дополнительным средством поддержания репродуктивного здоровья женщин.
По результатам совета экспертов рекомендуется:
- применять биологически активную добавку к пище Дикироген в составе комплексной терапии СПКЯ и нарушений менструального цикла;
- подготовить систематический обзор публикаций, характеризующих эффекты мио- и D-хиро-инозитола, марганца и фолиевой кислоты у пациенток с нарушениями менструального цикла, в том числе при подготовке к беременности;
- опубликовать данные наблюдательного исследования с использованием средства Дикироген в составе комплексной терапии пациенток с гиперандрогенией после его завершения.
Литература/References
1. Регистр Лекарственных Средств России, Москва, 2002
2. https://www.kp.ru/daily/24113/336580
3. Gerli S, Papaleo E, Ferrari A, Di Renzo GC. Randomized, double blind placebo-controlled trial: effects of myo-inositol on ovarian function and metabolic factors in women with PCOS. Eur Rev Med Pharmacol Sci. 2007;11(5):347–354.
4. Di Paolo G, De Camilli P. Phosphoinositides in cell regulation and membrane dynamics. Nature. 2006;443(7112):651–657. doi:10.1038/nature05185
5. Larner J, et al. Rat liver insulin mediator which stimulates pyruvate dehydrogenase phosphate contains galactosamine and D-chiroinositol. Biochem Biophys Res Commun. 1988;151:1416–26.
6. Lauretta R, Lanzolla G, Vici P, Mariani L, Moretti C, Appetecchia M. Insulin-Sensitizers, Polycystic Ovary Syndrome and Gynaecological Cancer Risk. Int J Endocrinol. 2016;2016:8671762. doi: 10.1155/2016/8671762. Epub 2016 Sep 20. PMID: 27725832; PMCID: PMC5048026.
7. Croze ML, Soulage CO. Potential role and therapeutic interests of myo-inositol in metabolic diseases. Biochimie. 2013;95(10):1811–1827. doi:10.1016/j.biochi.2013.05.011
8. Sun TH, Heimark DB, Nguygen T, Nadler JL, Larner J. Both myo-inositol to chiro-inositol epimerase activities and chiro-inositol to myo-inositol ratios are decreased in tissues of GK type 2 diabetic rats compared to Wistar controls. Biochem Biophys Res Commun. 2002;293(3):1092–1098. doi:10.1016/S0006-291X(02)00313-3
9. Yap A, Nishiumi S, Yoshida K, Ashida H. Rat L6 myotubes as an in vitro model system to study GLUT4-dependent glucose uptake stimulated by inositol derivatives. Cytotechnology. 2007 Dec;55(2-3):103-8. doi: 10.1007/s10616-007-9107-y. Epub 2007 Oct 31. PMID: 19002999; PMCID: PMC2104555.
10. Dang NT, Mukai R, Yoshida K, Ashida H. D-pinitol and myo-inositol stimulate translocation of glucose transporter 4 in skeletal muscle of C57BL/6 mice. Biosci Biotechnol Biochem. 2010;74(5):1062–1067. doi:10.1271/bbb.90963
11. Громова О.А., Торшин И.Ю., Лиманова О.А. Перспективы использования мио-инозитола у женщин с поликистозом яичников и инсулинорезистентностью в программах прегравидарной подготовки к экстракорпоральному оплодотворению. Эффективная фармакотерапия. 2013;51:12–23.
12. Гуляев А.Е., Нургожин Т.С., Ермекбаева Б.А., Кушугулова А.Р., Жаугашева С.К., Супиев А.Т., Кенесары А.У., Нургожина Э.Б. Метформин как перспективный геропротектор (обзор литературы). Русский медицинский журнал. 2011;19(31):1986-1989.
Gulyaev AE, Nurgozhin TS, Yermekbayeva BA, Kushugulova AR, Zhaugasheva SK, Supiev AT, Kenesary AU, Nurgozhina EB. Metformin as a promising geroprotector (literature review). Russkii meditsinskii zhurnal. 2011;19(31):1986-1989. (In Russ.).
13. Papaleo E, Unfer V, Baillargeon JP, Chiu TT. Contribution of myo-inositol to reproduction. Eur J Obstet Gynecol Reprod Biol 2009; 147 (2): 120–3
14. Berridge MJ. Inositol trisphosphate and calcium signalling. Nature1993; 361 (6410): 315–25
15. Tesarik J, Sousa M. Mechanism of calcium oscillations in human oocytes: a two-store model. Mol Hum Reprod 1996; 2 (6): 383–6.
16. Goud PT, Goud AP, Leybaert L et al. Inositol 1, 4, 5-trisphosphate receptor function in human oocytes: calcium responses and oocyte activation related phenomena induced by photolytic release of InsP (3) are blocked by a specific antibody to the type I receptor. Mol Hum Reprod 2002; 8 (10):912–8
17. Cavalli P, Copp AJ. Inositol and folate resistant neural tube defects. J Med Genet. 2002 Feb;39(2):E5
18. Fazleen N.E., Whittaker M., Mamun A. Risk of metabolic syndrome in adolescents with polycystic ovarian syndrome: A systematic review and meta-analysis. Diabetes Metab Syndr. 2018
19. Franks S., Gharani N., Waterworth D., Batty S., White D., Williamson R., et al. The genetic basis of polycystic ovary syndrome. Hum. Reprod. 12 1997б2641–2648. 10.1093/humrep/12.12.264,
20. Urbanek M. The genetics of the polycystic ovary syndrome. Nat. Clin. Pract. Endocrinol. Metab. 3 2007,103–111. 10.1038/ncpendmet0400
21. Chen Z. J., Zhao H., He L., Shi Y., Qin Y., Shi Y., et al. (2011). Genome-wide association study identifies susceptibility loci for polycystic ovary syndrome on chromosome 2p16.3, 2p21 and 9q33.3. Nat. Genet. 43 55–59. 10.1038/ng.732
22. Du J., Wang J., Sun X., Xu X., Zhang F., Wang B., et al. (2014). Family-based analysis of INSR polymorphisms in Chinese PCOS. Reprod. Biomed. 29 239–244. 10.1016/j.rbmo.2014.03.028
23. De Leo V., Musacchio M. C., Cappelli V., Massaro M. G., Morgante G., Petraglia F. (2016). Genetic, hormonal and metabolic aspects of PCOS: an update. Reprod. Biol. Endocrinol. 14 38 10.1186/s12958-016-0173-x
24. El Hayek S., Bitar L., Hamdar L. H., Mirza F. G., Daoud G. (2016). Poly cystic ovarian syndrome: an updated overview. Front. Physiol. 7:124 10.3389/fphys.2016.00124
25. Piouka A., Farmakiotis D., Katsikis I., Macut D., Gerou S., Panidis D. (2009). Anti-mullerian hormone levels reflect severity of PCOS but are negatively influenced by obesity: relationship with increased luteinizing hormone levels. Am. J. Physiol. Endocrinol. Metab. 296 E238–E243. 10.1152/ajpendo.90684.2008
26. Liu N., Ma Y., Wang S., Zhang X., Zhang Q., Zhang X., et al. (2012). Association of the genetic variants of luteinizing hormone, luteinizing hormone receptor and polycystic ovary syndrome. Reprod. Biol. Endocrinol. 10:36 10.1186/1477-7827-10-36
27. Cadagan D., Khan R., Amer S. (2016). Thecal cell sensitivity to luteinizing hormone and insulin in polycystic ovarian syndrome. Reprod. Biol. 16 53–60. 10.1016/j.repbio.2015.12.006
28. Qiao J., Feng H. L. (2011). Extra- and intra-ovarian factors in polycystic ovary syndrome: impact on oocyte maturation and embryo developmental competence. Hum. Reprod. Update 17 17–33. 10.1093/humupd/dmq032
29. Toprak S., Yönem A., Akir B. C., Güler S., Azal O., Ozata M., et al. (2001). Insulin resistance in nonobese patients with polycystic ovary syndrome. Horm. Res. 55 65–70. 10.1159/000049972
30. Genazzani A. D., Prati A., Santagni S., Ricchieri F., Chierchia E., Rattighieri E., et al. (2012). Differential insulin response to myo-inositol administration in obese polycystic ovary syndrome patients. Gynecol. Endocrinol. 28 969–973. 10.3109/09513590.2012.685205
31. Sutton L.N. Fetal surgery for neural tube defects Best Practice & Research Clinical Obstetrics and Gynecology (2014) 1-9
32. Schmandt. Obesity and endometrial cancer risk. Am J Obstet Gynecol 2011
33. Nestler et al OVULATORY AND METABOLIC EFFECTS OF D-CHIRO-INOSITOL IN THE POLYCYSTIC OVARY SYNDROME N Engl J Med 1999;340:1314-20
34. F. Facchinetti, B. Orrù, G.Grandi , V. Unfer Short-term effects of metformin and myo-inositol in women with polycystic ovarian syndrome (PCOS): a meta-analysis of randomized clinical trials, Gynecological Endocrinology. Jan 2019
35. Teede, H. J., Misso, M. L., Costello, M. F., Dokras, A., Laven, J., Moran, L., … Azziz, R. (2018). Recommendations from the international evidence-based guideline for the assessment and management of polycystic ovary syndrome. Fertility and Sterility, 110(3), 364–379. doi:10.1016/j.fertnstert.2018.05.004
36. M. Noventa et al., Preventive and Therapeutic Role of Dietary Inositol Supplementation in Periconceptional Period and During Pregnancy: A Summary of Evidences and Future Applications PENNSYLVANIA STATE UNIV September 17, 2016
37. Scarselli F. et al. Analysis of MYO-Inositol effect on spermatozoa motility, in hyper viscous ejaculates and in patients with grades II and III varicocele. Arch Ital Urol Androl. 2016 Dec 30;88(4):279-283. doi: 10.4081/aiua.2016.4.279
38. PA.Regidor Management of women with PCOS using myo-inositol and folic acid. New clinical data and review of the literature Hormone Molecular Biology and Clinical Investigation. 2018; 20170067
39. P Cavalli, A J Copp Inositol and folate resistant neural tube defects J Med Genet 2002;39:e5 (http://www.jmedgenet.com/cgi/content/full/39/2/e5)
40. Sortino MA, Salomone S, Carruba MO, Drago F. Polycystic Ovary Syndrome: Insights into the Therapeutic Approach with Inositols. Frontiers in Farmacology. 2017;8:341.
https://doi.org/10.3389/fphar.2017.00341
