Кальшейк: Клинико-фармакологические аспекты применения
Статьи Опубликовано в :«Научный информационный бюллетень продукта энтерального питания»
Предыдущий раздел | Оглавление | Список литературы
3. Клинико-фармакологические аспекты применения Кальшейка
3.1. Принципы нутритивной терапии больных муковисцидозом.
Нутритивный статус и выживаемость больных муковисцидозом.
А.В.Черняк, Е.Л.Амелина, А.Г.Чучалин.
Сб. статей и тезисов 6-го национального Конгресса по муковисцидозу, 2003, СПб., с.58.
Нутритивный статус (массо-ростовой индекс), как и показатели функции внешнего дыхания (ОФВ1), является значимым прогностическим критерием выживаемости у взрослых больных муковисцидозом. Однако нутритивный статус больных муковисцидозом также оказывает влияние на степень тяжести заболевания.
Выводы: 1. Измерение массо-ростового индекса является необходимой и обязательной процедурой у больных муковисцидозом для адекватной оценки степени тяжести заболевания. 2. Нутритивный статус (массо-ростовой индекс), как и показатели функции внешнего дыхания (ОФВ1) является значимым прогностическим критерием выживаемости у взрослых больных муковисцидозом.
Питание пациентов с цистическим фиброзом (муковисцидозом). Европейский консенсус. 2002 Sinaasappel M, Stern M, Littlewood J, Wolfe S, Steinkamp G, Heijerman H, Robberecht E, Doring G. Nutrition in patients with cystic fibrosis: a European Consensus. J Cyst Fibros 2002; 1:51-75.
Основные Положения Европейского Консенсуса:
Муковисцидоз (цистический фиброз) – МВ - орфанное генетическое заболевание, наблюдаемое у 1 из 2500 родившихся ребенка. При этом заболевании наблюдается нарушение транспорта воды и электролитов в легких, ЖКТ, репродуктивных органах и железах, с развитием недостаточности соответствующих органов.
Нутритивная недостаточность при МВ проявляется задержкой роста и развития, недостаточным функционированием практически всех органов и систем. Энергетическая недостаточность обусловлена плохим всасыванием нутриентов в кишечнике из-за снижения функции поджелудочной железы и воспаления. Развивается дефицит жирорастворимых витаминов, незаменимых жирных кислот, субклинический дефицит селена и цинка.
Предотвращение нутритивной недостаточности требует следующих мер: неонатальный скрининг малнутриции; при недостаточности роста ребенка или неудовлетворительного нутритивного статуса – назначение диеты, обеспечивающей превышение минимум на 20% рекомендованной для данного возраста суточной потребности в энергии, за счет дополнительных высокоэнергетических пищевых добавок (смесей) или даже энтерального зондового питания.
Лечение взрослых пациентов с МВ преследует цель увеличения линейной (тощей) массы тела. На первом этапе – использование высококалорийной высокоэнергетической диеты, но, в то же время, часто необходимы специальные смеси, поскольку диета не всегда обеспечивает необходимое количество калорий в сутки (требуется большое количество калорий в малом объеме питания). Если этот вариант не дает желаемого эффекта (увеличение тощей массы тела), используют зондовое питание (назогастральный зонд или гастростому). Парентеральное питание – исключительный случай – из-за риска развития сепсиса.
Нутритивная терапия пациентов с муковисцидозом (кистозным фиброзом). 2009.
Г.Саболова, Издание Фонда «Во имя жизни» (помощь больным муковисцидозом).
Муковисцидоз и питание. Муковисцидоз (кистозный фиброз) (МВ) – это генетически обусловленное заболевание, которое характеризуется образованием очень густой слизи в легких и желудочно-кишечном тракте (поджелудочная железа, кишечник, печень). Это явление обусловлено нарушением обмена ионов натрия и хлора между внутренней и внешней средами клеток. Диагностическими критериями цистического фиброза являются клинические признаки – высокая концентрация хлоридов в поту и/ или наличие мутаций гена CFTR. Поэтому детям с МВ часто говорят также «соленые дети». Приблизительно у 2% пациентов может быть концентрация соли в поту в норме, предварительное генетическое обследование не выявит наличие более редких мутаций, но и вопреки тому у них можно наблюдать остальные классические проявления МВ. Определение диагноза в таких случаях сложное и основано на проявленных клинических признаках. Густая слизь, которая содержится в поджелудочной железе пациентов c МВ ограничивает или мешает секреции пищеварительных энзимов, необходимых для нормального пищеварения пищи. Вследствие отсутствующих энзимов дети и взрослые с МВ не могут переваривать питательные вещества, присутствующие в еде. Поэтому пациенты без лечения МВ часто страдают дистрофией. На современном этапе у нас еще нет в распоряжении препаратов для лечения цистического фиброза. Целью лечения и заботы о пациентах с МВ является, прежде всего повышение качества их жизни. Недостаточное питание ухудшает течение заболевания у детей, замедляет рост и развитие.
|
Ежедневный энергетический прием пищи пациента с МВ должен быть на 30–50% выше по калорийности в сопоставлении со средними рекомендациями по его полу и возрасту. В случае инфекции, повышенной нагрузки дыхания или дистрофии требование увеличивается вплоть до 150–200% обыкновенно рекомендуемого калорийного приема. Однако точные данные об энергетической потребности конкретного пациента с МВ зависят не только от его возраста и пола, но и от нутритивного состояния, степени панкреатической недостаточности, физической активности и функций легких. В то время как некоторые дети растут нормально, при потреблении нормальной пищи, дети с прогрессирующими инфекциями легких требуют на 50% энергии больше. Таблица № 1 показывает ориентировочные энергетические требования организма пациента с МВ, установленные как 150% рекомендуемого ежедневного энергетического приема.
Таблица № 1. Рекомендуемый энергетический прием пищи пациентов с MB в зависимости от возраста
| Возраст | Рекомендуемый ежедневный энергетический прием для пациента с MB |
| Дети грудного возраста | 150-200 ккал/кг |
| Дети с 1 до 9 лет | 130-180 ккал/кг |
| Мальчики с 11 до 18 лет | 100-130 ккал/кг |
| Девушки с 11 до 18 лет | 80-110 ккал/кг |
| Мужчины | 100-120 ккал/кг |
| Женщины | 80-120 ккал/кг |
Единственно надежным измерителем энергетически достаточной пищи, потребляемой пациентом с МВ, является подсчитывание ее калорийности и взвешивание. Нужно повышать калорийную ценность пищи или увеличивать частоту потребления еды у детей тогда, когда ребенок бледнеет и не прибавляет в весе более одного месяца. У взрослых пациентов с МВ причиной для повышения энергетической ценности пищи является уменьшение веса, продолжающееся более двух недель. У детей в возрасте до восемнадцати месяцев рекомендуется дневная доза жира 5–7 г на каждый килограмм веса ребенка (максимальная дневная доза жира 8 г/кг). В первом полугодии жизни это количество жира обеспечивает материнское молоко или смеси для кормления в количестве 150–200 мл на каждый килограмм веса ребенка. В метаболизме пациентов, страдающих цистическим фиброзом можно уже с раннего детства наблюдать определенную аномалию – хронический недостаток эсенциальных жирных кислот (ЭЖК).
Это проявляется у пациентов, у которых панкреас функциональный, а также у тех, которые настроены на панкреатическое субституционное лечение. Первые проявления этого дефицита – задержка роста, ухудшение функций легких и кожные реакции.
Предполагается, что вследствие этого дефицита возникают экземы и стеатоз печени. Малнутриция в случае муковисцидоза вызвана не низким приемом белка, а недостаточной функцией поджелудочной железы. Достаточной является дневная доза белка в количестве 1,2 г белков на каждый килограмм веса. Например, ребенок с весом 10 кг должен ежедневно принять с пищей 12 г белков. В связи с необходимостью высококалорийного питания преимущество в составе питания отдается комплексным углеводам (сахаридам).
У всех больных муковисцидозом отмечается дефицит жирорастворимых витаминов, что требует их обязательного введения в составе пищи в дозировках:
Вит.А: грудные дети до 6 недель- 1000 IU/день; дети с 6 недель до 2-х лет – 2000-4000 IU/день; дети с 2 до 12 лет – 5000 IU/день; подростки и взрослые – 10000-20000 IU/день.
Вит.D: грудные дети до 6 недель – 200-400 IU/день; дети с 6 недель до года – 500-1000 IU/день; дети с года – 400-800 IU/день.
Вит.Е: грудные дети до 6 месяцев – 25 мг/день; дети с 6 месяцев до года – 50 мг/день; дети с 1 до 4 лет – 100 мг/день; дети с 4 до 10 лет – 100-200 мг/день; дети с 10 лет – 200-400 мг/день.
Вит.К: грудные дети с 1 года – 2-5 мг два раза в неделю; дети после 1 года – 5 мг два раза в неделю.
|
|
3.2. Принципы нутритивной поддержки онкологических больных
Изменение идеальной (тощей) массы тела при онкологических заболеваниях является основным показателем нутритивного статуса пациентов. Потеря 10% массы тела за последние 6 месяцев или 5% за месяц является показанием для обращения к специалисту и обязательного применения специализированных продуктов лечебного питания. Это положение должно строго выполняться в период до постановки диагноза, а также вне зависимости от стадии заболевания (Harriet Jager-Wittenaar и соавт., 2011).
Рис. 1. Причины и механизмы снижения нутритивного стутуса онкологических больных (модифицированная схема Soeters и соавт., 2008)
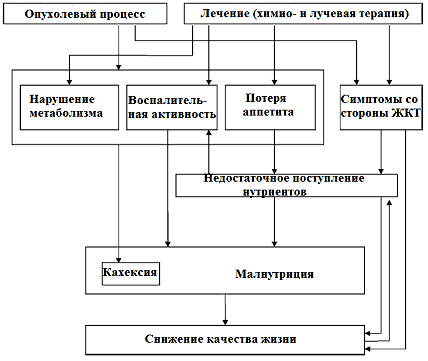
Вышеперечисленные факторы определяют необходимость использования таких энтеральных (желательно оральных) формул, которые бы обеспечивали в условиях нарушенного всасывания в ЖКТ, пониженного аппетита, отрицательного физиологического и психологического состояния пациента, влияния химио- и лучевой терапии, максимальное количество калорий в минимальном объеме питания и повышенные вкусовые качества. Улучшенный вкус продукта имеет важное клиническое значение.
|
3.3. Принципы нутритивной поддержки больных ВИЧ/СПИД
Питание играет важную роль в поддержании здоровья людей, живущих с ВИЧ. Надлежащее питание является существенно важным для поддержания иммунной системы человека, полезного уровня физической активности и качества жизни. Надлежащее питание также необходимо для получения максимальной пользы от антиретровирусного лечения. Нутритивная поддержка должна стать неотъемлемой частью национальных мер в ответ на ВИЧ. К данной категории должно относиться потребление нутриентов, а также все расходы на поставку и оказание нутритивной поддержки» (Объединённая программа ООН по ВИЧ/СПИДу (ЮНЭЙДС, 2009).
Синдром истощения и нарушение питания. Нарушение питания – одно из важнейших осложнений ВИЧ-инфекции (Nahlen и соавт., 1993), которое было описано как «синдром истощения» (СИ) в качестве значительного прогностического фактора развития болезни (Kotler и соавт., 1989; Guenter и соавт., 1993; Suttmann и соавт., 1995). СИ проявляется потерей веса более, чем на 10% по сравнению с обычным весом и ассоциируется с хронической диареей и/или лихорадкой и/или астенией при отсутствии других причин истощения, не связанных с ВИЧ-инфекцией. Нарушение питания является не только результатом ВИЧ-инфекции,но также ряда ассоциированных с ней осложнений (Macallan и соавт., 1993). Существует широкая вариабельность клинических проявлений этого состояния. Даже если нарушение питания наиболее часто проявляется в конечной стадии заболевания, оно также может наблюдаться и в самом начале хронического инфекционного процесса – до появления выраженной иммунодепрессии (Ott и соавт., 1993). Однако потеря веса относительно независима от уровня иммуносупрессии в процессе развития ВИЧ-инфекции (Guenter и соавт., 1993). Нутритивный статус (характеризуемый уровнями потери веса, абсолютной и/или относительной кривой массы тела, альбумином, преальбумином, С-реактивным белком) является значительным предиктором выживания у взрослых пациентов с ВИЧ (Melchior и соавт., 1999). Нарушение питания может оказывать существенное воздействие на долгосрочную выживаемость посредством ряда механизмов, включая скомпрометированную полиммунную функцию, служащую причиной нарушения функции органов, снижения ответа на проводимую терапию и прогрессирующую слабость (Kotler и соавт., 1989).
Нарушение питания в процессе развития ВИЧ является мультифакторным процессом (Macallan и соавт., 1993). Снижение поступления калорий (Grunfeld и соавт., 1992а), плохое всасывание нутриентов, увеличенный расход энергии в процессе вторичной бактериальной и/или системной оппортунистической инфекции (Melchior и соавт., 1993) вносят свой вклад в нарушение питания у этих пациентов. Кроме того, сообщалось о ряде метаболических аномалий в процессе развития ВИЧ-инфекции: возрастание печеночного липогенеза (Hellerstein и соавт., 1993), повышение чувствительности к инсулину (Hommes и соавт., 1991) и увеличение белкового обмена, которое ведет к преобладающему снижению массы тела по причине снижения поступления энергии (Macallan и соавт., 1995). Снижение поступления калорий, возрастание расхода энергии, хроническая диарея и оппортунистические инфекции – главные факторы, связанные с нарушением питания (Melchior и соавт., 1999). Нарушение питания может быть отчасти следствием прямого влияния ВИЧ-инфекции, вторичным воздействием на пищеварение наркотиков и лекарственных препаратов (Perlenicek и соавт., 1996; Wheeler и соавт., 1998). В США между 1987 и 1993 годами СИ был выявлен у 20% пациентов в период заболевания СПИДом, а непосредственно перед смертью этот показатель достигал 70%. СИ диагносцировался также у 1/3 пациентов, употреблявших наркотики внутривенно до постановки диагноза СПИД. Примерно в этот же период времени СИ был описан как второе по частоте проявление СПИДа после легочного пневмоцистоза. После возникновения эры антиретровирусной терапии (АРВТ) в западных странах количество случаев СИ и других форм нарушения питания увеличилось и достигло 6-33% (Wanke и соавт., 2000).
Нарушение питания, связанное с ВИЧ, значительно отличается от простого истощения. Обычное истощение является результатом преобладающей потери жиров организма и в меньшей степени линейной массы тела даже при неизмененном синтезе белка в течение продолжительного периода времени. В противоположность этому, в процессе ВИЧ-инфекции снижение линейной массы тела является преобладающим (Kotler и соавт., 1985). Для определения состояния тела и изменений, связанных с нутритивным статусом, использовались: антропометрия, измерение плотности тела и веса, неинвазивное определение подкожного жира (Gibson и соавт., 1990; Niyongabo и соавт.,1999). При ВИЧ-заболевании антропометрические измерения обеспечивают недорогие и неинвазивные данные мониторирования долгосрочного нутритивного статуса, характеризующего жировые отложения тела и оценку нутритивных рисков (Batterham и соавт., 1999). Изменение линейной массы тела, измеряемое антропометрически, хорошо коррелирует с изменениями массы тела, определяемыми с помощью абсорбциометрии двойными Х-лучами, и поэтому может рассматриваться в качестве законного метода у больных в критических состояниях (Paton, Castello, 1997). Биоэлектрический импедансный анализ одиночной частотой 50 kHz использовался для определения линейной массы тела, общей жидкости тела и клеточной массы тела (Lukaski и соавт.,1986; Baumgartner и соавт., 1989; Ellis, Bell, 1999).
За последние годы были сделаны значительные шаги в управлении (менеджменте) ВИЧ-инфекцией (антиретровирусная терапия, профилактика и лечение оппортунистических инфекций и глобальная медико-психо-социальная защита пациентов), но несмотря на этот прогресс, нарушение питания, которое плохо лечится в процессе ВИЧ-инфекции, остается важнейшим прогностическим фактором. Потеря веса и мышечное истощение, которые и ранее были уникальными идентификационными признаками ВИЧ-инфекции (Serwadda и соавт., 1985; Mhiri и соавт., 1992), представляют значительную клиническую проблему и сейчас в век антиретровирусной терапии (Wanke и соавт., 2000). Истощение, частичная потеря жира и протеинов в мышечной ткани (Yarasheski и соавт., 1998) ассоциируются с увеличением смертности (Kotler и соавт., 1989; Wheeler и соавт., 1998; Melchior и соавт., 1999), прогрессированием заболевания ((Wheeler и соавт., 1998) и нарушением физического статуса (Grinspoon и соавт., 1999) у больных с ВИЧ-инфекцией.
|
3.4. Принципы нутритивной поддержки больных туберкулезом
Food and Nutrition Assistance in TB programming – rationale and practice. Saskia de Pee, Nils Grede, United NationsWorld Food Programme, 2012, London
Рис. 2. Взаимосвязь между туберкулезом и малнутрицией
- Снижение аппетита и способности принимать пищу
- Снижение способности организма абсорбировать нутриенты
- Снижение доступа к пище из-за заболевания
- Возрастание потребности в нутриентах из-за изменения метаболизма
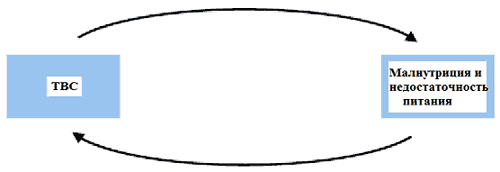
- Прогрессия заболевания, снижение иммунитета
- Повышение риска летального исхода
Рис. 3. Снижение летальных исходов в Великобритании у больных ТВС за счет лечения, гигиенических мероприятий и нутритивной поддержки
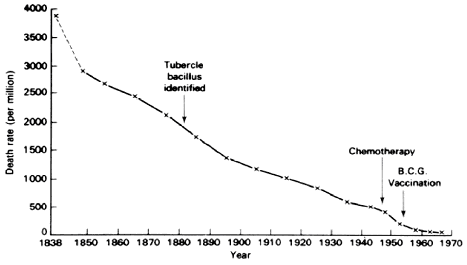
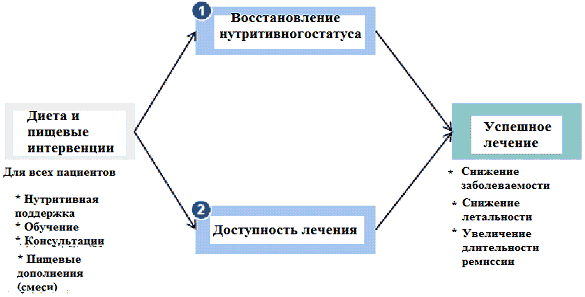
Рис. 4. Роль нутритивной поддержки в успешности лечения ТВС
Как отмечено в работе М.В.Титюхиной (2012) «При хроническом течении процесса нарастающий эндотоксикоз, является и причиной, и следствием нежелательных побочных реакций (НПР), приводит к нарушению деятельности желудочно-кишечного тракта (ЖКТ), сопровождающемуся анорексией и, следовательно, уменьшенным потреблением пищи, нарушением процессов пищеварения и всасывания питательных веществ. В этих условиях катаболические процессы в белковом обмене начинают преобладать над процессами синтеза белка, что, по сути своей, представляет синдром нутритивной (азотистой) недостаточности и создает неблагоприятный фон для течения инфекционного процесса». Дополнительное ЭП (сипинговое или зондовое) назначалось больным при недостаточности питания, неуклонном прогрессировании туберкулеза, осложнении или обострении сопутствующей патологии ЖКТ, а также для подготовки к плановым оперативным вмешательствам и после плановых и экстренных операций на легких и органах ЖКТ. В работе показана эффективность энтерального питания (сипингового) у больных туберкулезом органов дыхания для коррекции метаболических нарушений и повышения толерантности к противотуберкулезной химиотерапии. При этом сокращается число осложнений, сокращаются сроки пребывания больных в стационаре, предупреждается развитие белково-энергетической недостаточности.
3.5. Усиленное питание при повышенных белково-энергетических потребностях (включая спортивное питание) – относительная БЭН
Занятия спортом предъявляют особые требования к организации специализированного питания спортсменов. Питание должно обеспечить поступление в организм всех необходимых веществ для нормального осуществления большинства жизненных функций, поддержания высокого уровня здоровья и физической работоспособности. В дни наиболее напряженных тренировок и соревнований суточные затраты энергии у спортсменов могут достигать более 10 тыс. ккал, в то время как при обычных режимах жизнедеятельности человека они редко превышают 2 тыс. ккал в сутки. Восполнение столь значительных затрат энергии при сохранении сбалансированной диеты невозможно за счет употребления обычных пищевых продуктов. Таким образом, возникает риск развития дефицита целого ряда нутриентов (белков, жиров, углеводов, витаминов и минералов).
Рынок специализированного спортивного питания очень широк. На графике показаны основные цифры роста данного рынка:
Рис. 5. Суммарные цифры глобального рынка спортивного питания и высокоэнергетических добавок с проекцией на 2013 год
| SUMMARY FIGURE GLOBAL SPORTS NUTRITION SPORTS NUTRITION AND HIGH-ENERGY SUPPLEMENT MARKET PROJECTIONS BY SEGMENT, 2007-2013 ($ BILLIONS) |
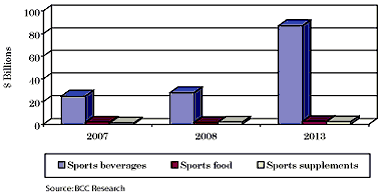
Как видно из графиков, глобальный рынок спортивного питания увеличится с 2007 года с 27,8 млрд $ до 91,8 млрд $ при ежегодном среднем приросте в 24,1%. Сегмент спортивной пищи (второй по величине сегмент) вырастет с 1,8 млрд $ в 2007 году до 2,5 млрд $ в 2013 году.
|
Предыдущий раздел | Оглавление | Список литературы
Комментарии
ПРАКТИКА ПЕДИАТРА
