Современные подходы к лечению больных с местно-распространённым и метастатическим немелкоклеточным раком лёгкого (НМРЛ)
Статьи ОнкологияОпубликовано в сборнике Новое в терапии рака легкого (Москва, 2003) В.А. Горбунова, А.Ф. Маренич, А.В. Голубев
Введение
Распространённость опухоли и возможность её хирургического удаления являются определяющими условиями успешного лечения больных НМРЛ.
На момент установления диагноза, всех пациентов НМРЛ можно условно разделить на 3 группы, что отражает распространённость заболевания и подходы к лечению.
Первая группа - это операбельные больные с I-й и II-й стадиями. Они имеют наилучший прогноз, зависящий от биологических особенностей опухоли и других факторов. Больные с операбельной опухолью, но имеющие противопоказания к операции, могут быть подвергнуты консервативному лечению.
Вторая группа (10-15%) - включает больных либо с местно-распространённым процессом (T3-4), либо с метастазами в регионарные лимфоузлы (N2-3). Большая часть больных в этой группе обычно получает консервативное лечение (лучевую или химио-лучевую терапию), лишь немногие больные с T3 или N2 могут эффективно лечиться хирургическим методом.
Третья группа больных (примерно 50%) имеет клинически определяемые отдалённые метастазы (M1) при постановке диагноза. Они могут получать химиотерапию или лучевую терапию для облегчения симптомов болезни.
Кроме того, более чем у половины пациентов после радикально выполненных операций возникает либо местный рецидив, либо отдалённые метастазы, а это значит, что 75% всех больных НМРЛ являются потенциальными кандидатами для проведения консервативной терапии на различных этапах лечения.
Определение стадии заболевания чрезвычайно важно для прогноза и выбора лечебной тактики. Стадия устанавливается на основании клинических (осмотр, рентгенологическое и лабораторное обследование) и морфологических (гистология/цитология биоптатов, полученных при бронхоскопии, биопсии лимфоузлов трансторакальной пункции, торакоскопии, медиастиноскопии) -методов (1).
Анализ стадирования 1400 больных, подвергнутых операции, показал, что клиническая стадия, установленная на основании рентгенологических методов, была правильно оценена по Т - у 78% больных и по N - у 47% больных. Ошибки по занижению и завышению стадий были одинаково часты (2). Чувствительность и специфичность компьютерной томографии (КТ) (по данным Radiology Diagnostic Oncology Group) составляет 52% и 69% соответственно (3). Магнитно-резонансная томография (МРТ) не улучшает правильность стадирования. Предварительная оценка позитронно-эмиссионной томографии (ПЭТ) даёт основания предположить, что комбинация КТ и ПЭТ может улучшить объективность стадирования (4). Алгоритм обследования больных НМРЛ, предложенный American Thoracic Society (ATS), представлен на рисунке 1 (5).
Помимо метастазов в надпочечники, при НМРЛ часто поражаются печень, кости, головной мозг. В связи с этим, по нашему мнению, целесообразно при первом обращении больного с НМРЛ проведение полного обследования, включающего скенирование скелета, неврологическое обследование, КТ головного мозга.
В результате применения новых технологий обследования больных (6), в 1997-м году Международная Система Стадирования НМРЛ была пересмотрена. Изменения были основаны на накопленном клиническом опыте. Небольшие дополнения относятся к классификации множественных лёгочных лимфоузлов. Пересмотренная система делит I и II - стадии на А и В подгруппы. Кроме того, стадия IIIA была модифицирована, чтобы более адекватно отразить влияние на прогноз анатомической распространённости опухолевого процесса для этой подгруппы. Новая группировка также совмещена с условными лечебными подходами.
Рисунок 1 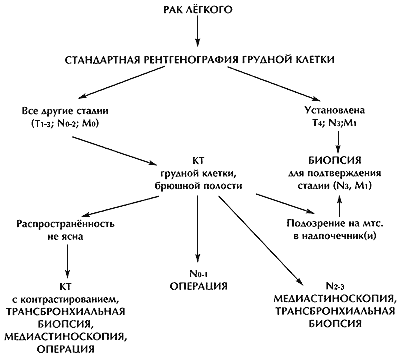
Клинические аспекты лечения НМРЛ
IIIА стадия НМРЛ (T1-2 N2 Мо, T3 N1-2 M0)
Больные с клинической стадией IIIA (N2) имеют 5-летнюю выживаемость от 10 до 15%. Однако, при массивном поражении медиастинальных лимфоузлов этот показатель снижается до 2-5%. В зависимости от клинических обстоятельств, основными методами лечения больных с IIIA стадией являются лучевая терапия, химиотерапия, хирургия и комбинация этих методов. Хотя большинство больных не достигают полной ремиссии на лучевой терапии, она обеспечивает воспроизводимое долговременное улучшение выживаемости у 5-10% пациентов при использовании стандартных доз и значительное симптоматическое улучшение.
Поскольку долгосрочный прогноз у больных с IIIA - стадией в целом плохой, следует включать их в клинические исследования, изучающие режимы с различным фракционированием, эндобронхиальную лазеротерапию, брахитерапию, сочетание этих методов, что может привести к улучшению результатов лечения (7). Например, в одном проспективном рандомизированном исследовании было показано улучшение общей выживаемости при проведении лучевой терапии по 3 фракции в день по сравнению с 1 фракцией (8).
Добавление современных платиносодержащих режимов химиотерапии к лучевой терапии улучшает выживаемость больных (9-12). Метаанализ 11 клинических исследований продемонстрировал снижение риска смерти на 10% у больных, получавших цисплатинсодержащие режимы + лучевую терапию, по сравнению с применением одной лучевой терапии (13). Оптимальная последовательность методов, фракционирование лучевой терапии и химиотерапевтические режимы продолжают изучаться.
Эффективным является проведение неоадъювантной химиотерапии. В двух исследованиях медиана выживаемости больных, получавших химиотерапию, оказалась в 3 раза больше, чем у больных после одной операции (14-15). В работе Vansteenkiste (16) проведение неоадъювантной химиотерапии позволило улучшить 2-летнюю выживаемость на 20% и 5-летнюю - на 6%.
В таблице 1 представлены современные режимы комбинированной неоадъювантной химиотерапии, опубликованные в материалах ASCO-2002.
Таблица 1
Современные режимы неоадъювантной химиотерапии при НМРЛ III-й стадии
|
Автор |
Количество больных |
Режим лечения (мг/м2) |
Общий эффект |
|
Betticher D. С. |
90 |
Таксотер 85 в 1 -й день |
62%, (8% ПЭ) 77 больных оперировано, радикально - 56 Патологич. ПЭ=16% |
|
Cappuzzo F. |
36 |
Гемзар 1000 в 1, 8-й дни |
72%, (2% ПЭ) 21 больной оперирован. Патологич. ПЭ=8% |
|
Esteban E. |
25 |
Цисплатин 50 в 1, 8-й дни |
72%. Оперировано 6 больных. Патологич. ПЭ=16% |
|
25 |
Цисплатин 50 в 1, 8-й дни |
73%. Оперировано 7 больных. Патологич. ПЭ=12% |
|
|
WuY. I. |
13 |
Гемзар 1000 в 1, 8-й дни |
69%. 9 больных оперировано. Патологич. ПЭ - у 8. |
Современные режимы комбинированной неоадъювантной химиотерапии показали хорошие результаты и удовлетворительную переносимость.
Наш собственный опыт неоадъювантной химиотерапии включал применение двух циклов химиотерапии по схеме цисплатин 100 мг/м2 в/в. в 1-й день+ навельбин 25 мг/м2 в/в. в 1, 8-й дни у 37 больных, на базе онкологического отделения Московского областного онкологического диспансера (к. м. н. Усков Д. А.). Всего оперировано 33 больных (89%).
Пневмонэктомия выполнена 18 больным, лобэктомия - 13 больным.
Объективный эффект составил 63%, стабилизация - 28,6%. Оценка лечебного патоморфоза показала III-IV степень - у 31% больных.
При оценке отдалённых результатов комбинированного лечения после 24-х месяцев наблюдения, при сравнении с больными, подвергшимися только радикальной операции, получено статистически достоверное увеличение продолжительности жизни у больных НМРЛ IIIA-стадии.
В РОНЦ РАМН проводится изучение неоадъювантной химиотерапии по схеме Гемзар -1250 мг/м2 в 1, 8-й дни и цисплатин 75 мг/м2 в 1 -й день; х 3 курса, далее - операция. Набор больных продолжается.
Ещё один лечебный подход, активно изучаемый в настоящее время - это неоадъювантная химио-лучевая терапия с использованием современных цитостатиков (21-24), которые по предварительной оценке оказались высокоэффективными и хорошо переносимыми.
Большинство ретроспективных исследований подтверждают, что послеоперационная лучевая терапия уменьшает частоту местных рецидивов, однако, остаётся спорным вопрос -улучшает ли это общую выживаемость (25-26). Метаанализ девяти рандомизированных исследований, сравнивавших результаты операции и лучевой терапии и одной операции, не показал различий в выживаемости у больных с N2 (27). В исследовании, сравнивавшем послеоперационную лучевую терапию (одну) и её сочетание с одновременной стандартной химиотерапией по схеме цисплатин + этопозид, преимуществ последней не выявило (28).
В настоящее время профилактическая послеоперационная химиотерапия не может быть рекомендована как стандартный метод лечения и находится в процессе изучения (29-31).
Ill В - стадия НМРЛ (Т4 или N3, M0)
Стандартным подходом к лечению больных с неоперабельной IIIB - стадией, при PS=0-1, является химио-лучевая терапия. Однако, больным со злокачественным плевритом редко проводится лучевая терапия и их лечение подобно лечению больных с IV-й стадией.
Многочисленные рандомизированные исследования показали преимущества по выживаемости у больных с нерезектабельной IIIB стадией при использовании одновременной цисплатин-содержащей химиотерапии и лучевой терапии, по сравнению с одной лучевой терапией (32-36). Ослабленные больные с IIIB стадией являются кандидатами для паллиативной лучевой терапии. Основными вопросами, которые обсуждаются в настоящее время, являются - выбор оптимальной последовательности химиотерапии и лучевой терапии, оптимального режима химиотерапии и конкретных цитостатиков с учётом их радиосенсибилизирующих свойств.
Результаты II-й фазы клинического исследования LAMP (Locally Advanced Multimodality Protocol) дали некоторую информацию по этим вопросам (37). В исследование было включено 276 больных, рандомизированных на 3 группы.
1. Таксол + карбоплатин х 2 цикла, затем лучевая терапия (ЛТ) в дозе 63 Гр. Медиана выживаемости - 12,5 мес.
2. Таксол + карбоплатин х 2 цикла, затем Таксол + карбоплатин в еженедельном режиме + ЛТ в течение 7-и недель, 63 Гр. Медиана выживаемости - 11 мес.
3. Таксол + карбоплатин + ЛТ в течение 7-и недель, 63 Гр., затем Таксол + карбоплатин х 2 цикла. Медиана выживаемости - 16,1 мес.
Медиана выживаемости в трёх рукавах этого исследования сравнивалась с медианой выживаемости 14,5 мес., продемонстрированной при последовательной химио-лучевой терапии в исследовании RTOG - 8808 (38). Анализ показал отсутствие улучшения выживаемости у больных в 1, 2-й группах по сравнению с историческим контролем. Наилучший терапевтический эффект был получен в 3-й группе. Лечение оказалось хорошо переносимым. Несмотря на частые эзофагиты в группе 3 - 67% больных закончили химио-лучевую терапию и 75% - консолидирующую химиотерапию.
Несколько текущих исследований по изучению сочетанной химио-лучевой терапии при лечении НМРЛ III В стадии представлены в таблице 2.
Таблица 2
Опубликованные текущие исследования по химио-лучевому лечению НМРЛ IIIB стадии
|
Исследование |
Фаза |
Режим лечения |
|
Curran et al., 2000 (RTOG-9410) (39) |
III |
Группа 1: Цисплатин + Винбластин, затем ЛТ |
|
FCCC 94-001, 2000 (40, 41) |
I/III |
Фаза III: Индукционная х/т. (Таксол + Карбоплатин + G-CSF) |
|
Furuse, 1999 (42) |
III |
Виндезин + Цисплатин + Митомицин + ЛТ |
|
Ratanatharathorn, et al., 2001 (43) |
II |
Таксол + Карбоплатин + ЛТ, затем консолидирующая химиотерапия (Таксол + Карбоплатин) |
|
SWOG - 9504, 2001 (44) |
II |
Цисплатин + Этопозид+ ЛТ, затем консолидирующая химиотерапия (Доцетаксел) |
|
LCCC - 9603, 2000 (45, 46) |
I/II |
Индукционная химиотерапия (Таксол + Карбоплатин), затем Таксол + Карбоплатин + ЛТ |
|
Akerlay et al. (CALGB), 2000 (47) |
II |
Индукционная химиотерапия (Таксол + Карбоплатин), затем Таксол + Карбоплатин + ЛТ |
|
Lau et al. (California Cancer Consortium), 2000 (48) |
II |
Индукционная химиотерапия (Таксол + Карбоплатин + ЛТ), затем консолидирующая химиотерапия Таксол + Карбоплатин |
|
Choy et al., 2000 (49) |
II |
Таксол + Карбоплатин + гиперфракционная ЛТ, затем Таксол + Карбоплатин. |
|
Belani et al., 1999 (50) |
II |
Таксол + Карбоплатин + ЛТ |
|
Choy et al., 1998 (51) |
II |
Таксол + Карбоплатин + ЛТ, затем Таксол + Карбоплатин |
|
Choy et al., 1998 (52) |
II |
Таксол + ЛТ |
Два исследования по III-й фазе показали преимущество одновременной химио-лучевой терапии, что отразилось на выживаемости (39-42). Исследование Furuze продемонстрировало улучшение непосредственной эффективности и выживаемости у больных, получавших одновременное химио-лучевое лечение (общий эффект -84% против 66%, р=0,0002; медиана выживаемости - 16,5 мес. против 13,3 мес., р=0,03998). Кроме того, были выше показатели 5-летней выживаемости (42). ll-я фаза SWOG - 9504 также показала преимущество совместной химио-лучевой терапии в комбинации с консолидирующей химиотерапией (44). Однако, проведение одновременной химио-лучевой терапии может привести к усилению токсичности (39-42).
В некоторых исследованиях использовались "старые" (традиционные) режимы химиотерапии (39, 42, 44). Пока нет рандомизированных исследований по III-й фазе, в которых бы изучалась последовательность применения современных химиотерапевтических режимов. В рамках I -II -й фазы определены некоторые современные комбинации, активные при НМРЛ, которые могут назначаться неоперабельным больным с III-й стадией (40, 43-52). Широко изучался режим Таксол + карбоплатин в сочетании с ЛТ, демонстрируя общий эффект 50-79%, и медиану выживаемости 14-26 мес., при хорошей общей переносимости. По мнению некоторых исследователей, назначение индукционной химиотерапии перед химио-лучевой терапией может ухудшать переносимость последней, что может привести к ухудшению отдалённых результатов (37). Целесообразность проведения консолидирующей химиотерапии после химио-лучевого лечения, остаётся в настоящее время предметом изучения.
Таким образом, сочетанная химио-лучевая терапия - стандартный метод лечения больных с неоперабельной III-й стадией НМРЛ, а также -для больных с любой стадией, которые не могут быть оперированы по медицинским причинам (53-55). Лечение может меняться в зависимости от индивидуальных особенностей пациента. Для ослабленных (PS >= 2) и пожилых полные дозы сочетанной химио-лучевой терапии могут оказаться токсичными. Возможно, новые менее токсичные режимы, включая расщеплённый курс лучевой терапии, могут стать приемлемыми для лечения этой категории больных. На сегодняшний день мало исследований, изучающих этот вопрос (56).
Лечение НМРЛ IV стадии (M1)
Доказано, что использование системной паллиативной химиотерапии у больных с неоперабельной IIIB и IV стадиями НМРЛ даёт улучшение выживаемости по сравнению с оптимальной симптоматической терапией (57-60).
Метаанализ показал, что применение цисплатин-содержащих режимов улучшает 1-летнюю выживаемость на 10% (59). Кроме того, у 65% больных отмечено симптоматическое улучшение. Часто пациенты с распространённым опухолевым процессом имеют серьезные сопутствующие заболевания, ухудшающие их состояние, что осложняет проведение агрессивной химиотерапии. Появление в последние годы новых, более эффективных и хорошо переносимых препаратов расширяет контингент больных, подлежащих лекарственному лечению.
Выбор метода лечения основывается на анализе прогностических факторов. Наиболее важными являются - общее состояние больного (Performance Status - PS), возраст и потеря веса (61-63). В многочисленных исследованиях было показано, что больные в хорошем общем состоянии имеют больше шансов достичь объективного ответа на химиотерапию и добиться лучшей выживаемости, а также меньшую вероятность развития серьезных осложнений (63-67).
По данным SWOG, 1-летняя выживаемость пациентов с PS=0-1, составила 20%, по сравнению с 9% для пациентов с PS=2-4 (63). Ретроспективный анализ 5-и клинических исследований ECOG (1960 больных), также подтвердил, что PS достоверно влияет на медиану выживаемости (68). Следует также учитывать пол, локализацию и количество метастатических очагов, уровень гемоглобина и ЛДГ, число лейкоцитов (62-66, 69). Что касается выбора препаратов, то в настоящее время предпочтение отдаётся платиносодержащим комбинациям, хотя в некоторых исследованиях показана сопоставимая эффективность неплатиновых и платиносодержащих режимов (70).
Мультицентровые рандомизированные исследования показали преимущество платиносодержащих режимов с включением новых препаратов, таких как Таксол, Таксотер, Гемзар, навельбин, иринотекан, по сравнению со стандартной комбинацией этопозид+ цисплатин (71-75). Сравнение в проспективном рандомизированном исследовании 4-х наиболее часто используемых в настоящее время режимов: цисплатин + Таксол, Гемзар + цисплатин, Таксотер + цисплатин, карбоплатин + Таксол не выявило достоверных различий в эффективности и выживаемости (76). В другом мультицентровом рандомизированном исследовании (TAX-326) сравнивались 3 режима: Таксотер+ цисплатин, Таксотер+ карбоплатин и навельбин + цисплатин. Выживаемость в группе больных, получавших комбинацию Таксотер + цисплатин, оказалась достоверно выше чем в группе, леченной навельбином и цисплатином. Качество жизни больных, получавших таксотер-содержащие режимы, также оценена как более высокое (77).
Химиотерапию у больных распространённым НМРЛ следует начинать как можно раньше. Длительность её зависит от результатов лечения и переносимости. Согласно практическим рекомендациям ASCO (1997г.), для лечения неоперабельных больных НМРЛ не следует проводить более 8-и курсов химиотерапии (83). Больные в хорошем состоянии, обладающие первичной резистентностью к 1-й линии химиотерапии, могут достичь частичной регрессии при проведении 2-й линии. Большие шансы на успешное лечение имеют пациенты, у которых отмечалось объективное улучшение и длительный период до прогрессирования Перспективным направлением в лечении распространённого НМРЛ является изучение принципиально новых препаратов, воздействующих на молекулярные мишени (ингибиторы эпидермального фактора роста, антисенсы, ингибиторы ангиогенеза и др.).
При распространённом НМРЛ лучевая терапия может использоваться как симптоматическое средство при сдавлении трахеи, пищевода, бронхов, синдроме верхней полой вены, а также при метастатическом поражении головного мозга и костей. В некоторых случаях возможно использование эндобронхиальной лазеротерапии и/или брахиотерапия (84).
Головной мозг часто поражается при НМРЛ. У редких больных с синхронным поражением -операбельной первичной опухолью и солитарным метастазом в головной мозг - возможно оперативное лечение метастаза и первичной опухоли и проведение послеоперационной химиотерапии и/или лучевой терапии. В случае, если солитарный метастаз в головном мозге обнаружен у больного после резекции первичной опухоли и отсутствуют другие проявления болезни, оперативное лечение метастаза и последующее облучение головного мозга позволяют улучшить безрецидивную выживаемость (85-86). Большинству больных, не подлежащих хирургическому лечению, следует проводить лучевую терапию, а у отдельных пациентов в хорошем состоянии при маленьких размерах метастазов в головном мозге возможно стереотаксическое радиохирургическое лечение (87).
Солитарные метастазы в лёгких у оперированных больных встречаются редко. Исследования показали, что у большинства больных с новыми очагами - это вторая первичная опухоль, которая, по возможности, должна быть резецирована (88, 89).
Больным, которым проведено специфическое лечение, следует находиться под наблюдением онколога. При отсутствии клинических симптомов, обследование следует проводить 1 раз в 3 месяца, в течение первых 2-х лет, 1 раз в 6 месяцев - в течение 5-и лет, затем - ежегодно. Для профилактики рецидива и развития 2-й опухоли, следует отказаться от курения и избегать контакта с канцерогенами. Хотя у больных с отдалёнными метастазами отказ от курения мало влияет на исход болезни, но он может улучшить дыхательную функцию. Химиопрофилактика немелкоклеточного рака лёгкого находится на стадии изучения.
Заключение
Таким образом, на современном этапе проблема лечения местно-распространённого НМРЛ решается на стыке разных дисциплин и требует участия различных специалистов - торакального хирурга, химиотерапевта, радиолога.
Выбор лечебной тактики зависит от объективного стадирования и общего состояния больного. Оптимальным методом лечения неоперабельных больных с III-й стадией НМРЛ является химио-лучевая терапия с использованием различных режимов химиотерапии и методик облучения.
Для больных с IV-й стадией в удовлетворительном состоянии, основным методом лечения является системная, паллиативная химиотерапия, На сегодняшний день не существует
единого стандарта среди современных равно эффективных химиотерапевтических режимов Выбор делается с учётом функциональны) резервов больного и токсического профиля препарата.
Лучевая терапия играет вспомогательную роль, и используется для купирования тягостных симптомов болезни.
Оптимальным для больных с местнораспространённым и метастатическим НМРЛ является участие в клинических исследовательских программах, что обеспечивает использование новейших технологий диагностики и лечения. К сожалению, сейчас количество больных, включённых в клинические исследования, не превышает 1-2%.
В настоящее время, одним из наиболее активно изучаемых направлений лечебной стратегии при НМРЛ является использование "таргетных" препаратов.
Другая область исследовательского интереса - это создание функциональных моделей для прогнозирования ответа на лечение и индивидуализацию лечебного плана.
Возможно, в будущем это улучшит результаты лечения больных НМРЛ.
Список литературы к данной статье предоставляется по запросу.
Пожалуйста, представьтесь.
Новое в терапии рака легкого - Содержание
